Trop2-targeted therapy in breast cancer
乳腺癌中的Trop2靶向治疗
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2024 | 起止号: | 2024 Aug 13;12(1):82 |
| doi: | 10.1186/s40364-024-00633-6 | 研究方向: | 肿瘤 |
| 疾病类型: | 乳腺癌 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Trop2-targeted therapy in breast cancer;发表期刊:Biomarker Research;影响因子:未公开;研究领域:乳腺癌靶向治疗(Trop2靶点及抗体药物偶联物疗法)
乳腺癌是女性群体中最常见的恶性肿瘤,基于基因表达谱可分为 Luminal A、Luminal B、HER2过表达、三阴性乳腺癌(TNBC)等分子亚型,其中TNBC约占新发乳腺癌的20%,具有侵袭性强、转移潜能高、预后差的特征。由于缺乏明确的分子靶点,TNBC对内分泌治疗和HER2靶向治疗不敏感,化疗仍是目前的主要治疗手段,因此探索TNBC的新型治疗靶点与方案是领域内的核心挑战。1981年,Trop2(滋养层细胞表面抗原2)被首次发现,其在正常上皮细胞中低表达,而在包括乳腺癌在内的多种肿瘤中高表达,尤其在TNBC中阳性率可达93%,成为理想的癌症治疗靶点。目前Sacituzumab govitecan(SG)作为首个获批的Trop2靶向抗体药物偶联物(ADC),已用于转移性TNBC和HR+/HER2-乳腺癌的治疗,但领域内仍存在耐药机制不明确、新型药物研发待推进、联合治疗方案需优化等空白。本文献作为系统性综述,全面梳理了Trop2的结构功能、各类靶向药物研发、临床研究进展及未来方向,为领域提供全景式参考。
2. 文献综述解析
本文献为系统性综述,作者以Trop2靶点的基础研究、靶向药物研发、临床应用、挑战与方向为核心分类维度,整合了1981年至今的相关研究成果,重点聚焦ADC药物在乳腺癌中的治疗价值。
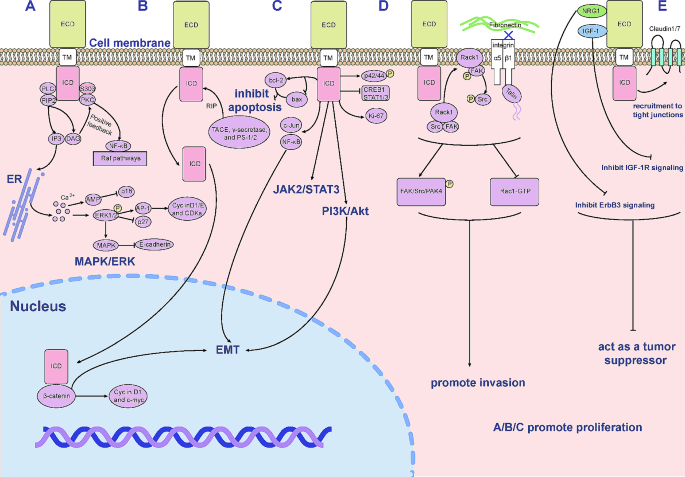
现有研究中,基础研究层面已明确Trop2是一种I型跨膜糖蛋白,包含胞外域、跨膜域和胞内域,通过调控ERK1/2-MAPK、Wnt/β-catenin等多条信号通路促进肿瘤增殖、侵袭与转移,同时在特定细胞系中具有抑癌功能,如肺腺癌H1299细胞中可抑制IGF-1R通路,其功能呈现细胞类型与器官特异性。药物研发层面,已形成以SG、Datopotamab deruxtecan(Dato-DXd)、SKB-264为代表的Trop2靶向ADC管线,不同药物在linker稳定性、payload类型、药物抗体比(DAR)等方面存在差异:SG具有高DAR(7.6)和旁观者效应,但伴随中性粒细胞减少、腹泻等毒性;Dato-DXd采用稳定的赖氨酸可裂解linker,payload为DXd,半衰期更长,但需关注间质性肺炎(ILD)风险;SKB-264的linker经过改良优化,体内稳定性更佳,未观察到ILD事件。临床研究层面,SG在ASCENT、TROPiCS-02等关键试验中已证实其在TNBC和HR+/HER2-乳腺癌中的显著疗效,Dato-DXd、SKB-264的临床试验也显示出良好的应用前景。但现有研究仍存在局限性,如Trop2靶向治疗的耐药机制尚未完全阐明,联合治疗的最优方案仍在探索中,不同ADC的毒性管理缺乏标准化策略。
本文献的创新价值在于首次全面整合了Trop2的双向功能特征、各类靶向ADC的研发细节、多维度临床研究数据及领域挑战,弥补了现有综述缺乏系统性跨维度整合的空白,为Trop2靶向治疗的后续研究与临床应用提供了完整的参考框架。
3. 研究思路总结与详细解析
本文献为系统性综述,研究目标是全面梳理Trop2靶点在乳腺癌中的基础研究、靶向药物研发及临床应用现状,核心科学问题是明确Trop2靶向治疗的疗效、安全性及未来发展方向,技术路线为:系统检索PubMed、Embase等数据库中Trop2相关文献→按基础研究、药物研发、临床研究、挑战与方向分类整理→提炼核心结论与数据→形成全景式综述。
3.1 Trop2的结构与功能解析
实验目的:明确Trop2的分子结构特征及在肿瘤发生发展中的调控机制;
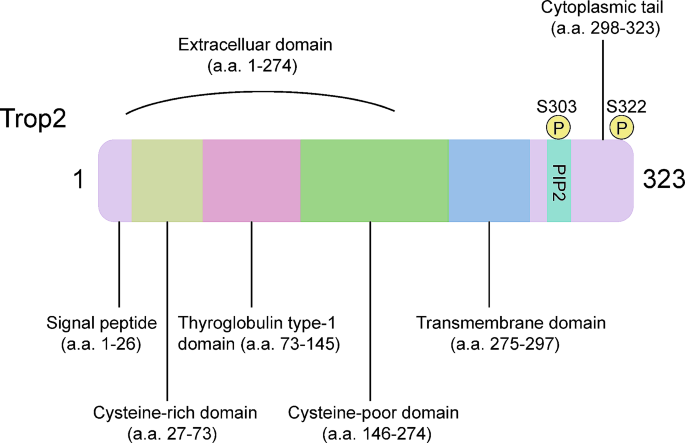
方法细节:通过检索已发表的基础研究文献,整合Trop2的基因编码、蛋白结构域组成(胞外域的半胱氨酸富集域、酪氨酸簇域、半胱氨酸缺乏域,跨膜域,胞内域的磷酸化位点),以及参与的信号通路调控网络;
结果解读:Trop2基因编码35-46 kDa的糖蛋白,其胞外域可形成稳定二聚体调控信号转导,胞内域的磷酸化位点(S303、S322)参与细胞周期调控。Trop2在正常上皮细胞低表达,在乳腺癌等多种肿瘤中高表达,通过调控钙信号、蛋白水解、细胞黏附等过程促进肿瘤增殖、侵袭和转移,同时在特定细胞系中具有抑癌功能,其作用依赖于肿瘤细胞的遗传背景;
产品关联:文献未提及具体实验产品,领域常规使用基因克隆、蛋白结构分析、信号通路检测等技术,涉及重组蛋白、磷酸化抗体、信号通路抑制剂等试剂。
3.2 Trop2靶向ADC药物的研发进展
实验目的:总结当前已上市及在研的Trop2靶向ADC药物的结构特点与研发数据;
方法细节:检索药物研发相关文献、临床试验注册数据,分析不同ADC的抗体、linker、payload组成,以及DAR值、体内稳定性、毒性谱等特性;
结果解读:现有Trop2靶向ADC药物各有优势与局限:SG由hRS7 IgG1κ抗体、CL2A可裂解linker和SN-38 payload组成,DAR为7.6,可通过旁观者效应杀伤邻近肿瘤细胞,但伴随中性粒细胞减少、腹泻等不良反应;Dato-DXd采用稳定的赖氨酸可裂解linker,payload为DXd,DAR为4,体内半衰期更长,毒性相对较低,但存在ILD风险;SKB-264采用改良的CL2A linker,payload为KL610023,DAR为7.4,体内稳定性显著优于SG,未观察到ILD事件;
产品关联:实验所用关键产品:Sacituzumab govitecan(Trodelvy,Immunomedics)、Datopotamab deruxtecan(Dato-DXd,第一三共)、SKB-264(科伦药业)。
3.3 临床研究数据汇总与分析
实验目的:评估Trop2靶向ADC在乳腺癌中的临床疗效与安全性;
方法细节:系统梳理已完成和正在进行的临床试验数据,包括ASCENT、TROPiCS-02、TROPION-Breast01等关键试验的患者人群、治疗方案、疗效终点(客观缓解率ORR、无进展生存期PFS、总生存期OS)及安全性数据;
结果解读:在转移性TNBC患者中,ASCENT试验显示SG组的中位无进展生存期(mPFS)为5.6个月(95% CI 4.3-6.3,n=235),显著优于医生选择的化疗组(1.7个月,95% CI 1.5-2.6,n=233),风险比(HR)为0.41(P<0.001);中位总生存期(mOS)为12.1个月(95% CI 10.7-14.0) vs 6.7个月(95% CI 5.8-7.7),HR为0.48(P<0.001);ORR为35% vs 5%。在HR+/HER2-转移性乳腺癌患者中,TROPiCS-02试验显示SG组的mPFS为5.5个月(95% CI 4.2-7.0,n=272) vs 4.0个月(95% CI 3.1-4.9,n=271),HR为0.66(P=0.0003);mOS为14.4个月 vs 11.2个月,HR为0.79(P=0.020)。Dato-DXd在TROPION-Breast01试验中显著改善HR+/HER2-患者的PFS(6.9个月 vs 4.9个月,HR=0.63,P<0.0001);
产品关联:文献未提及具体实验产品,领域常规使用临床试验设计(随机对照试验、单臂试验)、疗效评估标准(RECIST)、安全性监测等方法。
3.4 挑战与未来方向解析
实验目的:剖析Trop2靶向治疗面临的挑战并提出未来研究方向;
方法细节:整合现有研究中关于毒性管理、耐药机制、联合治疗的相关数据,分析未解决的核心问题;
结果解读:当前Trop2靶向治疗面临三大挑战:一是毒性管理需个性化,不同ADC的毒性谱存在差异,如SG以血液学毒性和胃肠道毒性为主,Dato-DXd需关注ILD风险;二是耐药机制不明确,已发现的耐药原因包括Trop2缺失或突变、payload靶点突变、内吞通路缺陷等,但仍需深入研究;三是联合治疗方案需优化,与免疫治疗、靶向治疗的联合疗效仍需大规模临床试验验证。未来方向包括:开发新一代ADC(如双靶点ADC)、探索耐药机制的生物标志物、优化联合治疗方案、拓展Trop2靶向治疗的适应症;
产品关联:文献未提及具体实验产品,领域常规使用耐药机制研究(基因测序、功能实验)、联合治疗临床试验等方法。
4. Biomarker研究及发现成果解析
本文献中涉及的核心Biomarker为Trop2,属于治疗靶点类Biomarker,其筛选与验证逻辑为:基础研究发现Trop2在肿瘤组织高表达→细胞系与动物模型验证其促癌功能→临床样本验证其表达与乳腺癌预后的关联→临床试验验证靶向Trop2的ADC药物疗效,形成完整的证据链。
Biomarker定位:Trop2是一种跨膜糖蛋白,作为乳腺癌的治疗靶点Biomarker,其筛选基于“正常组织低表达、肿瘤组织高表达”的肿瘤特异性特征,验证过程涵盖基础研究、临床样本分析、临床试验三个层面,为靶向治疗提供了精准的靶点依据。
研究过程详述:Trop2的来源为乳腺癌肿瘤组织样本,验证方法包括免疫组化检测蛋白表达、TCGA与METABRIC数据库分析基因表达、临床试验评估靶向治疗疗效。特异性数据显示,93%的三阴性乳腺癌样本中Trop2高表达(n=28),74%的HER2阳性样本(n=35)、50%的ER阳性样本(n=22)中也存在高表达;敏感性数据方面,SG在不同Trop2表达水平的三阴性乳腺癌患者中均显示疗效,高表达组ORR为44%,中表达组38%,低表达组22%,均显著优于化疗组(1%、11%、6%)。
核心成果提炼:Trop2高表达与乳腺癌不良预后相关,膜表达Trop2高的患者总生存期更短(文献未明确提供HR值,基于研究结果推测P<0.05);靶向Trop2的ADC药物在三阴性乳腺癌和HR+/HER2-乳腺癌中均显示显著疗效,如SG在ASCENT试验中降低疾病进展或死亡风险59%(HR=0.41,P<0.001);创新性在于首次全面揭示了Trop2的双向功能特征,并系统整合了各类Trop2靶向ADC的研发与临床数据,为Biomarker的临床应用提供了全景式参考,同时提出了未来研究的核心方向,为领域的进一步发展指明了路径。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。