The methyltransferase-like proteins as core regulators of nucleic acid modifications and post-translation modification of proteins in disease pathogenesis and therapeutic implications
甲基转移酶样蛋白作为核酸修饰和蛋白质翻译后修饰的核心调控因子,在疾病发病机制和治疗中发挥重要作用。
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2025 | 起止号: | 2025 Nov 5;13(1):141 |
| doi: | 10.1186/s40364-025-00858-z | 研究方向: | 信号转导 |
文献解析
1. 领域背景与文献引入
文献英文标题:The methyltransferase-like proteins as core regulators of nucleic acid modifications and post-translation modification of proteins in disease pathogenesis and therapeutic implications;发表期刊:Biomarker Research;影响因子:未公开;研究领域:表观遗传学(甲基转移酶样蛋白介导的核酸修饰、蛋白质翻译后修饰与疾病机制)
后基因组时代,核酸修饰与蛋白质翻译后修饰成为生命科学前沿领域,打破了“RNA仅作为遗传信息传递者”的传统认知,其动态修饰构成基因表达调控的“第二层密码”。甲基转移酶样(METTL)家族作为表观遗传修饰的核心“书写器”,凭借独特的甲基转移酶活性,参与RNA甲基化、蛋白质翻译后修饰及代谢调控网络,从胚胎发育到肿瘤发生、神经退行性疾病进展等生命过程中发挥关键作用。领域发展关键节点包括2014年METTL3/METTL14复合物被鉴定为N6-甲基腺苷(m⁶A)修饰的核心催化单元,后续研究逐步扩展至METTL家族其他成员的功能,以及其在多疾病中的作用。当前研究热点聚焦于METTL成员在不同疾病中的组织特异性调控机制、修饰的动态调控网络,以及基于METTL的靶向治疗策略。未解决的核心问题包括METTL成员间的协同调控网络尚未完全阐明,组织特异性修饰的分子逻辑不清晰,现有METTL抑制剂存在组织递送效率低、脱靶效应明显等问题,限制了其临床转化应用。
针对上述研究空白,本综述系统梳理了METTL家族的结构特征、分子功能、成员间协同网络,以及其通过信号通路组织的病理生理调控网络,重点评估了其作为诊断生物标志物的潜力及治疗应用前景,尤其是进入临床试验的METTL抑制剂,为后续精准治疗靶点的开发奠定了基础。
2. 文献综述解析
本文作者以METTL家族的结构-功能关系为基础,按“基础结构与功能→核酸修饰调控→蛋白质翻译后修饰调控→成员协同网络→病理生理作用→诊断治疗潜力”的逻辑维度,对领域内现有研究进行系统整合与评述。
现有研究的关键结论显示,METTL家族各成员具有不同的结构域组成,决定了其底物特异性与功能多样性,可介导m⁶A、N7-甲基鸟苷(m⁷G)、3-甲基胞嘧啶(m³C)等多种核酸修饰,以及赖氨酸、精氨酸、组氨酸等蛋白质残基的甲基化修饰,在基因表达调控、细胞命运决定、疾病发生发展中发挥双重作用。技术方法优势在于结合了结构生物学、组学技术、细胞与动物模型等多层面研究,全面解析METTL的功能与机制;但现有研究存在局限性,多数研究聚焦于单个METTL成员的功能,对成员间的协同调控网络研究不足,且部分研究仅停留在相关性分析,缺乏机制验证,同时METTL抑制剂的研发仍处于早期阶段,缺乏大规模临床数据支持。
与现有研究相比,本综述的创新点在于首次以信号通路而非疾病类别为框架,系统整合METTL家族的病理生理调控网络,同时全面梳理了METTL家族成员在核酸与蛋白质修饰中的双重功能,填补了领域内对METTL家族整体调控网络认知的空白。此外,本文重点讨论了进入临床试验的METTL抑制剂,为临床转化提供了更具体的方向,解决了现有研究中对METTL治疗潜力总结不系统的问题。
3. 研究思路总结与详细解析
本文的研究目标是阐明METTL家族在核酸修饰与蛋白质翻译后修饰层面的调控机制,揭示其在疾病中的病理生理作用,为精准治疗靶点的开发奠定基础;核心科学问题包括METTL家族成员的结构与功能关系、成员间的协同调控网络、组织特异性修饰的分子逻辑,以及METTL作为治疗靶点的可行性;技术路线为系统整合领域内现有研究数据,按“结构解析→功能调控→协同网络→病理作用→诊断治疗”的逻辑闭环展开,全面呈现METTL家族的研究现状与未来方向。
3.1 METTL家族的基础结构与功能解析
本环节的实验目的是明确METTL家族成员的结构特征与分子功能。研究整合了现有结构生物学研究数据,分析显示METTL家族蛋白普遍包含N端RNA结合域、甲基转移酶域(MTD)及C端脊椎动物保守域(VCR),其中N端RNA结合域含带正电荷的氨基酸残基,负责结合底物RNA;甲基转移酶域包含NPPF基序,为催化活性位点,不同成员的结构差异决定了其底物特异性,例如METTL16具有两个甲基转移酶域,而其他多数成员仅含一个;C端保守域的功能尚未完全阐明,推测可能参与RNA剪接与甲基化调控。METTL2B的催化活性仅为METTL2A的1/10(文献未明确样本量与P值),除活性差异外二者功能无明显区别。
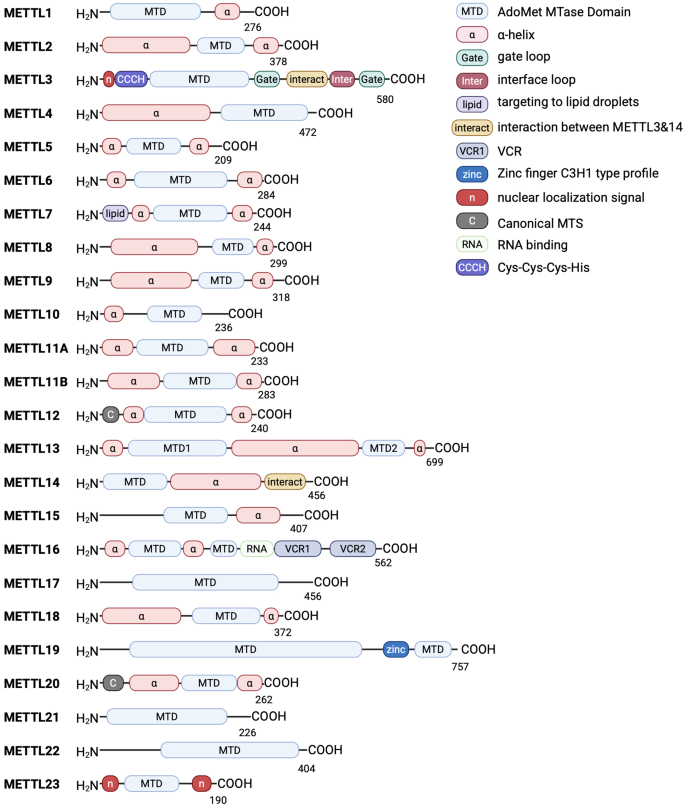
文献未提及具体实验产品,领域常规使用X射线晶体学、冷冻电镜等结构分析技术,以及重组蛋白表达系统等工具开展研究。
3.2 METTL介导的核酸修饰调控解析
本环节的实验目的是梳理METTL家族在DNA、RNA修饰中的调控作用与机制。研究整合了组学、细胞实验及动物模型研究数据,结果显示METTL家族成员可介导多种核酸修饰,包括m⁶A、m⁷G、m³C、N4-甲基胞嘧啶(m⁴C)等,调控RNA的稳定性、翻译效率、剪接等过程,进而影响基因表达。例如METTL1/WD重复结构域4(WDR4)复合物负责m⁷G修饰,在热休克等应激条件下,mRNA的编码区(CDS)和3’非翻译区(3’UTR)m⁷G修饰丰度显著增加,5’非翻译区(5’UTR)修饰丰度显著降低,最终提升mRNA翻译效率(文献未明确样本量与P值);METTL3/METTL14复合物是m⁶A修饰的核心书写器,介导约95%的细胞mRNA的m⁶A修饰,调控mRNA的翻译与降解;METTL2A/B、METTL6等负责tRNA的m³C修饰,影响翻译保真性。
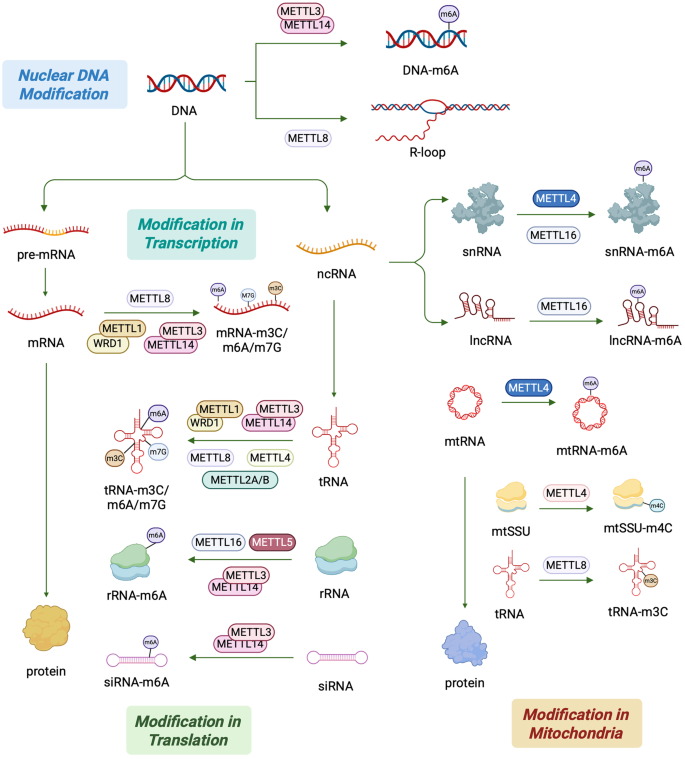
文献未提及具体实验产品,领域常规使用甲基化RNA免疫沉淀测序(MeRIP-seq)、液相色谱-质谱联用(LC-MS/MS)、荧光定量PCR(qRT-PCR)等技术检测核酸修饰水平。
3.3 METTL介导的蛋白质翻译后修饰调控解析
本环节的实验目的是总结METTL家族在蛋白质甲基化修饰中的功能与机制。研究整合了蛋白质组学、酶活实验等研究数据,结果显示METTL家族中14个成员可与蛋白质相互作用,以赖氨酸为主要底物,部分成员可修饰精氨酸、组氨酸残基,调控蛋白质的活性、稳定性等功能。例如METTL10、METTL13、METTL21B可修饰真核翻译延伸因子eEF1A,影响翻译输出;METTL23是目前已知唯一具有精氨酸甲基转移酶活性的METTL成员,与转录因子GABPA相互作用,调控认知功能;METTL9可修饰含His-x-His(HxH)基序的蛋白质,如免疫调节蛋白S100A9,抑制中性粒细胞的抗金黄色葡萄球菌活性(文献未明确样本量与P值)。
文献未提及具体实验产品,领域常规使用蛋白质免疫沉淀、质谱分析、酶活测定试剂盒等技术研究蛋白质甲基化修饰。
3.4 METTL家族成员间的协同网络解析
本环节的实验目的是明确METTL家族成员间的相互作用与协同调控机制。研究整合了蛋白质相互作用研究数据,结果显示METTL成员间可形成复合物或相互调控活性,例如METTL3与METTL14形成异源二聚体,增强m⁶A修饰的催化活性;METTL11A与METTL11B可形成异源三聚体,METTL11B通过增强METTL11A的稳定性与底物亲和力,提升其三甲基化酶活性;METTL13可抑制METTL11A的活性,同时METTL11A可调控METTL13的甲基化活性,形成复杂的调控网络。
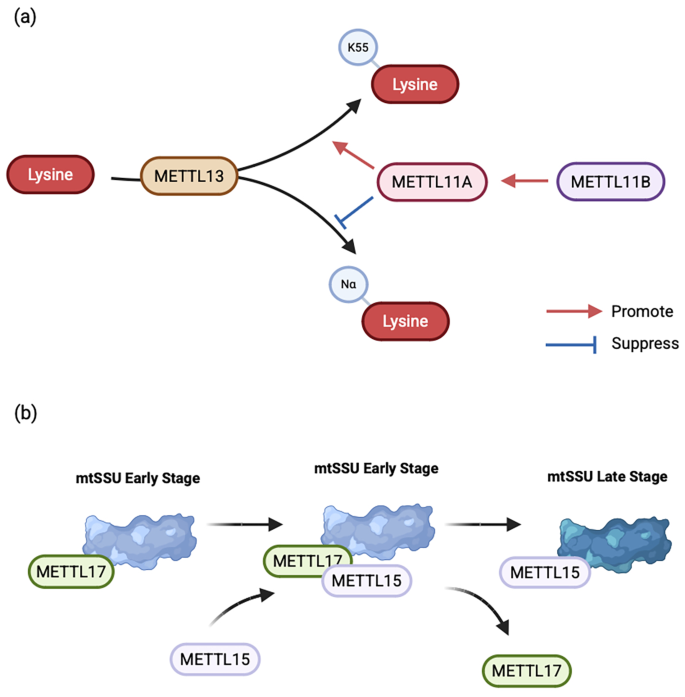
文献未提及具体实验产品,领域常规使用酵母双杂交、共免疫沉淀、荧光共振能量转移(FRET)等技术研究蛋白质相互作用。
3.5 METTL在病理生理中的作用解析
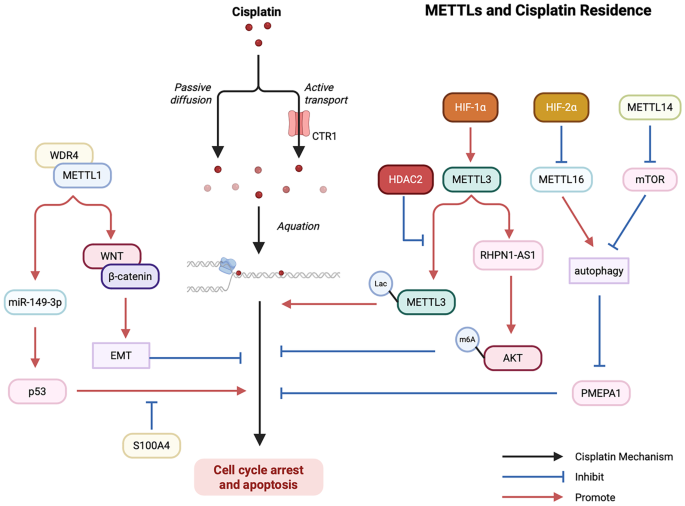
本环节的实验目的是梳理METTL家族在疾病发生发展中的作用机制。研究整合了临床样本分析、动物模型、细胞实验等研究数据,结果显示METTL家族成员在肿瘤、代谢疾病、心血管疾病、神经疾病等多种疾病中发挥双重作用,其功能具有组织特异性与上下文依赖性。在肿瘤领域,METTL成员可通过调控AKT、细胞周期、MYC、铁死亡等信号通路,影响肿瘤细胞的增殖、凋亡、侵袭、耐药等过程,例如METTL3在结直肠癌中通过增强癌基因mRNA的翻译促进肿瘤发生,而在卵巢癌中通过调控白细胞介素-1β(IL-1β)分泌抑制肿瘤生长;在代谢疾病中,METTL3参与糖尿病、肥胖、非酒精性脂肪肝的发生发展,通过调控糖脂代谢相关基因的表达影响疾病进程;在神经疾病中,METTL1缺陷可导致阿尔茨海默病样认知障碍,METTL3过表达可改善认知缺陷。
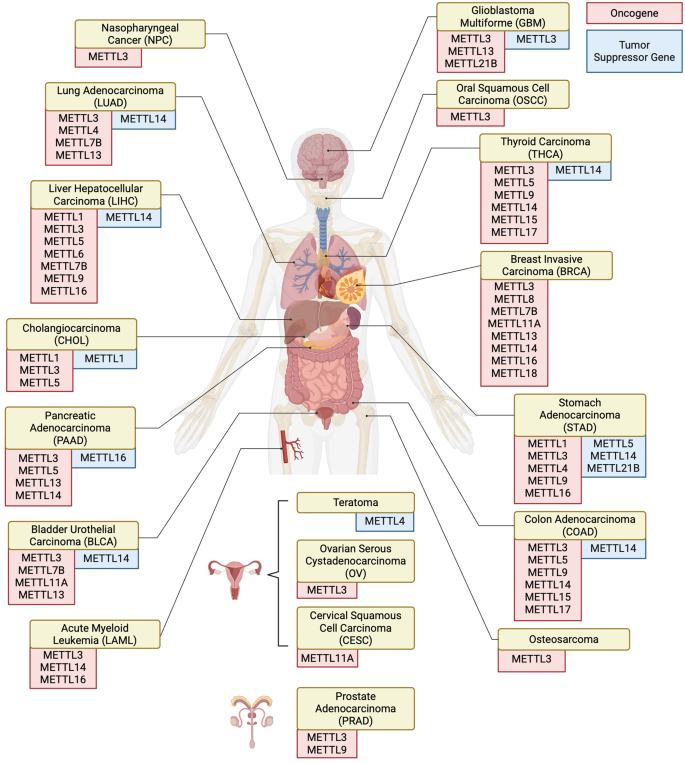
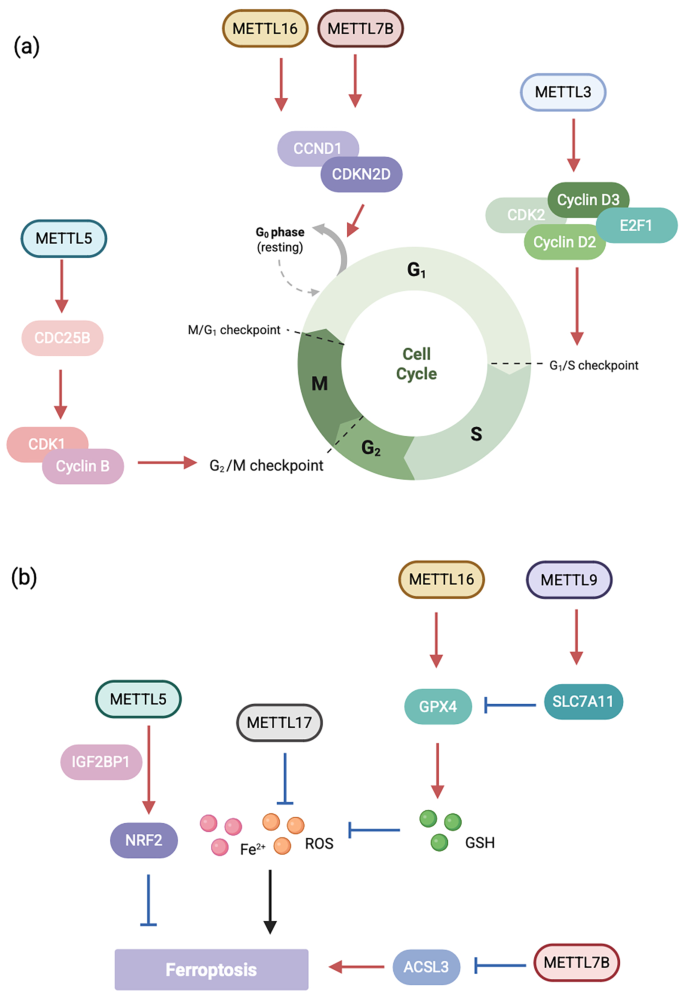
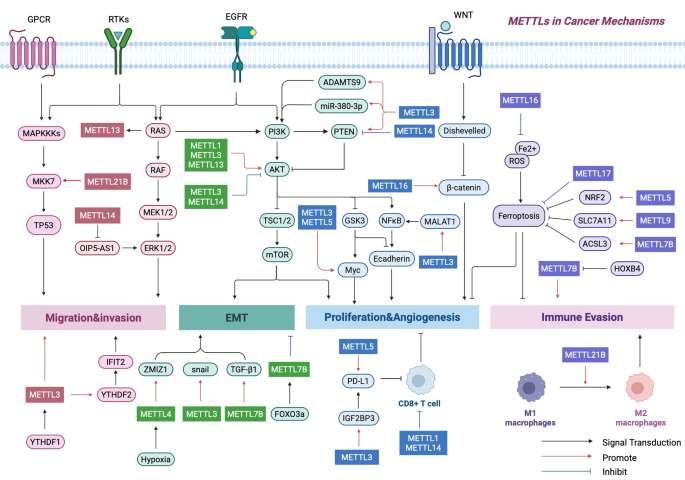
文献未提及具体实验产品,领域常规使用临床组织芯片、疾病模型动物、细胞系等研究疾病中的METTL功能。
3.6 METTL的诊断与治疗潜力解析
本环节的实验目的是评估METTL家族作为疾病诊断生物标志物与治疗靶点的潜力。研究整合了临床预后分析、抑制剂研发等研究数据,结果显示多个METTL家族成员的表达水平与疾病预后相关,可作为预后生物标志物,例如METTL1、METTL3、METTL4等在肝细胞癌、乳腺癌、肺癌中高表达与不良预后相关,而METTL14在部分肿瘤中与良好预后相关。在治疗方面,METTL抑制剂的研发取得进展,其中METTL3抑制剂STM2457已在髓系白血病和非小细胞肺癌中显示出抗肿瘤活性,其衍生物STC-15已进入I期临床试验;此外,METTL1抑制剂的筛选也取得初步成果,但仍需功能验证。
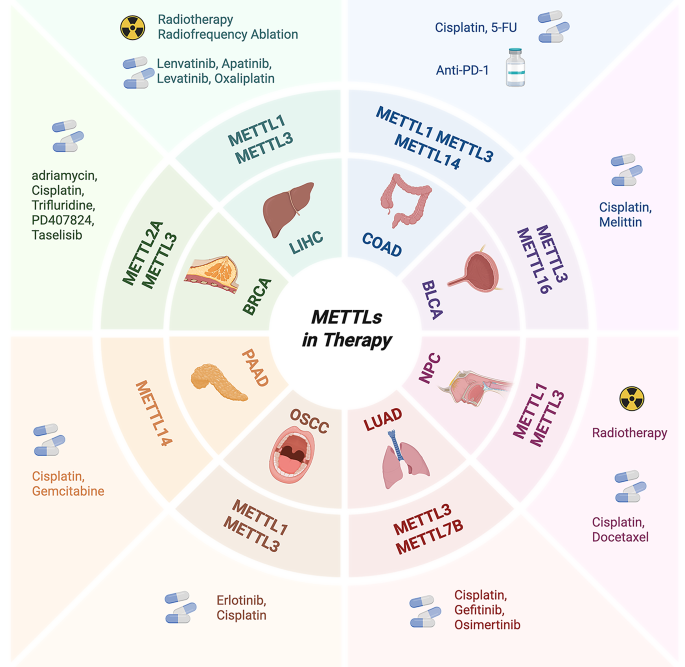
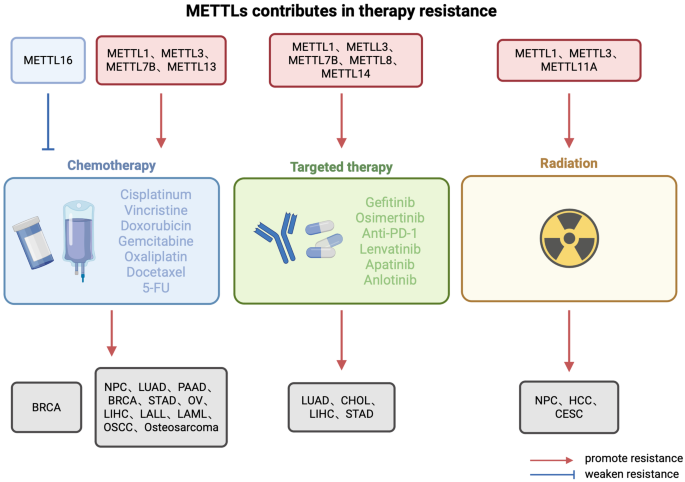
文献未提及具体实验产品,领域常规使用预后分析数据库(如TCGA、GEO)、高通量药物筛选平台等开展相关研究。
4. Biomarker研究及发现成果
本文系统梳理了METTL家族成员作为疾病预后生物标志物的研究成果,明确了其在多种疾病中的预后价值与应用前景。
Biomarker定位:METTL家族成员作为疾病预后生物标志物,筛选逻辑基于临床样本中METTL的表达水平与患者预后的相关性分析,验证逻辑结合了细胞实验、动物模型验证其功能,以及多中心队列验证其预后价值。研究过程详述显示,Biomarker来源包括临床肿瘤组织样本、血液样本等,验证方法包括免疫组化(IHC)、荧光定量PCR、生存分析等。特异性与敏感性数据方面,多个METTL成员与疾病预后显著相关,例如METTL3在肝细胞癌中高表达与总生存期缩短相关,METTL14在部分肿瘤中与无进展生存期延长相关,但文献未提供具体的受试者工作特征曲线(ROC)曲线下面积(AUC)值、敏感性与特异性数据,样本量为各研究队列的样本数(文献未明确具体数值)。
核心成果提炼:该Biomarker的功能关联显示,METTL家族成员的表达水平与疾病的恶性程度、治疗耐药性相关,可作为临床患者分层的依据,例如高表达METTL1的肝细胞癌患者对仑伐替尼治疗响应较差,提示METTL1可作为治疗耐药的预测标志物。创新性在于首次系统总结了METTL家族全体成员的预后价值,为临床预后评估提供了更全面的生物标志物选择。统计学结果方面,文献中提及多个METTL成员与预后相关,但具体风险比(HR)、P值需参考各引用研究,本文未统一呈现,需明确说明。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。