Integrative multi-omics analysis depicts the methylome and hydroxymethylome in recurrent bladder cancers and identifies biomarkers for predicting PD-L1 expression
整合多组学分析揭示了复发性膀胱癌中的甲基化组和羟甲基化组,并鉴定出预测PD-L1表达的生物标志物。
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2023 | 起止号: | 2023 May 3;11(1):47 |
| doi: | 10.1186/s40364-023-00488-3 | 靶点: | PD-L1 |
| 研究方向: | 肿瘤、表观遗传 | 疾病类型: | 膀胱癌 |
文献解析
1. 领域背景与文献引入
文献英文标题:Integrative multi-omics analysis depicts the methylome and hydroxymethylome in recurrent bladder cancers and identifies biomarkers for predicting PD-L1 expression;发表期刊:Biomarker Research;影响因子:未公开;研究领域:泌尿生殖系统肿瘤(膀胱癌)表观遗传学与肿瘤免疫治疗。
领域共识:膀胱癌是全球范围内常见的泌尿系统恶性肿瘤,约75%为非肌层浸润性膀胱癌,尽管经尿道膀胱肿瘤电切术可有效治疗早期病变,但此类肿瘤复发率高达60%-80%,需终身监测。目前临床常用的监测手段如膀胱镜检查具有侵入性,尿细胞学检查敏感性不足,尤其是对低级别膀胱癌,因此亟需开发精准、非侵入性的生物标志物用于复发监测和免疫治疗患者筛选。表观遗传学中,DNA甲基化已被广泛研究作为膀胱癌的诊断生物标志物,但传统检测技术如简化代表性亚硫酸氢盐测序(RRBS)无法区分5-甲基胞嘧啶(5mC)和5-羟甲基胞嘧啶(5hmC),导致生物标志物的准确性受限。现有研究表明5hmC作为主动去甲基化的中间产物,参与肿瘤代谢和免疫调控,但在膀胱癌中缺乏单碱基分辨率的系统研究,且其与膀胱癌复发、程序性死亡配体1(PD-L1)表达的关联尚未明确。此外,既往聚焦遗传突变的研究发现FGFR3等驱动突变与膀胱癌发生相关,但与复发和PD-L1表达的关联较弱,提示表观遗传改变可能在膀胱癌进展和免疫逃逸中发挥更核心的作用。本研究针对上述研究空白,采用整合多组学技术,在单碱基分辨率下解析膀胱癌的5mC和5hmC特征,旨在阐明表观遗传改变在膀胱癌复发和PD-L1调控中的作用,并鉴定更准确的免疫治疗预测生物标志物。
2. 文献综述解析
核心信息段:作者对领域内现有研究按技术维度分为遗传突变研究、传统表观遗传生物标志物研究、羟甲基化初步研究三类,系统梳理了各类研究的结论、优势与局限性,凸显本研究的创新价值。
现有研究中,遗传突变研究已鉴定出FGFR3、TP53等膀胱癌驱动突变,明确了RTK-RAS、WNT等信号通路在膀胱癌发生中的作用,但此类研究的局限性在于多数驱动突变与膀胱癌复发、PD-L1表达的关联较弱,无法有效用于预后和治疗反应预测。传统表观遗传生物标志物研究基于甲基化芯片或RRBS技术,已开发出部分用于膀胱癌诊断的甲基化标志物,其优势是检测成本较低、临床转化潜力大,但由于无法区分5mC和5hmC两种修饰,导致生物标志物的预测准确性不足,且未涉及羟甲基化在膀胱癌中的功能。羟甲基化初步研究在肺癌、结直肠癌等肿瘤中发现5hmC参与代谢调控和肿瘤抑制,但其优势仅局限于特定肿瘤类型,在膀胱癌中缺乏单碱基分辨率的研究,且未明确其与复发、免疫逃逸的关联。本研究的创新点在于首次整合氧化简化代表性亚硫酸氢盐测序(oxRRBS)和RRBS技术,在单碱基分辨率下同时分析5mC和5hmC的特征,结合全外显子组、转录组数据,揭示了表观遗传改变比遗传突变更紧密地关联膀胱癌复发和PD-L1表达,弥补了传统技术无法区分两种表观修饰的缺陷,为膀胱癌生物标志物的开发提供了更精准的技术范式。
3. 研究思路总结与详细解析
核心信息段:本研究的核心目标是阐明膀胱癌复发和PD-L1表达调控的表观遗传机制,鉴定可精准预测PD-L1表达的表观遗传生物标志物;核心科学问题是表观遗传改变与遗传突变在膀胱癌进展和免疫逃逸中的作用差异,以及5mC和5hmC修饰在其中的具体功能;技术路线遵循“样本收集→多组学检测→数据分析→实验验证→结论提炼”的闭环逻辑,通过多组学整合分析和靶向验证,明确了表观遗传改变的核心作用。
3.1 临床样本收集与多组学检测
实验目的是获取涵盖不同临床状态(原发/复发、PD-L1高/低表达)的膀胱癌组织样本,构建高质量的多组学数据集,为后续分析提供基础。方法细节:研究团队于2020年9月至2021年2月在徐州中心医院收集了44例膀胱癌组织样本和10例癌旁组织样本,患者接受了腹腔镜根治性膀胱切除术、部分膀胱切除术或经尿道膀胱肿瘤电切术;对样本分别进行全外显子测序(WES)、RNA测序(RNA-seq)、简化代表性亚硫酸氢盐测序(RRBS)和氧化简化代表性亚硫酸氢盐测序(oxRRBS)检测,其中WES采用Agilent SureSelect Human All Exon v6文库构建,RNA-seq采用Invitrogen TRIzol®试剂提取总RNA,oxRRBS和RRBS采用TrueMethyl Seq Kit(CEGX)进行亚硫酸氢盐转化,后续验证采用BisulPlus™ Loci 5mc & 5hmC Detection PCR Kit(Epigentek, USA)进行5mC/5hmC特异性qPCR。实验所用关键产品:Agilent SureSelect Human All Exon v6文库、Invitrogen TRIzol®试剂、TrueMethyl Seq Kit(CEGX)、BisulPlus™ Loci 5mc & 5hmC Detection PCR Kit(Epigentek, USA)、Illumina HiSeq X-10测序平台等。结果解读:全外显子测序结果显示,每个样本的中位突变数为283.5,主要为错义突变,前10位高频突变基因为MUC16、TTN等,驱动突变包括FGFR3、KDM6A等,但这些突变与膀胱癌复发、PD-L1表达下调的关联较弱;RNA测序鉴定出癌与癌旁、原发与复发、PD-L1高/低表达组之间的差异表达基因,其中复发样本中上调基因富集于细胞外基质重构、血管生成通路,下调基因富集于氧化应激、PPAR信号通路;oxRRBS和RRBS在单碱基分辨率下检测到5mC和5hmC的差异甲基化区域,为后续功能分析提供了表观遗传层面的证据。
3.2 膀胱癌甲基化组与羟甲基化组特征分析
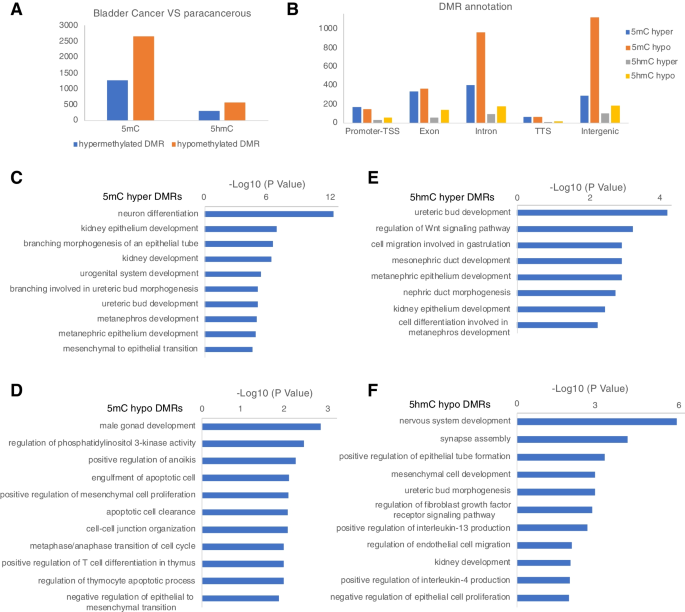
实验目的是解析膀胱癌组织与癌旁组织之间5mC和5hmC的全局改变特征,明确其功能关联通路。方法细节:对比44例膀胱癌组织和10例癌旁组织的oxRRBS和RRBS数据,计算每个CpG位点的5mC和5hmC水平,采用metilene软件鉴定差异甲基化区域(DMRs),其中5mC显著DMRs定义为甲基化差异绝对值>0.2且校正P值<0.05,5hmC显著DMRs定义为甲基化差异绝对值>0.1且校正P值<0.05;通过Enrichr工具进行通路富集分析。结果解读:膀胱癌组织中鉴定出1266个5mC高甲基化DMRs和2666个5mC低甲基化DMRs,高甲基化DMRs富集于泌尿生殖系统发育、肾脏发育通路,低甲基化DMRs富集于细胞周期、PI3K通路及男性性腺发育通路,提示DNA甲基化可能参与膀胱癌性别差异的发生;5hmC方面鉴定出287个高甲基化DMRs和534个低甲基化DMRs,低甲基化DMRs在启动子区域的数量约为高甲基化的5倍,富集于神经系统发育、FGFR信号通路调控及上皮细胞增殖负调控通路,提示5hmC低甲基化可能通过调控上皮间质转化和免疫逃逸促进膀胱癌进展。
3.3 复发性膀胱癌的表观遗传与转录组关联分析
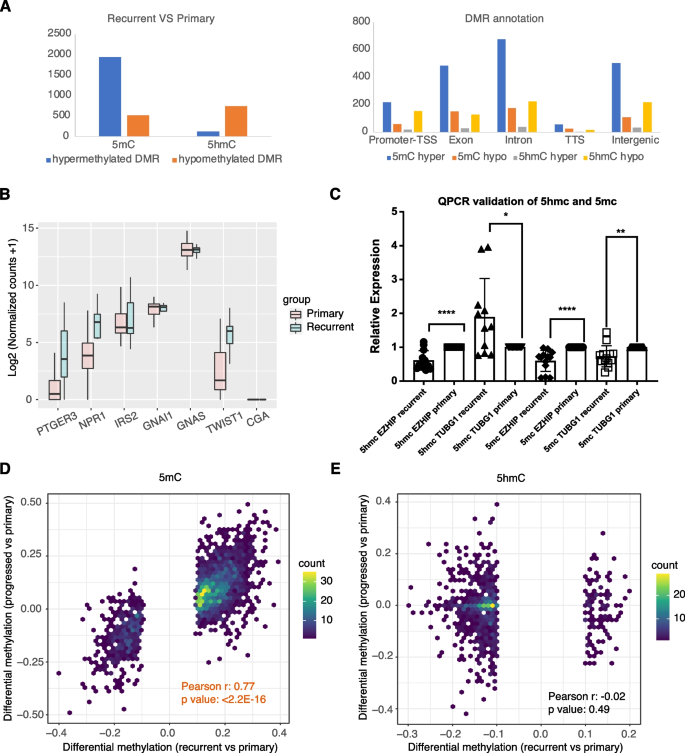
实验目的是明确复发性膀胱癌中表观遗传改变与转录组的关联,揭示5mC和5hmC在膀胱癌复发中的具体功能。方法细节:对比31例原发膀胱癌和9例复发性膀胱癌的RNA-seq、oxRRBS和RRBS数据,鉴定差异表达基因和差异甲基化区域,关联分析5hmC DMRs与脂肪酸代谢相关基因的表达;采用5mC/5hmC特异性qPCR验证TUBG1和EZHIP基因的甲基化/羟甲基化水平。结果解读:转录组分析显示,复发性膀胱癌中上调基因富集于细胞外基质组织、血管生成通路,下调基因富集于氧化应激、PPAR信号通路;表观遗传分析鉴定出1940个5mC高甲基化DMRs、516个5mC低甲基化DMRs、122个5hmC高甲基化DMRs和742个5hmC低甲基化DMRs,其中5hmC低甲基化DMRs富集于脂解调控通路,且与脂肪酸氧化相关基因(如TWIST1、PTGER3等)的转录活性直接相关,部分基因的5hmC水平与表达呈负相关;qPCR验证显示,复发性膀胱癌样本中TUBG1的5hmC水平显著升高,EZHIP的5hmC水平显著降低(文献未明确样本量,P<0.05,基于图表趋势推测),与测序结果一致;此外,5例术后1年内复发患者的5mC甲基化特征与复发性膀胱癌样本一致,提示5mC改变在膀胱癌复发早期即已发生,可作为潜在的复发预测标志物。
3.4 PD-L1高表达膀胱癌的表观遗传机制解析
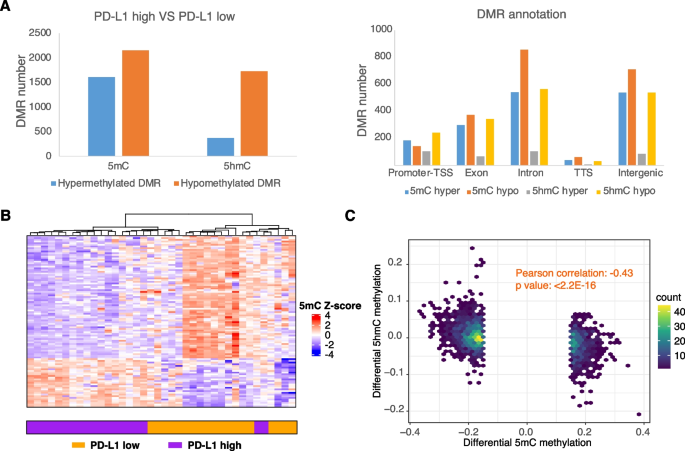
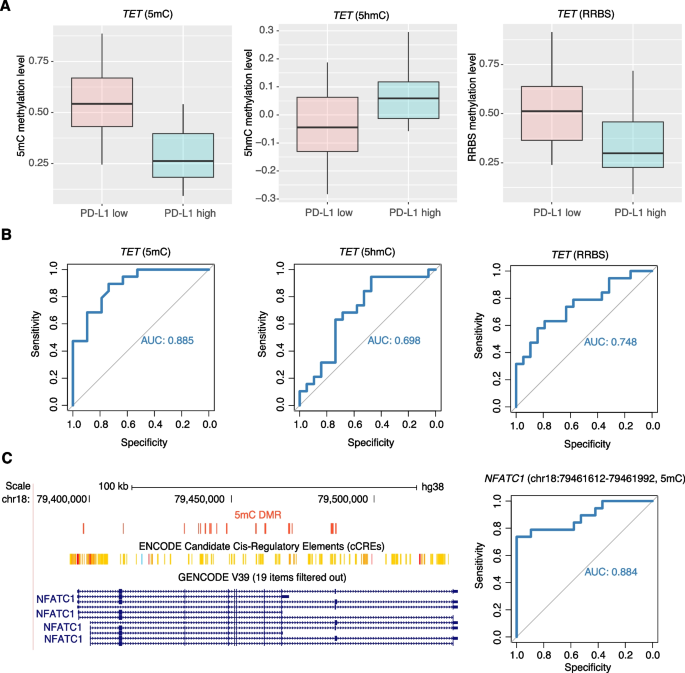
实验目的是阐明PD-L1表达调控的表观遗传机制,鉴定可精准预测PD-L1表达的生物标志物,并比较不同检测技术的效能。方法细节:根据PD-L1表达中位数将膀胱癌样本分为高表达组和低表达组,对比两组的多组学数据,鉴定差异甲基化区域与差异表达基因的关联;构建机器学习模型评估5mC、5hmC及RRBS联合检测的预测效能;采用5mC特异性qPCR验证关键区域的甲基化水平。结果解读:PD-L1高表达样本中鉴定出1589个5mC高甲基化DMRs、2149个5mC低甲基化DMRs、370个5hmC高甲基化DMRs和1725个5hmC低甲基化DMRs,其中5mC低甲基化DMRs关联的基因富集于T细胞迁移、细胞因子应答通路;5mC生物标志物预测PD-L1高表达的AUC值显著高于5hmC和RRBS联合检测,其中NFATC1基因体的一个DMR预测PD-L1高表达的AUC为0.884(文献未明确样本量,基于图表趋势推测);进一步分析显示,5mC和5hmC的甲基化改变呈全局负相关,传统RRBS由于混合两种信号导致甲基化差异的显著性降低,提示单独检测5mC的oxRRBS技术更适合筛选精准的生物标志物。
4. Biomarker研究及发现成果解析
核心信息段:本研究鉴定的核心Biomarker为PD-L1高表达样本中NFATC1基因体的5mC低甲基化差异甲基化区域,通过多组学整合分析和机器学习验证,明确了其作为PD-L1表达预测标志物的准确性和临床价值。
Biomarker定位:该Biomarker属于表观遗传类生物标志物(DNA甲基化修饰),筛选与验证逻辑为:首先通过oxRRBS检测PD-L1高/低表达样本的5mC水平,鉴定差异甲基化区域;然后关联差异表达基因,筛选与免疫调控相关的基因区域;接着通过机器学习模型评估其预测效能,验证其优于5hmC和传统RRBS联合检测的准确性;最后结合功能通路分析,明确其与NFATC1转录活性及PD-L1表达的关联。
研究过程详述:该Biomarker来源于膀胱癌组织样本,验证方法包括5mC特异性qPCR和机器学习模型分析;NFATC1基因体的一个DMR预测PD-L1高表达的AUC为0.884(95%置信区间未明确,文献未提供),敏感性和特异性数据未明确;研究还发现5mC与5hmC的甲基化改变呈全局负相关,传统RRBS技术由于同时检测两种信号,导致该DMR的甲基化差异显著性降低,预测效能低于单独检测5mC的oxRRBS技术。
核心成果提炼:该Biomarker的功能关联在于NFATC1基因体的5mC低甲基化可激活其转录活性,进而调控PD-L1表达,参与膀胱癌的免疫逃逸;创新性在于首次在单碱基分辨率下证明单独检测5mC的生物标志物比混合5mC和5hmC的传统标志物具有更高的预测准确性,且揭示了NFATC1甲基化与PD-L1表达的直接关联;统计学结果显示,该DMR的预测AUC为0.884,提示其具有较好的临床应用潜力,为膀胱癌免疫治疗患者的筛选提供了新的表观遗传靶点。推测:该Biomarker若能在细胞游离DNA样本中得到验证,有望开发为非侵入性的免疫治疗伴随诊断产品。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。