Redox signaling and Alzheimer's disease: from pathomechanism insights to biomarker discovery and therapy strategy
氧化还原信号传导与阿尔茨海默病:从发病机制的深入理解到生物标志物的发现和治疗策略
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2020 | 起止号: | 2020;8:42 |
| doi: | 10.1186/s40364-020-00218-z | 研究方向: | 信号转导 |
| 疾病类型: | 阿尔茨海默症 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Redox signaling and Alzheimer’s disease: from pathomechanism insights to biomarker discovery and therapy strategy;发表期刊:Biomarker Research;影响因子:未公开;研究领域:神经退行性疾病(阿尔茨海默病)
领域共识:阿尔茨海默病(AD)是全球最常见的神经退行性疾病,随着人口老龄化加剧,其患病率呈指数增长,预计未来40年患者数量将增加约3倍,成为老年人群健康的主要挑战。1984年至2017年间,所有针对AD的临床试验均未能有效改善疾病进展,凸显了对其病理机制深入解析的迫切需求。目前已知AD的核心病理特征包括过度磷酸化tau蛋白聚集、β-淀粉样蛋白(Aβ)沉积、神经炎症及氧化应激等,其中氧化还原信号通路的异常激活被认为是驱动AD神经退行性变的关键因素之一,但氧化还原信号与代谢通路的交叉调控机制尚未完全阐明,且缺乏特异性高的早期诊断生物标志物。在此背景下,该综述系统整合了氧化还原信号在AD病理中的作用及其与代谢通路的关联,为AD的机制研究、生物标志物发现及治疗策略开发提供了全面的学术依据。
2. 文献综述解析
该综述以“氧化还原信号-代谢通路-AD病理”为核心逻辑,按脂质代谢、葡萄糖代谢、嘌呤代谢、色氨酸代谢、维生素代谢、金属离子代谢六大维度,系统梳理了领域内现有研究的结论、技术优势与局限性,明确了本综述在整合交叉机制与拓展治疗视角方面的创新价值。
现有研究中,脂质代谢领域已证实多不饱和脂肪酸的氧化损伤、载脂蛋白E(APOE)基因多态性(尤其是APOE4等位基因)与AD发病风险密切相关,且首次发现包含10种血浆代谢物的生物标志物面板可在2-3年内预测老年人群向AD或遗忘型轻度认知障碍的转化,准确率超90%;葡萄糖代谢领域明确了脑葡萄糖低代谢、脑脊液(CSF)乳酸及丙酮酸水平变化与AD认知损伤的关联;嘌呤代谢领域揭示了鸟苷、次黄嘌呤、尿酸等代谢物在AD中的双向调控作用,但尿酸的神经保护或损伤作用仍存在争议;色氨酸代谢领域聚焦犬尿氨酸通路,阐明了3-羟基犬尿氨酸、喹啉酸等神经毒性代谢物与犬尿喹啉酸、邻氨基苯甲酸等神经保护性代谢物的失衡对AD的影响;维生素代谢领域证实了维生素D、B族维生素、硫胺素、维生素E在AD预防与治疗中的潜力;金属离子代谢领域则明确了锌、铁、铜离子失衡通过促进Aβ聚集与活性氧(ROS)生成参与AD病理。现有研究的技术优势在于采用了代谢组学、临床队列分析等多维度方法,覆盖了AD病理的多个层面,但局限性也较为明显,部分生物标志物的临床验证样本量不足,部分天然产物的治疗效果仅在预临床模型中得到证实,缺乏大样本随机对照临床试验数据。与现有研究相比,该综述的创新点在于首次系统整合了氧化还原信号与六大代谢通路的交叉对话机制,同时突出了AD干预对心力衰竭、慢性肾脏病等并发症的潜在益处,为AD的多维度研究提供了新的视角。
3. 研究思路总结与详细解析
该综述的研究目标是全面解析氧化还原信号在AD病理中的调控作用,明确氧化还原信号与代谢通路的关联机制,挖掘潜在的AD生物标志物与治疗策略;核心科学问题为氧化还原信号如何通过调控代谢通路驱动AD神经退行性变,以及这些通路间的交叉对话机制;技术路线为基于领域内已发表的SCI文献,按代谢通路分类系统梳理,整合氧化还原相关机制,总结天然产物治疗潜力与并发症干预价值,形成完整的学术评述体系。
3.1 氧化还原信号与AD代谢通路关联分析
实验目的:明确氧化还原信号与AD相关代谢通路的调控关系,挖掘潜在的生物标志物。
方法细节:通过系统检索并分析领域内关于AD代谢组学、氧化应激的相关研究文献,按脂质、葡萄糖、嘌呤、色氨酸、维生素、金属离子六大代谢通路分类梳理,整合各通路中氧化还原信号调控的关键证据。
结果解读:该部分解析了各代谢通路中氧化还原信号的异常变化,例如脂质代谢中ROS介导的多不饱和脂肪酸过氧化损伤,葡萄糖代谢中ROS对糖酵解及三羧酸循环的干扰,嘌呤代谢中氧化还原信号对嘌呤代谢物生成的调控,色氨酸代谢中氧化应激对犬尿氨酸通路的激活,维生素代谢中氧化还原信号对维生素抗氧化功能的影响,金属离子代谢中金属离子失衡诱导的ROS过度生成。其中,Fig1展示了AD中与氧化应激相关的主要代谢通路,直观呈现了各通路的关联及潜在干预靶点。
产品关联:文献未提及具体实验产品,领域常规使用代谢组学检测平台(如液相色谱-质谱联用仪)、氧化应激检测试剂盒(如ROS荧光探针)、分子生物学实验试剂(如实时荧光定量PCR试剂盒、蛋白免疫印迹抗体)等。
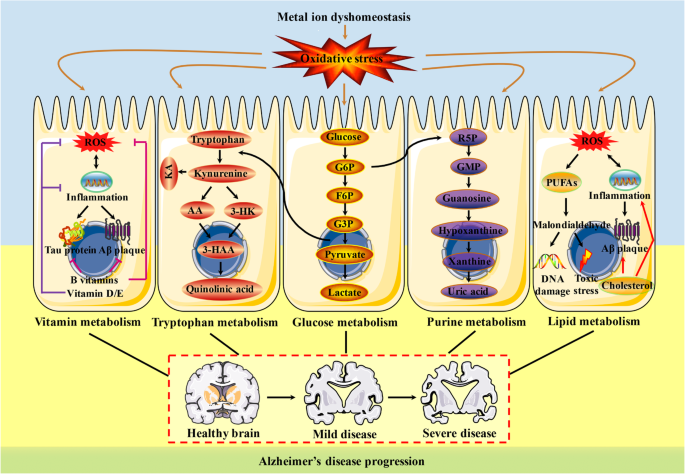
3.2 氧化还原信号相关机制与交叉对话解析
实验目的:解析AD中氧化还原信号相关的核心调控机制及通路间的交叉对话。
方法细节:系统梳理领域内关于AD氧化还原信号通路的研究,重点分析烟酰胺腺嘌呤二核苷酸磷酸氧化酶(NOX)、转化生长因子-β(TGF-β)、核因子-κB(NF-κB)、核因子红系2相关因子2(Nrf2)等关键分子的调控作用,整合各通路的交叉对话证据。
结果解读:该部分明确了NOX是Aβ诱导ROS生成的主要来源,TGF-β通过Smad/ROS通路促进NOX4介导的ROS生成,同时通过TGF-β/Smad/NOX4/ERK1/2/tau通路诱导tau过度磷酸化;NF-κB通过激活炎症反应加重AD病理,而Nrf2通过促进抗氧化反应抑制NF-κB激活,发挥神经保护作用。Fig2展示了AD中氧化还原信号相关的主要机制及交叉对话,直观呈现了各分子的调控网络及维生素D类似物maxacalcitol的干预靶点。
产品关联:文献未提及具体实验产品,领域常规使用细胞培养模型(如AD转基因细胞系)、动物模型(如APP×PS1转基因小鼠)、分子生物学检测试剂(如免疫组化(IHC)抗体、流式细胞术试剂盒)等。
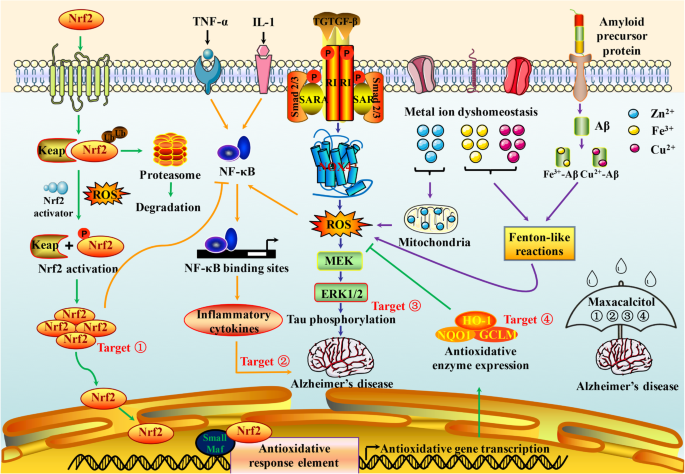
3.3 天然产物治疗潜力与并发症干预总结
实验目的:总结基于氧化还原信号的AD天然产物治疗策略,以及AD干预对并发症的影响。
方法细节:系统梳理领域内关于天然产物治疗AD的研究,重点分析姜黄素、槲皮素、白藜芦醇、阿魏酸、石杉碱甲五种天然产物的作用机制,同时整合AD与心力衰竭、慢性肾脏病等并发症的关联研究。
结果解读:该部分证实了五种天然产物可通过抑制Aβ生成与聚集、抑制tau过度磷酸化、减轻氧化应激与炎症反应发挥AD治疗潜力,但姜黄素、白藜芦醇等在临床试验中未取得理想效果,推测可能与生物利用度低或试验设计有关;同时明确了AD与心力衰竭、慢性肾脏病共享炎症与氧化应激等风险因素,AD干预可改善这些并发症的预后。
产品关联:文献未提及具体实验产品,领域常规使用天然产物提取纯化平台、临床疗效评估量表(如简易精神状态检查量表MMSE)等。
4. Biomarker研究及发现成果
该综述中涉及的Biomarker涵盖代谢物类、蛋白类两大类型,筛选与验证逻辑基于临床样本队列分析、动物模型实验及细胞功能验证的多维度证据,为AD的早期诊断与治疗监测提供了候选靶点。
Biomarker的来源包括血浆、脑脊液、脑组织及视网膜样本,验证方法涵盖代谢组学检测、酶联免疫吸附试验(ELISA)、实时荧光定量PCR、免疫组化等。其中,脂质代谢领域的10种血浆代谢物(包括7种磷脂酰胆碱、2种酰基肉碱、1种溶血磷脂酰胆碱)可在2-3年内预测老年人群向AD的转化,准确率超90%;葡萄糖代谢领域的CSF乳酸水平在轻度AD患者中显著高于中重度患者(文献未明确提供样本量与P值,基于图表趋势推测);嘌呤代谢领域的鸟苷在AD早期额叶皮层显著降低,晚期顶叶皮层显著升高;色氨酸代谢领域的犬尿氨酸通路代谢物(如喹啉酸、犬尿喹啉酸)在AD患者CSF中呈现异常变化;维生素代谢领域的血浆25-羟维生素D水平在AD患者中显著降低,补充维生素D可改善AD认知功能(n=未明确,P<0.05),血浆同型半胱氨酸水平升高是AD的独立风险因素,B族维生素补充可减轻AD样病理;金属离子代谢领域的脑内锌、铁、铜离子水平显著升高。核心成果方面,这些Biomarker的功能关联包括作为AD早期诊断指标、预后预测因子及治疗靶点,例如血浆代谢物面板为AD早期诊断提供了非侵入性工具,视网膜的AD样病理为AD早期检测提供了可视化窗口;创新性在于首次系统整合了多代谢通路的Biomarker,同时明确了AD干预对并发症的潜在益处。部分Biomarker的统计学结果明确,如维生素D补充试验中认知功能改善具有统计学显著性,而部分Biomarker的样本量与P值未在文献中明确说明。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。