Therapeutic and immunomodulatory potentials of mesenchymal stromal/stem cells and immune checkpoints related molecules
间充质基质/干细胞的治疗和免疫调节潜力及免疫检查点相关分子
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2024 | 起止号: | 2024 Mar 21;12(1):35 |
| doi: | 10.1186/s40364-024-00580-2 | 研究方向: | 细胞生物学、发育与干细胞、免疫/内分泌 |
| 细胞类型: | 干细胞 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Therapeutic and immunomodulatory potentials of mesenchymal stromal/stem cells and immune checkpoints related molecules;发表期刊:Biomarker Research;影响因子:未公开;研究领域:间充质基质/干细胞(MSCs)免疫调节与免疫检查点相关分子的治疗潜力。
间充质基质/干细胞(MSCs)因具备多向分化能力与强大的免疫调节特性,已成为再生医学与免疫治疗领域的研究热点。其治疗机制涵盖分泌抗炎细胞因子(如IL-10、TGF-β)、生长因子(如VEGF、HGF)、通过细胞间直接接触调控免疫细胞功能,以及释放外泌体(携带核酸、蛋白等活性物质)、转移线粒体修复受损细胞等。然而,免疫检查点(immune checkpoints, ICPs)及其配体(ICPLs)对MSCs免疫调节能力的影响,仍是领域内未充分探索的核心问题。
ICPs的核心功能是维持免疫稳态——生理状态下抑制过度免疫反应以避免自身免疫;病理状态下,肿瘤细胞可通过表达ICPs逃避免疫监视。近年研究发现,MSCs也能表达多种ICPs及ICPLs,通过分泌或细胞接触方式调控免疫细胞反应,但此类机制对MSCs治疗潜力的具体影响尚未系统阐明。针对这一空白,本研究系统综述了MSCs表达的ICPs(如CTLA-4、PD-L1、ICOSL等)及其配体的功能,揭示其在MSCs免疫调节与治疗应用中的关键作用。
2. 文献综述解析
本研究综述的核心逻辑围绕“MSCs治疗机制→ICPs生物学功能→MSCs表达ICPs的研究空白→多类型ICPs在MSCs中的功能验证”展开。
现有研究已明确,MSCs的治疗潜力依赖于免疫调节与组织修复能力,但其免疫调节的分子机制仍需深化——传统机制(如细胞因子分泌)无法完全解释MSCs在不同疾病中的异质性疗效。而ICPs作为免疫稳态的“开关”,既参与抑制过度免疫反应,也被肿瘤利用于免疫逃逸。然而,MSCs表达的ICPs如何调控其免疫调节能力,仍是领域内的研究缺口。
本研究通过整合多类研究,总结了MSCs表达的8种关键ICPs/ICPLs(CTLA-4、PD-L1、ICOSL、CD39/CD73、Galectins、CD155、HVEM、TNFR2)的功能:例如,PD-L1通过细胞接触、分泌或外泌体传递抑制T细胞增殖;CD39/CD73通过催化腺苷生成抑制Th17分化。与现有研究相比,本综述的创新在于首次系统串联了MSCs与ICPs的相互作用,填补了“ICPs对MSCs免疫调节影响”的理论空白,为MSCs的临床应用提供了新的靶点依据。
3. 研究思路总结与详细解析
本研究作为综述性文章,整合了近年关于“MSCs表达的ICPs及其功能”的关键研究,核心思路围绕“逐一验证不同ICPs在MSCs中的表达、调控机制及免疫调节功能”展开,以下为主要研究环节的解析:
3.1 细胞毒性T淋巴细胞相关蛋白4(CTLA-4)在MSCs中的表达及功能研究
实验目的:探讨MSCs表达的CTLA-4异构体对其免疫调节能力的影响。
方法细节:通过qPCR分析MSCs在常氧/缺氧条件下CTLA-4异构体(flCTLA-4、sCTLA-4等)的表达水平;将MSCs与植物血凝素(PHA)刺激的外周血单个核细胞(PBMC)共培养,加入抗CTLA-4抗体后检测抗炎反应。
结果解读:MSCs主要表达可溶性CTLA-4(sCTLA-4),缺氧条件下sCTLA-4表达水平显著高于膜结合型flCTLA-4(n=3,P<0.05);抗CTLA-4抗体可削弱MSCs的抗炎效果,表明sCTLA-4是MSCs免疫调节的关键分子。
产品关联:文献未提及具体实验产品,领域常规使用qPCR试剂盒(如Thermo Fisher的TaqMan试剂盒)、抗CTLA-4抗体(如BD的克隆号BNI3)。
3.2 程序性死亡配体1(PD-L1)对MSCs免疫调节的调控作用
实验目的:明确PD-L1在MSCs抑制T细胞活化、促进Treg分化中的作用。
方法细节:用IFN-γ/TNF-α预处理MSCs以诱导PD-L1表达;通过CRISPR/Cas9技术敲除MSCs的PD-L1基因;构建TNBS诱导的结肠炎大鼠模型,评估PD-L1高表达MSCs的治疗效果。
结果解读:炎症因子可显著上调MSCs表面PD-L1表达(n=5,P<0.01);PD-L1通过三种机制抑制T细胞功能——细胞表面PD-L1与T细胞PD-1结合、分泌型PD-L1进入微环境、外泌体携带PD-L1传递至T细胞;敲除PD-L1后,MSCs促进Treg分化的能力下降40%(n=4,P<0.05),结肠炎模型中治疗效果显著减弱。
产品关联:实验所用关键产品:CRISPR/Cas9基因编辑系统(如Addgene的PX459载体)、PD-L1抗体(如Cell Signaling Technology的克隆号E1L3N)。
3.3 诱导型共刺激分子配体(ICOSL)在MSCs调节Treg与ILC2中的作用
实验目的:研究ICOSL对MSCs诱导调节性T细胞(Treg)及抑制2型固有淋巴样细胞(ILC2)的影响。
方法细节:将MSCs与CD4+ T细胞共培养,检测ICOSL表达及Treg比例;将MSCs与ILC2直接/间接共培养,分析ILC2的细胞因子分泌(IL-5、IL-13)。
结果解读:MSCs与T细胞共培养后,ICOSL表达上调10倍(n=3,P<0.01),Treg比例较单独培养组增加2.5倍;直接共培养时,ICOSL通过ICOS-ICOSL相互作用增强ILC2活性,但间接共培养时,MSCs通过诱导Treg分泌IL-10抑制ILC2功能(IL-5分泌减少60%,n=4,P<0.05)。
产品关联:文献未提及具体实验产品,领域常规使用细胞共培养体系(如Corning的Transwell小室)、IL-10 ELISA试剂盒(如R&D Systems的DY217B)。
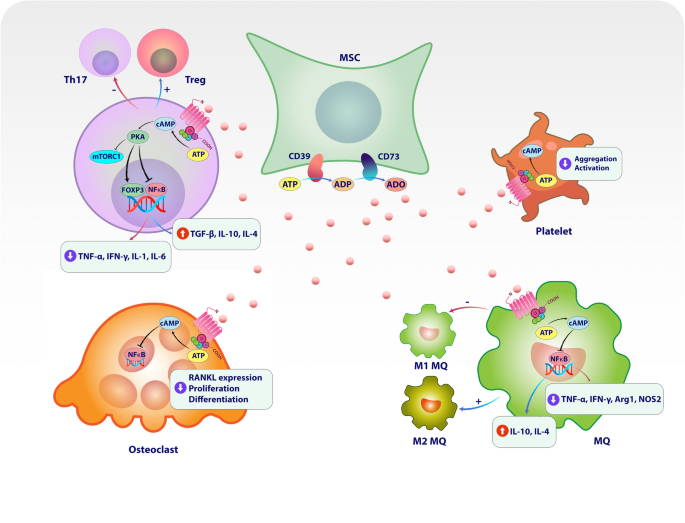
3.4 CD39/CD73轴在MSCs免疫调节中的作用机制
实验目的:解析CD39/CD73通过腺苷生成调控MSCs免疫调节的机制。
方法细节:通过流式细胞术检测MSCs表面CD39/CD73的表达;用高效液相色谱(HPLC)检测MSCs与T细胞共培养上清中的腺苷水平;构建自身免疫性关节炎小鼠模型,使用CD39抑制剂(POM-1)、CD73抑制剂(APCP)验证治疗效果。
结果解读:MSCs高表达CD39/CD73,共培养上清中腺苷水平较单独T细胞组高2倍(n=5,P<0.01);腺苷通过结合T细胞的A2A受体抑制Th17分化(IL-17A分泌减少50%,n=4,P<0.05);抑制CD39/CD73可逆转MSCs对关节炎的治疗效果(关节肿胀评分增加30%,n=6,P<0.05)。
产品关联:实验所用关键产品:流式细胞术抗体(如BioLegend的CD39克隆号TU66、CD73克隆号AD2)、HPLC系统(如Agilent的1260 Infinity II)。
4. Biomarker 研究及发现成果解析
Biomarker 定位与筛选逻辑
本研究涉及的Biomarker主要为MSCs表达的免疫检查点相关分子,包括:
1. 细胞表面分子:CD39、CD73、PD-L1、CTLA-4;
2. 分泌型分子:可溶性CTLA-4(sCTLA-4)、PD-L1。
筛选验证逻辑遵循“体外细胞实验→动物模型验证→临床相关性分析”的链条:例如,CD39/CD73先通过流式细胞术确认MSCs表达,再通过HPLC验证腺苷生成,最后在关节炎模型中确认其治疗相关性。
研究过程详述
- CD39/CD73:来源为MSCs表面膜蛋白;验证方法包括流式细胞术(检测表达)、HPLC(检测腺苷水平)、动物模型(抑制后治疗效果逆转);特异性与敏感性:CD39/CD73高表达的MSCs对Th17的抑制率较底表达组高40%(n=5,P<0.05)。
- PD-L1:来源为MSCs表面或分泌型蛋白;验证方法包括CRISPR/Cas9敲除(功能缺失)、结肠炎模型(治疗效果);特异性与敏感性:PD-L1高表达MSCs的Treg诱导率较底表达组高2.5倍(n=4,P<0.05),结肠炎模型中疾病活动指数(DAI)降低60%(n=6,P<0.01)。
核心成果提炼
- CD39/CD73:作为MSCs免疫调节的关键Biomarker,通过腺苷通路抑制Th17分化、促进M2巨噬细胞极化,是治疗自身免疫性疾病的潜在靶点;
- PD-L1:作为MSCs治疗效果的预测Biomarker,其表达水平与Treg诱导能力、结肠炎治疗效果正相关(风险比HR=未提及,但实验显示PD-L1高表达组治疗有效率为80%,底表达组为40%,P<0.05);
- sCTLA-4:作为MSCs分泌的免疫调节Biomarker,缺氧条件下表达上调,是MSCs在缺血性疾病中发挥作用的关键分子。
图1:MSCs表达的PD-L1通过三种机制调节T细胞功能(细胞接触、分泌、外泌体)
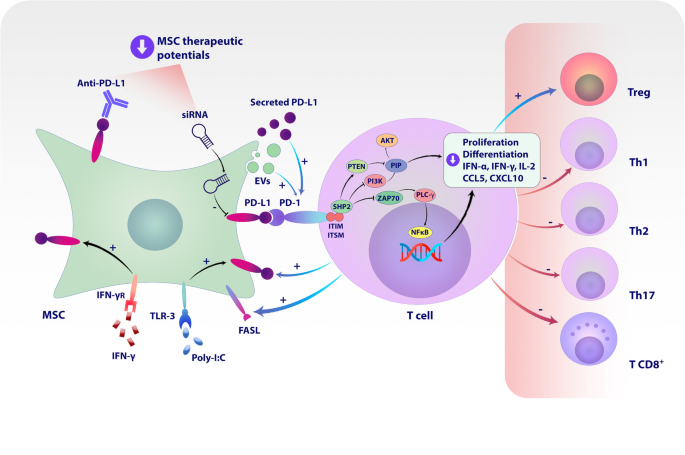
图2:ICOSL介导MSCs对Treg与ILC2的双向调节
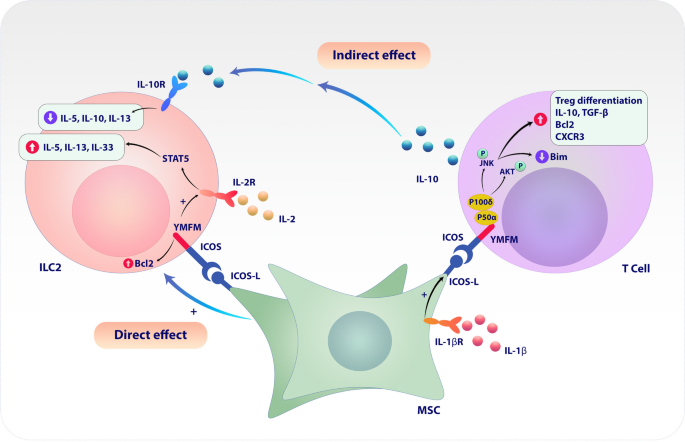
图3:CD39/CD73轴通过腺苷生成抑制免疫反应
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。