Primary porcine proximal tubular cells as an alternative to human primary renal cells in vitro: an initial characterization
体外培养中,猪原代近端肾小管细胞作为人原代肾细胞的替代品:初步表征
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2013 | 起止号: | 2013 Dec 5;14:55 |
| doi: | 10.1186/1471-2121-14-55 | 研究方向: | 细胞生物学 |
文献解析
1. 领域背景与文献引入
文献英文标题:Primary porcine proximal tubular cells as an alternative to human primary renal cells in vitro: an initial characterization;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:肾脏毒理学体外模型构建与验证
肾脏毒理学研究中,传统啮齿类动物模型和细胞模型因与人类生理差异显著,存在毒性机制外推的局限性,例如啮齿类特有的α2u-球蛋白肾病、钠-葡萄糖协同转运蛋白抑制剂介导的肾脏癌变等物种特异性毒性机制,无法准确反映人类肾脏对毒物的响应规律。人类原代肾细胞是体外毒理学研究的理想模型,能精准模拟人类肾脏生理功能,但存在获取难度大、样本量有限的问题,限制了其大规模应用。猪的肾脏在解剖学和生理学上与人类高度相似,且猪原代肾细胞易获取、成本低,成为潜在的替代模型,但此前缺乏系统的转运体表达与功能验证数据,无法明确其是否能可靠替代人类原代肾细胞用于体外毒理学研究,本研究正是针对这一空白开展系统表征。
2. 文献综述解析
作者按模型类型分类评述现有肾脏毒理学体外模型研究,涵盖啮齿类动物/细胞模型、人类原代肾细胞模型、猪肾细胞模型三大类。现有研究中,啮齿类模型的优势是操作简便、成本低廉,可快速开展大规模毒性筛选,但存在物种特异性毒性机制,外推至人类的准确性较差;人类原代肾细胞模型能准确反映人类肾脏的生理功能与毒物响应,但获取难度大、样本量有限,难以满足大规模实验需求;猪肾细胞模型虽具备解剖生理相似性的潜力,但此前仅开展了初步形态学研究,缺乏转运体表达与功能的系统验证,无法明确其作为替代模型的可靠性。本研究的创新点在于首次系统表征了猪原代近端肾小管细胞的转运体表达谱、功能活性及培养过程中的稳定性,填补了猪肾细胞模型转运体功能验证的空白,为其替代人类原代肾细胞提供了关键实验依据,解决了现有模型“潜力明确但数据不足”的核心问题。
3. 研究思路总结与详细解析
本研究的整体目标是系统表征猪原代近端肾小管细胞(PKC)的形态、生长特性、转运体表达与功能,验证其作为人类原代肾细胞替代模型的可行性;核心科学问题是PKC是否具有与人类肾细胞相似的转运体表达谱与功能,能否在体外稳定维持这些特性;技术路线遵循“细胞分离培养→基础特性分析→转运体表达检测→功能验证→稳定性评估→结论”的闭环逻辑,确保研究结果的系统性与可靠性。
3.1 猪原代近端肾小管细胞分离培养与基础特性表征
实验目的是获取高纯度的猪原代近端肾小管细胞,并验证其形态与生长特性,明确体外培养的基本规律。方法细节为从新鲜屠宰的德国杂交猪肾脏皮质中,采用胶原酶消化法分离细胞,使用含DMEM-D-Val的培养基抑制成纤维细胞生长,通过台盼蓝排斥实验筛选活力≥90%的细胞,通过γ-谷氨酰转移酶和己糖激酶活性鉴定细胞来源(近端肾小管细胞占比>85%);采用Z1颗粒计数器每日计数细胞,绘制生长曲线并分析生长参数。结果解读显示,PKC培养后形成典型上皮细胞单层,出现穹顶结构,提示具有上皮细胞极性(

);生长曲线显示滞后期约50小时,汇合时最大细胞密度约1×10^5个细胞/cm²,细胞倍增时间约29小时(n=3,P>0.05),0-3代细胞生长特性无显著差异,但3代细胞中出现衰老迹象(细胞体增大、细胞骨架改变)(
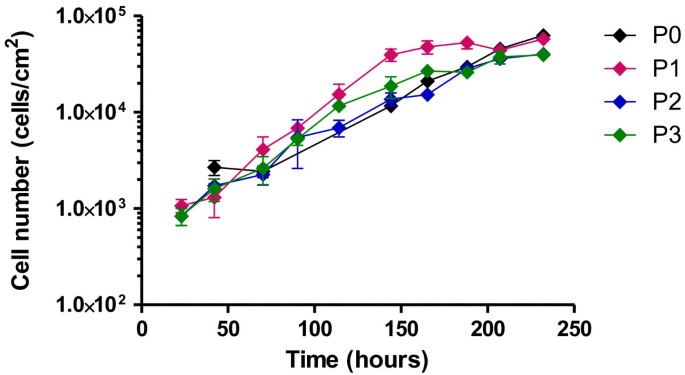
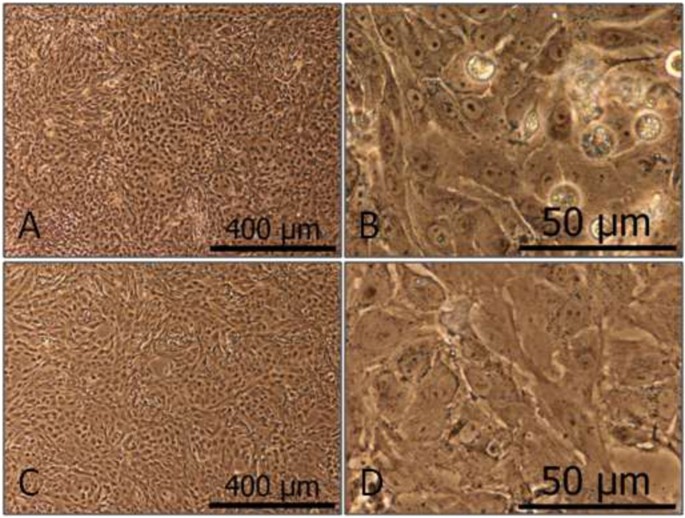
)。实验所用关键产品:胶原酶(Type I from Clostridium histolyticum)、DMEM-D-Val培养基(PAA,cat# E15-055)、FBS gold(PAA,cat# A15-649)、Z1颗粒计数器(Beckman Coulter)等。
3.2 转运体mRNA与蛋白表达谱检测
实验目的是检测PKC中关键转运体的mRNA与蛋白表达谱,明确其表达特征,为功能验证提供基础。方法细节为采用Trizol法提取细胞与组织总RNA,通过逆转录-聚合酶链反应(RT-PCR)检测pMdr1、pMrp1、pMrp2、pOatp1a2、pOat1、pOat3的mRNA表达,以猪甘油醛-3-磷酸脱氢酶(GAPDH)为内参;通过差速离心法富集细胞膜蛋白,采用十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)结合免疫印迹(Western Blotting)法,使用兔抗大鼠有机阴离子转运体1/3(Oat1/Oat3)多克隆抗体、兔抗人多药耐药相关蛋白1/2(MRP1/MRP2)多克隆抗体检测蛋白表达。结果解读显示,RT-PCR结果表明PKC中可检测到pMrp1、pMrp2、pOat1、pOat3的mRNA表达,未检测到pMdr1和pOatp1a2的mRNA(
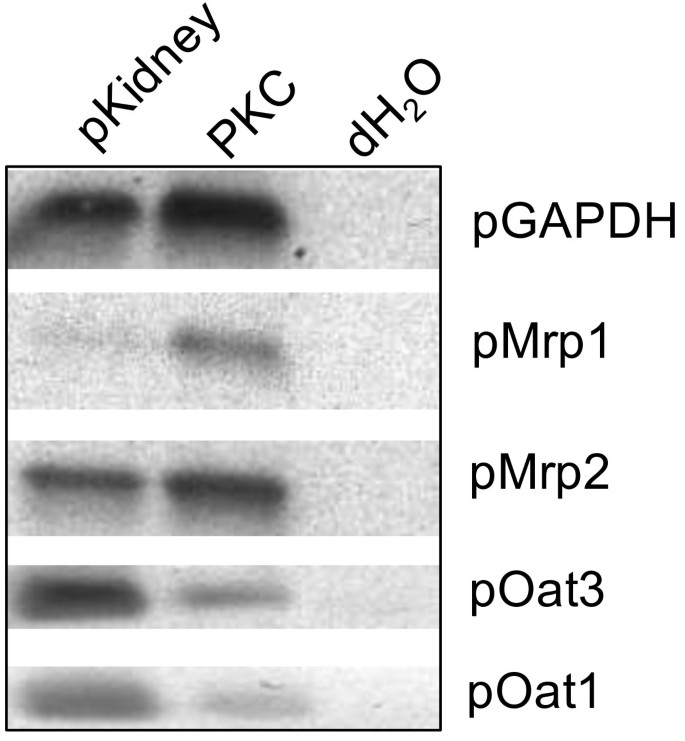
);免疫印迹结果显示PKC中可检测到Oat1蛋白(约75kDa、45kDa、40kDa条带),Oat3蛋白仅在0-1代细胞中低表达,未检测到MRP蛋白(
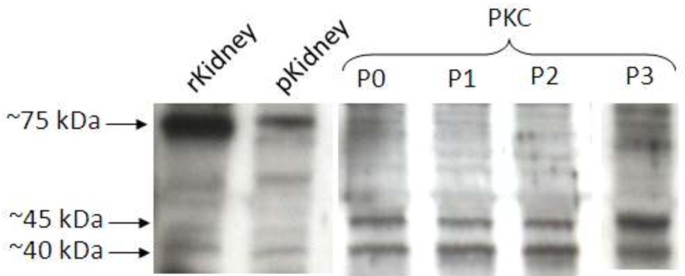
)。实验所用关键产品:Trizol试剂(Invitrogen)、兔抗大鼠Oat1/Oat3多克隆抗体(Alpha Diagnostics)、兔抗人MRP1/MRP2多克隆抗体(Abcam)、ECL Plus化学发光试剂盒(GE Healthcare)等。
3.3 转运体功能验证与动力学分析
实验目的是验证PKC中有机阴离子转运体的功能活性,明确其转运动力学特征,对比与人类肾细胞的相似性。方法细节为将PKC接种于聚对苯二甲酸乙二醇酯(PET)滤膜插入式培养板,形成紧密单层后,采用放射性标记的对氨基马尿酸([¹⁴C]PAH)作为模型底物,检测基底外侧膜(BLM)和刷状缘膜(BBM)的转运功能;通过时间-course实验和浓度依赖实验分析转运动力学,通过抑制剂实验验证转运体的特异性。结果解读显示,PAH在PKC的BLM和BBM均存在饱和性转运,BBM的转运容量约为BLM的3倍,米氏常数(Kₘ)值分别为58.8±12.6μM(BBM)和187.2±70.2μM(BLM)(n=3,P<0.05),转运在5-10分钟达到饱和(
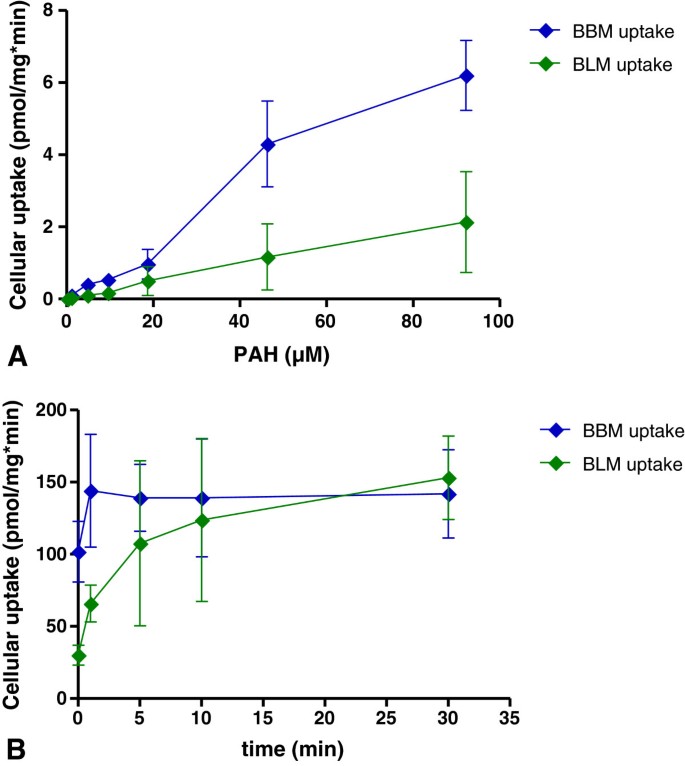
);抑制剂实验显示,甲氨蝶呤(MTX)、赭曲霉毒素A(OTA)等可抑制BBM的PAH转运(最高抑制率30%),西咪替丁(CIM)、叶酸(FA)等可抑制BLM的PAH转运(
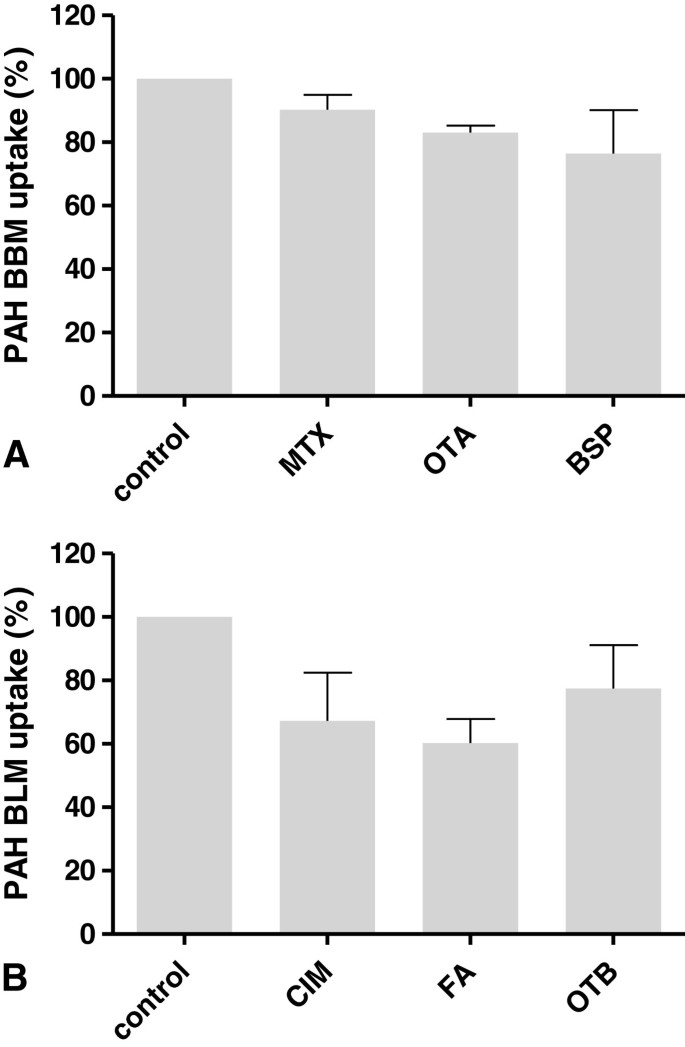
),表明PKC的有机阴离子转运体具有功能活性,且与人类肾细胞的转运特征相似。实验所用关键产品:[¹⁴C]PAH(Perkin Elmer)、Beckman LS 6500闪烁计数器等。
3.4 转运体表达稳定性与诱导实验
实验目的是检测PKC在培养过程中转运体表达的稳定性,验证激素与底物对转运体表达的诱导作用,明确模型的适用范围。方法细节为检测不同汇合度、不同培养时间及不同传代次数的PKC中Oat1和Oat3的mRNA与蛋白表达;采用50nM或1μM的溴磺酞(BSP)、PAH、牛磺胆酸(TCA)、三碘甲状腺原氨酸(T3)等处理细胞48小时,检测转运体mRNA表达变化;采用MTT实验验证诱导剂的细胞毒性。结果解读显示,Oat1和Oat3的mRNA表达随细胞密度降低、培养时间延长而下降,1代及以后细胞中未检测到其mRNA表达;Oat1蛋白可稳定表达至3代,Oat3蛋白仅表达至1代(
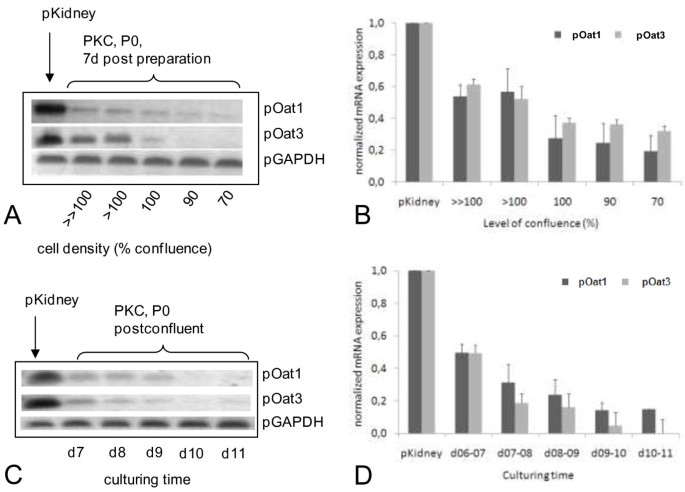
);所有测试的诱导剂均未显著上调转运体mRNA表达(n=3,P>0.05),且诱导剂在96小时内无细胞毒性(
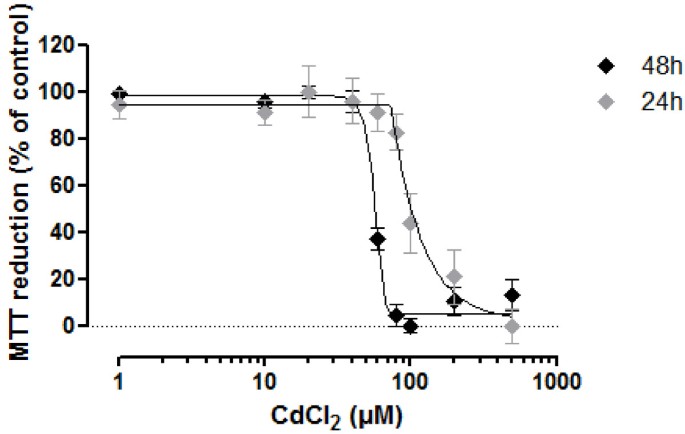
)。实验所用关键产品:MTT试剂、Infinite M200酶标仪(Tecan)等。
4. Biomarker研究及发现成果
本研究以有机阴离子转运体Oat1、Oat3为核心功能生物标志物,验证PKC作为肾脏毒理学模型的可靠性,筛选与验证逻辑为“细胞分离培养→mRNA/蛋白表达检测→功能验证→稳定性分析”的完整链条,确保标志物的有效性与可靠性。
Biomarker的研究过程详述:标志物来源为猪原代近端肾小管细胞,采用RT-PCR、免疫印迹法验证表达特征,采用放射性底物转运实验验证功能活性;特异性方面,PKC中Oat1的转运动力学与人类有机阴离子转运体1(OAT1)相似,Kₘ值接近人类原代肾细胞的特征;敏感性方面,PAH转运实验可检测到抑制剂的特异性抑制作用,验证了转运体的功能活性。
核心成果提炼:首次明确PKC中Oat1、Oat3的表达与功能特征,Oat1可在体外稳定表达至3代,具有与人类肾细胞相似的有机阴离子转运功能,表明PKC可作为人类原代肾细胞的替代模型,用于肾脏毒理学体外研究;研究还发现PKC的转运体表达随培养时间延长而下降,提示其在体外培养的早期代次(0-2代)应用更可靠,相关数据为模型的标准化应用提供了关键依据;此外,研究未检测到pMdr1和pOatp1a2的表达,为模型的适用范围(如特定毒物的筛选)提供了参考,避免了模型的误用。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。