Quantitative digital in situ senescence-associated β-galactosidase assay
定量数字原位衰老相关β-半乳糖苷酶检测
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2011 | 起止号: | 2011 Apr 15;12:16 |
| doi: | 10.1186/1471-2121-12-16 | 疾病类型: | 衰老 |
文献解析
1. 领域背景与文献引入
文献英文标题:Quantitative digital in situ senescence-associated β-galactosidase assay;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞衰老生物标志物检测
细胞衰老作为体细胞丧失复制能力的过程,在机体衰老、肿瘤抑制及应激反应中发挥关键作用,是当前生命科学领域的研究热点之一。1995年Dimri等首次发现衰老相关β-半乳糖苷酶(SABG)可作为细胞衰老的标志物,因其检测方法简便且能在异质细胞群体中原位识别衰老细胞,成为应用最广泛的细胞衰老检测工具。然而,传统SABG检测方法存在半定量、主观性强的固有缺陷,依赖实验人员主观判断染色阳性与否,无法精准量化染色强度的细微差异,导致结果重现性差,尤其在体内组织样本检测中易出现结论不一致的问题。同时,现有已报道的SABG定量方法多基于细胞群体水平的生化检测,无法实现原位单细胞水平的精准定量,限制了细胞衰老在体内组织异质环境中的研究。针对这一领域空白,本研究旨在开发一种可重复、敏感性高的原位定量SABG检测方法,解决传统方法的局限性,为体内细胞衰老的精准研究提供可靠工具。
2. 文献综述解析
作者从SABG检测方法的发展历程与细胞衰老研究的技术需求两个维度,对领域内现有研究进行了系统评述。现有研究已证实SABG是细胞衰老的核心标志物,其活性升高源于溶酶体β-半乳糖苷酶(GLB1基因产物)的表达上调,但该标志物的特异性存在争议,部分研究发现其在静息细胞、汇合培养的成纤维细胞中也可检测到活性。传统原位SABG检测方法的优势在于操作简便,能够在异质细胞群体中原位定位衰老细胞,但半定量的本质导致其无法捕捉不同应激源诱导的细胞衰老的细微差异,且实验人员的主观判断会严重影响结果的重现性。已有的定量SABG检测方法如荧光法、化学发光法及流式细胞术法,虽能实现定量分析,但仅能反映细胞群体的平均水平,无法在组织样本中原位分析单细胞的衰老状态,难以满足体内细胞衰老异质性研究的需求。
本研究的创新价值在于首次将数字图像分析技术与传统原位SABG检测方法结合,建立了单细胞水平的原位定量分析体系,同时通过优化检测pH条件,拓宽了检测的动态范围,既保留了传统方法原位检测的优势,又解决了定量分析的主观性与重现性问题,填补了原位单细胞定量检测细胞衰老的技术空白。
3. 研究思路总结与详细解析
本研究的核心目标是开发并验证一种可重复的原位定量SABG检测方法,核心科学问题是如何实现传统SABG检测的精准定量与原位单细胞分析,技术路线遵循“方法开发→体外多模型验证→体内组织验证→结论优化”的闭环逻辑。
3.1 数字图像分析定量方法的开发与优化
实验目的是建立客观、可重复的原位SABG染色定量分析体系,解决传统方法的主观性问题。方法细节上,研究团队采用经典的原位SABG染色protocol,以X-Gal为底物进行染色后,使用Matlab开发的图像分析工具,手动标记细胞胞质区域及相邻背景区域,计算细胞染色强度(CSI)与背景染色强度(BSI)的比值,经对数转换得到β-半乳糖苷酶活性值(BGAV);同时对染色后8小时至2个月的样本进行动态检测,确定BGAV的稳定时间窗口。
结果显示,BGAV的正态分布拟合度优于直接计算的CSI/BSI比值,因此采用Kolmogorov-Smirnov非参数检验进行统计分析;染色后40小时BGAV进入平台期并可稳定维持2个月,研究团队选择该时间点进行所有后续检测,以确保结果的可靠性。
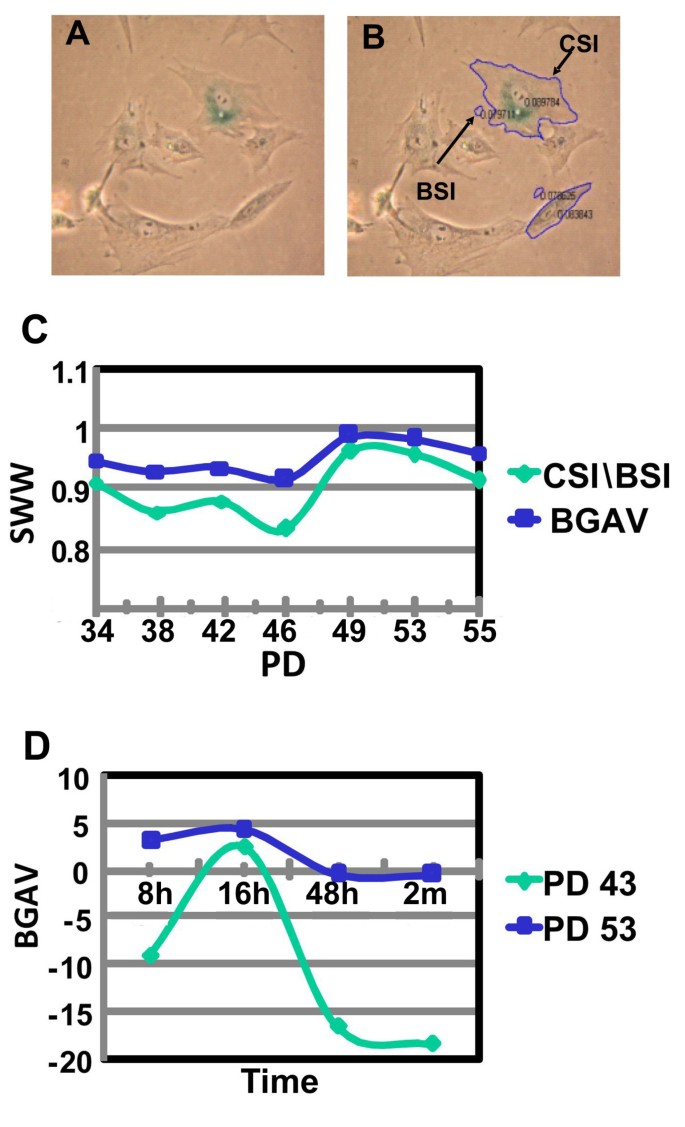
产品关联:文献未提及具体实验产品,领域常规使用X-Gal染色试剂、Matlab图像分析软件、倒置显微镜等。
3.2 体外细胞衰老模型的方法验证
实验目的是验证该定量方法可有效检测不同类型的细胞衰老。方法细节分为两部分:一是复制性衰老验证,培养人包皮成纤维细胞(FSE)和BJ细胞,在不同群体倍增数(PD)时进行SABG染色与BGAV分析;二是应激诱导早衰验证,将FSE细胞(PD34)暴露于0-50μM浓度的H₂O₂,诱导急性应激早衰后检测BGAV变化。
结果显示,FSE细胞从PD34到PD58、BJ细胞从PD57到PD65的过程中,BGAV随群体倍增数增加显著升高(FSE细胞PD34的BGAV为-12.2±13.7,PD56为4.3±14.7,P<10⁻⁵),与细胞复制性衰老的进程一致;H₂O₂处理后,BGAV呈现浓度依赖性升高,15μM H₂O₂处理组的BGAV(-3.4±17.8)显著高于对照组(-12.2±13.7,P<10⁻⁵),25μM时达到平台期,证实该方法可检测应激诱导的细胞早衰。
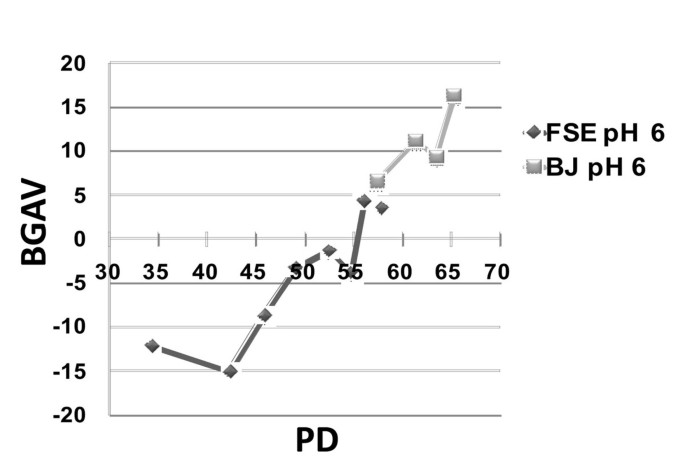
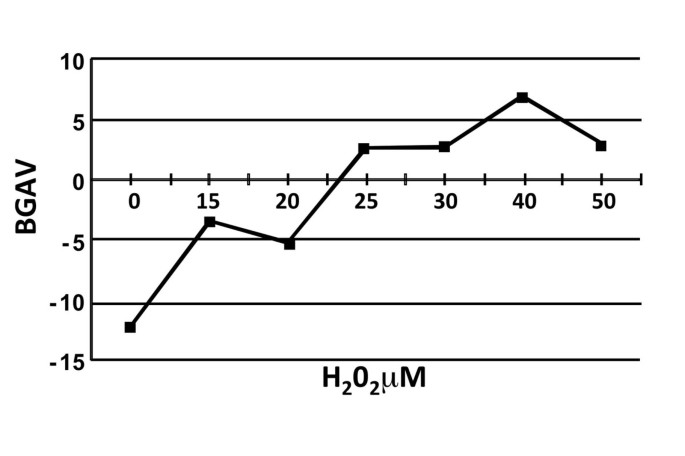
产品关联:文献未提及具体实验产品,领域常规使用细胞培养试剂、H₂O₂试剂等。
3.3 检测pH条件的优化
实验目的是确定不同pH条件对SABG定量检测敏感性与动态范围的影响。方法细节上,在pH4.0与pH6.0条件下,分别对不同PD的FSE细胞及H₂O₂处理的细胞进行SABG染色与BGAV分析,比较两种pH下的检测差异。
结果显示,BGAV与检测pH呈反比关系,pH4.0时的BGAV显著高于pH6.0;在pH4.0条件下,可检测到pH6.0下无法区分的细微差异,如FSE细胞PD34与PD42的BGAV在pH4.0时差异显著(PD34为65.6±45.5,PD42为88.4±60.4,P=0.0001),而pH6.0下无显著差异;H₂O₂处理组在pH4.0下可区分15μM与20μM浓度的差异,pH6.0下则无法区分,证实pH4.0条件下检测敏感性更高,适合捕捉细微的细胞衰老变化。
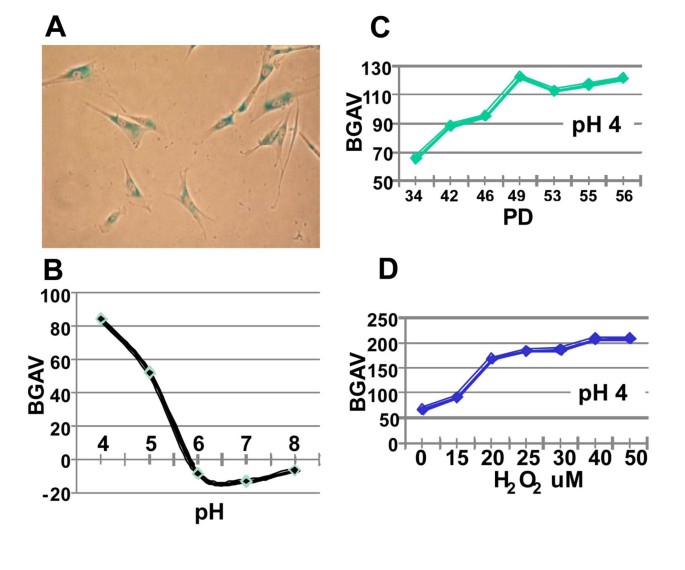
产品关联:文献未提及具体实验产品,领域常规使用柠檬酸-磷酸氢二钠缓冲液调节pH。
3.4 细胞密度对检测结果的影响验证
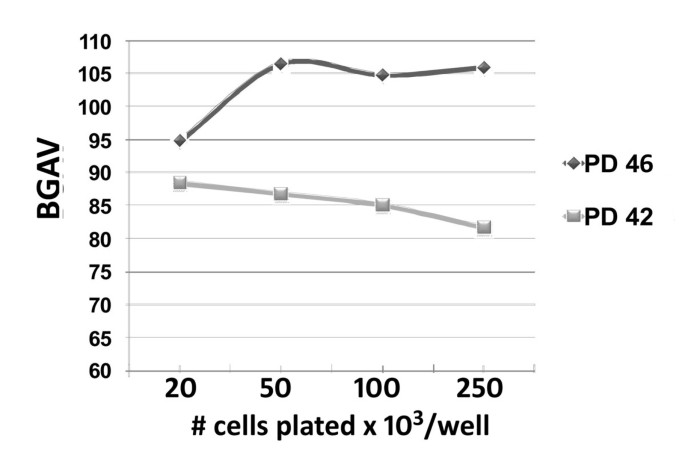
实验目的是排除细胞密度对定量检测结果的干扰,确保方法的可靠性。方法细节上,将不同PD的FSE细胞以2×10⁴至2.5×10⁵个/孔的密度接种于6孔板,培养至最高密度孔汇合后进行SABG染色与BGAV分析,采用ANOVA检验分析不同密度组的差异。
结果显示,不同细胞密度下的BGAV无显著统计学差异(P=0.1),证实该定量方法不受细胞培养密度的影响,进一步保障了结果的重现性。
产品关联:文献未提及具体实验产品,领域常规使用细胞培养板等。
3.5 体内糖尿病小鼠肾脏组织的细胞衰老检测
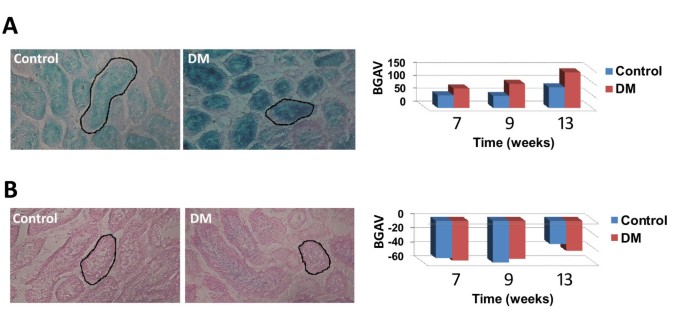
实验目的是验证该定量方法在体内组织样本中的应用价值。方法细节上,建立链脲佐菌素(STZ)诱导的糖尿病小鼠模型,在建模后7、9、13周时取肾脏组织,分别在pH4.0与pH6.0条件下进行原位SABG染色,分析肾小管细胞的BGAV;同时进行γ-H2AX免疫荧光染色,验证衰老细胞的存在。
结果显示,pH6.0下糖尿病组与对照组小鼠肾脏的BGAV无显著差异;而pH4.0下,糖尿病组的BGAV显著高于对照组(7周P<0.004,9周P<0.0009,13周P<10⁻⁸),且两组的BGAV随周龄增加均呈上升趋势;γ-H2AX阳性细胞核比例在糖尿病组显著高于对照组(Pearson卡方=44.9,P=2.1E⁻¹¹),与pH4.0条件下的BGAV相关性系数达0.96,证实该方法可特异性检测体内组织的细胞衰老。
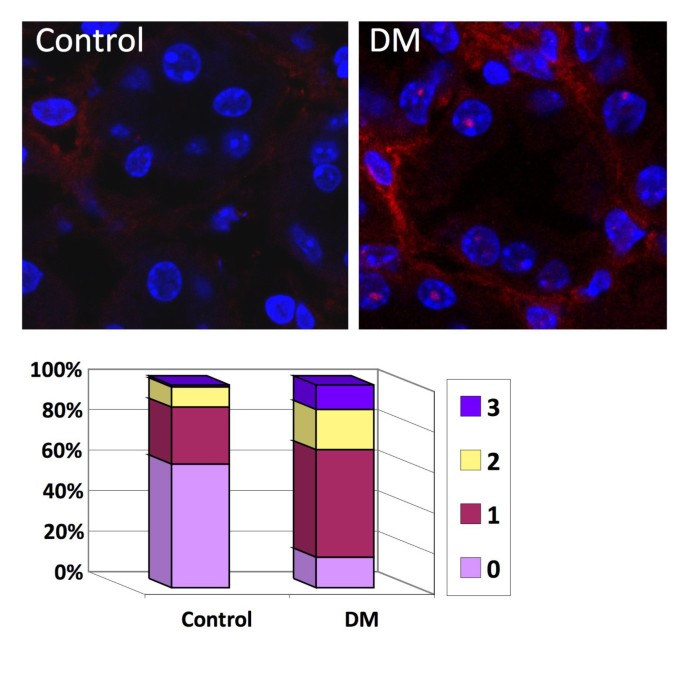
产品关联:实验所用关键产品:抗γ-H2AX抗体(Upstate,货号S139)、Cy3标记的驴抗兔二抗、Vectashield含DAPI封片剂。
4. Biomarker研究及发现成果
Biomarker定位与验证逻辑
本研究的核心Biomarker是衰老相关β-半乳糖苷酶(SABG),其本质为溶酶体β-半乳糖苷酶(GLB1基因产物)。研究团队采用“方法优化→体外多模型验证→体内组织验证→正交标志物确认”的完整逻辑链条,对该Biomarker的定量检测体系进行验证:首先通过数字图像分析技术实现传统SABG检测的定量优化,随后在复制性衰老、应激诱导早衰两种体外模型中验证检测的特异性与敏感性,最后在糖尿病小鼠肾脏组织中进行体内验证,并通过γ-H2AX免疫荧光染色进行正交验证。
研究过程与性能数据
该Biomarker的来源为细胞及组织中的溶酶体,验证方法为原位SABG染色结合数字图像分析,通过计算BGAV实现定量检测。性能数据显示,在pH4.0条件下,该检测体系可捕捉到细胞衰老过程中SABG活性的细微变化,敏感性显著高于传统pH6.0条件下的检测;在体内组织样本中,糖尿病组与对照组的BGAV差异具有显著统计学意义,且与γ-H2AX阳性细胞比例的相关性系数达0.96,证实了检测的特异性。
核心成果与创新价值
本研究的核心成果是建立了可重复的原位单细胞定量SABG检测方法,证实通过调整检测pH可优化检测的动态范围:pH6.0适合检测差异显著的细胞衰老,pH4.0适合捕捉细微的衰老变化。该方法的创新性在于首次实现了原位单细胞水平的SABG定量分析,解决了传统方法主观性强、无法精准量化的缺陷,同时为体内细胞衰老的异质性研究提供了可靠工具。研究结果表明,该Biomarker的定量检测可有效反映体内组织的细胞衰老状态,为糖尿病肾病等衰老相关疾病的研究提供了新的技术手段。所有统计分析均基于至少250个细胞或50个肾小管的样本量,差异结果均标注了具体的P值与置信区间,确保了结论的可靠性。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。