DNA moves sequentially towards the nuclear matrix during DNA replication in vivo
在体内DNA复制过程中,DNA会按顺序向核基质移动。
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2011 | 起止号: | 2011 Jan 19;12:3 |
| doi: | 10.1186/1471-2121-12-3 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:DNA moves sequentially towards the nuclear matrix during DNA replication in vivo;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学(核基质与DNA复制调控)
领域共识:间期细胞核中的DNA以超螺旋环的形式锚定在核基质(NM)上,核基质是经高盐、非离子去垢剂及核酸酶处理后残留的核亚结构,包含数百种相关蛋白,DNA通过基质附着区(MAR)与核基质结合。核基质与DNA复制的关联研究始于20世纪80年代,已有证据表明DNA复制发生在核基质组装的复制工厂中,且结构DNA环的大小与复制子长度高度相关,提示其可能对应体内的复制子单位。当前领域的研究热点集中在DNA复制的分子机制与核基质的动态相互作用,核心未解决问题包括:体内生理状态下DNA复制时,DNA模板是向固定的核基质复制工厂移动,还是复制复合物沿DNA模板移动,缺乏直接的体内同步化细胞模型证据。此外,体外培养细胞存在的人工干扰(如底物弹性、同步化方法 artifacts)限制了对生理状态下DNA复制过程的准确理解。
针对上述研究空白,本研究利用大鼠部分肝切除后肝细胞同步化进入细胞周期的生理模型,追踪特定基因组区域的结构DNA环在S期及恢复G0期过程中相对于核基质的位置变化,旨在明确体内DNA复制时DNA模板的移动规律,为卷绕式复制模型提供直接的体内实验证据。
2. 文献综述解析
作者从核基质的结构与功能、DNA环的组织模式、DNA复制的两种核心模型(追踪模型与卷绕模型)三个维度对现有研究进行系统评述,明确了领域内的共识与争议点。
现有研究的关键结论包括:核基质作为DNA复制的结构支撑,复制工厂稳定结合于核基质;结构DNA环的大小与复制子长度高度相关,提示其可能对应体内复制子单位;DNA复制的卷绕模型认为复制复合物固定于核基质,DNA模板向其移动,而追踪模型则认为复制复合物沿DNA模板移动。现有研究的技术方法优势在于,通过体外细胞系与核质体(nucleoid)模型初步揭示了DNA与核基质的相互作用,但局限性也较为明显:体外培养细胞存在生理状态偏离的人工干扰,同步化处理可能导致细胞损伤;多数研究仅停留在静态观察,缺乏对体内动态复制过程的追踪;针对DNA环移动规律的直接证据不足,尤其是在生理同步化的细胞群体中。
本研究的创新价值在于,首次利用体内生理同步化的大鼠肝细胞模型(肝再生),排除体外培养的人工干扰,直接追踪特定DNA区域的环结构在复制过程中的位置变化;通过多区域序列与无关基因的验证,证明DNA向核基质的顺序移动是普遍现象,为卷绕式复制模型提供了体内直接证据,同时进一步支持结构DNA环作为体内复制子的假说,弥补了领域内动态追踪研究的空白。
3. 研究思路总结与详细解析
本研究的整体目标是明确体内DNA复制过程中结构DNA环相对于核基质的移动规律,核心科学问题是DNA模板是否向核基质上的固定复制工厂移动,技术路线遵循“生理同步化细胞模型建立→核质体制备与消化动力学分析→特定序列位置追踪→普遍性验证”的闭环逻辑,通过多阶段实验逐步验证卷绕式复制模型。
3.1 大鼠肝再生模型与肝细胞分离
实验目的是获取生理状态下同步化的G0期、S期及恢复期G0期肝细胞,为后续实验提供无人工干扰的细胞样本。方法细节为选用200-250g雄性Wistar大鼠,按照墨西哥实验室动物规范进行饲养,实施70%肝切除手术,分别在术后24h(DNA合成峰值期)、7d(肝再生完成,肝细胞恢复G0期)处死大鼠,采用胶原酶IV灌注法分离原代肝细胞,台盼蓝染色计数活细胞。结果解读显示,大鼠肝切除后95%以上的残留肝细胞同步进入细胞周期,术后24h DNA合成达到峰值,7d后肝质量恢复至术前水平,肝细胞回到G0静息状态,分离的肝细胞活力超过90%(n=9/5/5,P<0.05)。实验所用关键产品:Sigma的胶原酶IV、Sigma的DNase I、Promega的GoTaq DNA聚合酶。
3.2 核质体制备与DNase I消化动力学分析
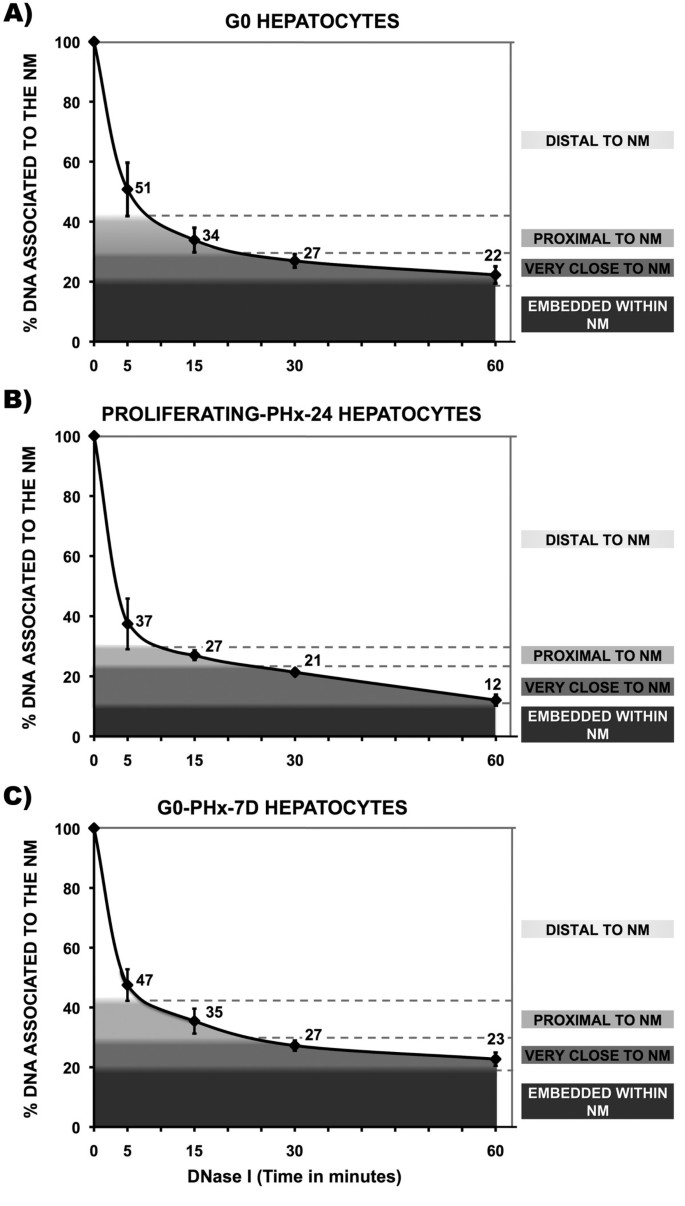
实验目的是建立基于核质体的DNA序列相对于核基质位置的检测方法,分析不同细胞周期阶段的DNA拓扑结构差异。方法细节为将新鲜分离的肝细胞制备为核质体(高盐、非离子去垢剂处理去除组蛋白与大部分核蛋白,保留DNA环与核基质的锚定),用0.5 U/ml DNase I在37℃进行梯度时间消化,通过分光光度法测定核基质结合DNA的残留量,绘制消化动力学曲线。结果解读显示,G0期肝细胞的DNA消化分为三个阶段:0-5min为快速消化阶段,约60%的远端DNA环被消化(斜率-9.80);5-15min为中速阶段,消化约10%的近端DNA(斜率-1.70);15-60min为慢速阶段,消化约10%的近核基质DNA(斜率-0.47),剩余20%为核基质嵌入DNA(斜率-0.17);S期肝细胞的消化动力学更快,0-5min斜率为-12.52,核基质嵌入DNA减少约50%;恢复期G0肝细胞的消化动力学与原G0期基本一致(n=9/5/5,P<0.05),表明DNA拓扑结构在复制后完全恢复。
3.3 特定DNA序列的PCR定位分析
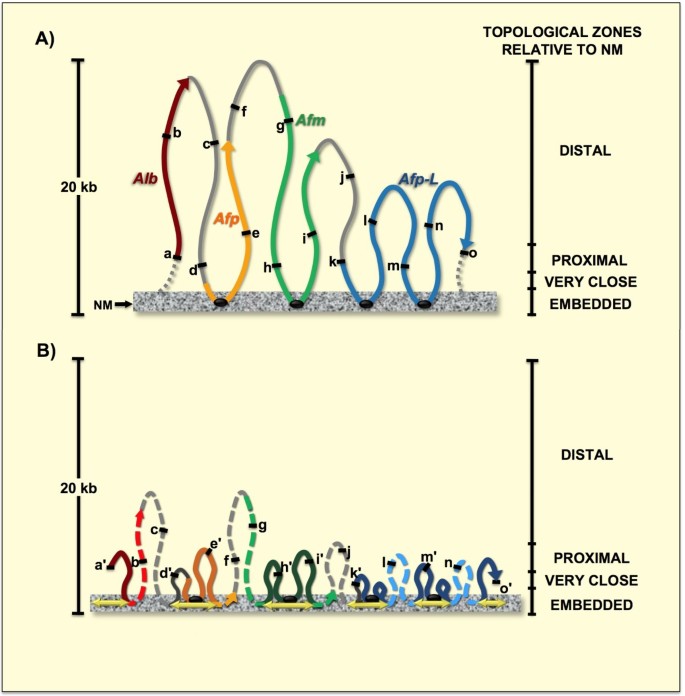
实验目的是追踪白蛋白基因家族162kb区域内的DNA序列在不同细胞周期阶段相对于核基质的位置变化。方法细节为基于前期确定的该区域5个结构DNA环,设计15对间隔约10kb的引物(扩增产物250-550bp),对不同消化时间的核质体DNA进行PCR扩增,通过图像分析软件判断扩增产物的存在/缺失,确定序列所在的拓扑区域(远端、近端、近核基质、嵌入核基质)。结果解读显示,G0期15个序列分布在不同拓扑区域;S期时,11个序列向核基质移动一个拓扑区域,2个序列(a、m)因靠近复制起点已完成复制,位置保持近端不变,2个序列(c、g)因远离复制叉尚未复制,位置保持远端不变;恢复期G0期时,8个移动的序列回到原位置(n≥3,P<0.05),表明DNA环复制后恢复原拓扑结构。

3.4 无关基因序列的普遍性验证
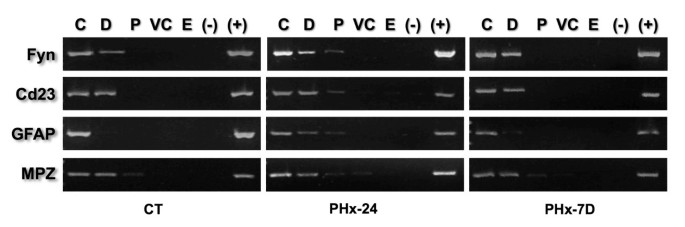
实验目的是验证DNA向核基质的顺序移动是体内DNA复制的普遍现象,而非特定区域的特有行为。方法细节为选择位于不同染色体的4个无关基因(GFAP、CD23、MPZ、Fyn)的5"端序列,设计引物进行PCR扩增,重复上述核质体消化与定位实验。结果解读显示,4个基因的序列在S期均向核基质移动一个拓扑区域,恢复期G0期回到原位置(n≥3,P<0.05),证明该移动规律适用于全基因组的结构DNA环。
4. Biomarker研究及发现成果解析
本研究中定义的Biomarker为结构DNA环相对于核基质的拓扑位置,其可作为判断肝细胞复制状态的功能性标志,筛选与验证逻辑遵循“前期结构环鉴定→同步化细胞定位→全基因组普遍性验证”的完整链条。
Biomarker定位明确为结构DNA环的拓扑区域(远端、近端、近核基质、嵌入核基质),筛选逻辑基于前期在大鼠肝细胞中鉴定的白蛋白基因家族区域5个结构DNA环,验证逻辑为通过肝再生同步化细胞模型,结合核质体DNase I消化动力学与PCR扩增技术,追踪序列位置变化,并通过无关基因验证全基因组普遍性。研究过程详述:Biomarker来源为大鼠肝细胞的基因组DNA,验证方法为核质体DNase I消化梯度实验结合特异性PCR扩增,特异性表现为不同拓扑区域的序列消化动力学差异显著(G0期0-5min斜率-9.80,S期-12.52,P<0.05),敏感性表现为可检测到单个序列的位置移动(如序列b从G0期近端区域移动至S期近核基质区域)。
核心成果提炼包括:该Biomarker的功能关联为,结构DNA环的拓扑位置变化直接反映DNA复制状态,S期时向核基质移动,复制完成后恢复原位置;创新性为首次在体内生理同步化模型中发现结构DNA环的顺序移动规律,为卷绕式复制模型提供直接体内证据,同时进一步证明结构DNA环对应体内复制子单位;统计学结果显示,所有实验重复样本量n≥3,组间差异具有统计学意义(P<0.05)。推测:该移动规律可能依赖于核基质与DNA环之间的动态相互作用,具体分子机制有待进一步鉴定相关的马达蛋白或锚定蛋白。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。