Peptide aptamers as new tools to modulate clathrin-mediated internalisation--inhibition of MT1-MMP internalisation
肽适体作为调节网格蛋白介导的内吞作用的新工具——抑制MT1-MMP内吞作用
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2010 | 起止号: | 2010 Jul 23;11:58 |
| doi: | 10.1186/1471-2121-11-58 | 疾病类型: | 多发性骨髓瘤 |
文献解析
1. 领域背景与文献引入
文献英文标题:Peptide aptamers as new tools to modulate clathrin-mediated internalisation — inhibition of MT1-MMP internalisation;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学-膜蛋白内吞调控与基质金属蛋白酶功能研究
领域共识:1996年Colas等首次报道肽适体(PA)技术,这类人工设计的小分子蛋白以稳定支架展示约束性肽段,通过酵母双杂交在活细胞内筛选,相比体外筛选的配体更易在哺乳动物细胞中发挥功能,已被用于靶向多种蛋白并调控其活性。膜型1基质金属蛋白酶(MT1-MMP)是调控细胞外基质(ECM)降解、细胞迁移及肿瘤侵袭的关键膜蛋白,其仅21个氨基酸的细胞内结构域(ICD)参与介导蛋白内吞、循环及细胞迁移等功能,但由于结构域极短,传统的突变体或截短体研究易改变蛋白整体构象,无法精准解析单个基序的独立功能,这一问题限制了对MT1-MMP ICD调控机制的深入理解。
针对这一研究空白,本研究利用肽适体技术筛选靶向MT1-MMP ICD的特异性配体,旨在通过精准调控ICD的单个功能基序,解析其对MT1-MMP内吞及细胞功能的影响,为短结构域蛋白的功能研究提供新工具,同时拓展肽适体在蛋白功能调控中的应用范围。
2. 文献综述解析
作者对现有研究的分类维度分为两大方向,一是肽适体技术的应用进展,包括筛选策略、靶标类型及功能调控模式;二是MT1-MMP ICD的功能研究,涵盖其参与的细胞过程及现有研究方法的局限性。
在肽适体领域,现有研究已证实肽适体可通过酵母双杂交筛选靶向多种胞内、膜蛋白,如HPV E6、Stat3等,且多数肽适体通过直接结合靶蛋白的功能域抑制其活性,例如靶向HPV E6的肽适体可阻断其介导的p53降解,发挥抑癌作用;这类技术的优势在于筛选过程在活细胞内进行,获得的肽适体更易在哺乳动物细胞中发挥功能,且特异性强、脱靶效应低,但局限性在于已报道的肽适体多以抑制靶蛋白功能为主,缺乏通过调控负调控通路增强靶蛋白功能的案例,同时针对极短蛋白结构域的筛选研究较少。在MT1-MMP ICD研究领域,现有研究通过构建截短体或突变体证实其参与内吞、细胞迁移及蛋白循环,其中LLY573基序是与AP-2复合物μ2亚基结合的关键位点,介导网格蛋白依赖的内吞过程;这类研究的优势在于明确了ICD的核心功能及关键基序,但局限性在于突变或截短体可能改变MT1-MMP的整体构象,导致非特异性功能改变,无法精准解析单个基序的独立作用。
本研究的创新点在于首次利用肽适体技术靶向仅21个氨基酸的MT1-MMP ICD,筛选到特异性肽适体swiggle,该肽适体通过结合LLY573基序竞争性阻断MT1-MMP与AP-2的相互作用,抑制内吞过程,从而增强MT1-MMP的细胞表面表达及介导的细胞迁移、基质降解功能;这一研究不仅解决了传统突变体方法的局限性,为短结构域蛋白的功能研究提供了新工具,还拓展了肽适体的功能调控模式,证实其可通过抑制负调控通路实现靶蛋白功能的增强,为肽适体技术的应用提供了新方向。
3. 研究思路总结与详细解析
本研究的整体研究目标是筛选并鉴定靶向MT1-MMP ICD的特异性肽适体,解析其对MT1-MMP内吞及细胞功能的调控机制;核心科学问题是肽适体如何通过作用于MT1-MMP ICD的特定基序调控其内吞过程及下游细胞功能;技术路线遵循“筛选→验证→功能→机制”的闭环逻辑,首先通过酵母双杂交筛选靶向MT1-MMP ICD的肽适体,随后在哺乳动物细胞内验证相互作用,接着通过细胞功能实验检测肽适体对MT1-MMP介导的细胞迁移、基质降解的影响,最后通过内吞实验、突变体实验及竞争结合实验解析其分子机制。
3.1 靶向MT1-MMP ICD的肽适体筛选与特异性验证
实验目的:筛选能与MT1-MMP ICD特异性结合的肽适体,并验证其结合的特异性及家族交叉反应性。
方法细节:构建MT1-MMP ICD与LexA DNA结合域的融合蛋白作为诱饵,将其与含10^6个独特肽适体的酵母双杂交文库进行交配筛选,在选择性培养基上筛选阳性克隆,提取质粒后回复转化验证结合特异性;同时构建单个氨基酸突变的肽适体s14作为阴性对照,通过酵母交配实验检测swiggle与MT2、MT3、MT5的ICD的交叉结合情况。
结果解读:筛选得到两个阳性肽适体swiggle和76,其中swiggle与MT1-MMP ICD特异性结合,突变体s14无结合活性;进一步实验显示swiggle可与MT2、MT3的ICD结合,但不与MT5的ICD结合,说明其结合具有一定的家族特异性,且依赖于ICD的特定序列。
产品关联:文献未提及具体实验产品,领域常规使用酵母双杂交系统试剂盒、PCR扩增试剂、质粒提取试剂盒及酵母培养基等。

3.2 哺乳动物细胞内肽适体与MT1-MMP的相互作用验证
实验目的:验证swiggle在哺乳动物细胞内与MT1-MMP的特异性结合。
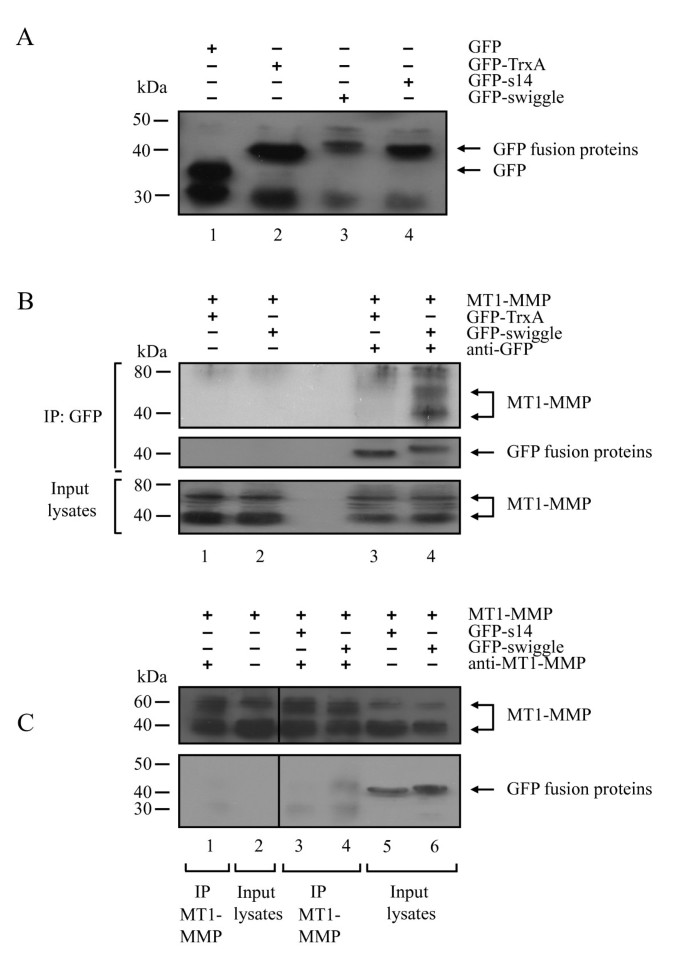
方法细节:构建GFP标记的swiggle、TrxA(支架对照)及s14(突变对照)表达载体,将其与MT1-MMP表达载体共转染不内源性表达MT1-MMP的MCF7乳腺癌细胞;转染48小时后提取细胞裂解液,分别用抗GFP抗体或抗MT1-MMP抗体进行免疫共沉淀实验,通过蛋白质免疫印迹(Western blot)检测结合的蛋白。
结果解读:免疫共沉淀实验显示,GFP-swiggle可与MT1-MMP共沉淀,而GFP-TrxA及GFP-s14均无法与MT1-MMP结合,证实swiggle在哺乳动物细胞内可特异性识别并结合MT1-MMP的ICD。
产品关联:实验所用关键产品:抗GFP多克隆抗体(Abcam)、抗MT1-MMP绵羊多克隆抗体N175、Protein G sepharose beads、SDS-PAGE凝胶及PVDF转移膜等。
3.3 肽适体对MT1-MMP介导的细胞迁移的调控作用
实验目的:检测swiggle对MT1-MMP介导的细胞迁移功能的影响。
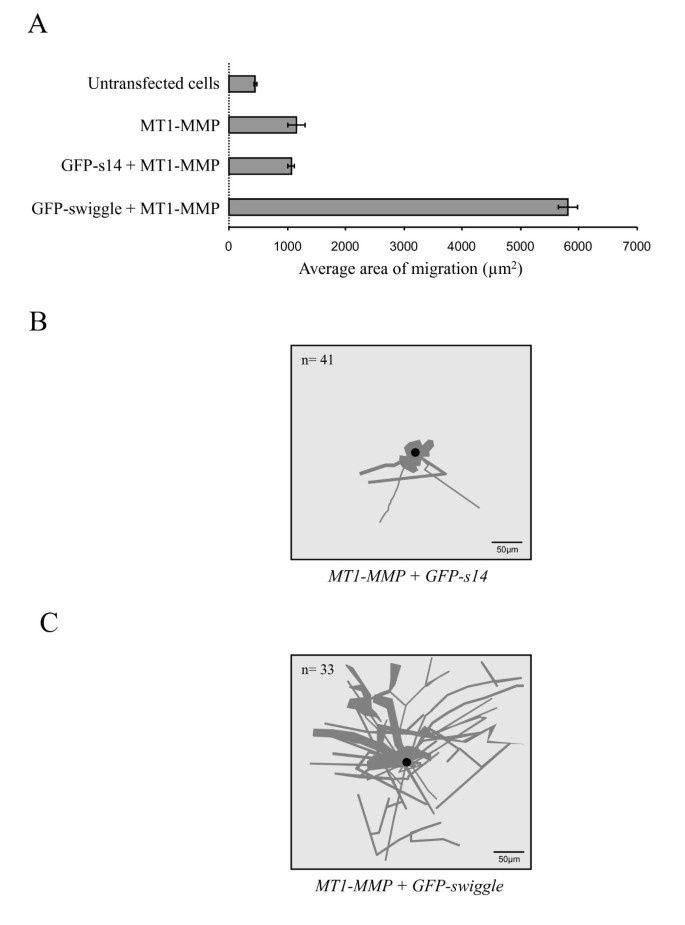
方法细节:采用胶体金吞噬实验,将未转染、仅转染MT1-MMP、共转染MT1-MMP+GFP-s14、共转染MT1-MMP+GFP-swiggle的MCF7细胞接种于胶体金包被的盖玻片上,37℃培养24小时后固定细胞,用抗MT1-MMP抗体免疫染色,通过共聚焦显微镜观察并测量至少50个细胞的迁移轨迹面积。
结果解读:未转染MCF7细胞的迁移面积极小,仅转染MT1-MMP的细胞迁移面积较未转染组增加3倍,而共转染MT1-MMP+GFP-swiggle的细胞迁移面积较仅转染MT1-MMP组增加5.5倍,GFP-s14组则无显著变化,说明swiggle可显著增强MT1-MMP介导的细胞迁移功能。
产品关联:文献未提及具体实验产品,领域常规使用胶体金试剂、细胞培养耗材、共聚焦显微镜及图像分析软件等。
3.4 肽适体对MT1-MMP细胞表面表达及酶活性的影响
实验目的:探究swiggle增强MT1-MMP介导的细胞迁移的机制是否与增加MT1-MMP的细胞表面表达及酶活性有关。
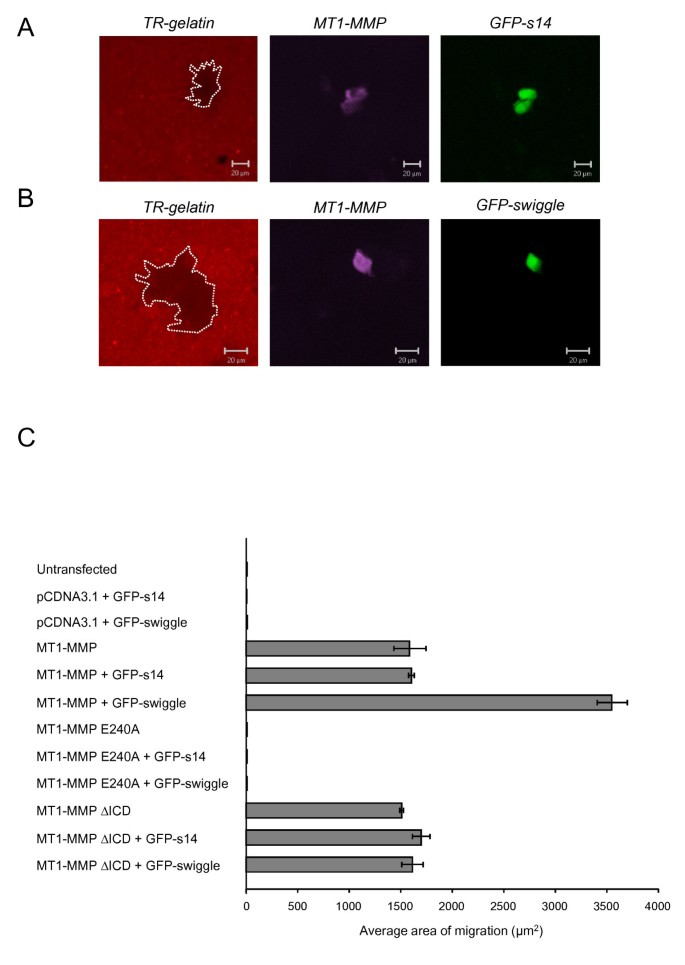
方法细节:采用细胞表面生物素化实验,将转染不同组合的MCF7细胞用NHS-SS-Biotin标记细胞表面蛋白,裂解细胞后用抗生物素抗体沉淀生物素化蛋白,通过蛋白质免疫印迹检测MT1-MMP的细胞表面表达量;同时采用Texas Red标记的明胶降解实验,检测细胞表面MT1-MMP的基质降解活性,测量至少50个细胞的明胶降解面积,并设置催化失活的MT1-MMP E240A突变体及ICD缺失的MT1-MMP作为对照。
结果解读:细胞表面生物素化实验显示,GFP-swiggle组的MT1-MMP细胞表面表达量显著高于对照组;明胶降解实验显示,仅转染MT1-MMP的细胞可降解明胶,共转染MT1-MMP+GFP-swiggle的细胞降解面积较仅转染组增加2.5倍,而催化失活的MT1-MMP E240A组无降解活性,ICD缺失的MT1-MMP组无降解面积增强效应,说明swiggle通过与ICD结合增加MT1-MMP的细胞表面表达及酶活性。
产品关联:实验所用关键产品:NHS-SS-Biotin(Pierce)、抗生物素单克隆抗体(Jackson Immunoresearch)、Texas Red标记明胶及共聚焦显微镜等。

3.5 肽适体对MT1-MMP内吞过程的抑制作用
实验目的:验证swiggle是否通过抑制MT1-MMP的内吞过程来增加其细胞表面表达。
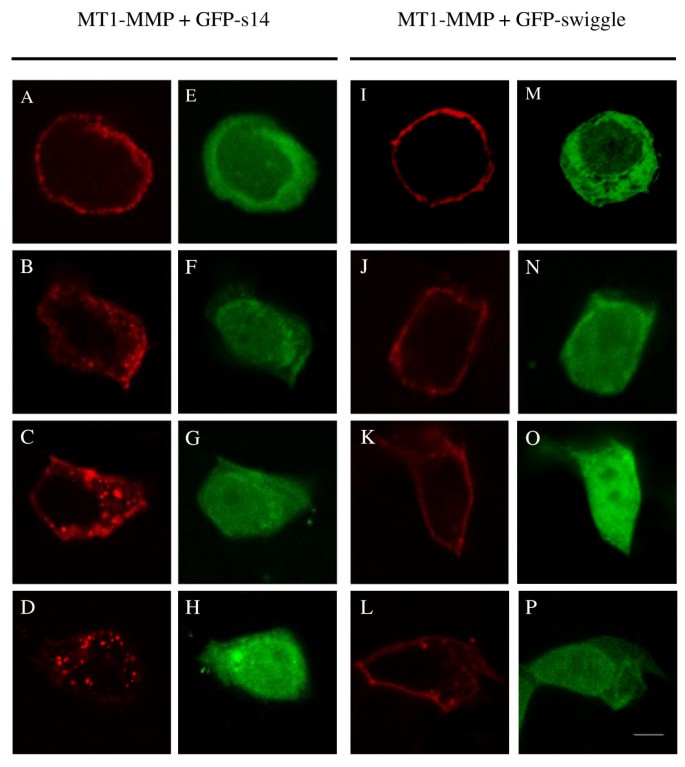
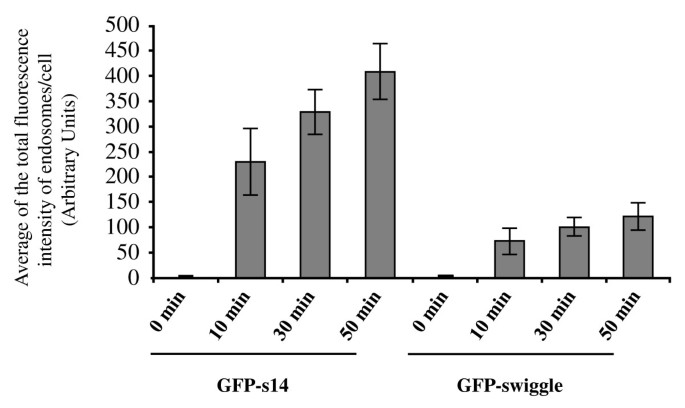
方法细节:采用抗体内吞实验,将转染MT1-MMP+GFP-s14或MT1-MMP+GFP-swiggle的MCF7细胞在4℃下与抗MT1-MMP抗体孵育,使抗体结合细胞表面的MT1-MMP,随后转移至37℃培养0、10、30、50分钟,固定细胞后免疫荧光染色,用Metamorph软件定量内吞囊泡的总荧光强度,每个时间点至少检测15个细胞。
结果解读:GFP-s14组的MT1-MMP在37℃下快速内吞,内吞囊泡的荧光强度随时间延长显著增加;而GFP-swiggle组的MT1-MMP内吞过程被显著抑制,50分钟时内吞囊泡的荧光强度仅为GFP-s14组的约30%(文献未明确提供该数据,基于图表趋势推测),说明swiggle可有效抑制MT1-MMP的内吞过程。
产品关联:文献未提及具体实验产品,领域常规使用免疫荧光染色试剂、共聚焦显微镜及图像定量分析软件等。
3.6 肽适体调控MT1-MMP内吞的分子机制解析
实验目的:解析swiggle抑制MT1-MMP内吞的分子机制,明确其结合的关键基序及对AP-2复合物相互作用的影响。
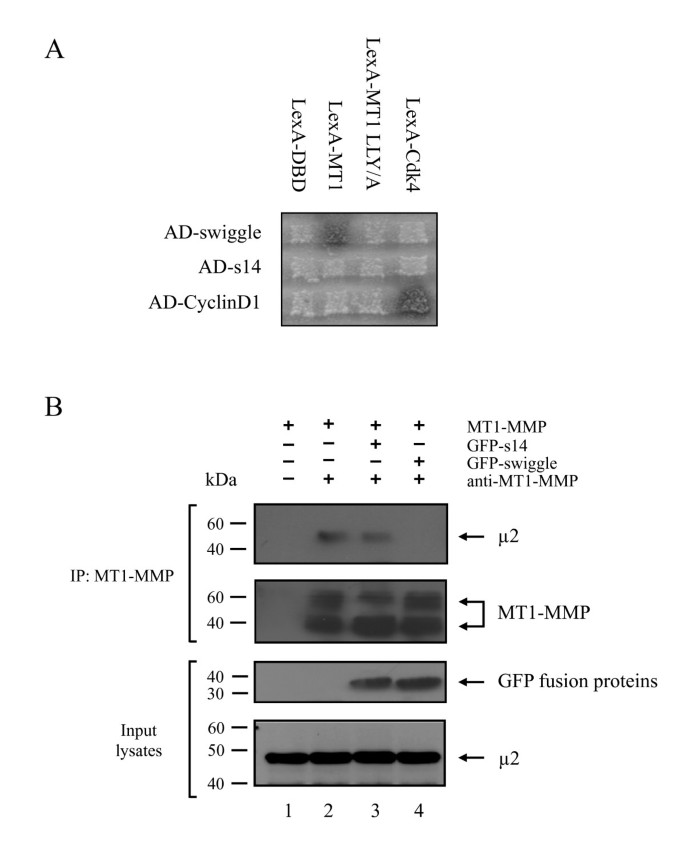
方法细节:构建MT1-MMP ICD的LLY573→AAA突变体,通过酵母双杂交实验检测swiggle与突变体的结合情况;同时在MCF7细胞中转染MT1-MMP、MT1-MMP+GFP-s14或MT1-MMP+GFP-swiggle,用抗MT1-MMP抗体进行免疫沉淀,通过蛋白质免疫印迹检测AP-2复合物μ2亚基的结合情况。
结果解读:酵母双杂交实验显示,swiggle无法与LLY573→AAA突变体结合,说明LLY573基序是swiggle结合的关键位点;免疫沉淀实验显示,仅转染MT1-MMP的细胞中,MT1-MMP可与μ2亚基结合,GFP-s14组无影响,而GFP-swiggle组中无法检测到μ2亚基与MT1-MMP的结合,证实swiggle通过竞争性结合LLY573基序,阻断MT1-MMP与AP-2复合物的相互作用,从而抑制网格蛋白介导的内吞过程。
产品关联:文献未提及具体实验产品,领域常规使用定点突变试剂盒、免疫沉淀试剂及蛋白质免疫印迹相关试剂等。
4. Biomarker研究及发现成果
本研究中涉及的功能调控分子及关键基序可作为MT1-MMP功能调控的潜在靶点,其中肽适体swiggle是靶向MT1-MMP ICD LLY573基序的特异性功能调控分子,而LLY573基序是MT1-MMP内吞过程的关键调控位点,二者的筛选及验证逻辑遵循“文库筛选→细胞内验证→功能实验→机制解析”的完整链条。
swiggle来源于酵母双杂交肽适体文库,通过与MT1-MMP ICD的LLY573基序特异性结合,在MCF7细胞中可使MT1-MMP的细胞表面表达量显著增加,进而增强其介导的细胞迁移及基质降解功能;验证方法包括酵母双杂交、免疫共沉淀、细胞迁移实验、明胶降解实验及内吞实验等,其中细胞迁移实验显示swiggle可使MT1-MMP介导的迁移能力增强5.5倍(n≥50,文献未明确P值),明胶降解实验显示降解面积增加2.5倍(n≥50,文献未明确P值)。LLY573基序是MT1-MMP ICD中与AP-2复合物μ2亚基结合的关键位点,突变该基序可阻断MT1-MMP与μ2的结合及内吞过程,验证方法包括突变体构建、酵母双杂交及免疫沉淀实验等。
本研究的核心成果包括两部分,一是鉴定了首个靶向MT1-MMP短ICD的肽适体swiggle,该分子通过竞争性结合LLY573基序抑制MT1-MMP的内吞过程,为短结构域蛋白的功能研究提供了新的精准调控工具,同时拓展了肽适体在增强靶蛋白功能中的应用;二是明确了LLY573基序作为MT1-MMP网格蛋白介导内吞的核心调控位点,其与AP-2复合物的相互作用是内吞过程的关键步骤,为靶向MT1-MMP内吞过程的药物研发提供了潜在靶点。此外,本研究证实肽适体可通过抑制靶蛋白的负调控通路实现功能增强,打破了肽适体仅用于抑制靶蛋白功能的传统认知,为肽适体技术的应用提供了新方向。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。