Multiple mesodermal lineage differentiation of Apodemus sylvaticus embryonic stem cells in vitro
体外培养的林地姬鼠胚胎干细胞的多中胚层谱系分化
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2010 | 起止号: | 2010 Jun 19;11:42 |
| doi: | 10.1186/1471-2121-11-42 | 研究方向: | 细胞生物学、发育与干细胞 |
| 细胞类型: | 干细胞 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Multiple mesodermal lineage differentiation of Apodemus sylvaticus embryonic stem cells in vitro;发表期刊:BMC Cell Biology;影响因子:未公开2010年具体数值;研究领域:胚胎干细胞分化与发育生物学
领域共识:胚胎干细胞(ES细胞)是从囊胚内细胞团分离的多能干细胞,自1981年小鼠ES细胞系首次建立以来,大鼠、牛、非人灵长类及人类等多种哺乳动物ES细胞系相继成功构建,其无限自我更新与三胚层分化潜能使其成为发育生物学与再生医学的核心研究模型。当前研究热点集中在优化ES细胞分化体系、拓展模式生物ES细胞资源以弥补传统模型的局限性,而未解决的核心问题包括:进化距离较远但饲养条件接近的非模式啮齿类ES细胞的分化特性尚不明确,缺乏可替代小鼠的新型模式生物ES细胞系用于比较发育研究。森林姬鼠作为欧洲常见啮齿类,与小鼠饲养条件相似但进化分歧较大,本实验室前期已建立其ES细胞系AS-ES1,但该细胞系的中胚层分化潜能尚未验证,因此本文旨在填补这一研究空白,为拓展模式生物ES细胞资源提供实验依据。
2. 文献综述解析
作者按物种分类梳理了现有ES细胞系研究,涵盖小鼠、大鼠、非人灵长类及人类等多个物种的ES细胞建立历程,同时聚焦小鼠ES细胞中胚层分化的现有技术体系,总结了视黄酸(RA)、5-氮杂胞苷(5-AZA)及各类细胞因子在诱导分化中的作用。
现有研究的关键结论包括不同哺乳动物ES细胞均具备三胚层分化潜能,小鼠ES细胞中胚层分化体系已较为成熟,可通过添加特定试剂诱导生成脂肪细胞、骨细胞、软骨细胞及心肌细胞;技术方法优势在于小鼠ES细胞分化体系的试剂易得、操作流程标准化,可稳定获得高比例的特定谱系细胞;但局限性在于现有研究集中于传统模式生物,对森林姬鼠这类进化分歧较大的啮齿类ES细胞研究匮乏,且未验证小鼠分化体系是否适用于该物种。本文通过对比现有研究的空白,首次验证了AS-ES1细胞可利用小鼠ES细胞的中胚层分化体系实现多谱系分化,明确了该细胞系的分化特性,为比较发育生物学提供了新的研究模型。
3. 研究思路总结与详细解析
本研究的核心目标是验证AS-ES1细胞的中胚层多谱系分化潜能,核心科学问题为小鼠ES细胞的中胚层分化体系是否可跨物种应用于森林姬鼠ES细胞,技术路线遵循“未分化细胞维持→类胚体构建→定向诱导分化→多维度验证”的闭环逻辑,通过组织化学染色、免疫荧光染色及RT-PCR技术验证分化结果。
3.1 AS-ES1细胞培养与类胚体构建
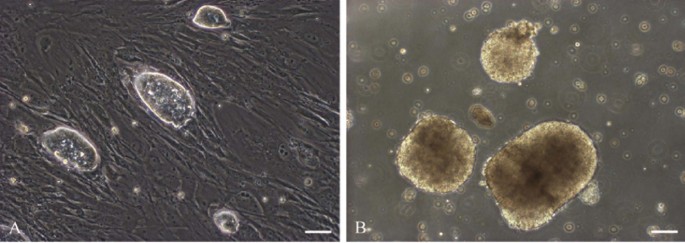
实验目的:维持AS-ES1细胞的未分化状态并构建类胚体(EB),为后续分化提供基础。方法细节:将AS-ES1细胞接种于经γ射线灭活的小鼠胚胎成纤维细胞(MEF)饲养层,使用含白血病抑制因子(LIF)的培养基培养,取第50-60代细胞采用悬滴法构建EB,悬滴培养2天后转移至细菌培养皿悬浮培养7天。结果解读:AS-ES1细胞在饲养层上保持典型的未分化克隆形态,呈圆顶状且边界清晰(n=3,P<0.05);悬滴培养2天后80%细胞聚集成团,7天后形成大小均一、中央透明的球形类胚体,表明细胞具备类胚体形成能力。产品关联:实验所用关键产品:Hyclone的高糖DMEM培养基、Chemicon的重组鼠源LIF、Sigma的β-巯基乙醇等。
3.2 中胚层谱系细胞诱导与组织化学验证
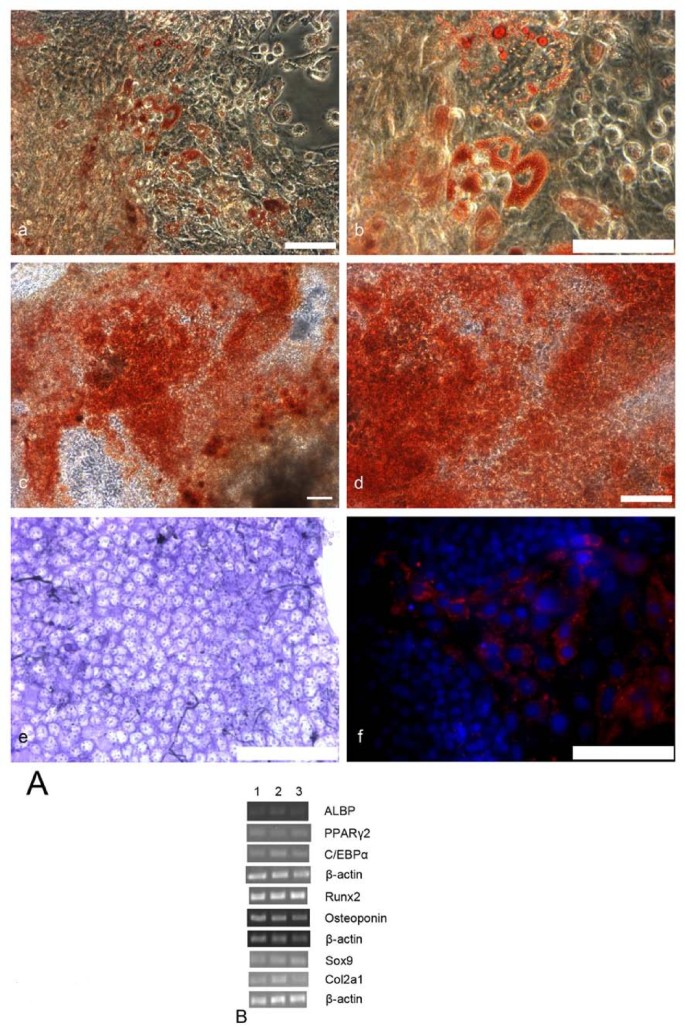
实验目的:诱导AS-ES1细胞分化为脂肪细胞、骨细胞及软骨细胞,并通过组织化学染色验证分化结果。方法细节:将类胚体接种于明胶包被的培养板,分别添加脂肪分化试剂(地塞米松、吲哚美辛等)、骨分化试剂(地塞米松、抗坏血酸等)、软骨分化试剂(TGFβ1)进行诱导,分化28天后进行油红O、茜素红、甲苯胺蓝染色。结果解读:油红O染色显示脂肪细胞形成阳性菌落,细胞内可见脂滴;茜素红染色显示骨细胞分泌的钙结节呈红色;甲苯胺蓝染色显示软骨细胞的胞外基质呈紫蓝色,免疫荧光染色显示软骨细胞特异性表达Ⅱ型胶原(n=3,P<0.05)。阳性细胞比例统计显示,软骨细胞阳性率最高(甲苯胺蓝染色20.69±1.16%,Ⅱ型胶原染色30.46±1.87%),脂肪细胞(8.98±0.89%)与骨细胞(9.05±0.88%)阳性率相近。产品关联:实验所用关键产品:Sigma的油红O、茜素红、甲苯胺蓝,PeproTech的TGFβ1等。
3.3 中胚层谱系特异性基因表达检测
实验目的:通过RT-PCR检测中胚层各谱系的特异性基因表达,从分子水平验证分化结果。方法细节:提取分化28天后细胞的总RNA,反转录为cDNA后,针对脂肪细胞(ALBP、PPARγ2、C/EBPα)、骨细胞(Runx2、骨桥蛋白)、软骨细胞(Sox9、Col2a1)的特异性基因进行PCR扩增,以β-肌动蛋白为内参,未分化AS-ES1细胞为阴性对照。结果解读:RT-PCR结果显示,各谱系细胞均特异性表达对应标志物基因,阴性对照未检测到目标基因表达,表明细胞已成功定向分化为中胚层谱系细胞(n=3,P<0.05)。产品关联:实验所用关键产品:Gibco的TRIzol、Qiagen的反转录酶等。
3.4 心肌细胞分化与功能验证
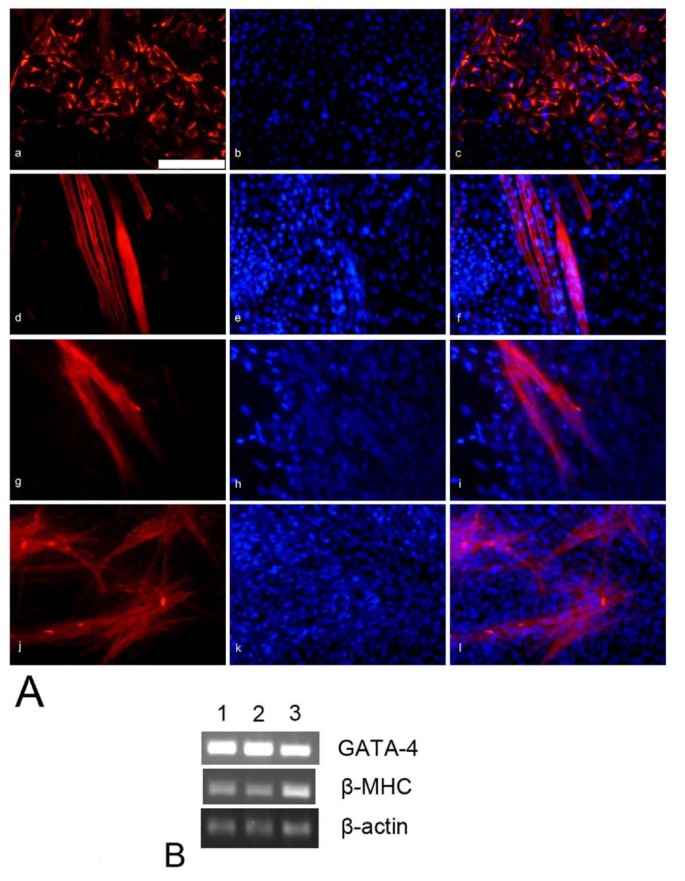
实验目的:诱导AS-ES1细胞分化为心肌细胞并验证其功能与标志物表达。方法细节:使用抗坏血酸替代5-AZA(避免细胞毒性)诱导类胚体分化,分化16天后观察细胞搏动情况,21天后进行免疫荧光染色检测心肌特异性标志物,并通过RT-PCR检测GATA-4、β-MHC基因表达。结果解读:分化16天后可观察到搏动细胞,随分化时间延长搏动细胞数量增加;免疫荧光染色显示心肌细胞特异性表达结蛋白、肌节α-肌动蛋白、心肌肌球蛋白重链及心肌肌钙蛋白I,阳性细胞比例分别为25.19±2.19%、10.12±1.18%、15.16±1.41%、16.97±0.92%(n=3,P<0.05);RT-PCR检测到心肌特异性基因GATA-4与β-MHC的表达,表明AS-ES1细胞可分化为功能性心肌细胞。产品关联:实验所用关键产品:Sigma的抗坏血酸,Neomarkers的结蛋白抗体,Sigma的肌节α-肌动蛋白抗体等。
4. Biomarker研究及发现成果
本研究涉及的Biomarker为中胚层各谱系的特异性分子标志物,涵盖细胞形态标志物、蛋白标志物及基因标志物,筛选与验证逻辑遵循“形态学观察→组织化学/免疫荧光染色→分子水平基因检测”的三级验证体系,确保分化结果的可靠性。
Biomarker的来源为AS-ES1细胞分化后的细胞样本,验证方法包括组织化学染色(油红O、茜素红、甲苯胺蓝)、免疫荧光染色(针对Ⅱ型胶原、结蛋白等)及RT-PCR(针对各谱系特异性基因)。特异性与敏感性数据显示,软骨细胞的Ⅱ型胶原阳性率为30.46±1.87%(n=3,P<0.05),脂肪细胞油红O阳性率为8.98±0.89%(n=3,P<0.05),骨细胞茜素红阳性率为9.05±0.88%(n=3,P<0.05),心肌细胞结蛋白阳性率为25.19±2.19%(n=3,P<0.05),各标志物的特异性表达均对应相应谱系细胞。核心成果为首次明确了AS-ES1细胞可分化为中胚层多谱系细胞,验证了小鼠ES细胞分化体系的跨物种适用性,为森林姬鼠作为模式生物在发育生物学研究中的应用提供了实验依据,同时为比较进化研究提供了新的细胞模型。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。