Chronic glucolipotoxic conditions in pancreatic islets impair insulin secretion due to dysregulated calcium dynamics, glucose responsiveness and mitochondrial activity
胰岛慢性糖脂毒性会因钙动力学、葡萄糖反应性和线粒体活性的失调而损害胰岛素分泌。
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2013 | 起止号: | 2013 Jul 1;14:31 |
| doi: | 10.1186/1471-2121-14-31 | 研究方向: | 毒理研究、免疫/内分泌 |
文献解析
1. 领域背景与文献引入
文献英文标题:Chronic glucolipotoxic conditions in pancreatic islets impair insulin secretion due to dysregulated calcium dynamics, glucose responsiveness and mitochondrial activity;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:2型糖尿病与胰腺β细胞功能障碍
领域共识:2型糖尿病是全球高发的代谢性疾病,核心病理特征为胰腺β细胞胰岛素分泌不足与外周组织胰岛素抵抗。1985年Unger等提出“糖脂毒性”概念,指出持续升高的血糖与游离脂肪酸协同损伤β细胞功能,成为2型糖尿病进展的关键机制。当前研究热点聚焦于糖脂毒性对β细胞代谢通路、线粒体功能、钙信号转导的调控机制,但现有研究多集中于单一环节,缺乏对糖脂毒性影响β细胞功能的整合性机制解析,这一空白限制了针对β细胞保护的糖尿病治疗靶点开发。本文旨在通过体外实验构建标准化的慢性糖脂毒性模型,系统解析其对β细胞糖脂代谢、线粒体功能、钙信号及胰岛素合成分泌的多环节影响,为2型糖尿病的病理机制研究提供整合性数据支撑。
2. 文献综述解析
作者按糖脂毒性对β细胞的不同功能环节分类综述现有研究,涵盖葡萄糖代谢、脂肪酸代谢、线粒体功能、钙信号通路及胰岛素合成分泌五大模块。现有研究的关键结论包括高糖是介导脂毒性效应的必要条件,可抑制葡萄糖刺激的胰岛素分泌(GSIS)、下调胰岛素基因表达并诱导β细胞凋亡;技术方法上,体外细胞模型能精准控制糖脂浓度,实现对特定通路的机制研究,但不同研究使用的脂肪酸浓度差异较大,导致实验结果的可比性不足,且多数研究仅关注单一通路的变化,缺乏对糖脂毒性影响β细胞功能的系统性整合分析。本文的创新价值在于首次采用标准化的体外糖脂毒性条件(16.7mM葡萄糖+500μM棕榈酸),整合分析了糖脂代谢、线粒体功能、钙信号及胰岛素合成分泌的多环节变化,填补了现有研究缺乏系统性机制解析的空白,为糖脂毒性介导β细胞功能障碍的研究提供了统一的实验范式。
3. 研究思路总结与详细解析
本文的研究目标是明确慢性糖脂毒性对胰腺β细胞功能的多环节影响机制,核心科学问题是慢性糖脂毒性如何通过调控糖脂代谢、线粒体功能及钙信号通路抑制胰岛素分泌,技术路线遵循“模型构建→代谢通路分析→功能验证→机制整合”的闭环逻辑。
3.1 糖脂毒性模型构建与胰岛素分泌验证
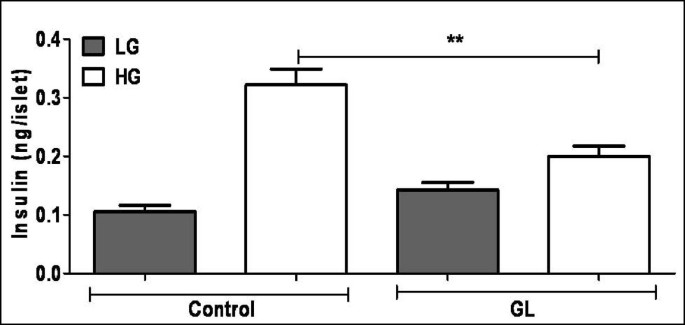
实验目的是验证慢性糖脂毒性对大鼠胰岛及β细胞系胰岛素分泌功能的影响。方法细节:将大鼠胰岛及NIT1β细胞分别在正常条件(5.5mM葡萄糖)或慢性糖脂毒性条件(16.7mM葡萄糖+500μM棕榈酸)下培养72小时,随后用2mM(低糖)或11mM(高糖)葡萄糖处理2小时,检测葡萄糖刺激的胰岛素分泌水平;同时通过内质网应激、氧化应激标志物验证模型的代谢应激状态。结果解读:如图1所示,慢性糖脂毒性条件下,高糖刺激的胰岛素分泌显著降低(n=4,P<0.001),且内质网应激标志物CHOP、BiP的蛋白水平显著升高,氧化应激水平增加,证实模型成功模拟了糖尿病病理状态下的β细胞功能障碍。产品关联:文献未提及具体实验产品,领域常规使用ELISA试剂盒检测胰岛素、细胞培养试剂等。
3.2 葡萄糖代谢通路分析
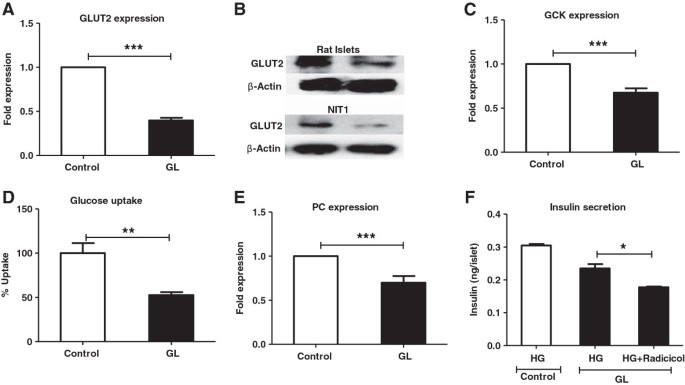
实验目的是明确慢性糖脂毒性对β细胞葡萄糖摄取与代谢的影响。方法细节:采用qRT-PCR检测葡萄糖转运蛋白Glut2、葡萄糖激酶(Gck)、丙酮酸羧化酶(Pc)的mRNA水平,蛋白免疫印迹(WB)检测Glut2的蛋白水平;使用荧光葡萄糖类似物2-NBDG检测葡萄糖摄取能力,同时检测NADPH水平与乳酸释放量。结果解读:如图2所示,慢性糖脂毒性条件下,Glut2的mRNA及蛋白水平显著降低(n=4,P<0.01),Gck与Pc的mRNA水平也显著下调(n=4,P<0.001);2-NBDG摄取量降低约40%(n=4,P<0.001),NADPH水平降低且乳酸释放量增加,证实葡萄糖摄取与氧化代谢均受损;进一步抑制ATP柠檬酸裂解酶(ACLY)后,胰岛素分泌进一步降低,提示糖脂毒性通过影响回补/溢出通路调控胰岛素分泌。产品关联:文献未提及具体实验产品,领域常规使用qRT-PCR试剂盒、蛋白免疫印迹试剂、荧光葡萄糖类似物等。
3.3 脂肪酸代谢通路分析
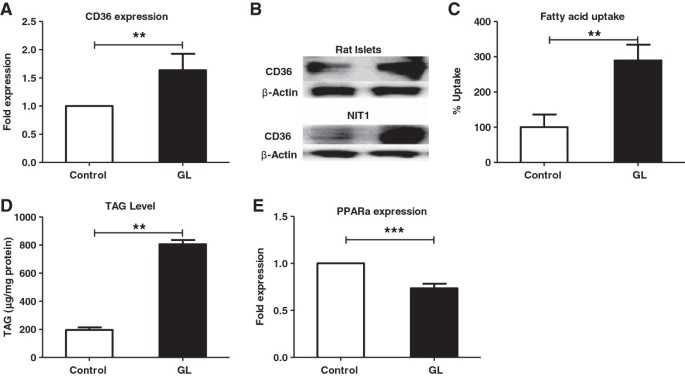
实验目的是解析慢性糖脂毒性对β细胞脂肪酸摄取与代谢的调控作用。方法细节:采用qRT-PCR检测脂肪酸转运蛋白CD36、过氧化物酶体增殖物激活受体α(PPARα)的mRNA水平,蛋白免疫印迹检测CD36的蛋白水平;使用荧光脂肪酸类似物BODIPY检测脂肪酸摄取能力,同时检测细胞内甘油三酯含量。结果解读:如图3所示,慢性糖脂毒性条件下,CD36的mRNA及蛋白水平显著升高(n=4,P<0.001),BODIPY摄取量增加3倍(n=4,P<0.001),细胞内甘油三酯含量增加4倍(n=4,P<0.001);PPARα的mRNA水平显著降低,证实脂肪酸氧化代谢受损,脂肪蓄积增加。产品关联:文献未提及具体实验产品,领域常规使用荧光脂肪酸类似物、甘油三酯检测试剂盒、蛋白免疫印迹抗体等。
3.4 线粒体功能与ATP水平检测
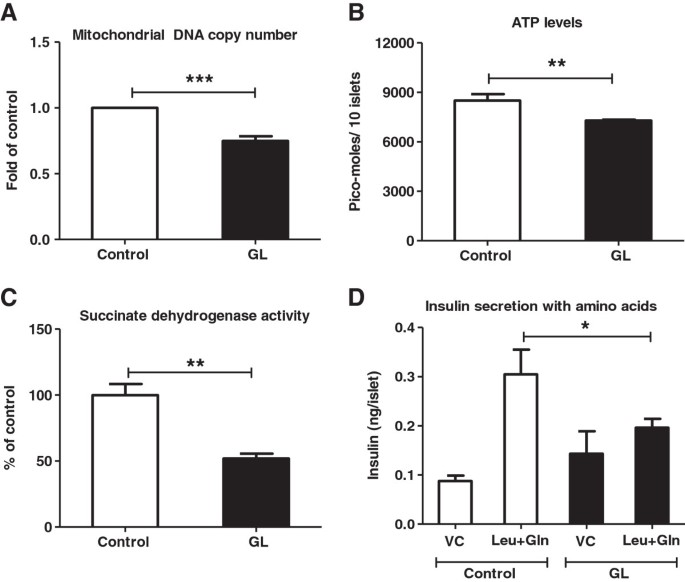
实验目的是明确慢性糖脂毒性对β细胞线粒体数量与功能的影响。方法细节:采用qRT-PCR检测线粒体DNA编码的细胞色素C氧化酶1(mtCox1)的拷贝数,以核基因HPRT为内参;检测细胞ATP水平、琥珀酸脱氢酶活性,同时通过氨基酸刺激的胰岛素分泌验证三羧酸循环功能。结果解读:如图4所示,慢性糖脂毒性条件下,mtCox1的拷贝数显著降低(n=4,P<0.01),提示线粒体数量减少;细胞ATP水平降低,琥珀酸脱氢酶活性降低约50%(n=4,P<0.001);氨基酸刺激的胰岛素分泌显著降低,证实三羧酸循环功能受损,线粒体能量代谢障碍。产品关联:文献未提及具体实验产品,领域常规使用ATP检测试剂盒、琥珀酸脱氢酶活性检测试剂盒、qRT-PCR试剂盒等。
3.5 钙信号通路分析
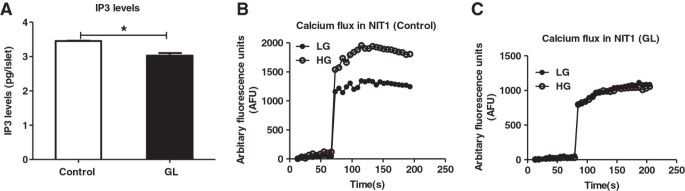
实验目的是解析慢性糖脂毒性对β细胞钙信号转导的调控机制。方法细节:检测大鼠胰岛中肌醇三磷酸(IP3)的水平;采用Fluo-3AM钙指示剂标记NIT1细胞,检测低糖(2.5mM)或高糖(16.7mM)刺激下的胞质钙动员;同时通过L型钙通道抑制剂硝苯地平、IP3受体抑制剂2-APB验证钙信号对胰岛素分泌的影响。结果解读:如图5所示,慢性糖脂毒性条件下,IP3水平显著降低(n=4,P<0.05);高糖刺激的胞质钙动员效应消失,而正常条件下高糖可显著升高胞质钙水平;抑制剂实验证实L型钙通道与内质网钙动员均参与胰岛素分泌调控,且糖脂毒性可损伤这两条通路的钙信号转导。产品关联:文献未提及具体实验产品,领域常规使用钙指示剂、信号通路抑制剂、IP3检测试剂盒等。
3.6 胰岛素合成与颗粒转运检测
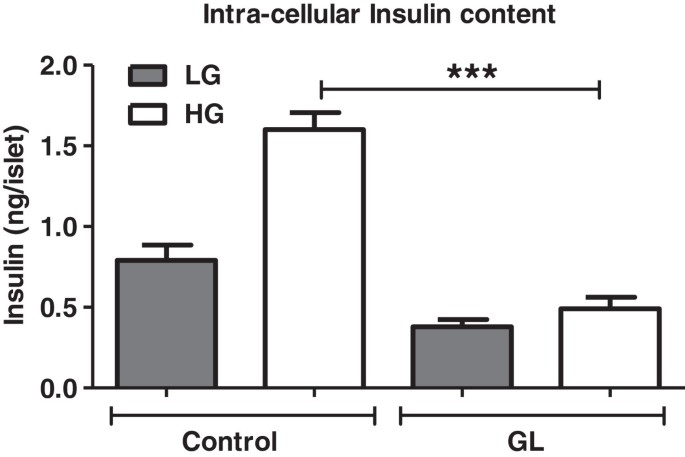
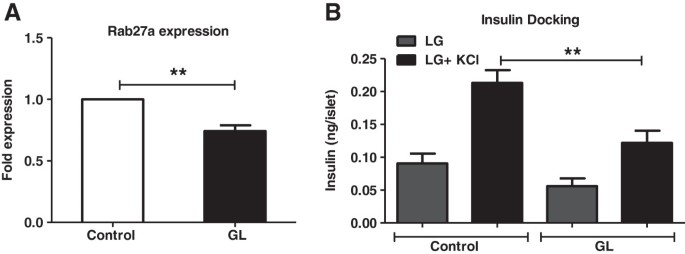
实验目的是明确慢性糖脂毒性对β细胞胰岛素合成、含量及颗粒转运的影响。方法细节:采用qRT-PCR检测胰岛素转录因子Pdx1、胰岛素(Ins2)及颗粒转运蛋白Rab27a的mRNA水平;检测胰岛胰岛素含量,同时通过氯化钾(KCl)刺激验证胰岛素颗粒的膜停靠能力。结果解读:如图6、7所示,慢性糖脂毒性条件下,Pdx1与Ins2的mRNA水平显著降低(n=4,P<0.01),胰岛胰岛素含量显著减少(n=4,P<0.001);Rab27a的mRNA水平显著降低(n=4,P<0.05),KCl刺激的胰岛素分泌显著减少,证实胰岛素颗粒的膜停靠能力受损,胰岛素分泌的转运环节受抑制。产品关联:文献未提及具体实验产品,领域常规使用qRT-PCR试剂盒、胰岛素含量检测试剂盒等。
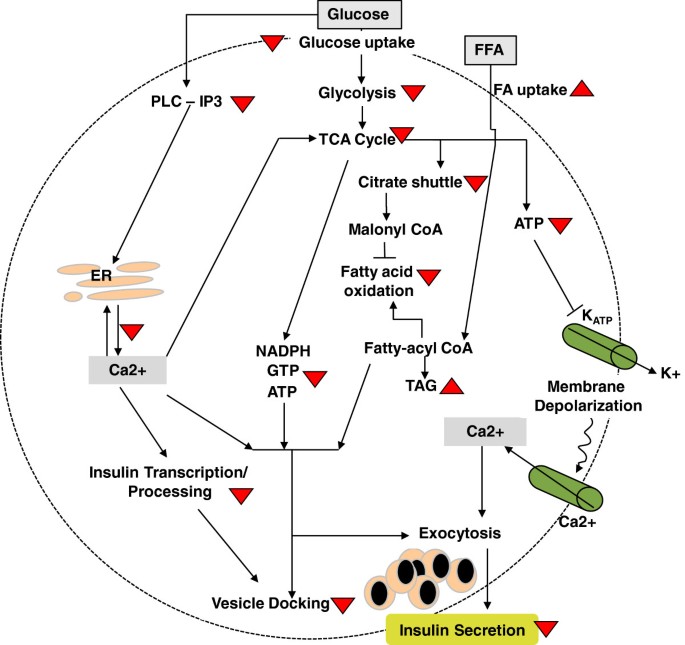
作者整合上述结果提出慢性糖脂毒性介导β细胞功能障碍的模型,如图8所示,高糖与棕榈酸通过抑制糖代谢、促进脂肪蓄积、损伤线粒体功能、抑制钙信号转导,进而下调胰岛素合成与颗粒转运,最终导致胰岛素分泌功能受损。
4. Biomarker研究及发现成果
本文涉及的Biomarker主要为糖脂代谢、线粒体功能及胰岛素转运相关的分子,包括Glut2、CD36、mtCox1、Rab27a等,筛选逻辑基于慢性糖脂毒性对β细胞功能的多环节影响,通过转录组、蛋白组及功能实验逐步验证其与β细胞功能障碍的关联。
这些Biomarker均来源于体外培养的大鼠胰岛及NIT1β细胞,验证方法包括qRT-PCR检测mRNA水平、蛋白免疫印迹检测蛋白水平、功能实验验证其对胰岛素分泌的影响;特异性与敏感性数据显示,Glut2的mRNA水平在糖脂毒性条件下降低约60%(n=4,P<0.01),CD36的蛋白水平升高约2.5倍(n=4,P<0.001),mtCox1的拷贝数降低约40%(n=4,P<0.01),Rab27a的mRNA水平降低约30%(n=4,P<0.05),这些分子的变化与胰岛素分泌功能呈显著相关性。
核心成果提炼:这些分子可作为慢性糖脂毒性介导β细胞功能障碍的潜在Biomarker,其中mtCox1可反映线粒体功能损伤程度,Glut2与CD36可反映糖脂代谢紊乱状态,Rab27a可反映胰岛素颗粒转运功能;本文首次在体外模型中证实这些分子的协同变化与β细胞胰岛素分泌功能受损的关联,但未涉及临床样本验证,因此暂不具备临床诊断或预后价值。推测:这些分子可作为后续临床研究的候选Biomarker,用于评估糖尿病患者的β细胞功能状态。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。