Collagen/β(1) integrin interaction is required for embryoid body formation during cardiogenesis from murine induced pluripotent stem cells
胶原蛋白/β(1)整合素相互作用是小鼠诱导多能干细胞心脏发生过程中胚状体形成所必需的。
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2013 | 起止号: | 2013 Jan 25;14:5 |
| doi: | 10.1186/1471-2121-14-5 | 研究方向: | 细胞生物学、发育与干细胞 |
| 细胞类型: | 干细胞 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Collagen/β₁ integrin interaction is required for embryoid body formation during cardiogenesis from murine induced pluripotent stem cells;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:诱导多能干细胞心脏分化、细胞外基质-整合素相互作用调控。
胚胎干细胞(ESC)因具有无限增殖能力和多向分化潜能,成为心血管再生医学的核心研究对象,但胚胎来源的伦理争议及异体移植的免疫排斥问题严重限制了其临床转化。2006年诱导多能干细胞(iPSC)技术的突破为解决上述问题提供了新方向,iPSC由体细胞重编程获得,可分化为包括心肌细胞在内的多种体细胞,且能实现患者特异性细胞制备,避免免疫排斥风险。拟胚体(EB)形成是诱导iPSC向心肌细胞分化的经典方法,该过程模拟体内早期胚胎发育,是启动谱系特异性分化的关键中间步骤。领域共识:细胞外基质(ECM)与整合素介导的细胞-微环境相互作用是调控干细胞命运决定的核心机制之一,参与多种干细胞的增殖、分化及组织发育过程。然而,现有研究多集中于人iPSC或ESC的EB分化体系,针对小鼠iPSC(miPSC)来源EB形成过程中ECM/整合素相互作用的功能研究仍存在空白,尚未明确其对心脏分化的具体调控作用。基于此,本研究聚焦I型胶原与β₁整合素的相互作用,系统探究其在miPSC来源EB形成及心脏分化中的调控功能。
2. 文献综述解析
本文综述部分以“ESC的局限→iPSC的优势与应用→EB形成在分化中的核心地位→ECM/整合素的调控作用→miPSC心脏分化中EB形成的机制空白”为逻辑主线,逐步明确研究的科学必要性。
现有研究的关键结论可分为三类:一是ESC具有心血管再生的潜在价值,但伦理和免疫排斥问题难以突破;二是iPSC可通过EB形成高效分化为功能性心肌细胞,为个性化心血管再生提供了可行路径;三是ECM与整合素的相互作用是调控干细胞命运的核心机制之一,参与多种干细胞的增殖、分化及组织发育过程。现有研究的技术方法优势在于,EB形成体系能较好模拟体内胚胎发育过程,为体外研究干细胞分化提供了接近生理的模型;但局限性也较为明显,多数研究集中于ESC或人iPSC的EB分化,针对miPSC来源EB形成的微环境调控机制研究不足,尤其缺乏对ECM/整合素相互作用在该过程中功能的系统解析。通过对比现有研究的未解决问题,本研究的创新价值凸显:首次针对miPSC心脏分化的EB形成过程,明确了I型胶原/β₁整合素相互作用的必需调控功能,填补了该领域的机制研究空白,为优化干细胞心脏分化的微环境提供了直接的实验依据。
3. 研究思路总结与详细解析
本研究的整体框架围绕“明确分子表达模式→验证功能调控作用→评估分化能力影响”的逻辑闭环展开,研究目标为揭示I型胶原/β₁整合素相互作用在miPSC来源EB形成及心脏分化中的作用,核心科学问题是该相互作用是否通过调控EB的结构与生长进而影响后续心脏分化命运,技术路线涵盖分子表达检测、功能阻断实验及分化表型验证三个核心环节。
3.1 细胞培养与EB形成模型构建
实验目的为建立稳定的miPSC及小鼠ESC(mESC)培养体系,构建EB形成的体外模型,为后续分子机制研究提供实验基础。方法细节方面,研究人员培养携带Oct4-eGFP报告基因的miPSC及mESC,分别采用悬滴法和静态悬浮法诱导EB形成,悬滴法通过控制细胞数量保证EB均一性,静态悬浮法允许细胞自发聚集,在分化第3、5天通过光学显微镜及荧光显微镜观察EB形态。结果解读显示,未分化的miPSC在饲养层或明胶包被板上的形态与mESC高度相似,均呈现典型的干细胞克隆形态;两种诱导方法均能成功形成EB,第3、5天的EB形态与mESC来源EB一致,Oct4-eGFP荧光信号随分化进程逐渐减弱,提示多能性的丧失。
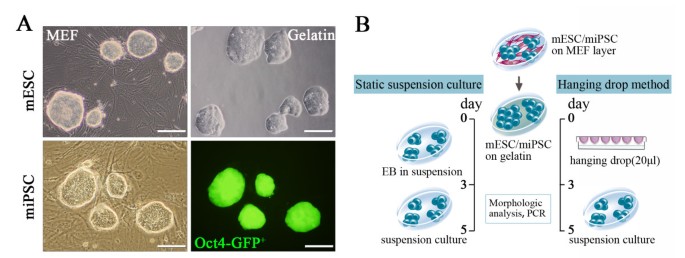
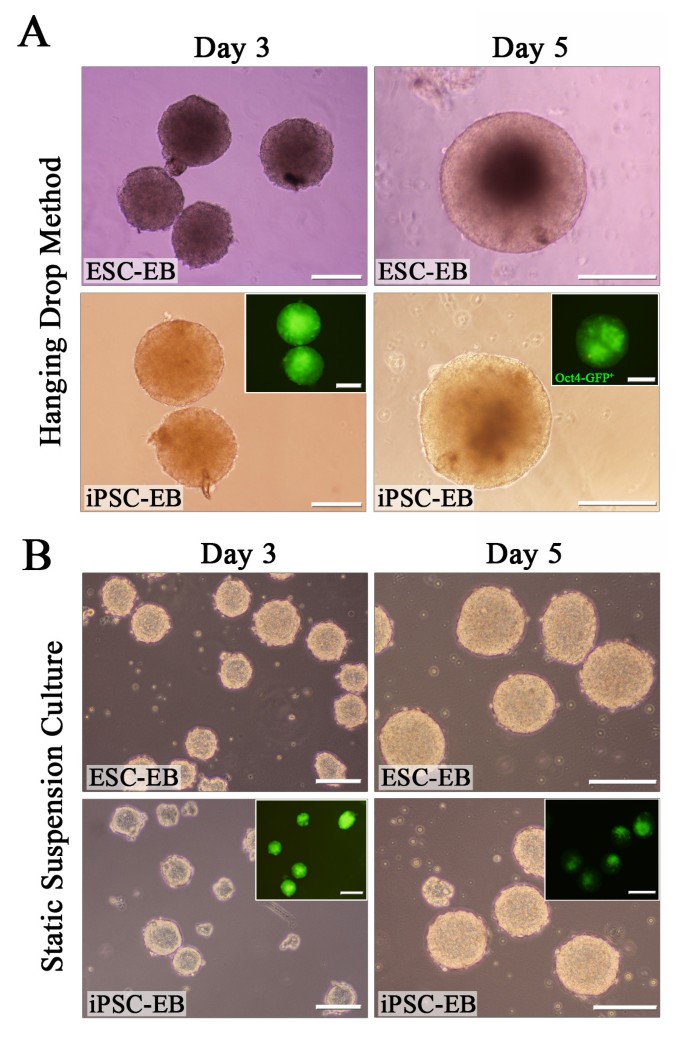
实验所用关键产品:BD Pharmingen的β₁整合素阻断抗体(克隆号Ha2/5)、Abcam的心肌肌钙蛋白T抗体、Abcam的I型胶原抗体、Invitrogen的Trypsin-EDTA、Sigma的抗坏血酸(Vc)、Sigma的顺式-4-羟基-D-脯氨酸(CIS)。
3.2 胶原与整合素的表达模式检测
实验目的为分析EB形成过程中胶原及其整合素受体的时序表达变化,筛选潜在的功能相互作用分子对。方法细节包括采用半定量RT-PCR检测未分化细胞及分化第3、5天EB中I型胶原(Col1A1、Col1A2)、III型胶原(Col3A1)及整合素α₁、α₂、β₁的mRNA表达,通过实时定量PCR验证关键分子的表达趋势,同时对第3天EB进行免疫染色检测I型胶原的蛋白表达。结果解读表明,未分化的mESC和miPSC仅表达整合素α₁和β₁,不表达I型胶原;在EB形成过程中,Col1A1和β₁整合素(Itgb1)的mRNA表达协同上调,在分化第3天达到峰值,随后下降至未分化细胞水平,免疫染色结果显示第3天EB中存在I型胶原的蛋白表达,提示该分子对在EB形成的关键阶段发挥调控作用。
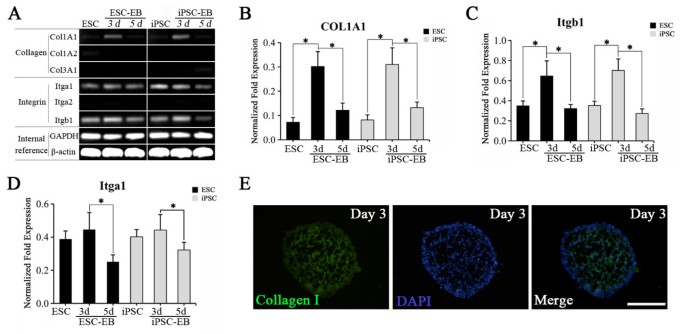
实验所用关键产品:Takara的PrimeScript™ First Strand cDNA Synthesis Kit、Takara的SYBR Premix Ex Taq™ II、Abcam的I型胶原抗体。
3.3 胶原/β₁整合素相互作用的功能阻断实验
实验目的为验证I型胶原/β₁整合素相互作用对EB生长及结构形成的调控功能。方法细节为在EB形成前分别添加Vc(胶原合成刺激剂,100μM)、CIS(胶原合成抑制剂,300μM)或β₁整合素阻断抗体(10μg/ml),采用静态悬浮法和悬滴法诱导EB形成,在分化第5天测量EB直径,通过扫描电镜观察EB表面结构。结果解读显示,静态悬浮培养体系中,Vc处理组EB平均直径增大至263.3±59.6μm,CIS处理组减小至179.6±30.3μm,β₁整合素阻断组减小更为显著,平均直径为127.0±22.2μm(n=50,P<0.05);悬滴法形成的EB大小不受阻断影响,但无法形成对照组中典型的致密原始内胚层壳状结构,扫描电镜显示阻断组EB表面呈纤毛状,缺乏对照组的光滑ECM涂层,提示该相互作用是EB结构形成的必需条件。
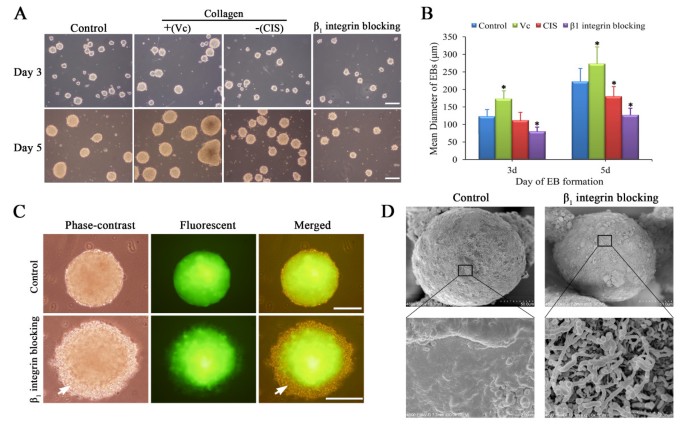
实验所用关键产品:BD Pharmingen的β₁整合素阻断抗体、Sigma的抗坏血酸、Sigma的顺式-4-羟基-D-脯氨酸。
3.4 心脏分化能力评估
实验目的为明确阻断I型胶原/β₁整合素相互作用对miPSC来源EB心脏分化潜能的影响。方法细节为将分化第5天的EB接种于明胶包被板,从分化第6天开始每日观察自发搏动EB的比例,第21天通过免疫染色检测心肌肌钙蛋白T(cTnT)的表达,采用半定量RT-PCR和实时定量PCR检测心脏相关转录因子及结构基因的表达。结果解读显示,阻断组的自发搏动EB比例显著低于对照组,在分化第16天达到平台期时,阻断组比例为18.0±3.0%,对照组为33.8±4.4%(n=3,P<0.05);免疫染色显示阻断组心肌肌钙蛋白T阳性细胞数量减少,肌丝排列紊乱;心脏相关转录因子(GATA-4、Nkx2.5、Mef2c)及结构基因(α-MHC、MLC2a、MLC2v)的mRNA表达均显著下调(n=3,P<0.05),提示该相互作用的阻断显著抑制了miPSC的心脏分化能力。
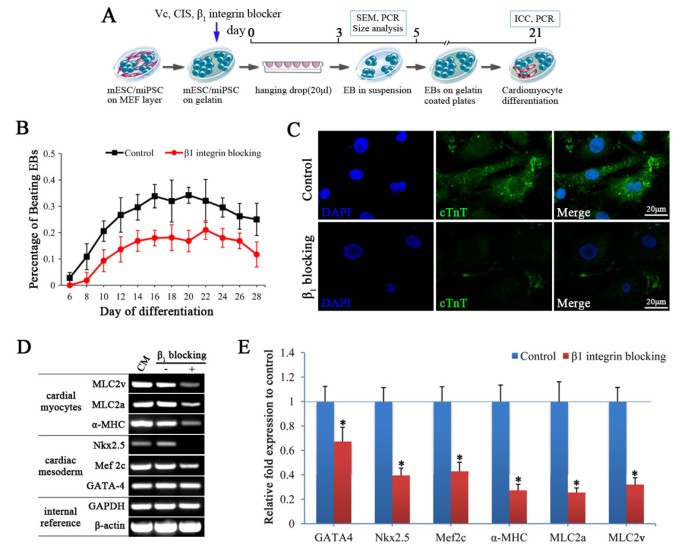
实验所用关键产品:Abcam的心肌肌钙蛋白T抗体、Takara的RT-PCR相关试剂。
4. Biomarker研究及发现成果
本研究涉及的Biomarker为I型胶原(Col1A1)和β₁整合素(Itgb1),属于调控性功能性Biomarker,其筛选与验证遵循“时序表达分析→功能阻断验证→分化表型关联”的完整逻辑链条。
Biomarker定位方面,I型胶原与β₁整合素作为EB形成及心脏分化的关键调控分子,筛选逻辑为通过转录组分析(RT-PCR)在EB形成过程中筛选出协同上调的分子对,再通过功能阻断实验验证其对EB结构、生长及心脏分化的调控作用。研究过程详述:该Biomarker的来源为miPSC来源的EB细胞,验证方法包括半定量RT-PCR、实时定量PCR检测mRNA的时序表达,免疫染色检测蛋白表达,以及功能阻断实验验证其生物学功能;特异性表现为,I型胶原与β₁整合素仅在EB形成的关键阶段(分化第3天)显著上调表达,而未分化细胞中I型胶原不表达;敏感性方面,阻断该相互作用后,EB的大小、结构及心脏分化能力均出现显著变化,提示该分子对的表达变化与EB的功能状态高度相关。核心成果提炼:I型胶原/β₁整合素相互作用是miPSC来源EB生长及心脏分化的必需条件,阻断该相互作用可导致EB大小减小、壳状结构缺失,心脏分化能力显著降低;其创新性在于首次明确了该相互作用在miPSC心脏分化的EB形成过程中的核心调控作用,为优化干细胞心脏分化的微环境提供了直接的靶点;统计学结果显示,EB直径测量的样本量n=50,P<0.05;自发搏动比例检测的样本量n=3,P<0.05;基因表达检测的样本量n=3,P<0.05。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。