Low physiologic oxygen tensions reduce proliferation and differentiation of human multipotent mesenchymal stromal cells
低生理氧张力会降低人多能间充质干细胞的增殖和分化。
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2010 | 起止号: | 2010 Jan 28;11:11 |
| doi: | 10.1186/1471-2121-11-11 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Low physiologic oxygen tensions reduce proliferation and differentiation of human multipotent mesenchymal stromal cells;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:间充质基质细胞(MSC)生物学、干细胞微环境与再生医学。
间充质基质细胞是一类具有多向分化潜能和免疫调节功能的成体干细胞,1995年首次被报道可体外扩增用于临床治疗,2002年成功应用于儿童成骨不全症的再生治疗,2004年开启了其在移植物抗宿主病免疫调节治疗中的应用,此后成为再生医学领域的研究热点。当前研究聚焦于MSC的微环境调控机制,尤其是骨髓微环境的生理低氧(1%-7%)对MSC功能的影响,但现有研究存在结论矛盾:部分研究认为低氧促进MSC增殖和分化,另一部分研究则得出相反结论,核心争议源于实验培养基的差异(胎牛血清vs临床级血小板裂解液),且缺乏针对临床级培养体系下MSC的系统研究,这一空白限制了MSC临床培养条件的优化与转化应用。
针对上述研究空白,本研究采用临床级血小板裂解液培养基,系统评估1%、3%、5%、21%氧浓度对人MSC的形态、增殖、染色体稳定性、免疫表型和分化能力的影响,旨在明确生理低氧张力对临床级培养MSC的生物学特性调控,为MSC的临床应用提供实验依据。
2. 文献综述解析
作者按研究结论的矛盾性对现有文献分类,重点关注低氧对MSC增殖和分化的调控作用,同时分析实验条件(培养基、氧浓度、物种)对结果的影响,核心逻辑为“矛盾结论归因于实验体系差异”。
支持低氧促进MSC增殖和分化的研究多采用胎牛血清培养基,发现低氧可通过激活缺氧诱导因子-1α(HIF-1α)通路增强MSC的成骨、成脂分化能力,部分研究还观察到低氧延长MSC体外寿命,这类研究的优势在于揭示了低氧调控MSC功能的分子通路,为机制研究提供基础,但局限性在于胎牛血清不符合临床GMP标准,结果难以直接转化。支持低氧抑制MSC功能的研究更贴近体内生理氧浓度,发现低氧降低MSC增殖速率和分化能力,优势在于真实模拟骨髓微环境,但局限性在于样本量小且未涉及临床级血小板裂解液体系,无法为临床培养提供直接指导。
本研究的创新价值在于首次在临床级血小板裂解液培养基中设置多氧浓度梯度,明确了生理低氧对人MSC增殖和分化的抑制作用,解决了之前研究因培养基差异导致的结果矛盾;同时通过高分辨率矩阵比较基因组杂交(array-CGH)验证了低氧培养下MSC的染色体稳定性,为临床MSC培养的氧浓度优化提供安全性依据,弥补了现有研究在临床转化层面的不足。
3. 研究思路总结与详细解析
本研究整体框架为“分离培养MSC→多氧浓度分组处理→多维度生物学特性检测→功能机制分析”,研究目标是明确生理低氧张力对临床级培养人MSC的生物学特性影响,核心科学问题是低氧如何调控MSC的增殖、分化和干细胞特性,技术路线遵循“假设→实验验证→结论总结”闭环逻辑,即假设生理低氧维持MSC的静息干细胞状态(低增殖、低分化),通过多维度实验验证该假设并分析分子机制。
3.1 MSC分离培养与氧浓度分组处理
实验目的是获得高纯度人MSC并建立不同氧浓度的临床级培养体系。方法细节为从儿童骨髓样本中分离MSC,采用含5%人新鲜冷冻血浆、10^7/ml血小板的LG-DMEM培养基培养,细胞融合至80%时传代,将相同供体的MSC分别置于21%、5%、3%、1%氧浓度的培养箱中适应至少1周。结果解读显示,成功获得形态均一的纺锤形MSC,不同氧浓度下MSC形态存在供体差异:10名供体中3名的MSC在1%氧下可正常生长形成融合单层,7名的MSC在1%氧下1周内死亡,表明MSC对低氧的耐受性具有个体差异。
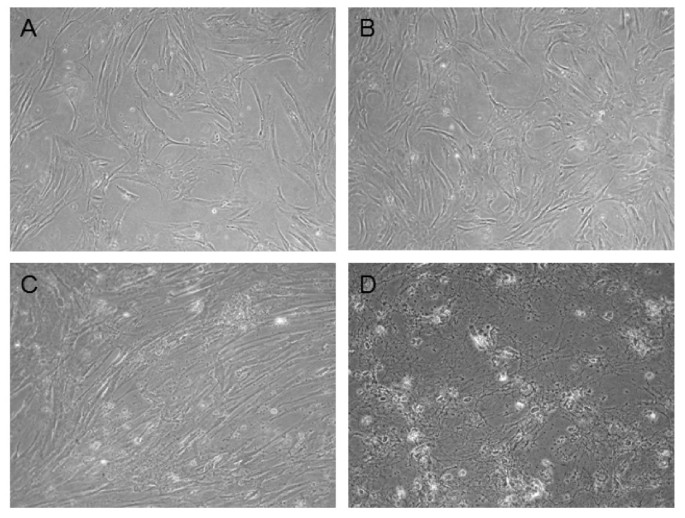
产品关联:实验所用关键产品:Lonza的LG-DMEM培养基、University of Tübingen血库的血小板和新鲜冷冻血浆、Lonza的0.5%胰蛋白酶。
3.2 低氧对MSC免疫表型与HIF-1α表达的影响
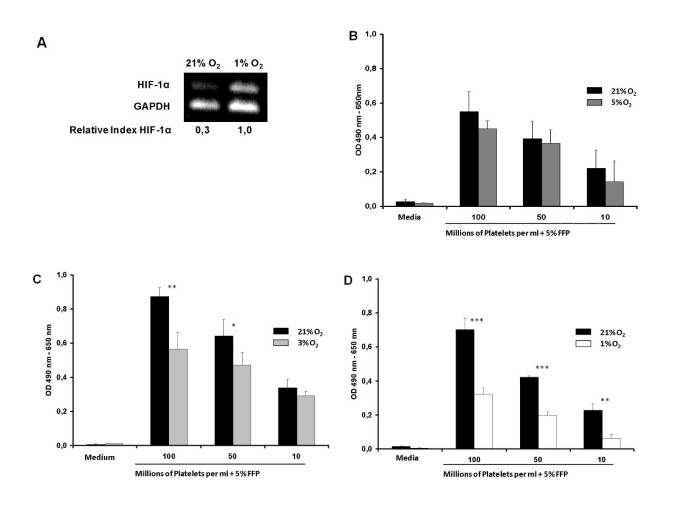
实验目的是验证低氧对MSC免疫表型的影响,同时确认低氧环境是否成功激活HIF-1α通路。方法细节为MSC在不同氧浓度下培养14天后,用流式细胞术检测表面标志物(CD73、CD90、CD105、CD45等)表达,用半定量反转录PCR(RT-PCR)检测HIF-1α的mRNA表达水平,以甘油醛-3-磷酸脱氢酶(GAPDH)为内参归一化。结果解读显示,不同氧浓度下MSC的免疫表型无显著差异,均符合国际细胞治疗协会的MSC标准(高表达CD73、CD90、CD105,低表达CD45、CD34、HLA-DR);1%氧浓度下HIF-1α的mRNA表达较21%氧升高超过3倍(n=3,P<0.001),表明低氧环境成功激活MSC的HIF-1α通路。
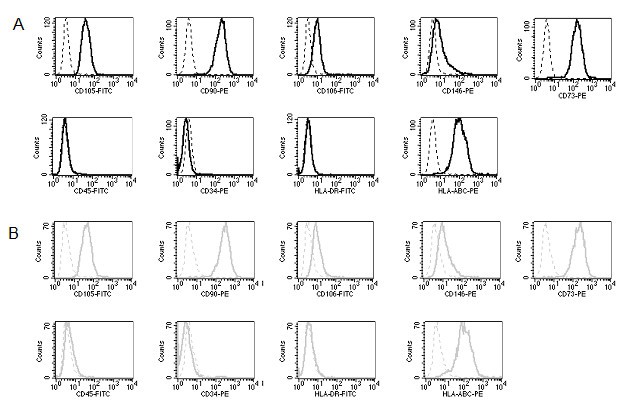
产品关联:实验所用关键产品:BD的流式抗体(抗CD45-FITC、抗CD34-PE等)、Ancell的CD105-FITC抗体、Serotec的CD90-PE抗体、PEQLAB的peqGOLD TriFast™ RNA提取试剂、Invitrogen的反转录试剂盒。
3.3 低氧对MSC增殖与细胞周期的调控
实验目的是明确低氧对MSC增殖能力的影响及细胞周期变化规律。方法细节为用MTS增殖检测试剂盒检测不同氧浓度下MSC培养7天后的增殖活性(以OD值表示),用流式细胞术结合碘化丙啶染色分析细胞周期分布。结果解读显示,随着氧浓度降低,MSC增殖活性显著下降,1%氧下的OD值显著低于21%氧(n=3,P<0.001);细胞周期分析显示,1%氧下MSC的G2/M期细胞比例为1.37%,显著低于21%氧下的2.50%(n=3,P<0.05),表明低氧诱导MSC停滞在G1期,抑制细胞增殖。
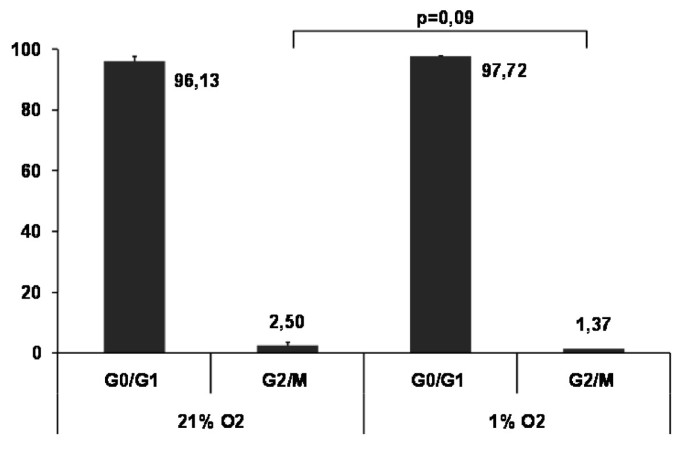
产品关联:实验所用关键产品:Promega的MTS增殖检测试剂盒、BD的碘化丙啶/RNase染色缓冲液、BD的FACS Calibur流式细胞仪。
3.4 低氧对MSC染色体稳定性的影响
实验目的是评估低氧培养对MSC遗传稳定性的影响,为临床应用安全性提供依据。方法细节为MSC在21%和1%氧浓度下培养4周后提取基因组DNA,用高分辨率array-CGH检测染色体异常,以健康志愿者外周血单个核细胞DNA为对照。结果解读显示,两种氧浓度下培养的MSC均未检测到染色体异常,仅存在正常基因组多态性(n=3),表明低氧培养不会导致MSC染色体不稳定,具有良好的临床应用安全性。
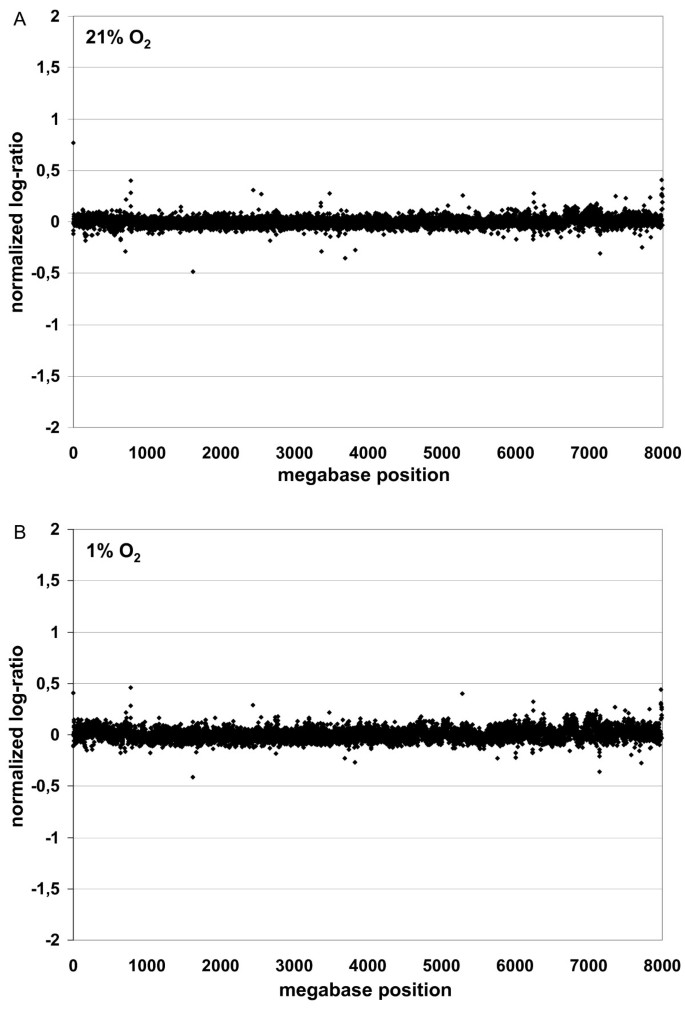
产品关联:文献未提及具体实验产品,领域常规使用商业化array-CGH芯片(如Agilent或Illumina芯片)及配套数据分析软件。
3.5 低氧对MSC分化能力的调控
实验目的是明确低氧对MSC成脂、成骨分化能力的影响及氧浓度的剂量依赖性效应。方法细节为将MSC置于成脂或成骨诱导培养基中,在21%、1%、3%氧浓度下培养14天,成脂分化用油红O染色检测脂滴形成,成骨分化用茜素红S染色检测钙沉积。结果解读显示,21%氧下MSC成脂分化明显,可见大量红色脂滴,1%氧下成脂分化显著减弱(n=3,P<0.01);21%氧下MSC成骨分化可见大量红色钙沉积,1%氧下无钙沉积,而3%氧下成骨分化与21%氧无显著差异,表明低氧严重抑制MSC成脂和成骨分化能力,且氧浓度从1%提升至3%可完全恢复成骨分化能力。
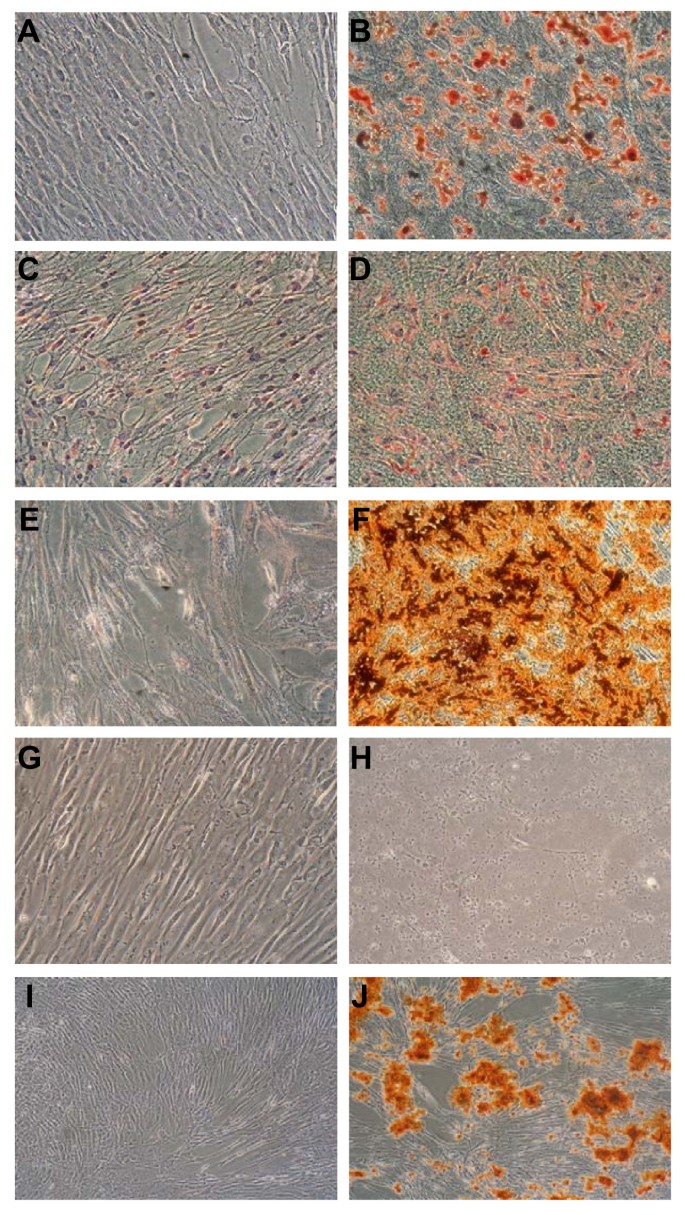
产品关联:实验所用关键产品:Sigma的地塞米松、吲哚美辛、β-甘油磷酸钠、茜素红S染色液、油红O染色液。
4. Biomarker研究及发现成果解析
本文未聚焦特定疾病诊断或预后Biomarker,而是将HIF-1α作为低氧响应的功能Biomarker,研究其在低氧调控MSC功能中的作用,同时明确氧浓度作为MSC功能调控的关键环境参数,可作为MSC培养条件优化的核心指标。
HIF-1α被定位为MSC低氧暴露的功能Biomarker,筛选与验证逻辑为:低氧环境诱导MSC中HIF-1α表达上调→验证HIF-1α表达与MSC增殖抑制、分化减弱的关联→明确HIF-1α在低氧调控MSC功能中的作用。HIF-1α的来源为MSC的mRNA,验证方法为半定量RT-PCR,特异性数据显示1%氧浓度下HIF-1α相对表达量较21%氧升高3倍以上(n=3,P<0.001),具有显著的低氧响应特异性;MSC对氧浓度变化具有高度敏感性,3%氧浓度即可逆转1%氧对成骨分化的抑制作用。
核心成果提炼:HIF-1α的上调与MSC增殖抑制、分化减弱直接相关,首次在临床级培养基中明确了HIF-1α通路在低氧调控MSC功能中的核心作用;同时揭示了氧浓度对MSC分化的剂量依赖性效应,为MSC临床培养和再生医学应用提供了关键氧浓度参数;统计学结果显示,HIF-1α表达差异P<0.001,增殖差异P<0.001,分化差异P<0.01,所有数据均具有显著统计学意义。此外,本文验证了低氧培养下MSC的染色体稳定性,为MSC临床应用提供了安全性保障,进一步提升了研究成果的转化价值。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。