Regulation of actin cytoskeleton architecture by Eps8 and Abi1
Eps8 和 Abi1 对肌动蛋白细胞骨架结构的调控
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2005 | 起止号: | 2005 Oct 14;6:36 |
| doi: | 10.1186/1471-2121-6-36 | 研究方向: | 信号转导、细胞生物学 |
文献解析
1. 领域背景与文献引入
文献英文标题:Regulation of actin cytoskeleton architecture by Eps8 and Abi1;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学(肌动蛋白细胞骨架调控与胚胎发育)
肌动蛋白细胞骨架的重塑是调控细胞形态、迁移、黏附及胚胎发育等生理过程的核心机制,由肌动蛋白结合蛋白(如封端蛋白、成核因子)和Rho家族GTPases(如Rac、RhoA)协同维持动态平衡。领域共识:Rac主要诱导膜褶皱和丝足形成,RhoA调控应力纤维组装,二者共同介导细胞的定向运动。当前研究已明确部分肌动蛋白结合蛋白的体外生化功能,但这些蛋白在体内形成多蛋白复合物协同调控肌动蛋白架构的具体机制仍存在空白;同时,Eps8作为EGF受体的底物蛋白,被报道可作为支架蛋白激活Rac,且其C端片段具有体外肌动蛋白barbed-end封端活性,但其在体内的功能及与其他蛋白的协同作用尚未完全阐明。
针对上述研究空白,本研究以哺乳动物高迁移性细胞系和爪蟾胚胎为模型,系统解析Eps8与Abi1协同调控肌动蛋白细胞骨架的分子机制,同时探究其通过招募Dishevelled(Dsh)参与非经典Wnt信号通路、调控胚胎原肠运动的功能,为肌动蛋白细胞骨架的体内调控机制及胚胎发育的分子基础提供新的实验证据。
2. 文献综述解析
本文综述部分以“肌动蛋白细胞骨架调控的分子网络-Eps8家族的功能特性-现有研究的局限性”为逻辑主线,系统梳理了领域内的研究进展,并明确了本文的研究切入点。
现有研究可分为三个方向:一是肌动蛋白细胞骨架的整体调控网络,明确了肌动蛋白结合蛋白通过调控肌动蛋白的组装、解聚、分支和束化维持细胞骨架的动态平衡,Rho家族GTPases作为上游信号分子介导细胞骨架的重塑;二是Eps8家族的功能研究,发现Eps8可作为支架蛋白形成包含p85、Abi1、Sos1的复合物激活Rac,且其C端片段具有体外肌动蛋白barbed-end封端活性,该活性依赖于Abi1的结合;三是Eps8与Wnt信号通路的关联,报道了Eps8与Dsh的相互作用,但未明确该相互作用的功能意义。现有研究的优势在于建立了Eps8的体外功能体系,但其局限性在于缺乏体内模型的验证,尤其是Eps8与Abi1协同调控肌动蛋白架构的体内机制,以及其在胚胎发育中的功能尚未被揭示。
与现有研究相比,本文的创新点在于首次在体内模型(爪蟾胚胎)中验证了Eps8与Abi1的协同作用对不同肌动蛋白结构的调控,明确了该过程存在Rac依赖和非依赖两种机制;同时,揭示了Eps8通过招募Dsh到细胞膜和肌动蛋白丝参与非经典Wnt信号通路,进而调控胚胎原肠运动中的收敛延伸运动,填补了Eps8体内功能及与Wnt信号通路关联机制的研究空白。
3. 研究思路总结与详细解析
本研究的整体框架为“体外细胞模型验证→体内胚胎模型解析→分子机制探究→发育功能验证”,研究目标是明确Eps8在体内调控肌动蛋白细胞骨架的分子机制及在胚胎发育中的功能,核心科学问题是Eps8如何通过与Abi1、Dsh的相互作用调控肌动蛋白架构及细胞运动,技术路线遵循“假设-实验验证-结论”的闭环逻辑,通过多模型、多技术手段系统解析Eps8的功能。
3.1 哺乳动物细胞中Eps8对肌动蛋白架构的调控
实验目的:验证Eps8过表达对高迁移性哺乳动物细胞肌动蛋白骨架的调控作用。
方法细节:选用B16F1小鼠黑色素瘤细胞、MDA-MB231人乳腺癌细胞及其高转移亚系MDA-MB231BO,通过脂质体转染法将c-myc标签的Eps8表达载体导入细胞,培养后用4%多聚甲醛固定细胞,采用鬼笔环肽染色标记肌动蛋白细胞骨架,通过免疫荧光染色检测Eps8的亚细胞定位,使用共聚焦显微镜观察细胞形态及蛋白分布。
结果解读:超过90%的转染细胞形成大量丝足样结构,这些结构从细胞的侧面和背侧伸出,Eps8定位于丝足样结构的全长区域,且在结构尖端富集;约50%的MDA-MB231BO细胞还形成长蛇状的胞质肌动蛋白缆线,而该结构在B16F1和MDA-MB231亲本细胞中未观察到,提示Eps8对肌动蛋白架构的调控具有细胞系特异性。
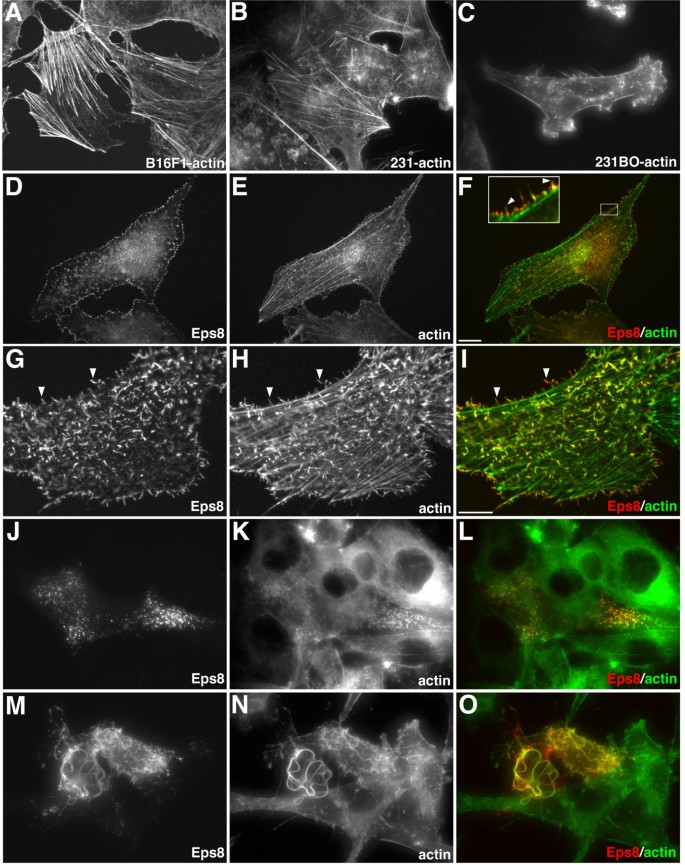
产品关联:文献未提及具体实验产品,领域常规使用c-myc单克隆抗体、Alexa Fluor标记的鬼笔环肽、共聚焦激光扫描显微镜等试剂/仪器。
3.2 Abi1对Eps8调控肌动蛋白架构的协同作用
实验目的:验证Abi1与Eps8的相互作用对肌动蛋白骨架重塑的调控效应,明确该作用的分子依赖关系。
方法细节:在B16F1、MDA-MB231和MDA-MB231BO细胞中,分别共转染Eps8-myc与Abi1-GFP表达载体,或Eps8-myc与不能结合Eps8的Abi1突变体(Abi1DY-GFP)表达载体,固定细胞后通过免疫荧光染色检测蛋白定位,观察肌动蛋白细胞骨架的变化。
结果解读:共转染Eps8与野生型Abi1的细胞中,胞质内形成大量无分支的肌动蛋白缆线,Eps8与Abi1共定位于这些缆线的全长区域;而转染Eps8与Abi1DY的细胞中,Abi1DY无法与Eps8共定位,且不能诱导肌动蛋白缆线形成,说明Eps8与Abi1的相互作用是调控肌动蛋白缆线形成的必要条件。
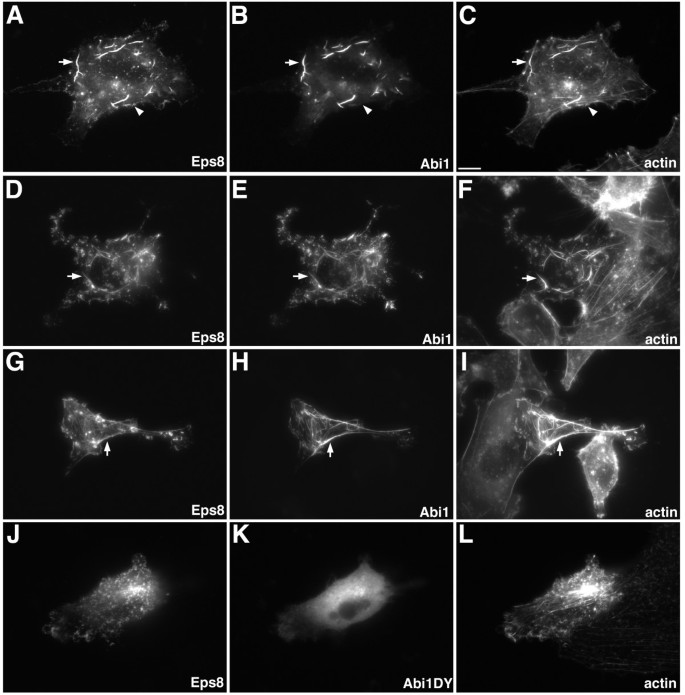
产品关联:文献未提及具体实验产品,领域常规使用GFP多克隆抗体、免疫荧光染色试剂盒等试剂/仪器。
3.3 爪蟾胚胎中Eps8对肌动蛋白架构的体内调控
实验目的:在脊椎动物体内模型中验证Eps8对肌动蛋白细胞骨架的调控作用,明确其在不同细胞类型中的功能差异。
方法细节:制备爪蟾囊胚期动物帽外植体,通过显微注射法将Eps8-myc mRNA注入外植体细胞,培养至原肠胚期后固定细胞,采用免疫荧光染色检测Eps8的定位,同时用鬼笔环肽染色标记肌动蛋白细胞骨架,通过共聚焦显微镜观察细胞内肌动蛋白的分布变化。
结果解读:在爪蟾动物帽的表层上皮细胞中,Eps8表达导致肌动蛋白在细胞间连接处显著积累;在深层细胞中,Eps8诱导胞质内形成大量肌动蛋白缆线,且Eps8定位于这些肌动蛋白结构上,说明Eps8在体内可调控不同细胞类型的肌动蛋白架构。
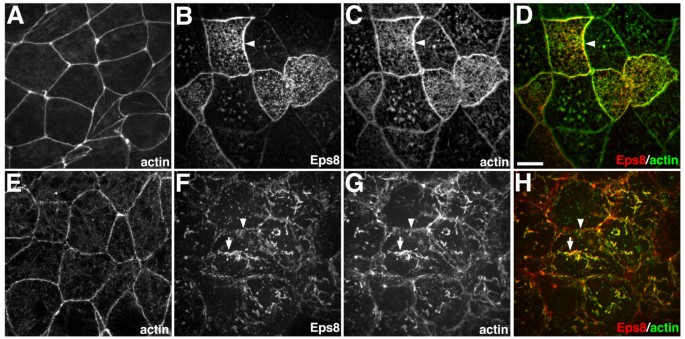
产品关联:文献未提及具体实验产品,领域常规使用mRNA体外合成试剂盒、显微注射系统、共聚焦显微镜等试剂/仪器。
3.4 Abi1与Eps8在爪蟾胚胎中的协同作用及Rac独立性验证
实验目的:验证Abi1在爪蟾胚胎中对Eps8功能的调控效应,明确该过程是否依赖Rac的激活。
方法细节:在爪蟾动物帽外植体中共注射Eps8-myc与Abi1-GFP mRNA,固定后通过免疫荧光染色检测肌动蛋白结构及内源性Rac的定位;同时,共注射Eps8-myc、Abi1-GFP与显性负性RacN17 mRNA,观察肌动蛋白结构的变化。
结果解读:共表达Eps8与Abi1的表层上皮细胞顶膜形成星状肌动蛋白结构,该结构由放射状的肌动蛋白棘突从中心焦点伸出,Eps8与Abi1共定位于星状结构上;内源性Rac未被招募到该星状结构,且显性负性RacN17不抑制星状结构的形成,说明Eps8与Abi1协同调控肌动蛋白架构的过程不依赖Rac的激活。
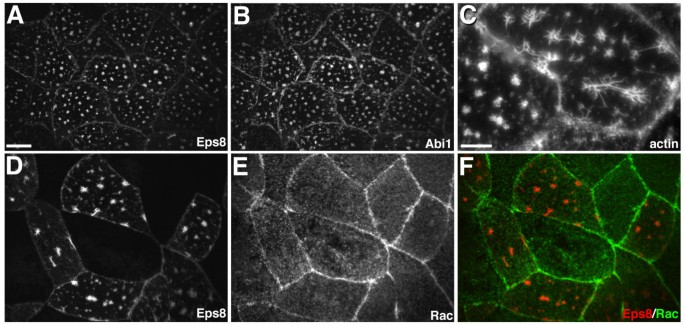
产品关联:文献未提及具体实验产品,领域常规使用Rac单克隆抗体、显性负性基因表达载体等试剂/仪器。
3.5 肌动蛋白调控蛋白在Eps8/Abi1诱导结构中的招募分析
实验目的:解析Eps8与Abi1协同调控肌动蛋白架构的下游分子机制,明确关键调控蛋白的参与情况。
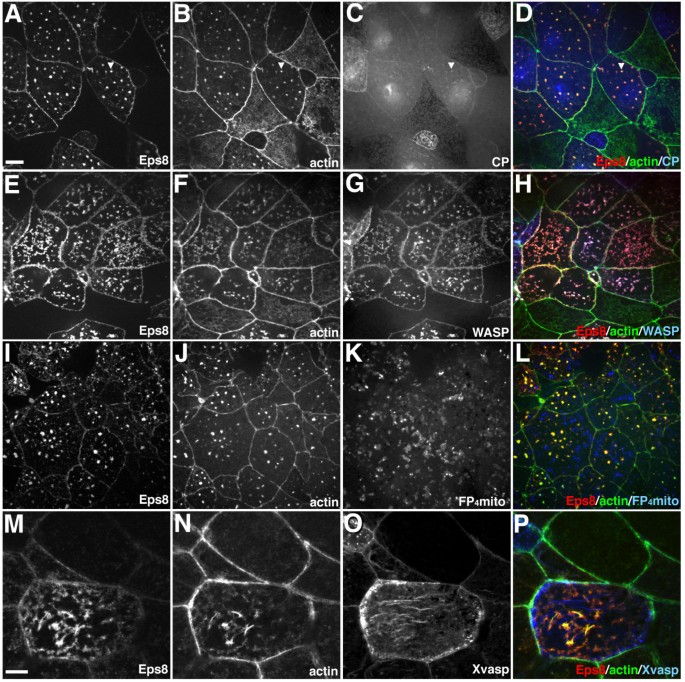
方法细节:在爪蟾动物帽外植体中,分别共注射Eps8-myc、Abi1-GFP与封端蛋白(CP)α/β亚基的GFP表达载体,或N-WASP-GFP、显性负性Ena/VASP突变体(FP4-mito-GFP)、Xvasp-GFP表达载体,固定后通过免疫荧光染色检测这些蛋白与Eps8/Abi1诱导的肌动蛋白结构的共定位情况。
结果解读:封端蛋白过表达不影响Eps8/Abi1诱导的星状肌动蛋白结构形成,且仅少量封端蛋白共定位于该结构;N-WASP被显著招募到星状结构上,但显性负性N-WASP不抑制星状结构的形成;显性负性Ena/VASP突变体或过表达Xvasp均不影响星状结构的形成,且Xvasp不与该结构共定位,提示Eps8与Abi1可能通过招募肌动蛋白成核因子而非依赖封端活性或Ena/VASP功能调控肌动蛋白架构。
产品关联:文献未提及具体实验产品,领域常规使用GFP标记的肌动蛋白调控蛋白载体、免疫荧光染色试剂等。
3.6 Eps8对Dsh的招募及多蛋白复合物形成验证
实验目的:验证Eps8对Dsh亚细胞定位的调控作用,明确Eps8、Abi1与Dsh是否能形成三蛋白复合物。
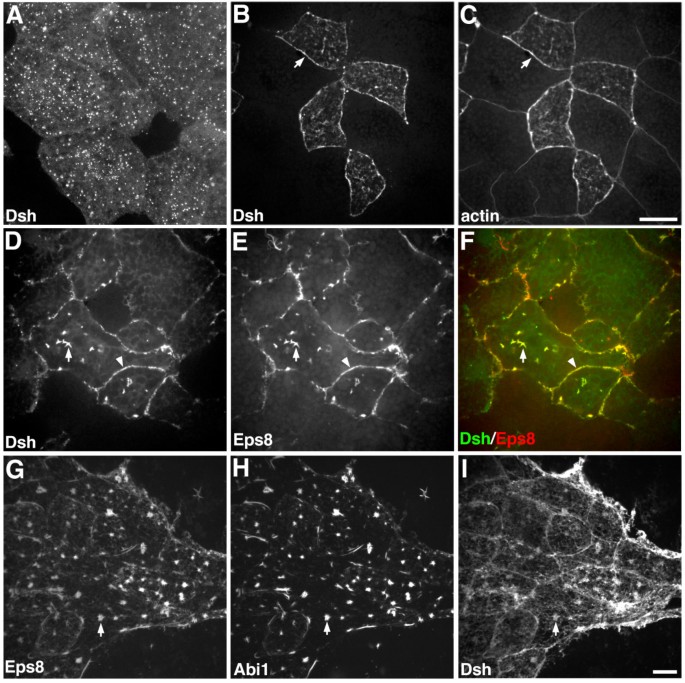
方法细节:在爪蟾动物帽外植体中,单独注射Dsh-GFP mRNA,或共注射Dsh-GFP与Eps8-myc mRNA,或共注射Eps8-myc、Abi1-GFP与Dsh-flag mRNA,固定后通过免疫荧光染色检测蛋白的亚细胞定位。
结果解读:单独表达Dsh时,其呈点状胞质分布;共表达Eps8后,Dsh被显著招募到细胞膜和胞质肌动蛋白丝上,与Eps8共定位;三者共表达时,Eps8、Abi1与Dsh在细胞内存在共定位区域,说明三者可在体内形成三蛋白复合物,提示Eps8可能通过调控Dsh的定位影响其功能。
产品关联:文献未提及具体实验产品,领域常规使用flag单克隆抗体、Dsh多克隆抗体等试剂/仪器。
3.7 爪蟾Eps8的表达模式及原肠运动功能验证
实验目的:明确爪蟾Eps8(XEps8)的时空表达模式,验证其在胚胎原肠运动中的功能。
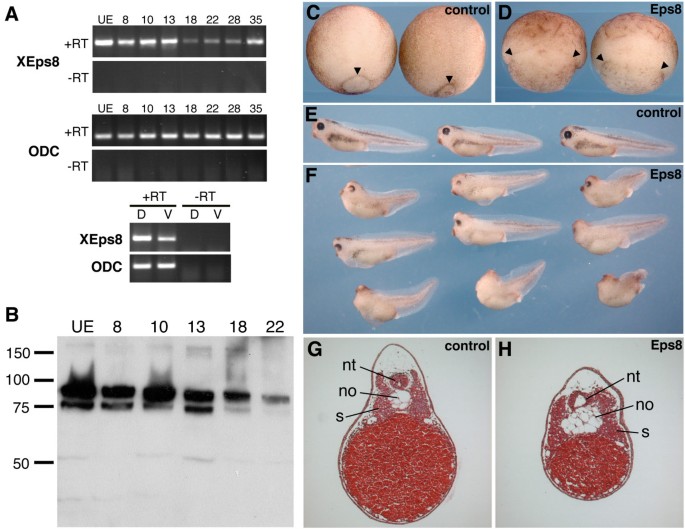
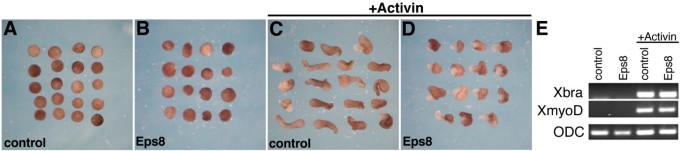
方法细节:通过RT-PCR和Western blot检测XEps8在爪蟾不同发育阶段的表达水平;向爪蟾4细胞期胚胎的背侧卵裂球注射Eps8 mRNA,观察胚胎的发育表型,通过组织学切片分析原肠运动的缺陷;同时,制备激活素处理的动物帽外植体,验证Eps8对细胞收敛延伸运动的影响。
结果解读:XEps8为母源表达,且在原肠胚期背侧边缘区的表达量高于腹侧;过表达Eps8导致胚胎原肠胚期胚孔闭合延迟、组织褶皱,tadpole期出现轴缩短、小头、独眼等表型;组织学分析显示脊索变宽、神经管和体节紊乱;激活素处理的动物帽外植体伸长被抑制,但中胚层标记基因Xbra和XmyoD的表达不受影响,说明Eps8通过抑制细胞的收敛延伸运动影响胚胎原肠运动。
产品关联:文献未提及具体实验产品,领域常规使用RT-PCR引物、组织学染色试剂盒、激活素蛋白等试剂/仪器。
4. Biomarker研究及发现成果解析
本文未涉及疾病诊断或预后相关的传统Biomarker研究,而是鉴定了Eps8作为肌动蛋白细胞骨架调控和非经典Wnt信号通路中的关键功能分子,其功能关联及调控机制为胚胎发育和细胞运动的研究提供了新的分子靶点。
Biomarker定位
本文中的功能分子Eps8属于“细胞骨架调控分子”类型,其筛选逻辑为“已知体外功能→体内模型验证→分子机制解析→发育功能验证”,通过细胞和胚胎模型的层层验证,明确了Eps8与Abi1、Dsh的相互作用对肌动蛋白架构及细胞运动的调控功能。
研究过程详述
Eps8的来源为细胞内源性表达或外源过表达,验证方法包括免疫荧光共定位、RT-PCR、Western blot、胚胎显微注射表型分析等;未涉及特异性与敏感性相关数据(文献未明确提供该数据,基于图表趋势推测)。
核心成果提炼
Eps8具有多效性的肌动蛋白调控功能,可单独诱导哺乳动物细胞形成丝足样结构,与Abi1协同诱导肌动蛋白缆线(细胞系)和星状结构(爪蟾胚胎)的形成,该过程存在Rac依赖和非依赖两种机制;Eps8通过招募Dsh到细胞膜和肌动蛋白丝参与非经典Wnt信号通路,进而抑制胚胎原肠运动中的收敛延伸运动;首次在体内模型中证明Eps8、Abi1与Dsh可形成三蛋白复合物,为非经典Wnt信号通路调控细胞运动的分子机制提供了新的实验证据。无统计学显著性数据(文献未明确提供该数据,基于图表趋势推测)。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。