Arf6 recruits the Rac GEF Kalirin to the plasma membrane facilitating Rac activation
Arf6 将 Rac 鸟苷酸交换因子 Kalirin 募集到质膜上,从而促进 Rac 活化。
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2007 | 起止号: | 2007 Jul 18;8:29 |
| doi: | 10.1186/1471-2121-8-29 | 靶点: | Arf6 |
文献解析
1. 领域背景与文献引入
文献英文标题:Arf6 recruits the Rac GEF Kalirin to the plasma membrane facilitating Rac activation;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学(小G蛋白信号通路与细胞骨架调控)
小G蛋白是细胞内信号转导网络的核心调控分子,其中Arf家族与Rho家族是参与膜运输和细胞骨架重塑的关键分支。Arf6作为Arf家族成员,主要负责质膜内吞循环运输与皮层肌动蛋白结构的动态调控;Rac1属于Rho家族,通过调控片状伪足与膜褶皱的形成,参与细胞迁移、粘附等重要生理过程。领域共识:两者在肌动蛋白重塑与膜运输事件中存在交叉调控,已有研究证实Arf6激活可诱导Rac1的激活,但Arf6调控Rac1功能的具体分子机制尚未完全阐明,缺乏直接的分子相互作用证据与明确的作用模式,这是当前领域未解决的核心问题。针对这一研究空白,本研究旨在解析Arf6与Rac1之间的关键调控分子与作用机制,填补小G蛋白交叉调控通路的分子细节空白,为细胞骨架调控的信号网络研究提供新的分子靶点与机制模型。
2. 文献综述解析
作者的综述逻辑以小G蛋白家族分类为核心维度,先分别阐述Arf6与Rac1的独立功能,再聚焦两者的交叉调控研究现状,系统梳理现有研究的结论、技术优势与局限性。现有研究的关键结论包括:Arf6与Rac1在质膜及循环内体存在共定位,Arf6的激活可触发Rac1的激活,部分研究推测Dock180/ELMO复合物可能参与这一过程;这些研究的技术优势在于通过细胞功能实验明确了两者的功能关联,为交叉调控提供了功能层面的证据,但局限性在于缺乏直接的分子相互作用数据,未揭示Arf6调控Rac1的具体中间分子与作用细节,且未关注GDP结合态Arf6在其中的潜在作用。本研究的创新价值在于,首次发现GDP结合态Arf6可通过与Rac鸟苷酸交换因子(GEF)Kalirin的血影蛋白重复区域直接结合,将Kalirin招募至膜结构,进而介导Rac1的激活,明确了Arf6调控Rac1的关键分子节点与具体作用模式,弥补了现有研究中分子机制的核心空白。
3. 研究思路总结与详细解析
本研究的整体框架为:以“Arf6调控Rac1的分子机制”为核心科学问题,通过酵母双杂交筛选候选互作蛋白,结合生化实验验证分子结合的特异性与结合态偏好,再通过细胞定位实验与功能实验验证其生物学功能,最终利用显性负突变实验确认通路的依赖性,形成“筛选-验证-功能-机制”的完整研究闭环。
3.1 互作蛋白筛选与结合特异性验证
实验目的:筛选与Arf6相互作用的蛋白分子,并验证两者结合的特异性及对Arf6结合态的偏好性。
方法细节:采用酵母双杂交系统筛选人胎儿脑cDNA文库,获得Kalirin的血影蛋白重复区域5;通过GST pull-down实验,在COS7细胞中转染HA标签的Arf1、Arf5、Arf6,与GST融合的Kalirin血影蛋白重复4-7片段孵育,检测结合情况;同时在COS7细胞中进行免疫共沉淀实验,共转染FLAG标签的Kalirin5与不同结合态的Arf6突变体(野生型Arf6、激活态Arf6Q67L、GDP结合态Arf6T27N),验证结合偏好;此外通过共表达Arf6的鸟苷酸交换因子EFA6、能量耗竭处理(50mM 2-脱氧葡萄糖+0.02%叠氮化钠)进一步验证结合态特异性。
结果解读:GST pull-down实验显示仅Arf6可与Kalirin的血影蛋白重复区域结合,Arf1、Arf5无结合信号(图1B);免疫共沉淀实验显示野生型Arf6与GDP结合态Arf6T27N可与Kalirin5共沉淀,激活态Arf6Q67L则无法结合(n=3,P<0.01)(图1C);共表达EFA6可显著降低Arf6与Kalirin5的结合水平,能量耗竭处理则随时间延长增强两者结合(n=3,P<0.05)(图1D、E);同时发现Trio的血影蛋白重复区域5-6也可与GDP结合态Arf6结合(图2),说明GDP结合态Arf6可特异性结合含血影蛋白重复区域的Rho家族鸟苷酸交换因子。
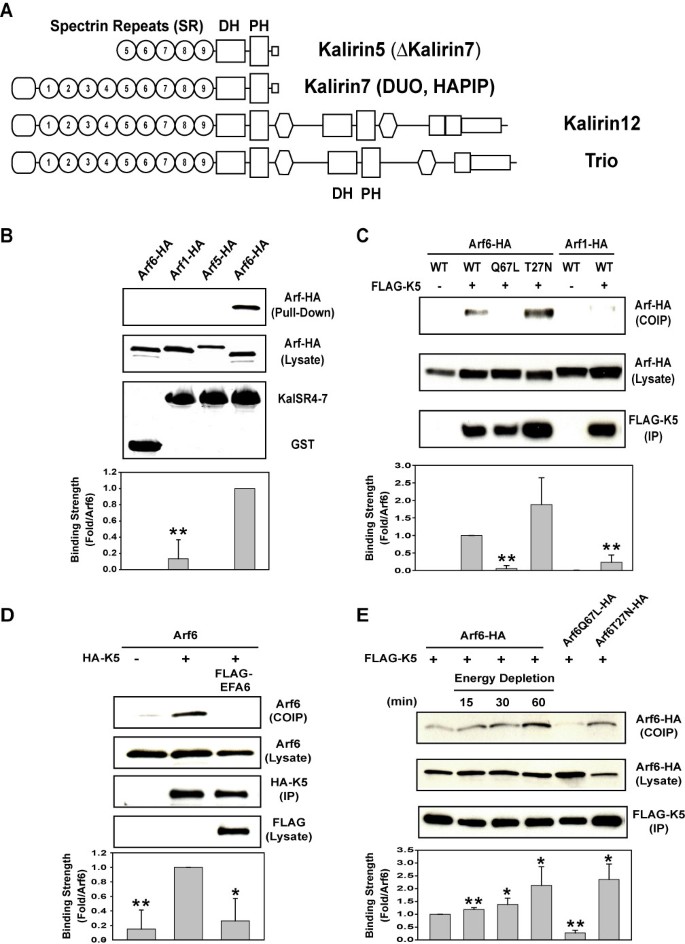
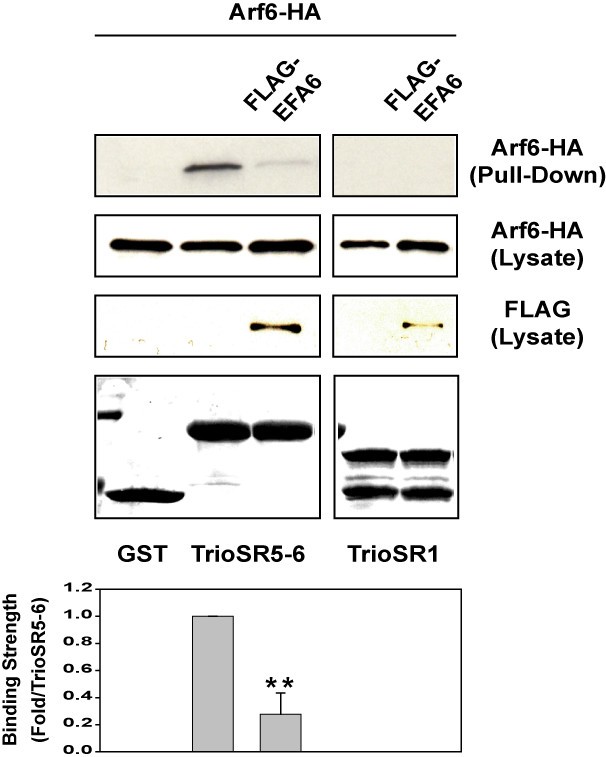
产品关联:文献未提及具体实验产品,领域常规使用GST融合蛋白纯化试剂盒、免疫共沉淀特异性抗体、Western blot检测试剂等。
3.2 细胞内定位与膜招募功能验证
实验目的:验证Arf6对Kalirin5细胞内定位的调控作用,明确其膜招募的生物学效应。
方法细节:在HeLa细胞中转染FLAG标签的Kalirin5、血影蛋白重复区域5(SR5)及不同Arf6突变体,免疫荧光染色后通过共聚焦显微镜观察蛋白定位;在COS7细胞中进行亚细胞组分分离,检测Kalirin5在膜组分中的比例变化。
结果解读:单独表达Kalirin5时,仅约7%的蛋白定位于质膜,其余分布于细胞质;共表达野生型Arf6后,Kalirin5的质膜定位比例提升至约14%(n=3,P<0.01),且细胞膜褶皱显著增强(图3B、C);共表达GDP结合态Arf6T27N时,Kalirin5被招募至管状内体膜,质膜定位减少,且膜褶皱被抑制(图3D);共表达EFA6则降低Kalirin5的质膜定位(图3E),说明GDP结合态Arf6负责将Kalirin招募至膜结构,而Arf6的激活是后续功能实现的必要条件。
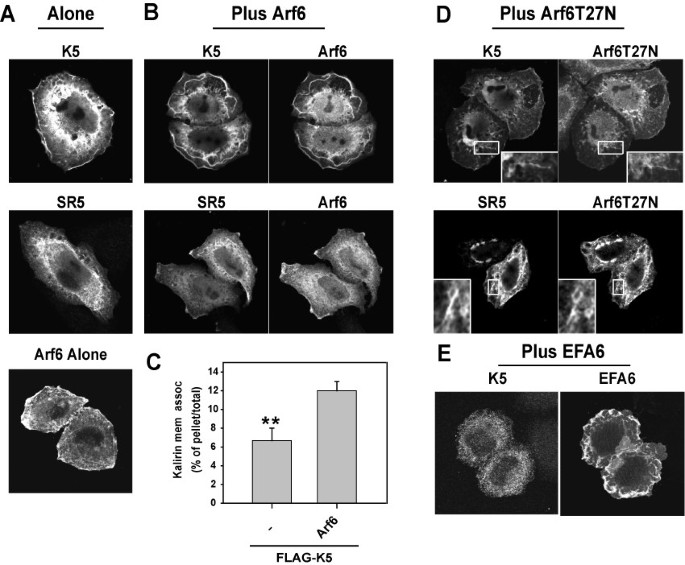
产品关联:文献未提及具体实验产品,领域常规使用免疫荧光染色试剂盒、亚细胞组分分离试剂、激光共聚焦显微镜等。
3.3 Rac1激活的功能依赖性验证
实验目的:验证Arf6通过Kalirin5调控Rac1激活的功能关联,确认通路的特异性。
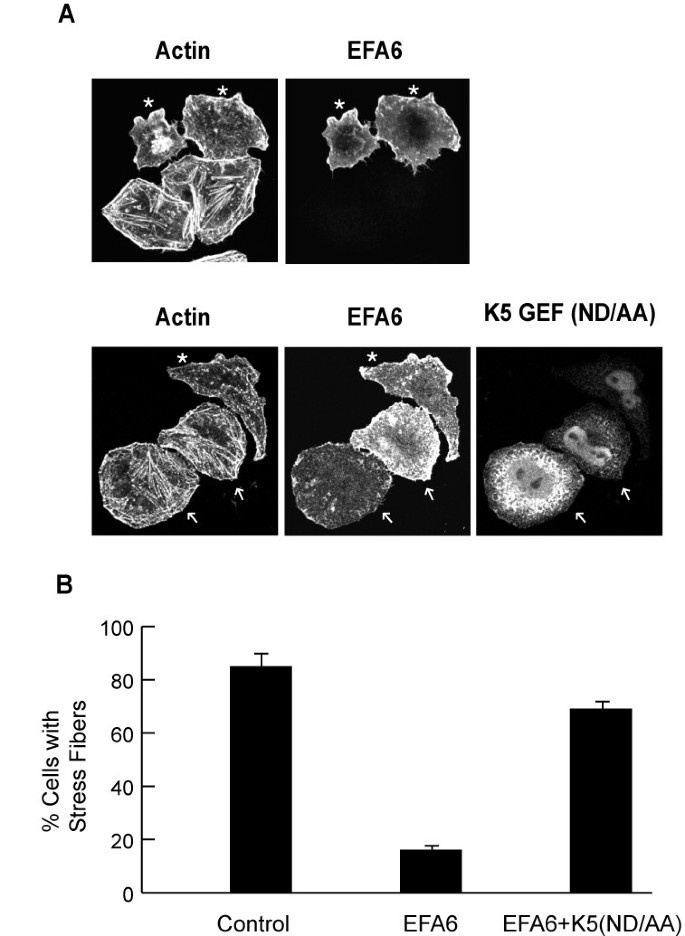
方法细节:在COS7细胞中转染AU5标签的Rac1,与Kalirin5、不同Arf6突变体共转染,通过GST-Pak1-CRIB pull-down实验检测活化态Rac1(Rac1-GTP)的水平;同时在HeLa细胞中转染Arf6的鸟苷酸交换因子EFA6与Kalirin5的显性负突变体(N813A/D814A,催化活性缺失),观察细胞骨架的变化并统计具有放射状应力纤维的细胞比例。
结果解读:共表达野生型Arf6可显著增强Kalirin5诱导的Rac1-GTP水平,而共表达Arf6T27N则显著降低该水平(n=3,P<0.01)(图4);单独表达EFA6时,仅20%的细胞保留放射状应力纤维,共表达Kalirin5显性负突变体后,该比例提升至70%(n=3,P<0.01)(图5B),说明Arf6通过Kalirin5介导Rac1的激活,且Kalirin的催化活性是Arf6诱导细胞骨架变化的必要条件。
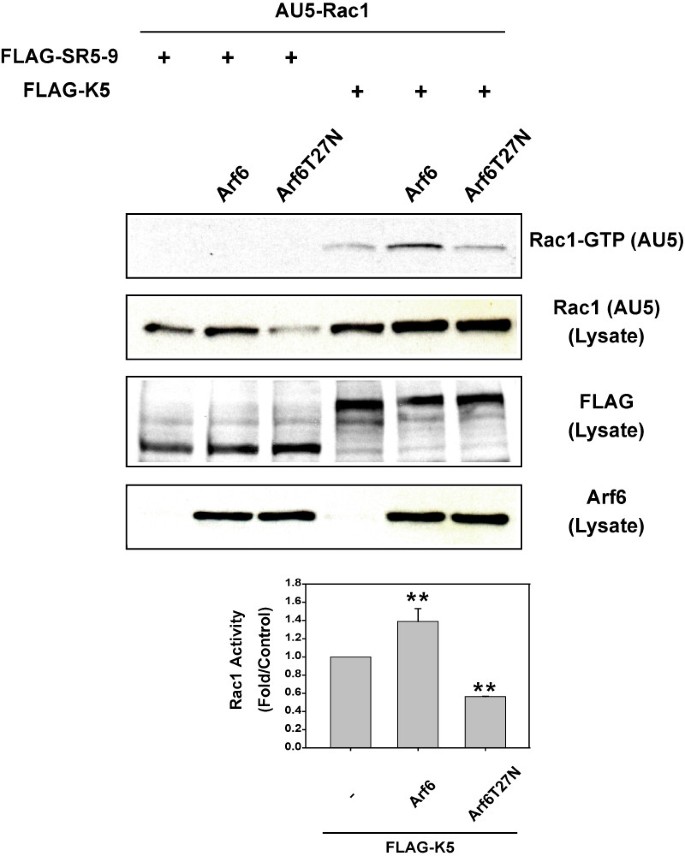
产品关联:文献未提及具体实验产品,领域常规使用Rac激活检测试剂盒、肌动蛋白染色试剂等。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究中涉及的功能型Biomarker为GDP结合态Arf6与Kalirin5的相互作用复合物,其筛选与验证逻辑为:通过酵母双杂交筛选候选互作蛋白→生化实验验证结合的特异性与结合态偏好→细胞实验验证其膜招募功能→功能实验验证对Rac1激活的调控作用,形成完整的验证链条。
研究过程详述
该Biomarker的来源为细胞内蛋白-蛋白相互作用,验证方法包括GST pull-down、免疫共沉淀、免疫荧光共定位、功能抑制实验;特异性数据显示,仅GDP结合态Arf6可与Kalirin5结合,激活态Arf6无结合信号,且该结合可被Arf6的鸟苷酸交换因子EFA6抑制,能量耗竭处理可增强结合;敏感性数据未明确提供,但功能实验显示该相互作用可显著调控Rac1的激活水平与细胞骨架结构。
核心成果提炼
该复合物的功能关联为:作为Arf6调控Rac1激活的关键中间节点,介导Arf6对Rac1的招募与激活;创新性在于首次发现GDP结合态Arf6的招募功能,明确了Arf6通过自身GTP酶循环(GDP结合态招募、GTP结合态激活下游)调控Rac1的分子机制;统计学结果显示,共表达Arf6使Kalirin5的质膜定位比例提升约1倍(n=3,P<0.01),Kalirin5显性负突变体可使EFA6处理细胞中保留放射状应力纤维的比例从20%升至70%(n=3,P<0.01)。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。