Nuclear envelope transmembrane proteins (NETs) that are up-regulated during myogenesis
肌生成过程中上调的核膜跨膜蛋白(NETs)
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2006 | 起止号: | 2006 Oct 24;7:38 |
| doi: | 10.1186/1471-2121-7-38 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Nuclear envelope transmembrane proteins (NETs) that are up-regulated during myogenesis;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:骨骼肌分化与核膜蛋白功能研究
核膜作为真核细胞核的边界结构,分为内层核膜(INM)、外层核膜(ONM)及核孔复合物,其中内层核膜内侧的核纤层由核纤层蛋白与内层核膜跨膜蛋白组成,参与核结构维持、染色质组织及细胞骨架锚定等核心功能。领域共识:核纤层蛋白突变可引发多种人类疾病(laminopathies),骨骼肌与心肌是最常受累的组织类型,如Emery-Dreifuss肌营养不良与emerin蛋白突变直接相关。此前研究通过传统细胞生物学方法仅鉴定出约15种核膜跨膜蛋白,且多数蛋白在肌肉分化中的功能尚未明确。作者团队此前通过MudPIT蛋白质组学技术筛选出67个新的候选核膜跨膜蛋白(NETs),但这些分子的组织特异性表达及功能仍未得到系统验证。本研究聚焦肌肉分化过程中NETs的表达调控模式,旨在筛选参与肌肉发育或维持的核膜蛋白,填补肌肉分化中核膜蛋白功能研究的空白,为肌肉疾病机制研究提供新的分子靶点。
2. 文献综述解析
作者从核膜结构与功能、核膜蛋白疾病关联、核膜蛋白鉴定技术三个维度对领域研究进行系统综述,梳理现有研究的成果与局限性,明确本研究的创新方向。
现有研究表明,核纤层不仅参与核机械强度维持,还通过结合染色质及转录调控因子参与基因表达调控,已知的核膜跨膜蛋白如emerin、MAN1等部分与肌肉疾病相关,其中MAN1可通过结合Smad转录因子调控TGF-β信号通路。传统细胞生物学方法在鉴定核膜蛋白方面具有特异性高的优势,但存在通量低的局限性,仅能鉴定少量已知功能的核膜蛋白;作者团队此前采用的MudPIT蛋白质组学技术实现了核膜蛋白的高通量筛选,发现大量新的候选NETs,但这些分子的组织特异性表达及功能尚未得到验证。现有研究的核心未解决问题在于,肌肉分化过程中核膜蛋白的表达调控模式及功能意义尚不明确,缺乏针对肌肉特异性核膜蛋白的系统研究。本研究的创新点在于首次通过转录组筛选结合组织表达验证,鉴定出6个在C2C12成肌细胞分化过程中上调的NETs,并验证其核膜定位,为肌肉核膜功能研究提供了新的候选分子。
3. 研究思路总结与详细解析
本研究以“筛选肌肉分化相关核膜跨膜蛋白-验证组织表达与亚细胞定位-预测功能”为核心逻辑,通过转录组分析、定量实时PCR(qRT-PCR)、免疫荧光染色、免疫印迹等技术,系统鉴定并验证了6个在肌生成过程中上调的NETs,明确其组织表达模式与核膜定位,为后续功能研究奠定基础。
3.1 C2C12成肌细胞分化模型建立与转录组筛选
实验目的是筛选C2C12成肌细胞分化过程中表达显著变化的NETs,明确其转录水平的调控模式。方法细节为将C2C12成肌细胞接种于明胶包被的培养皿,16小时后更换为含2%马血清的低血清培养基诱导分化,以更换培养基当天为第0天,第6天收集分化后的肌管样本;采用Affymetrix Mouse Genome 430 v2.0芯片分析增殖期和分化期细胞的转录组差异,同时通过qRT-PCR验证筛选结果,每个样本重复6次独立实验。结果解读显示,芯片分析发现6个NETs(NET9、14a、25、32、37、39)的转录水平在分化过程中显著上调(P<0.05,倍数变化>1.5),其中NET39的转录水平上调39.5倍(n=6,P<0.05);qRT-PCR验证结果与芯片分析趋势一致,同时肌肉分化标志物肌浆蛋白(desmin)、MEF2C和肌生成素(myogenin)的转录水平也显著上调,核纤层蛋白lamin A/C、lamin B1等转录水平则显著下调。
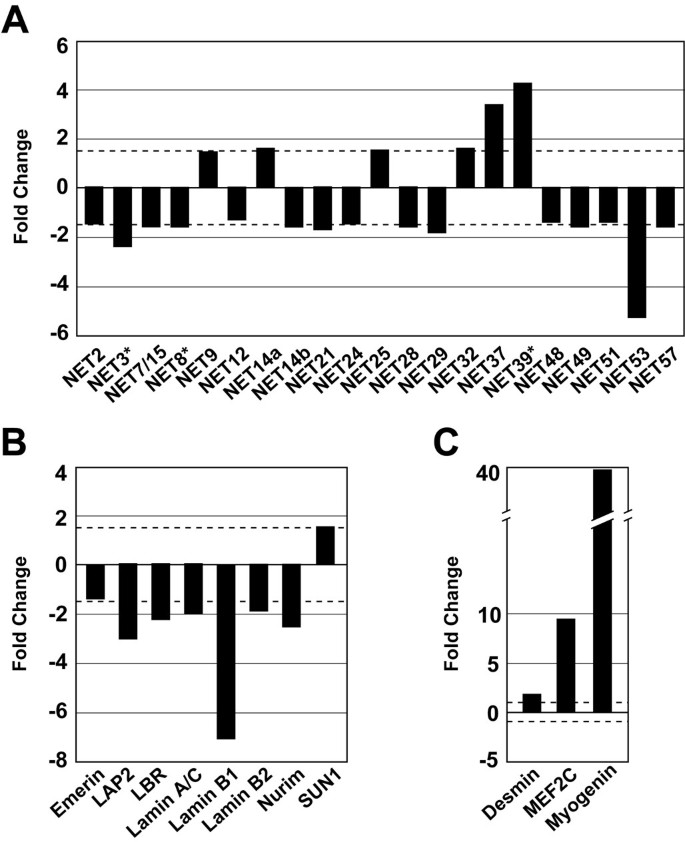
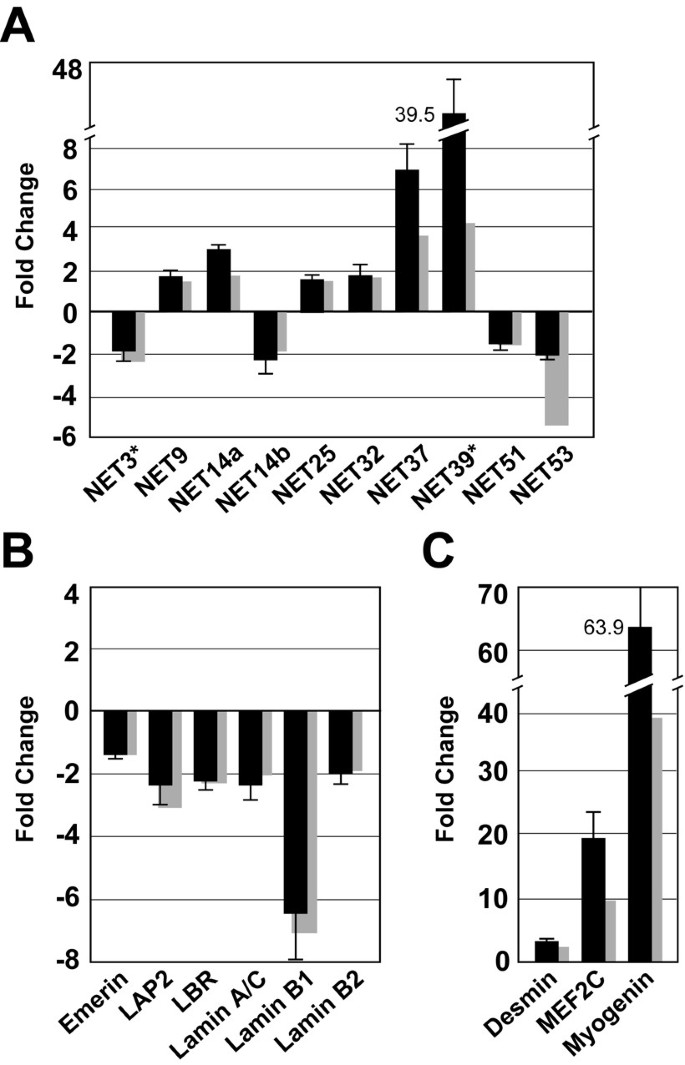
实验所用关键产品:Invitrogen的pcDNA 3.1 D/V5-His-TOPO载体、Lipofectamine 2000转染试剂,Roche的Transcriptor First Strand cDNA Synthesis Kit,Affymetrix的Mouse Genome 430 2.0 GeneChip芯片,Novocastra的desmin和emerin单克隆抗体。
3.2 小鼠组织表达谱验证
实验目的是确认上调NETs在成年小鼠不同组织中的表达模式,明确其组织特异性。方法细节为采集10种成年C129小鼠组织(脑、胸腺、心脏、肺、肝、脾、胃、肠、肾、后肢骨骼肌),每个组织样本来自3-4只小鼠,采用RNA Later保存组织,提取总RNA后通过qRT-PCR检测NETs和对照基因的转录水平,以肽基脯氨酰异构酶A(Ppia)作为内参基因归一化。结果解读显示,6个上调的NETs在骨骼肌中均呈高表达,其中NET14a、25、37、39在骨骼肌中的表达量显著高于其他组织(为多数组织的5倍以上,n=3-4,P<0.05),NET32在骨骼肌中的表达量为其最高表达组织的50%,NET9和32在多数组织中均有较高表达(>20%的最高表达水平);同时心脏中NET14a、37、39的表达量也相对较高。
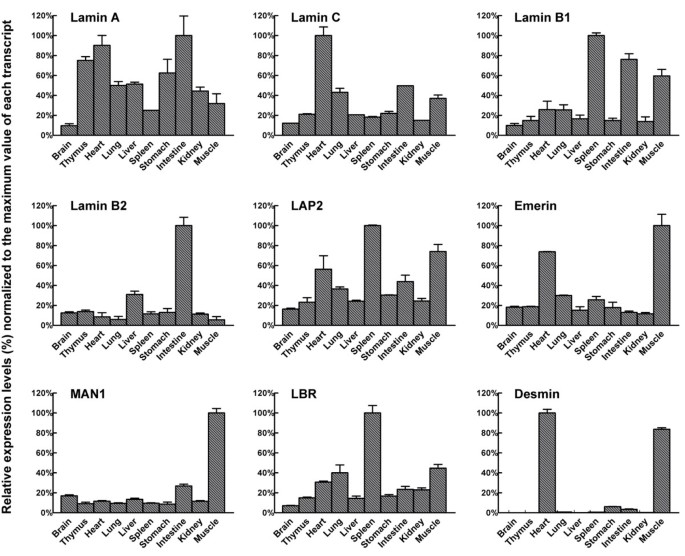
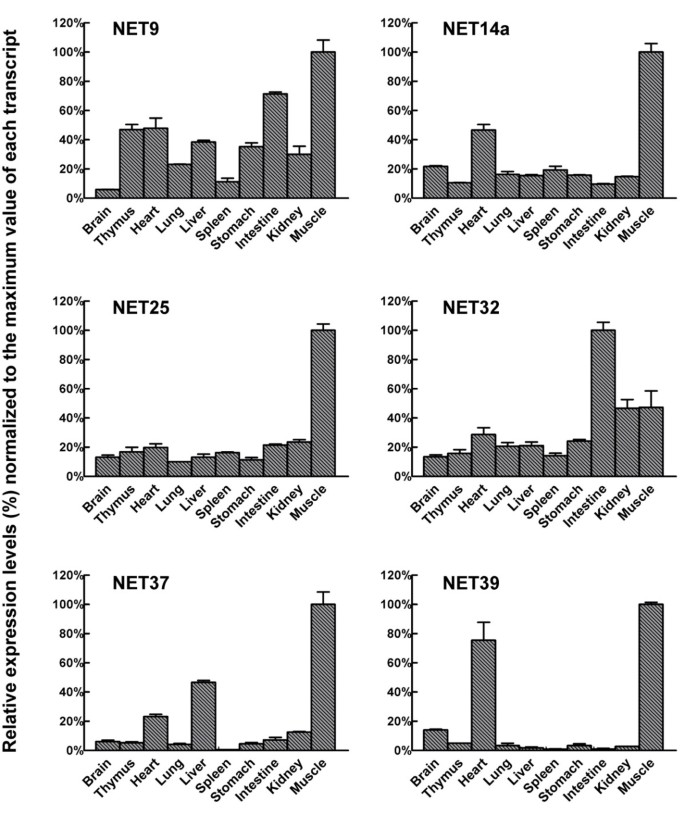
实验所用关键产品:Ambion的RNA Later组织保存液,Qiagen的RNeasy Total RNA Isolation Kit,Roche的LightCycler 2.0热循环仪及FastStart DNA MasterPLUS SYBR Green I试剂。
3.3 核膜定位与亚细胞富集验证
实验目的是验证上调NETs的核膜定位,确认其为核膜跨膜蛋白。方法细节为构建C端融合V5标签的NETs表达载体,转染C2C12增殖期细胞和分化期肌管,采用Triton X-100预提取处理细胞后进行免疫荧光染色,检测V5标签的定位;同时分离小鼠肝细胞核膜(NE)和微粒体膜(MM),通过免疫印迹检测NET25、32、37在两种膜组分中的富集情况,以磷脂含量归一化样本。结果解读显示,NET9、25、32、37、39在增殖期C2C12细胞中定位于核膜,Triton X-100预提取后核膜部分的蛋白仍保留,而内质网标志物calnexin则完全被提取;分化期肌管中,NET9、25、32、37仍定位于核膜,NET39的核膜定位可能被胞质中的高表达量掩盖;免疫印迹结果显示,NET25、37在核膜中的富集倍数>90倍,NET32在核膜中的富集倍数为16倍(n=3,P<0.05),与核膜标志物emerin的富集模式一致。
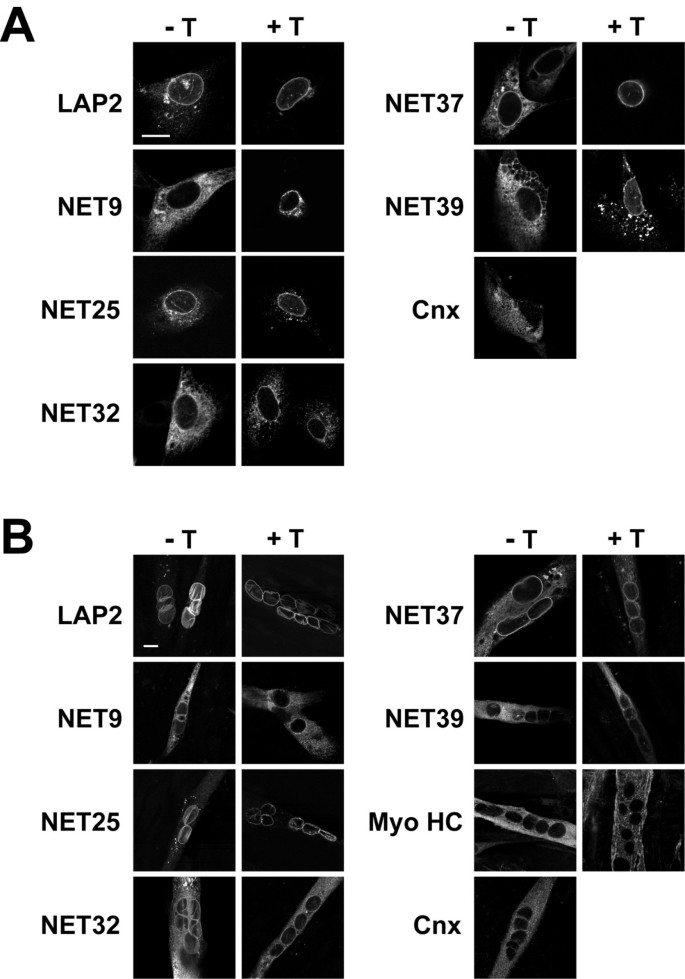
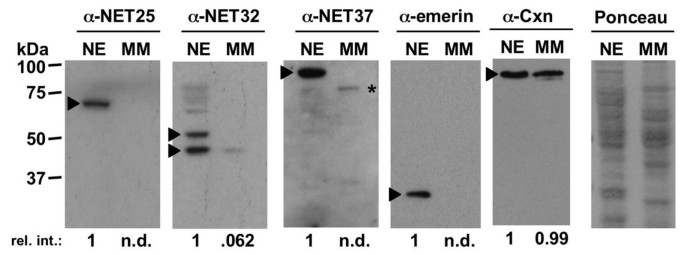
实验所用关键产品:Bio-Rad的GS-800 Calibrated Densitometer密度扫描仪,Pierce的SuperSignal West Pico化学发光检测试剂,Invitrogen的V5标签单克隆抗体、TOPRO-3核酸染料。
3.4 分化过程中蛋白表达水平验证
实验目的是确认NET25在C2C12细胞分化过程中的蛋白表达变化,验证转录水平变化与蛋白水平的一致性。方法细节为收集分化0天和6天的C2C12细胞总蛋白,以组蛋白H2B作为内参归一化样本量,通过免疫印迹检测NET25、核纤层蛋白(lamin A/C、lamin B1)、emerin和desmin的蛋白水平。结果解读显示,NET25的蛋白水平在分化6天时上调约9.4倍(n=3,P<0.05),与转录水平的上调趋势一致;同时desmin的蛋白水平上调约5.4倍,lamin A/C、lamin B1、emerin的蛋白水平则呈上调趋势,与转录水平的下调趋势不一致,提示存在转录后调控机制。
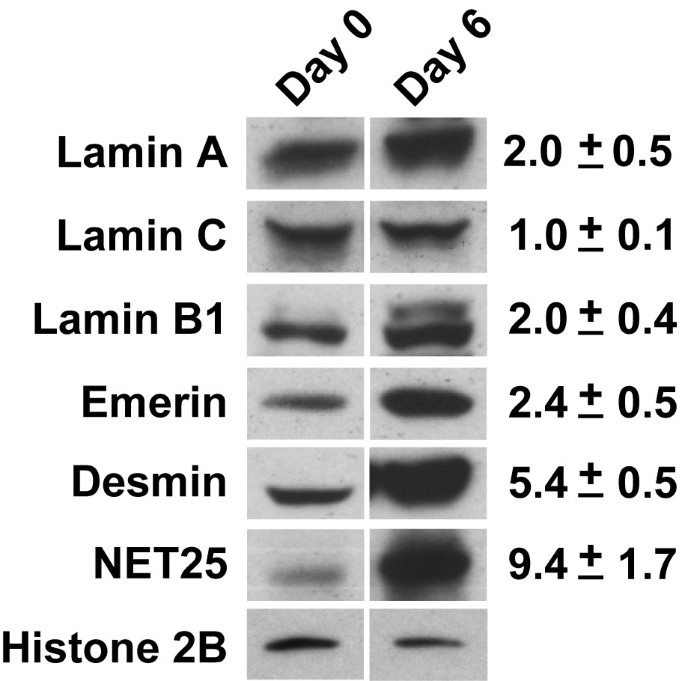
实验所用关键产品:Pierce的抗肽抗体(针对NET25、32、37),Novocastra的desmin和emerin单克隆抗体,自制的lamin A/C和lamin B1多克隆抗体。
4. Biomarker研究及发现成果
本研究鉴定的6个在肌生成过程中上调的NETs可作为肌肉分化及肌肉组织特异性的潜在生物标志物,为肌肉发育和肌肉疾病研究提供新的分子靶点。
Biomarker定位:6个NETs(NET9、14a、25、32、37、39)属于组织特异性核膜跨膜蛋白标志物,筛选与验证逻辑为:首先通过C2C12成肌细胞分化模型的转录组芯片筛选出表达显著上调的NETs,随后通过qRT-PCR验证转录水平变化,再通过小鼠多组织表达谱分析确认其骨骼肌特异性表达,最后通过免疫荧光和免疫印迹验证其核膜定位,形成完整的筛选验证链条。
研究过程详述:这些Biomarker的来源为C2C12成肌细胞和成年小鼠组织样本,验证方法包括转录组芯片分析、定量实时PCR(qRT-PCR)、免疫荧光染色和免疫印迹检测。特异性方面,NET14a、25、37、39在骨骼肌中具有高度特异性,表达量显著高于其他9种组织(为多数组织的5倍以上,n=3-4,P<0.05);敏感性方面,qRT-PCR检测显示NET39在分化过程中转录水平上调39.5倍(n=6,P<0.05),具有较高的检测敏感性。
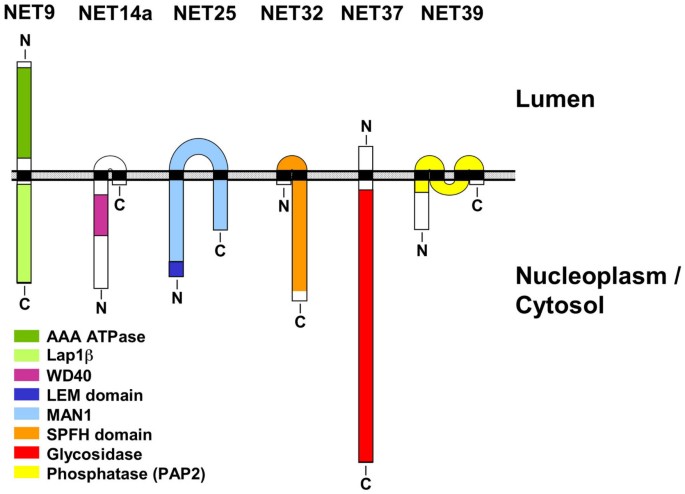
核心成果提炼:这些NETs的功能关联主要体现在肌肉发育与维持方面,基于其在肌肉分化过程中的上调表达和骨骼肌特异性表达模式,推测其参与肌肉分化的调控或成熟肌肉细胞的功能维持。其中4个NETs(NET25、32、37、39)具有信号转导相关的结构域:NET25含LEM结构域(与MAN1同源,可能参与TGF-β信号调控),NET32含SPFH结构域(可能参与脂筏介导的信号转导),NET37含糖苷酶结构域(可能参与糖基化修饰相关信号),NET39含磷脂酸磷酸酶结构域(可能参与磷脂信号调控)。本研究首次发现这些NETs在肌肉分化中的上调表达和核膜定位,为肌肉核膜功能和肌肉疾病的机制研究提供了新的候选分子,目前尚未获得这些分子作为疾病诊断或预后标志物的临床数据,需进一步开展功能验证和临床样本研究。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。