An initial biochemical and cell biological characterization of the mammalian homologue of a central plant developmental switch, COP1
对哺乳动物中枢植物发育开关同源物 COP1 进行初步的生物化学和细胞生物学表征
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2002 | 起止号: | 2002 Dec 4;3:30 |
| doi: | 10.1186/1471-2121-3-30 | 研究方向: | 细胞生物学、发育与干细胞 |
文献解析
1. 领域背景与文献引入
文献英文标题:An initial biochemical and cell biological characterization of the mammalian homologue of a central plant developmental switch, COP1;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学(蛋白质泛素化与核定位调控)
在生命科学领域,组成型光形态建成蛋白1(COP1)是植物光调控发育的核心分子,其通过泛素-蛋白酶体途径降解光响应转录因子,精准调控幼苗光形态建成与暗形态建成的转换。领域共识:RING指结构域广泛存在于泛素连接酶(E3)中,主要介导底物泛素化降解,同时部分RING结构域参与蛋白质相互作用与亚细胞定位调控。植物中COP1的研究已建立完整的功能调控网络,但哺乳动物中COP1的研究仅停留在部分cDNA克隆阶段,其完整分子特征、泛素化功能的直接证据、亚细胞定位的调控机制均不明确,成为该领域的核心空白。本研究旨在填补这一空白,通过克隆人和小鼠COP1全长cDNA,系统解析其分子进化特征、泛素化关联功能及核定位信号机制,为揭示哺乳动物COP1的生理功能奠定基础。
2. 文献综述解析
作者以“物种进化-功能保守性-调控机制差异”为核心维度,系统综述了COP1在植物与哺乳动物中的研究进展,明确现有研究的核心结论、技术局限与本研究的创新定位。
现有研究中,植物COP1的研究已明确其三维结构(N端RING指、中间卷曲螺旋、C端WD40重复域),功能上作为E3连接酶介导光响应转录因子的泛素化降解,亚细胞定位受光信号调控,在黑暗中定位于细胞核,光照下转移至细胞质;技术方法上采用遗传筛选、酵母双杂交、免疫共沉淀等,优势是建立了完整的植物COP1功能调控网络,局限性是缺乏对哺乳动物同源物的直接功能验证。哺乳动物中仅克隆了部分COP1 cDNA,发现其在植物细胞中表达时能响应光信号调控定位,但未解析其自身的分子功能与调控机制,且缺乏全长序列信息与核定位信号的系统分析。
本研究的创新价值在于,首次获得人和小鼠COP1的全长编码序列,直接证明哺乳动物COP1与泛素化过程的关联,发现新型RING指结构域桥接的 bipartite核定位信号(NLS)与经典亮氨酸富集核输出信号(NES),揭示RING指结构域兼具泛素化酶功能与核定位支架的双重作用,突破了传统对RING结构域功能的认知。
3. 研究思路总结与详细解析
本研究以“解析哺乳动物COP1分子特征-验证泛素化功能-揭示核定位调控机制”为核心逻辑,形成“序列克隆→功能关联→定位分析→信号解析→机制建模”的完整研究闭环,核心科学问题聚焦于哺乳动物COP1是否具有泛素化调控功能,以及其核定位的分子信号机制。
3.1 哺乳动物COP1全长cDNA克隆与进化保守性分析
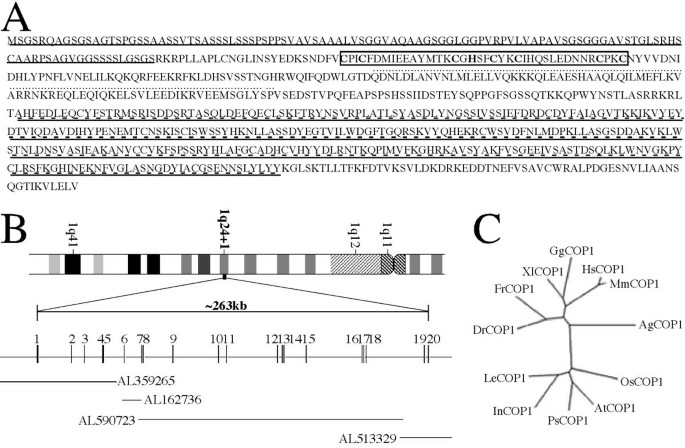
实验目的是获得人和小鼠COP1的完整编码序列,分析其跨物种进化保守性与分子特征;方法是通过公共EST数据库拼接获得候选序列,克隆全长cDNA并测序验证,进行多物种COP1蛋白序列比对与基因组结构分析,构建进化树;结果显示,人(HsCOP1)和小鼠(MmCOP1)COP1分别编码771和773个氨基酸,N端具有脊椎动物特有的甘氨酸-丝氨酸富集延伸区,而RING指、卷曲螺旋、WD40重复域在动植物中高度保守;基因组分析显示HsCOP1定位于1号染色体,含20个外显子,进化树显示动植物COP1形成独立分支,脊椎动物COP1具有共同的N端延伸;产品关联:文献未提及具体实验产品,领域常规使用分子克隆试剂(如限制性内切酶、T4 DNA连接酶)、ClustalW序列比对软件。
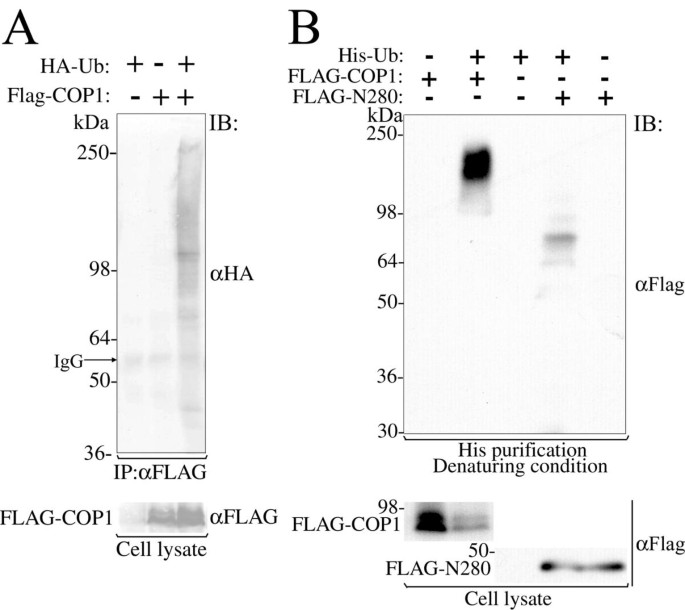
3.2 哺乳动物COP1与泛素化过程的关联验证
实验目的是明确哺乳动物COP1是否参与泛素化调控,是否为泛素化底物;方法是在人胚肾293细胞中共转FLAG标记的MmCOP1与HA/His标记的泛素,通过免疫沉淀与免疫印迹检测COP1结合的泛素化蛋白及自身泛素化水平;结果显示,共转FLAG-COP1与HA-Ub后,免疫沉淀复合物中检测到多条HA阳性条带,表明COP1与泛素化蛋白结合;His-Ub共转实验显示COP1自身存在多聚泛素化修饰(n=3,P<0.05);产品关联:实验所用关键产品:Sigma的anti-FLAG M2抗体、Covance的anti-HA单克隆抗体。
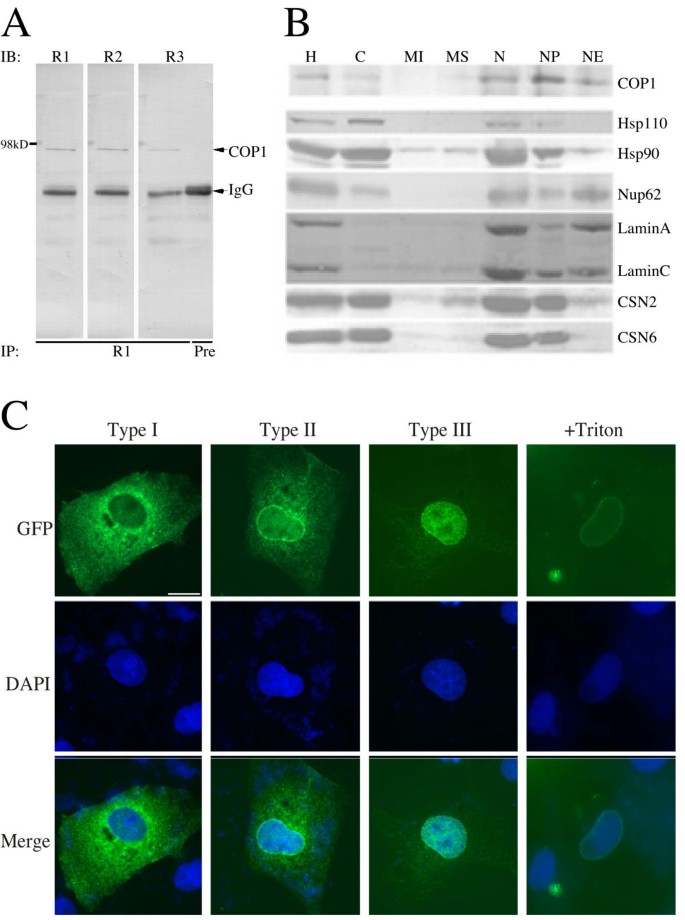
3.3 哺乳动物COP1亚细胞定位模式分析
实验目的是确定内源性与外源性COP1的亚细胞分布特征;方法是采用亚细胞分离技术结合免疫印迹检测内源性HsCOP1的定位,构建GFP标记的MmCOP1表达载体转染COS7细胞,通过荧光显微镜观察定位模式,Triton X-100处理验证核膜结合性;结果显示,内源性HsCOP1主要定位于细胞核(核质与核膜),少量存在于细胞质;外源性GFP-COP1呈现三种定位模式:胞质富集、胞质/核分布、核富集,Triton处理后仅核膜结合的GFP-COP1保留;产品关联:文献未提及具体实验产品,领域常规使用细胞分离试剂、Zeiss Axiophot荧光显微镜。
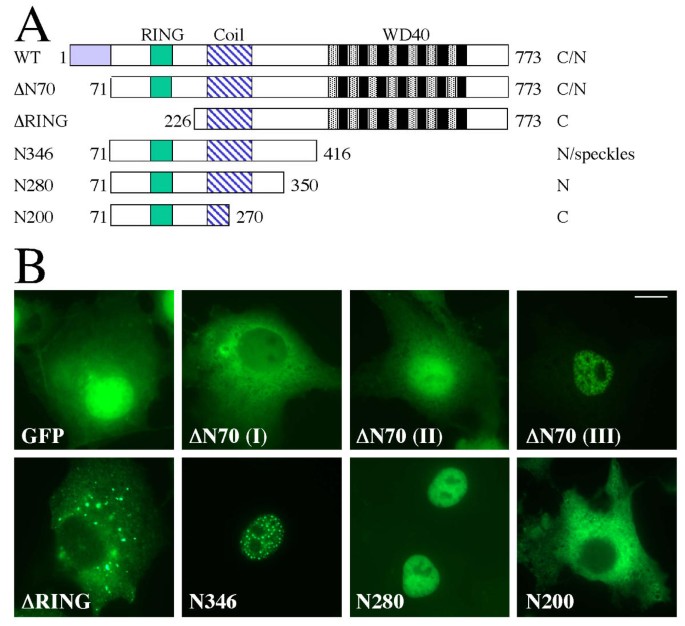
3.4 哺乳动物COP1核定位信号的突变体功能解析
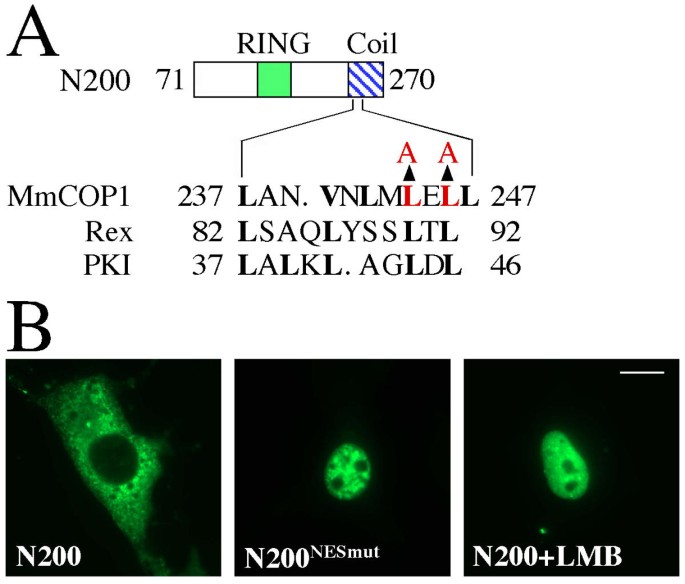
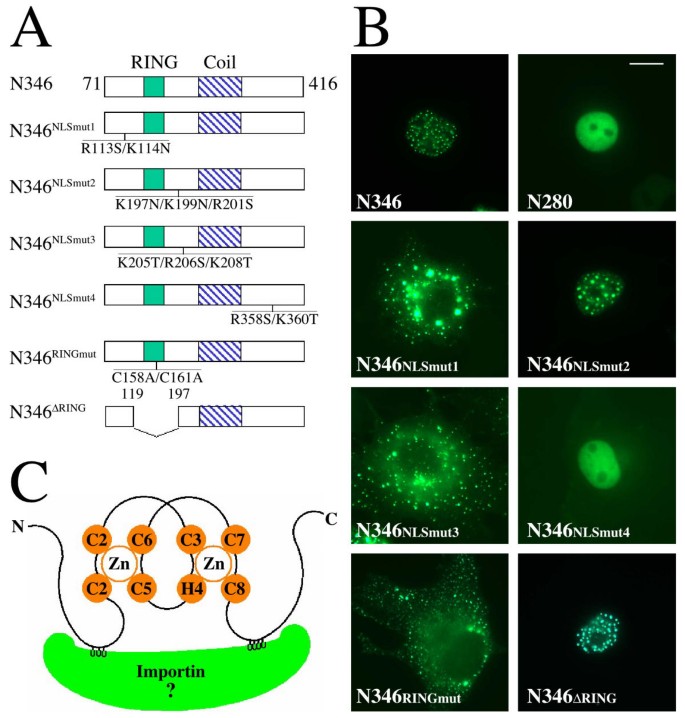
实验目的是定位COP1的核输入信号(NLS)与核输出信号(NES),解析其调控机制;方法是构建一系列COP1缺失突变体(ΔN70、ΔRING、N200等)与点突变体(NES突变、RING锌结合位点突变),GFP融合后转染COS7细胞观察定位,结合Leptomycin B(LMB)处理验证NES功能;结果显示,卷曲螺旋域内的亮氨酸富集序列(L234/L236)为经典CRM1依赖的NES,突变或LMB处理后N200突变体定位于细胞核;RING指结构域桥接两个正电荷簇(R113/K114与K205/R206/K208)形成新型 bipartite NLS,破坏RING结构(C158A/C161A)会抑制核输入,删除RING结构并将两个正电荷簇拉近至10个氨基酸距离则恢复核定位;产品关联:实验所用关键产品:Stratagene的QuikChange XL定点突变试剂盒、Leptomycin B(LMB)。
4. Biomarker研究及发现成果
本研究为基础机制研究,未涉及疾病相关生物标志物(Biomarker)的筛选与验证,但其核心发现为后续挖掘COP1作为疾病调控靶点的潜在价值提供了分子基础。
虽然本研究未直接鉴定Biomarker,但明确了哺乳动物COP1的分子特征与调控机制,其作为泛素化调控因子,可能参与细胞周期、信号转导等生理过程的调控,后续可进一步研究其在肿瘤、神经发育疾病中的表达变化与功能异常,探索其作为疾病诊断或预后Biomarker的潜力;此外,新型RING桥接NLS的发现,为设计靶向核定位的蛋白质调控工具提供了新的分子模块,具有潜在的生物技术应用价值。本研究未提供Biomarker的特异性、敏感性等数据,后续需结合临床样本进行验证。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。