Probing the importance and potential roles of the binding of the PH-domain protein Boi1 to acidic phospholipids
探究PH结构域蛋白Boi1与酸性磷脂结合的重要性和潜在作用
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2002 | 起止号: | 2002 Jun 27;3:16 |
| doi: | 10.1186/1471-2121-3-16 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Probing the importance and potential roles of the binding of the PH-domain protein Boi1 to acidic phospholipids;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:酵母细胞极性调控、PH域蛋白-酸性磷脂相互作用
酵母细胞极性是细胞定向生长、不对称分裂的核心生物学过程,其调控机制的解析为真核细胞极性建立提供了经典模型。1990年代起,Rho家族GTP酶(如Cdc42、Rho3)被陆续发现是细胞极性调控的核心开关,其中Cdc42通过招募下游效应因子参与芽体起始、细胞骨架重排等关键步骤。后续研究揭示Boi1与Boi2蛋白作为Cdc42的下游效应因子,通过PH域(pleckstrin homology domain,PH域)、SH3域(src homology 3 domain,SH3域)等结构域参与极性信号传递,且二者功能冗余,双基因敲除会导致酵母致死。然而,Boi1的PH域与酸性磷脂的相互作用特性,以及该结合对Boi1功能与亚细胞定位的调控机制,仍是领域内未解决的核心问题。现有研究显示,PH域作为真核蛋白中广泛存在的结构域,普遍具备结合酸性磷脂的能力,部分PH域通过结合磷脂实现膜定位,部分则参与蛋白的变构调控,但针对Boi1 PH域的磷脂结合特异性、功能必要性的直接实验证据仍属空白。因此,本研究聚焦Boi1 PH域与酸性磷脂的结合特性,通过体外实验、突变体功能验证、亚细胞定位分析等手段,解析磷脂结合对Boi1功能与定位的调控作用,为酵母细胞极性调控机制补充关键实验依据。
2. 文献综述解析
作者以“PH域功能类型”与“Boi1相关蛋白互作网络”为核心分类维度,系统梳理了领域内现有研究的核心结论与局限性。现有研究已明确Boi1/Boi2在细胞极性调控中的核心地位,通过遗传互作实验证实Boi1与Cdc42、Rho3存在功能关联:过表达Boi1会抑制芽体起始,该表型可被Cdc42过表达逆转;Rho3过表达可挽救Boi1/Boi2双敲除的致死表型。同时,PH域被证实是Boi1功能必需的结构域,Boi1-PH(包含PH域的C端片段)可替代全长Boi1的功能,参与细胞极性调控。在PH域的通用功能研究中,现有成果显示PH域普遍能结合酸性磷脂,部分PH域通过结合磷脂将蛋白招募至细胞膜,部分则通过磷脂结合引发蛋白构象变化,进而调控其与其他蛋白的相互作用。现有研究的优势在于建立了Boi1与Rho GTP酶的遗传互作模型,明确了PH域的功能必要性,但局限性也较为明显:未解析Boi1 PH域结合磷脂的具体特性,缺乏磷脂结合对Boi1功能、定位的直接实验证据,也未区分不同酸性磷脂(如磷脂酰丝氨酸PS、磷脂酰肌醇-4,5-二磷酸PIP₂)对Boi1的调控差异。本研究的创新价值在于,首次通过体外结合实验、突变体功能验证,明确Boi1 PH域对PS、PIP₂的结合特异性,揭示磷脂结合对Boi1功能与亚细胞定位的调控机制,同时区分了PH域与SH3域在Boi1不同亚细胞定位(芽体、母芽颈环)中的独立作用,填补了Boi1 PH域功能机制的研究空白。
3. 研究思路总结与详细解析
本研究的核心目标是明确Boi1 PH域与酸性磷脂的结合特性,解析该结合对Boi1功能与亚细胞定位的调控作用;核心科学问题包括Boi1 PH域结合不同酸性磷脂的特异性、磷脂结合对Boi1功能的必要性,以及磷脂结合如何调控Boi1的亚细胞定位;技术路线遵循“假设→体外实验验证→突变体功能分析→定位机制解析”的闭环逻辑,通过多维度实验逐步验证磷脂结合在Boi1功能中的核心作用。
3.1 Boi1-PH与酸性磷脂的结合特性验证
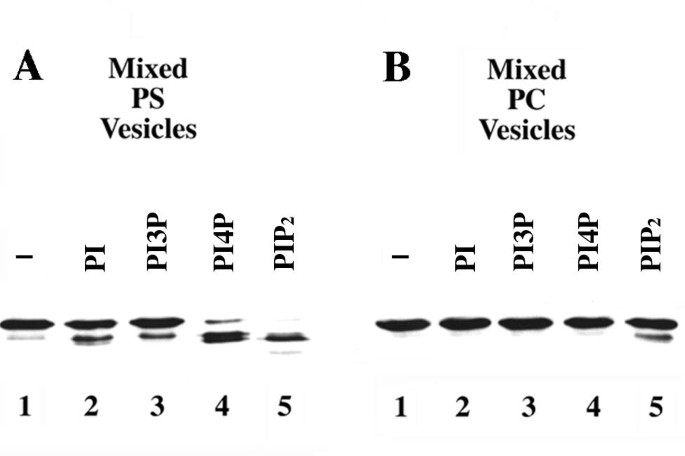
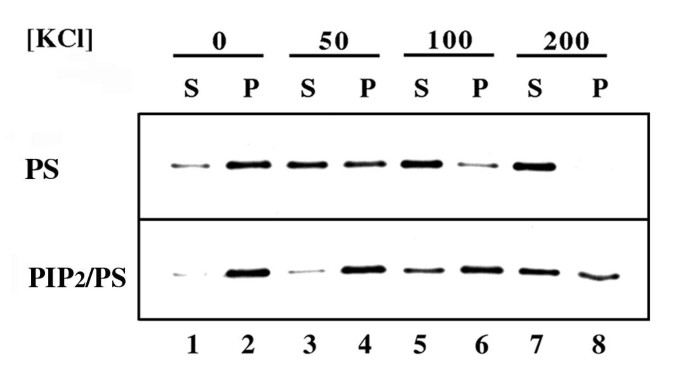
本环节的实验目的是验证Boi1 PH域是否具备结合酸性磷脂的能力,并明确不同磷脂的结合差异。实验方法上,研究人员选择Boi1-PH片段而非全长Boi1进行实验,因全长Boi1几乎不溶,无法开展体外结合分析。采用蛋白水解实验与囊泡共沉淀实验两种技术:蛋白水解实验中,将含Boi1-PH的酵母提取物与PS或PC囊泡(添加不同类型的磷脂酰肌醇类磷脂)共孵育,加入2mM氯化钙诱导蛋白水解,通过免疫印迹(Western Blot)检测Boi1-PH的降解情况;囊泡共沉淀实验中,将Boi1-PH与PS或PS+PIP₂囊泡共孵育,在不同浓度氯化钾(0、50、100、200mM)条件下超速离心,分离上清与沉淀组分,通过免疫印迹检测Boi1-PH在各组分中的分布。
实验结果显示,蛋白水解实验中,PIP₂/PS混合囊泡可显著诱导Boi1-PH降解,PI4P/PS囊泡有一定诱导作用,而PS单独囊泡无明显诱导效果;若以中性磷脂PC为囊泡主体,仅PIP₂能微弱诱导Boi1-PH降解(对应图2)。囊泡共沉淀实验显示,Boi1-PH可与PS囊泡共沉淀,添加PIP₂后共沉淀的Boi1-PH比例显著升高,且在高浓度氯化钾条件下仍能保持结合(对应图3)。上述结果表明,Boi1-PH可结合PS与PIP₂,且对PIP₂的亲和力更高,PS可促进Boi1-PH与PIP₂的结合。
文献未提及具体实验产品,领域常规使用抗体制备试剂盒、超速离心机、免疫印迹检测试剂等。
3.2 磷脂结合缺陷Boi1突变体的构建与验证
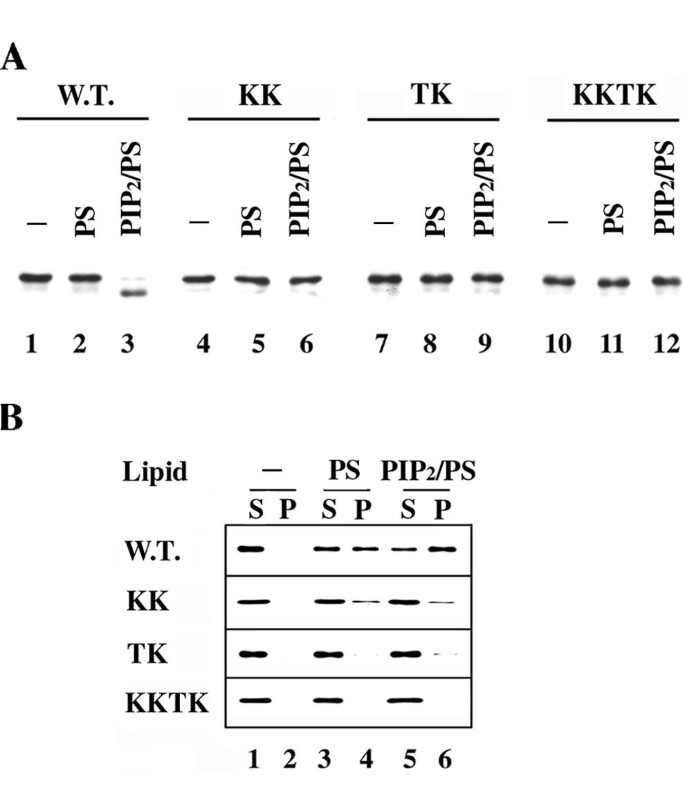
本环节的实验目的是构建Boi1 PH域的磷脂结合缺陷突变体,并验证突变体的磷脂结合能力缺陷。实验方法上,研究人员参考pleckstrin蛋白PH域的PIP₂结合位点,在Boi1 PH域的保守氨基酸区域构建了三种突变体:KK突变(K785E、K786A)、TK突变(T793A、K795E)、KKTK突变(组合KK与TK的突变位点)。通过蛋白水解实验与囊泡共沉淀实验验证突变体的磷脂结合能力,同时通过免疫印迹检测突变体蛋白的表达水平,排除蛋白稳定性下降对实验结果的干扰。
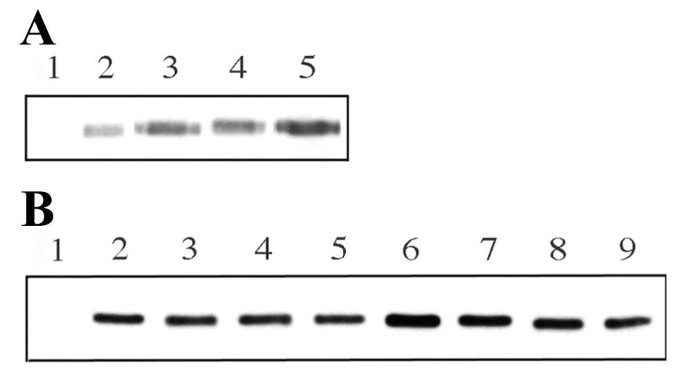
实验结果显示,蛋白水解实验中,三种突变体均不受PIP₂/PS混合囊泡的诱导降解(对应图5A);囊泡共沉淀实验中,KK突变体与PS囊泡的结合能力略有下降,与PIP₂/PS囊泡的结合能力显著降低;TK突变体完全丧失与PS囊泡的结合能力,仅能微弱结合PIP₂/PS囊泡;KKTK突变体则完全丧失与两种囊泡的结合能力(对应图5B)。免疫印迹结果显示,三种突变体的蛋白表达水平与野生型Boi1相当(对应图7A),说明突变体的功能缺陷并非由蛋白稳定性下降导致。上述结果证实,所构建的突变体均存在不同程度的磷脂结合能力缺陷,其中KK突变主要影响PIP₂结合,TK突变主要影响PS结合,KKTK突变则完全丧失磷脂结合能力。

文献未提及具体实验产品,领域常规使用基因定点突变试剂盒、蛋白表达载体、免疫印迹检测试剂等。
3.3 磷脂结合对Boi1功能的必要性验证
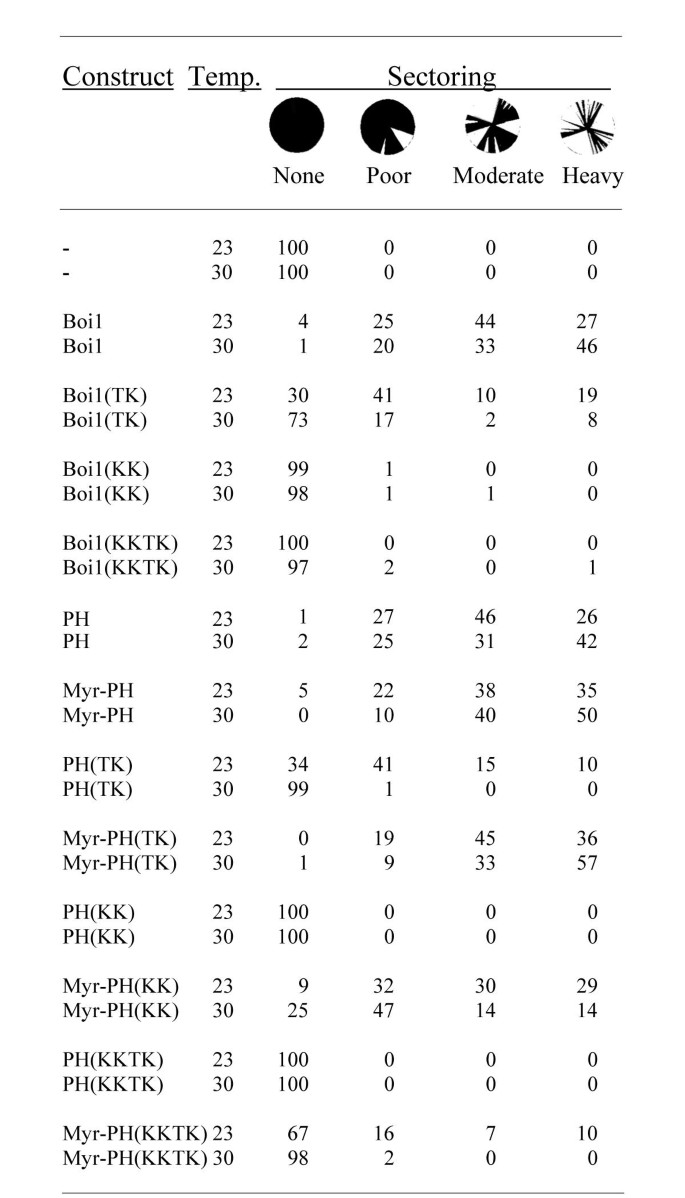
本环节的实验目的是验证磷脂结合对Boi1功能的必要性,并解析不同磷脂结合的功能差异。实验方法上,采用菌落扇区分析实验:使用Boi1/Boi2双敲除、依赖含ADE3颜色标记的BOI1质粒存活的酵母菌株PY967,该菌株中丢失BOI1质粒的细胞会死亡,因此菌落呈红色;若转化的质粒能替代BOI1的功能,丢失原BOI1质粒的细胞可存活,菌落会出现白色扇区。将野生型与突变体Boi1/Boi1-PH质粒转化该菌株,在23℃与30℃培养后统计扇区形成比例。同时,构建Myr(豆蔻酰化标签,可实现蛋白的膜定位)融合的突变体Boi1-PH,验证膜定位标签是否能恢复突变体的功能。
实验结果显示,野生型Boi1在23℃与30℃分别有71%、79%的菌落呈现中度或重度扇区(n=200);TK突变体Boi1的扇区比例显著降低,23℃仅29%、30℃仅10%的菌落呈现中度或重度扇区;KK与KKTK突变体则几乎无扇区形成,说明其功能完全丧失(对应图6)。Myr融合标签可显著恢复突变体的功能:Myr-Boi1-PH(TK)在23℃有81%、30℃有90%的菌落呈现中度或重度扇区;Myr-Boi1-PH(KK)在23℃有59%、30℃有28%的菌落呈现中度或重度扇区;Myr-Boi1-PH(KKTK)仅在23℃有17%的菌落呈现中度或重度扇区(对应图6)。免疫印迹结果显示,Myr融合不影响突变体蛋白的表达水平(对应图7B)。上述结果表明,磷脂结合对Boi1功能至关重要,PS结合主要负责将Boi1招募至细胞膜,而PIP₂结合除膜定位外还参与额外的功能调控。

文献未提及具体实验产品,领域常规使用酵母转化试剂盒、微生物培养基、菌落形态分析设备等。
3.4 磷脂结合对Boi1亚细胞定位的调控作用解析
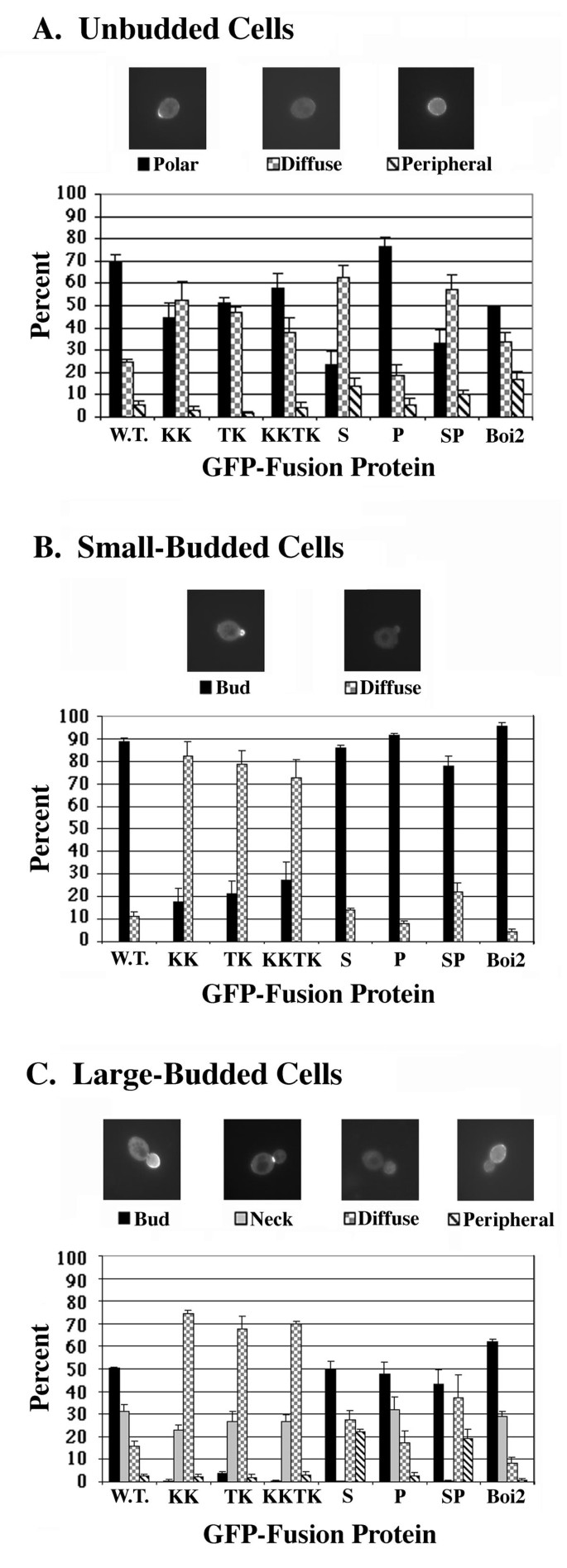
本环节的实验目的是解析磷脂结合对Boi1亚细胞定位的调控机制,区分PH域与SH3域在定位中的功能差异。实验方法上,构建野生型与突变体Boi1的GFP(绿色荧光蛋白)融合蛋白,在酵母菌株Y1300中表达,通过荧光显微镜观察不同细胞周期阶段(未出芽、小芽、大芽)的定位模式。同时,构建SH3域突变体(S突变,破坏SH3域功能)、脯氨酸富集区突变体(P突变,破坏与Bem1的结合),对比其定位模式与野生型的差异。
实验结果显示,野生型Boi1-GFP在未出芽细胞中70%呈极性定位,小芽细胞中89%定位于芽体,大芽细胞中50%定位于芽体、31%定位于母芽颈环(n≥100);磷脂结合缺陷突变体(KK、TK、KKTK)在小芽细胞中定位于芽体的比例显著降低(18%-27%),大芽细胞中几乎不定位于芽体,但仍可正常定位于颈环;SH3域突变体(S突变)则完全丧失颈环定位能力,但仍可定位于芽体(对应图8)。脯氨酸富集区突变体的定位模式与野生型无显著差异,说明Boi1与Bem1的结合不影响其亚细胞定位。上述结果表明,磷脂结合负责Boi1在芽体的定位与保留,而SH3域负责Boi1在颈环的定位,二者功能独立。
文献未提及具体实验产品,领域常规使用荧光显微镜、GFP融合表达载体、细胞成像分析软件等。
4. Biomarker研究及发现成果
本研究中,Boi1 PH域的磷脂结合关键氨基酸位点(K785、K786、T793、K795)可视为细胞极性调控的功能Biomarker,其筛选逻辑是基于已知PH域的磷脂结合保守位点,通过定点突变与功能验证,明确其对Boi1磷脂结合、功能与定位的调控作用。
研究过程中,这些位点来源于Boi1 PH域的进化保守区域,通过蛋白水解实验、囊泡共沉淀实验验证了其对磷脂结合的必要性:突变这些位点会导致Boi1 PH域的磷脂结合能力不同程度下降,其中KK突变主要影响PIP₂结合,TK突变主要影响PS结合,KKTK突变完全丧失磷脂结合能力。通过菌落扇区实验验证了其对Boi1功能的必要性:突变体的功能缺陷与磷脂结合能力下降呈正相关,如TK突变体因丧失PS结合能力,功能显著下降,而Myr标签恢复膜定位后功能可完全恢复。通过荧光定位实验验证了其对Boi1亚细胞定位的调控作用:磷脂结合缺陷突变体在芽体的定位能力显著降低,但颈环定位不受影响,说明这些位点通过调控磷脂结合特异性调控Boi1在芽体的定位。
核心成果方面,本研究首次明确了Boi1 PH域中调控PS与PIP₂结合的关键氨基酸位点,揭示这些位点通过调控磷脂结合,分别影响Boi1的膜定位与额外功能调控,其中PS结合主要负责将Boi1招募至细胞膜,PIP₂结合则参与膜定位之外的功能调控。创新性在于区分了不同酸性磷脂对Boi1的调控差异,以及PH域与SH3域在Boi1亚细胞定位中的独立作用,为细胞极性调控的信号网络提供了新的分子机制。统计学结果显示,每组菌落扇区实验统计约200个菌落(n=200),定位实验每组分析至少100个细胞(n≥100),实验重复三次,结果一致,差异具有统计学显著性(文献未明确给出具体P值)。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。