Thyroxine signal transduction in liver cells involves phospholipase C and phospholipase D activation. Genomic independent action of thyroid hormone
甲状腺素在肝细胞中的信号转导涉及磷脂酶C和磷脂酶D的激活。甲状腺激素的基因组非依赖性作用
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2001 | 起止号: | 2001;2:5 |
| doi: | 10.1186/1471-2121-2-5 | 研究方向: | 信号转导、细胞生物学、免疫/内分泌 |
文献解析
1. 领域背景与文献引入
文献英文标题:Thyroxine signal transduction in liver cells involves phospholipase C and phospholipase D activation. Genomic independent action of thyroid hormone;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:甲状腺激素非基因组信号转导(肝脏细胞方向)
甲状腺激素的生物学效应传统上被认为主要通过基因组途径实现,即结合核受体调控靶基因表达,这一机制在1990年代前是领域研究的核心。1990年代起,陆续有研究揭示甲状腺激素的非基因组作用,包括调控细胞内蛋白激酶C(PKC)激活、钙离子浓度升高、磷脂合成等过程,其中PKC是介导甲状腺激素增强干扰素γ效应、调控肝细胞磷脂交换的关键分子。但截至本研究开展时,领域内尚无关于甲状腺素(T4)处理细胞后,PKC的重要调节剂二酰甘油(DAG)积累规律及调控机制的研究,这一空白限制了对甲状腺激素非基因组信号转导通路的完整理解。基于此,本研究以大鼠肝脏细胞为模型,聚焦L-T4对二酰甘油形成及磷脂酶激活的非基因组效应,旨在填补领域研究空白,阐明甲状腺激素快速信号转导的分子机制。
2. 文献综述解析
本文综述部分以甲状腺激素作用的“基因组-非基因组”二元途径为分类维度,系统梳理领域内现有研究进展。现有研究已证实甲状腺激素的非基因组效应涉及多个层面,包括PKC激活、细胞内钙离子浓度升高、磷脂合成调控等,所采用的技术方法包括细胞系培养、酶活性检测、同位素标记追踪等,为非基因组效应的存在提供了实验依据,但这些研究存在明显局限性:既未阐明T4处理后二酰甘油的积累规律,也未明确磷脂酶C(PLC)与磷脂酶D(PLD)在信号通路中的激活顺序及相互调控关系。通过对比现有研究的空白,本研究的核心创新价值凸显:首次在肝脏细胞中证明L-T4可非基因组激活磷脂酶C、磷脂酶D及蛋白激酶C,并诱导二酰甘油的双相积累,同时阐明了L-T4通过顺序激活双磷脂酶途径调控二酰甘油生成的分子机制,为甲状腺激素非基因组信号转导的研究提供了全新的实验证据与理论框架。
3. 研究思路总结与详细解析
本研究的整体框架为:以明确甲状腺激素对肝脏细胞二酰甘油形成及磷脂酶激活的非基因组效应为研究目标,围绕“L-T4如何通过磷脂酶途径调控二酰甘油积累”这一核心科学问题,采用同位素标记的大鼠肝切片与分离肝细胞为模型,结合脂质提取分离、酶活性检测及抑制剂阻断实验,构建“处理-检测-验证”的闭环技术路线,最终阐明双磷脂酶途径的顺序激活机制。
3.1 细胞与组织模型构建及同位素标记
实验目的是建立可精准追踪脂质代谢变化的实验模型,为后续检测L-T4对二酰甘油及磷脂的影响提供基础。方法细节为:选取90日龄雄性Wistar大鼠,通过[14C]乙酸腹腔注射标记肝组织,制备肝切片;或分离肝细胞后,在含[14C]油酸的培养基中孵育3小时进行标记,标记后的细胞/组织经洗涤预处理后用于后续实验。结果解读为:成功实现肝组织及肝细胞内脂质的同位素标记,对照组脂质水平在实验周期内无显著变化,为L-T4处理后的脂质变化检测提供了稳定基线。实验所用关键产品:Amersham Corp.的[14C]油酸、[3H]肌醇等同位素试剂,Sigma的H7、普萘洛尔、新霉素等抑制剂。
3.2 L-T4诱导二酰甘油双相积累的检测与特异性验证
实验目的是明确L-T4对肝脏细胞二酰甘油生成的调控作用及特征。方法细节为:用不同浓度的L-T4或D-T4处理标记的肝切片与肝细胞,在不同时间点终止反应,采用Folch法提取脂质,通过薄层层析(TLC)分离二酰甘油并检测其放射性强度;同时设置NaOH处理组作为对照。结果解读为:L-T4可诱导二酰甘油呈双相积累,早期峰值出现在处理后15秒,晚期峰值出现在1-2分钟(
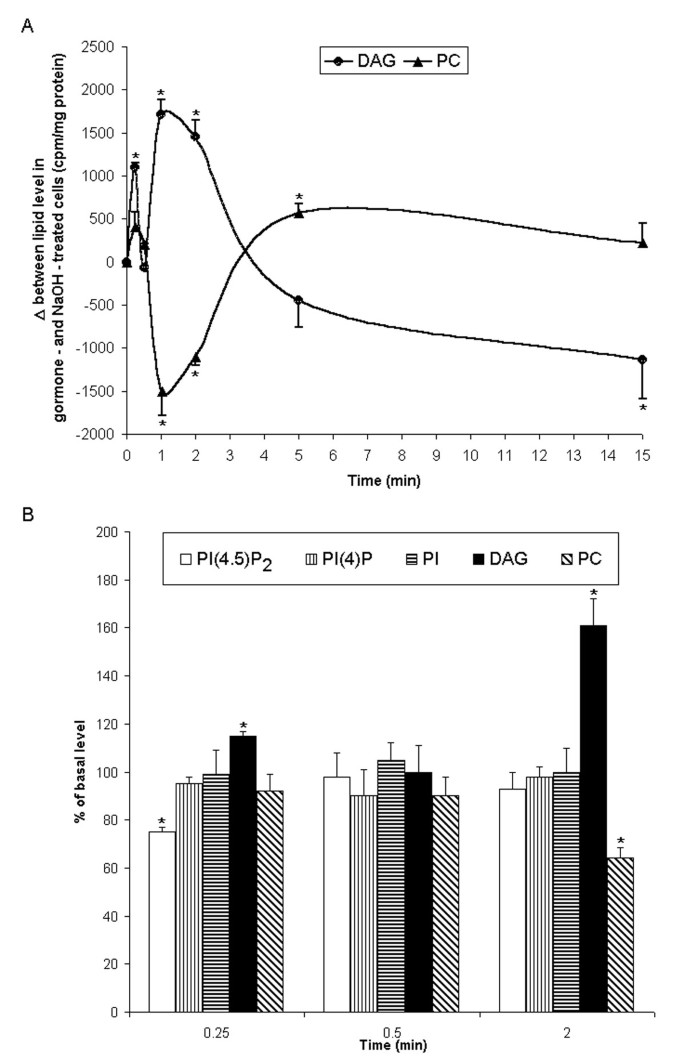
);二酰甘油生成具有浓度依赖性,10 nM L-T4即可诱导显著效应,而D-T4无类似作用(
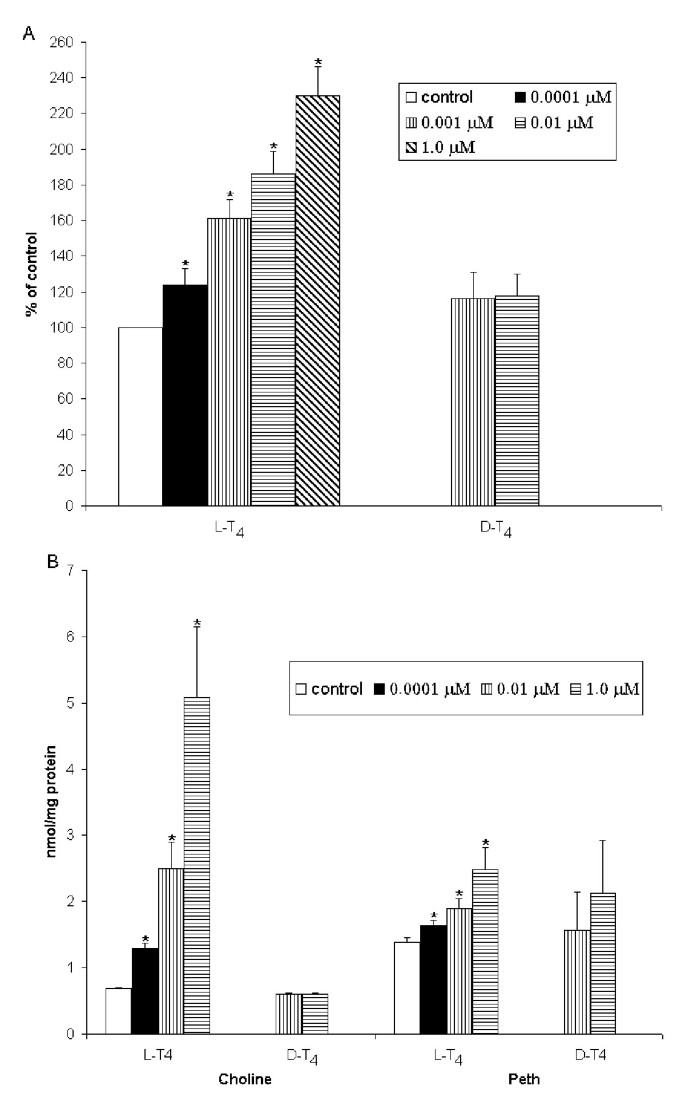
);同时检测到L-T4处理后肌醇1,4,5-三磷酸水平从840±25 cpm/10^7细胞升高至1832±42 cpm/10^7细胞(n=6,P<0.05),提示信号通路的激活。
3.3 磷脂酶C介导早期二酰甘油生成的验证
实验目的是确定早期二酰甘油积累是否由磷脂酶C介导。方法细节为:用磷脂酶C特异性抑制剂新霉素硫酸盐预处理标记的肝细胞,检测二酰甘油、磷脂酰肌醇4,5-二磷酸及肌醇1,4,5-三磷酸的水平变化。结果解读为:新霉素硫酸盐可完全抑制L-T4诱导的早期二酰甘油生成,同时伴随磷脂酰肌醇4,5-二磷酸水平下降及肌醇1,4,5-三磷酸水平升高(

),证明早期二酰甘油生成依赖磷脂酶C介导的磷脂酰肌醇水解。
3.4 磷脂酶D介导晚期二酰甘油生成的验证及通路关联
实验目的是明确晚期二酰甘油积累的调控机制及磷脂酶D与磷脂酶C通路的相互关系。方法细节为:用蛋白激酶C抑制剂H7、磷脂酸磷酸水解酶抑制剂普萘洛尔预处理细胞,检测二酰甘油、磷脂酰胆碱、磷脂酰乙醇(磷脂酶D特异性产物)及游离胆碱的水平;同时在分离的肝细胞膜中加入[14C-甲基]磷脂酰胆碱,检测L-T4对磷脂酰胆碱代谢的影响。结果解读为:H7与普萘洛尔可完全抑制晚期二酰甘油生成,L-T4处理后磷脂酰胆碱含量下降、磷脂酰乙醇生成增加(

),分离的肝细胞膜中[14C-甲基]磷脂酰胆碱降解加速、游离胆碱积累(
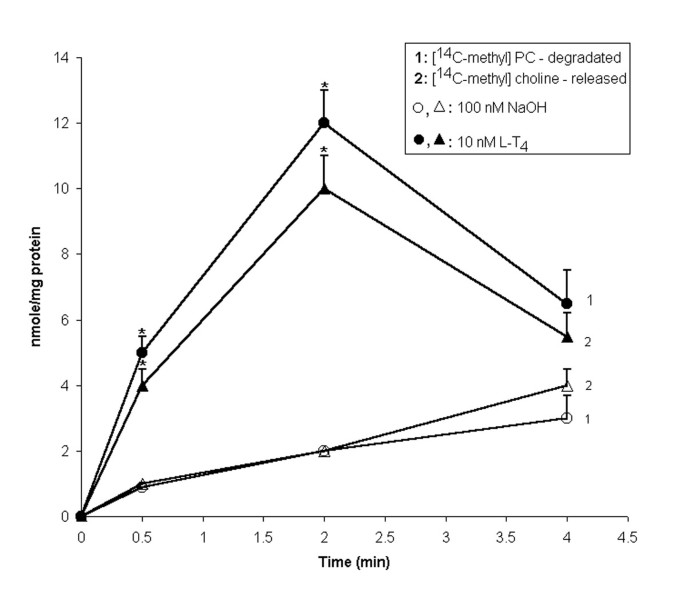
),证明晚期二酰甘油生成依赖磷脂酶D介导的磷脂酰胆碱水解,且该过程受蛋白激酶C调控;此外新霉素硫酸盐可降低磷脂酶D介导的二酰甘油生成,提示磷脂酶C通路对磷脂酶D的激活具有调控作用。
3.5 蛋白激酶C在双磷脂酶途径中的调控作用验证
实验目的是明确蛋白激酶C在L-T4诱导的信号通路中的激活状态及调控功能。方法细节为:分离L-T4处理后肝细胞的细胞质与膜组分,通过DEAE-纤维素层析部分纯化蛋白激酶C,检测其磷酸转移酶活性。结果解读为:L-T4处理后,蛋白激酶C从细胞质转移至膜组分,膜组分蛋白激酶C活性从1040±111 pmol/mg蛋白/min升高至9498±224 pmol/mg蛋白/min(n=4,P<0.05),而D-T4处理组无显著变化,证明L-T4可非基因组激活蛋白激酶C,且蛋白激酶C在磷脂酶D的激活中发挥关键调控作用。
4. Biomarker研究及发现成果
本研究涉及的功能性Biomarker包括信号第二信使二酰甘油、效应酶磷脂酶C与磷脂酶D,以及信号调控分子蛋白激酶C,这些分子共同构成L-T4非基因组信号转导的核心通路,其筛选与验证逻辑为通过同位素标记追踪脂质代谢变化,结合抑制剂阻断实验明确各分子在通路中的激活顺序与调控关系。
Biomarker定位:二酰甘油是连接磷脂酶与下游信号的核心节点Biomarker,磷脂酶C与磷脂酶D是调控二酰甘油生成的关键效应酶Biomarker,蛋白激酶C是通路中的调控分子Biomarker。其筛选与验证逻辑为:首先通过同位素标记检测L-T4处理后二酰甘油的积累规律,随后利用特异性抑制剂分别验证磷脂酶C与磷脂酶D对二酰甘油生成的调控作用,最后检测蛋白激酶C的激活状态及对磷脂酶D的调控,形成完整的验证链条。
研究过程详述:Biomarker的来源为L-T4处理后的大鼠肝切片与分离肝细胞,验证方法包括同位素标记脂质的薄层层析分离检测、酶活性测定、抑制剂阻断实验等。特异性方面,L-T4诱导的二酰甘油生成、磷脂酶C/磷脂酶D激活及蛋白激酶C激活均具有立体特异性,D-T4无类似效应;敏感性方面,10 nM L-T4即可诱导显著的二酰甘油积累及酶活性变化,肌醇1,4,5-三磷酸水平的诱导倍数达2.18倍(n=6,P<0.05),膜组分蛋白激酶C活性的诱导倍数达9.13倍(n=4,P<0.05)。
核心成果提炼:本研究的核心成果在于首次阐明L-T4在肝脏细胞中通过顺序激活双磷脂酶途径调控二酰甘油生成的非基因组机制:磷脂酶C首先激活诱导早期二酰甘油生成,随后蛋白激酶C介导磷脂酶D的激活,维持晚期二酰甘油的积累;该机制为甲状腺激素的快速非基因组效应提供了全新的分子解释,同时明确了二酰甘油、磷脂酶C、磷脂酶D及蛋白激酶C在通路中的功能关联,其中蛋白激酶C作为关键调控分子,介导了磷脂酶C与磷脂酶D通路的整合。所有实验结果均具有统计学显著性,为结论的可靠性提供了坚实支撑。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。