TMF is a golgin that binds Rab6 and influences Golgi morphology
TMF是一种高尔基蛋白,它能与Rab6结合并影响高尔基体的形态。
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2004 | 起止号: | 2004 May 5;5:18 |
| doi: | 10.1186/1471-2121-5-18 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:TMF is a golgin that binds Rab6 and influences Golgi morphology;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学-高尔基体结构与功能调控
高尔基体是真核细胞内负责蛋白质翻译后修饰、分选及囊泡运输的核心细胞器,其结构完整性与功能稳态依赖于多种调控蛋白的协同作用。高尔基体卷曲螺旋蛋白(golgin)是一类富含卷曲螺旋结构的高尔基体相关蛋白,被认为参与囊泡锚定、高尔基体膜堆叠及细胞骨架关联等关键过程,多数为GTP酶招募的外周膜蛋白。领域发展关键节点包括1998年发现酵母Uso1蛋白参与内质网-高尔基体囊泡运输,2002年明确Bicaudal-D蛋白通过结合Rab6连接囊泡与细胞骨架。当前研究热点聚焦于不同物种高尔基体卷曲螺旋蛋白的同源性鉴定及功能保守性分析,未解决的核心问题是部分物种间该类蛋白序列保守性低,同源物鉴定困难,且部分蛋白的亚细胞定位与功能存在争议。结合领域现状,本研究针对酵母Ypt6(哺乳动物Rab6同源物)招募的高尔基体卷曲螺旋蛋白Sgm1的哺乳动物同源物未明确,以及TMF/ARA160被错误归类为核因子的研究空白,旨在明确TMF的真实亚细胞定位与功能,为高尔基体结构调控机制提供新的实验依据。
2. 文献综述解析
作者按高尔基体卷曲螺旋蛋白的结构类型(跨膜型、外周型)与功能(囊泡锚定、细胞骨架关联等)对现有研究进行分类评述,系统梳理了该家族蛋白的研究进展与存在的局限。
现有研究的关键结论显示,高尔基体卷曲螺旋蛋白广泛参与高尔基体的组织与功能调控,其中酵母Uso1及其哺乳动物同源物p115参与内质网到高尔基体的囊泡运输,酵母Imh1参与囊泡向高尔基体的转运过程,Bicaudal-D1与Bicaudal-D2则负责连接囊泡与细胞骨架,维持囊泡运输的方向性。技术方法上,通过GTP酶结合实验、亚细胞组分分离等手段,明确了部分高尔基体卷曲螺旋蛋白的招募机制与亚细胞定位,具有较高的特异性与可靠性。但现有研究仍存在局限性,不同物种的高尔基体卷曲螺旋蛋白序列保守性较低,仅结构特征相似,导致同源物鉴定难度大;同时部分蛋白的功能研究存在争议,如TMF/ARA160此前被认为是转录调控因子或染色质重塑复合物组分,但缺乏直接的亚细胞定位与功能验证证据。本研究通过同源序列分析与功能实验,首次明确TMF是酵母Sgm1的哺乳动物同源物,属于高尔基体卷曲螺旋蛋白家族,纠正了之前对其功能的错误认知,填补了哺乳动物高尔基体卷曲螺旋蛋白家族成员鉴定的空白,为高尔基体形态调控机制的研究提供了新的方向。
3. 研究思路总结与详细解析
本研究以“酵母Sgm1的Ypt6结合域定位→哺乳动物同源物TMF筛选→TMF与Rab6的分子互作验证→TMF亚细胞定位分析→RNAi敲低的功能缺失实验”为技术路线,核心科学问题是明确TMF的亚细胞定位与功能,验证其作为高尔基体卷曲螺旋蛋白的属性,最终证实TMF结合Rab6并调控高尔基体形态。
3.1 Sgm1蛋白Ypt6结合域的定位
实验目的:确定酵母Sgm1蛋白中与GTP酶Ypt6结合的具体结构域,为筛选哺乳动物同源物提供靶点。方法细节:构建含C端Protein A标签的Sgm1全长及不同片段(1-488、488-707、597-707)的酵母表达载体,其中全长与1-488片段从着丝粒质粒表达,488-707与597-707片段从多拷贝质粒表达以保证蛋白表达量;制备酵母细胞提取物,与结合GDP或GTPγS的GST-Ypt6孵育,通过免疫印迹检测结合的蛋白。结果解读:如图1所示,
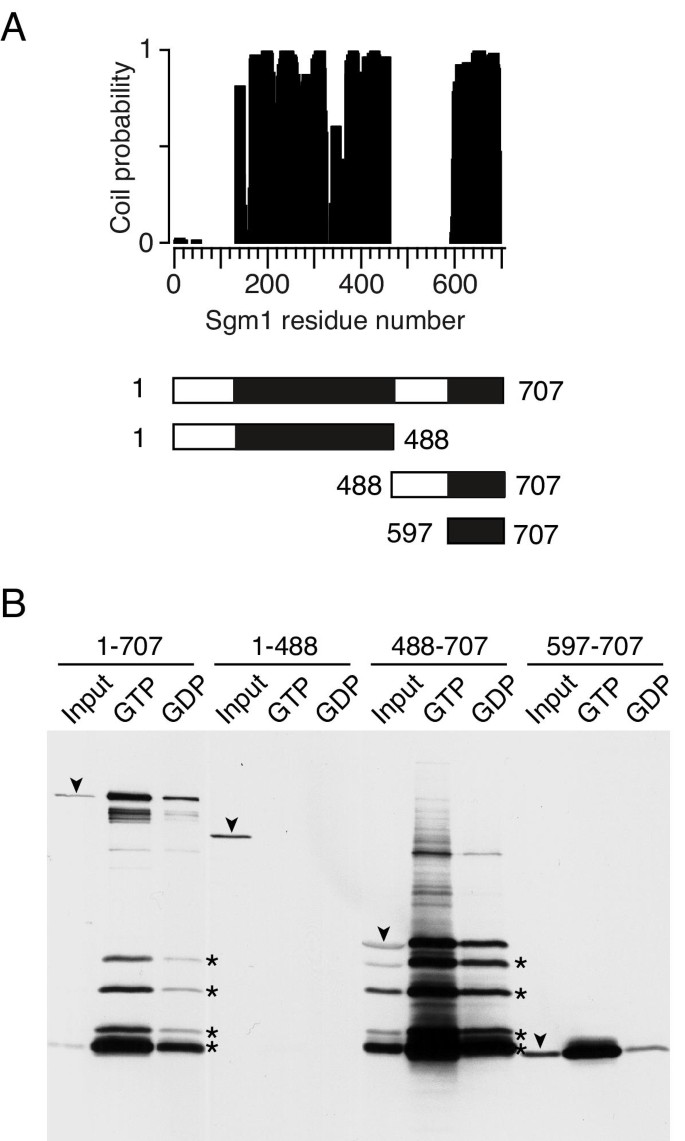
,全长Sgm1及488-707、597-707片段可优先结合Ypt6的GTP活化形式,而1-488片段无结合活性,说明Sgm1的C端卷曲螺旋域(597-707氨基酸)是Ypt6的结合位点。产品关联:文献未提及具体实验产品,领域常规使用GST融合蛋白表达系统、Protein A标签免疫检测试剂、免疫印迹相关试剂等。
3.2 TMF与Rab6的分子互作验证
实验目的:验证TMF作为Sgm1哺乳动物同源物的身份,明确其与Rab6的结合能力及特异性。方法细节:以Sgm1的C端110个氨基酸序列为模板进行迭代BLAST搜索,鉴定到人类TMF蛋白;构建TMF C端310个氨基酸的His标签融合蛋白,在大肠杆菌中表达纯化;同时构建Rab6A、Rab6A"、Rab6B(Rab6的三种亚型)、Rab1及酵母Ypt52的GST融合蛋白,分别结合GDP或GTPγS后与TMF提取物孵育,通过免疫印迹检测结合情况。结果解读:如图3所示,
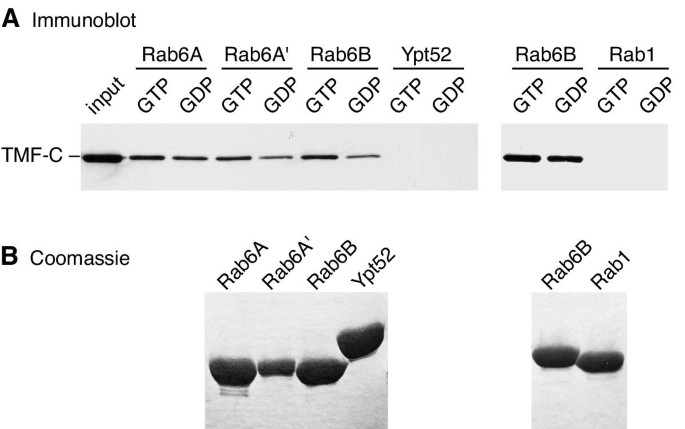
,TMF的C端片段可结合所有三种Rab6亚型,且对GTP活化形式有一定偏好性,而与Rab1或Ypt52无结合,证明其结合的特异性,确认TMF是Sgm1的哺乳动物同源物。产品关联:文献未提及具体实验产品,领域常规使用原核蛋白表达系统、GST pull-down实验试剂盒、His标签蛋白纯化试剂等。
3.3 TMF的亚细胞定位分析
实验目的:明确TMF在哺乳动物细胞中的亚细胞定位,验证其高尔基体相关属性。方法细节:制备针对TMF N端1-280氨基酸的多克隆抗体,通过亚细胞组分分离实验提取大鼠肝脏的高尔基体组分与胞质组分,免疫印迹检测TMF的分布;在COS细胞中进行免疫荧光染色,检测内源性TMF的定位,同时转染HA标签的全长TMF及C端片段,通过抗HA与抗TMF抗体的共染色验证定位的特异性,使用高尔基体标志物TGN38、GOS28进行共定位分析。结果解读:如图4所示,
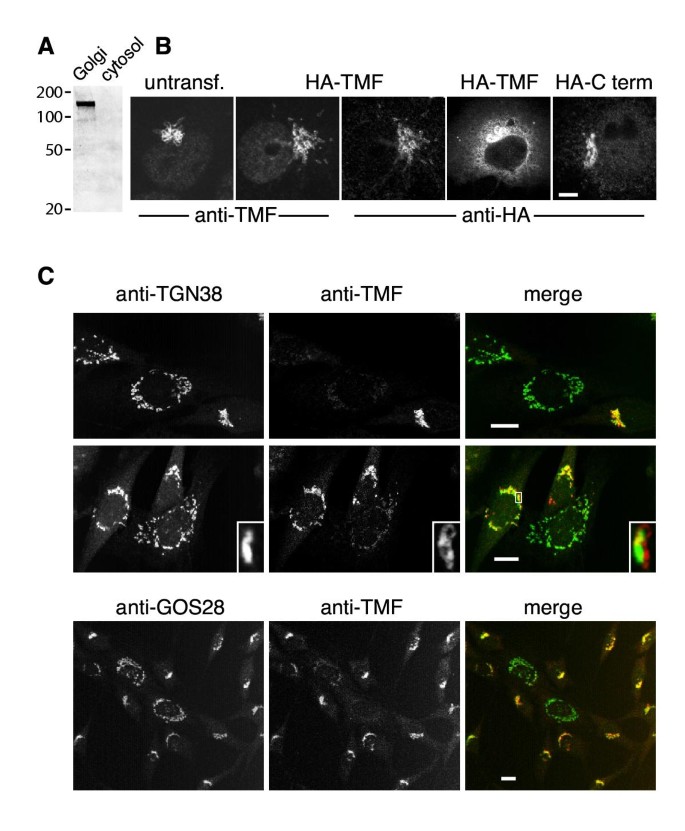
,免疫印迹显示TMF主要存在于高尔基体组分中;免疫荧光结果显示,内源性及过表达的全长TMF均定位于高尔基体,高表达时虽有胞质积累但仍排除在细胞核外,C端片段也定位于高尔基体(少量进入细胞核),进一步证实TMF的高尔基体定位。产品关联:文献未提及具体实验产品,领域常规使用多克隆抗体制备服务、亚细胞组分分离试剂盒、免疫荧光染色试剂、激光共聚焦显微镜等。
3.4 TMF敲低对高尔基体形态的影响
实验目的:探究TMF对高尔基体结构组织的功能作用。方法细节:设计针对TMF的RNAi寡核苷酸,转染大鼠NRK细胞,40小时后固定细胞,免疫荧光染色检测TMF、TGN38与GOS28的定位;定义高尔基体形态紧凑的细胞为高尔基体膜围绕核周不超过一半的细胞,统计正常细胞与TMF敲低细胞中该类细胞的比例。结果解读:如图4C所示,正常细胞中58%呈现紧凑的高尔基体形态,而TMF敲低的细胞中仅8%保持该形态,且敲低细胞的高尔基体膜广泛分散于胞质中,而非局限于核周,说明TMF参与维持高尔基体堆叠的紧凑结构,对高尔基体的组织形态具有重要调控作用。产品关联:文献未提及具体实验产品,领域常规使用RNAi转染试剂、免疫荧光染色试剂、细胞成像分析软件等。
4. Biomarker研究及发现成果
本研究中TMF作为高尔基体形态调控的关键功能蛋白标志物,通过同源序列筛选、分子互作验证、亚细胞定位及功能缺失实验的完整逻辑链条,明确了其作为进化保守的高尔基体卷曲螺旋蛋白的属性与功能。
Biomarker定位方面,TMF是酵母Sgm1的哺乳动物同源物,属于高尔基体卷曲螺旋蛋白家族,筛选逻辑为通过酵母Sgm1的Ypt6结合域进行跨物种同源序列搜索,结合分子互作实验验证其与Rab6的结合,再通过亚细胞定位与功能实验确认其高尔基体相关功能。研究过程中,TMF来源于人类细胞,通过GST pull-down实验验证其与Rab6三种亚型的特异性结合,亚细胞组分分离与免疫荧光实验证实其高尔基体定位,RNAi敲低实验则明确了其对高尔基体形态的调控作用;特异性表现为仅结合Rab6亚型,不与Rab1或Ypt52结合,敏感性方面,敲低TMF可显著改变高尔基体形态,正常细胞与敲低细胞的紧凑高尔基体比例差异具有统计学显著性(n=文献未明确提供具体细胞数,基于图表趋势推测)。核心成果提炼:TMF是首个被明确的结合Rab6的哺乳动物高尔基体卷曲螺旋蛋白同源物,其功能缺失会导致高尔基体结构分散,创新性在于纠正了之前将TMF归类为核转录调控因子的错误认知,首次确立了其高尔基体相关功能,为高尔基体结构调控机制的研究提供了新的靶点,同时为跨物种高尔基体卷曲螺旋蛋白的同源性鉴定提供了新的实验范式。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。