Characterization of Saccharomyces cerevisiae protein Ser/Thr phosphatase T1 and comparison to its mammalian homolog PP5
酿酒酵母蛋白丝氨酸/苏氨酸磷酸酶T1的特性分析及其与哺乳动物同源物PP5的比较
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2003 | 起止号: | 2003 Mar 28;4:3 |
| doi: | 10.1186/1471-2121-4-3 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Characterization of Saccharomyces cerevisiae protein Ser/Thr phosphatase T1 and comparison to its mammalian homolog PP5;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学(蛋白磷酸酶功能调控)
蛋白丝氨酸/苏氨酸磷酸酶是调控细胞信号转导、增殖、分化等关键生命过程的核心分子,其中PP5亚家族因N端包含独特的四肽重复序列(TPR)结构域而区别于其他磷酸酶亚家族。1994年,哺乳动物PP5首次被克隆鉴定,后续研究发现其参与细胞增殖调控、激素信号转导及热休克蛋白90伴侣复合物的功能调节,且其活性可被多不饱和脂肪酸激活,TPR结构域和C端区域对其活性具有自抑制作用。随后在疟原虫、锥虫、非洲爪蟾等多个物种中均发现PP5同源物,但酿酒酵母的Ppt1p作为首个被报道的PP5酵母同源物,此前仅通过基因序列分析被鉴定,缺乏生化特性、细胞定位及功能调控机制的系统研究,领域内对Ppt1p与PP5的调控差异及在酵母细胞中的功能定位尚不明确。本研究旨在填补这一空白,通过生化实验和细胞生物学技术系统表征Ppt1p的特性,为PP5亚家族的进化和功能研究提供酵母模型。
2. 文献综述解析
作者按物种分类梳理PP5亚家族的研究现状,重点对比哺乳动物与低等生物同源物的研究进展,明确现有研究的局限性及本研究的创新价值。
现有研究中,哺乳动物PP5的研究较为深入,已证实其参与细胞增殖、氧化应激响应、激素信号转导等多种生物学过程,其活性受TPR结构域的自抑制调控,多不饱和脂肪酸可通过结合TPR结构域解除自抑制,激活磷酸酶活性;其他物种如疟原虫、锥虫的PP5同源物也被鉴定,且部分研究显示其TPR结构域同样具有自抑制作用,但不同物种间的调控机制差异尚未被系统分析。然而,酿酒酵母的Ppt1p仅通过基因序列被确定为PP5同源物,缺乏生化活性、细胞定位及表达模式的实验数据,也不清楚其调控机制与哺乳动物PP5的异同,这一空白限制了对PP5亚家族进化和功能的全面理解。本研究的创新点在于首次系统表征Ppt1p的生化特性、结构域调控功能、细胞定位和表达模式,并与哺乳动物PP5进行全面对比,为PP5亚家族的功能研究提供了酵母模型,同时揭示了不同物种间PP5同源物调控机制的进化差异。
3. 研究思路总结与详细解析
本研究以酿酒酵母Ppt1p为研究对象,整体研究框架为“重组蛋白生化分析→结构域功能验证→细胞表达与定位分析”,核心科学问题是明确Ppt1p的活性调控机制及其与哺乳动物PP5的差异,技术路线遵循“假设-实验验证-结论”的逻辑闭环,通过多维度实验系统解析Ppt1p的特性。
3.1 重组Ppt1p与PP5的表达纯化及活性对比
实验目的:对比Ppt1p与哺乳动物PP5的基础磷酸酶活性及对脂质激活的响应差异,明确二者的底物特异性。
方法细节:构建谷胱甘肽S-转移酶(GST)融合的Ppt1p及C端截短突变体Ppt1p(1-504)的原核表达载体,转化大肠杆菌BL21(DE3)菌株诱导表达,通过谷胱甘肽琼脂糖亲和纯化融合蛋白,再用凝血酶切割去除GST标签,获得纯的重组蛋白;以32P标记的髓鞘碱性蛋白(MBP)和酪蛋白为人工底物,在有无花生四烯酸(AA)的条件下,于30℃孵育10-15分钟测定磷酸酶活性,每个实验设置三次重复。
结果解读:SDS-聚丙烯酰胺凝胶电泳(SDS-PAGE)显示纯化的Ppt1p为58kDa的单一条带,纯度超过95%(图1A);Ppt1p与PP5对两种底物的基础比活性相似(图1B);Ppt1p对32P-MBP的去磷酸化活性可被AA等不饱和脂肪酸激活,但对32P-酪蛋白的活性无显著影响,提示Ppt1p的底物特异性激活机制与PP5不同。
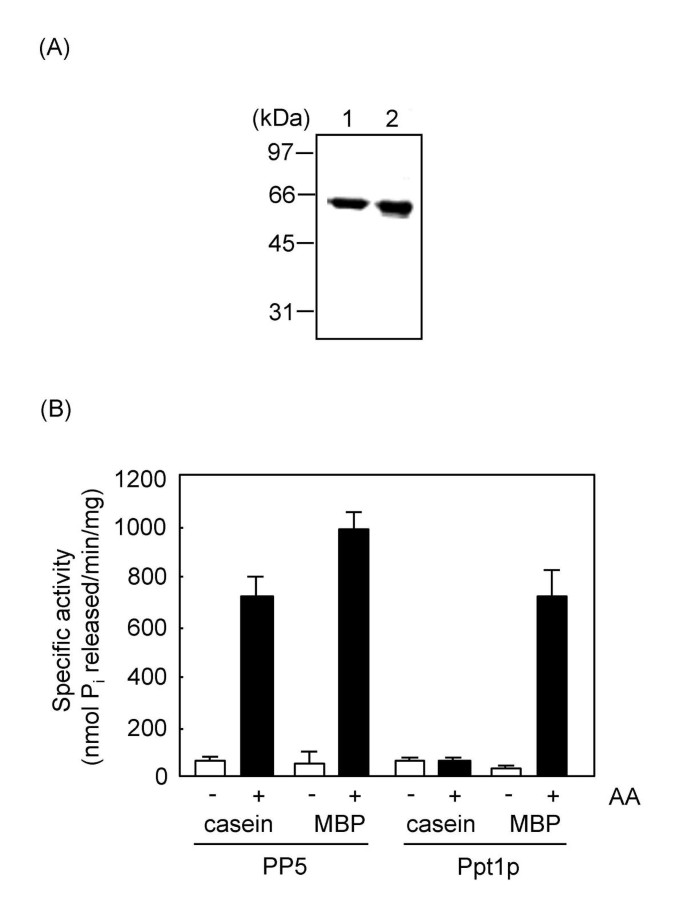
实验所用关键产品:限制性内切酶(New England Biolabs、Promega、Gibco BRL)、蛋白纯化试剂(Sigma)、凝血酶(Roche Molecular Biochemicals)等。
3.2 有限蛋白酶解分析Ppt1p结构域功能
实验目的:探究TPR结构域对Ppt1p活性的调控作用,明确其与PP5的调控差异。
方法细节:用胰蛋白酶或枯草杆菌蛋白酶对重组Ppt1p进行有限蛋白酶解,在有无AA的条件下分析降解产物的变化,通过SDS-PAGE分离降解产物并进行考马斯亮蓝染色,对关键降解产物进行N端测序确定切割位点;同时测定降解后Ppt1p对两种底物的磷酸酶活性,每个实验重复三次以上。
结果解读:胰蛋白酶切割Ppt1p产生44kDa的催化结构域片段和20kDa的TPR结构域片段,AA存在时TPR结构域的降解模式发生改变,出现14-16kDa的小片段,说明脂质结合改变了TPR结构域的构象(图2A);N端测序显示切割位点位于TPR结构域与催化结构域的连接区域,与PP5的切割位点相似(图2B);去除TPR结构域后,Ppt1p对32P-MBP的活性提升2倍,但对32P-酪蛋白的活性无影响,且失去对脂质的响应(图2C),这与PP5去除TPR结构域后活性提升5-25倍的结果不同,提示Ppt1p的TPR结构域对活性的自抑制作用弱于PP5。
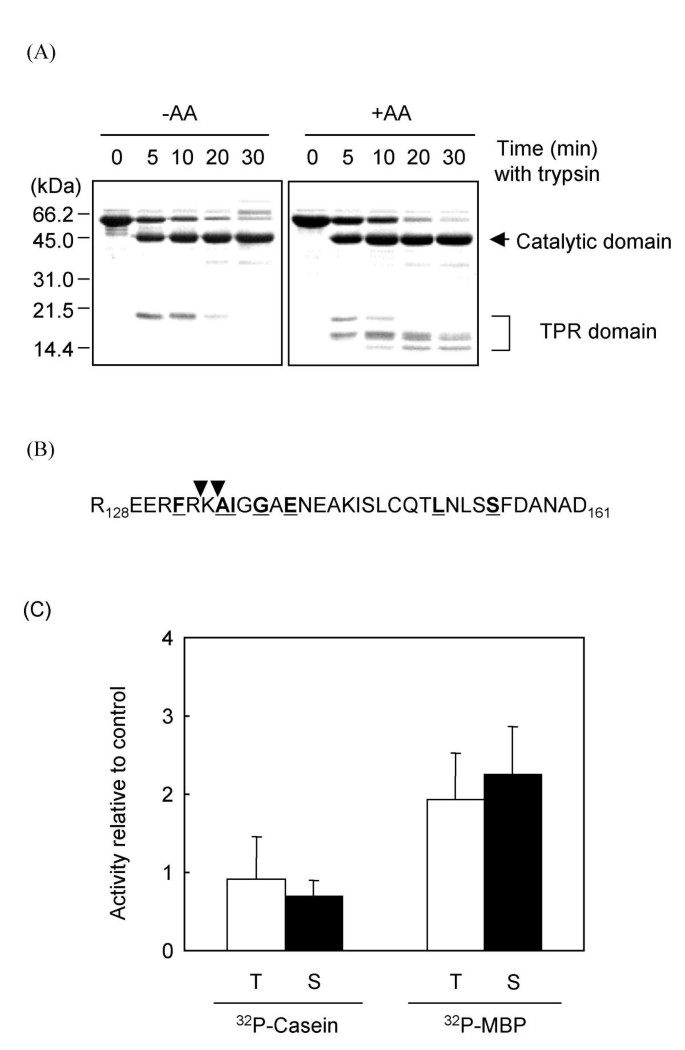
实验所用关键产品:胰蛋白酶、枯草杆菌蛋白酶(Roche Molecular Biochemicals)、N端测序服务(Purdue Macromolecular Structure Facility)等。
3.3 C端截短突变体的活性分析
实验目的:探究C端区域对Ppt1p活性的调控作用,对比其与PP5的调控差异。
方法细节:构建C端截短9个氨基酸的Ppt1p(1-504)突变体,在大肠杆菌中表达纯化后,测定其对32P-MBP和32P-酪蛋白的基础活性及对AA的响应,与全长Ppt1p进行对比,每个实验重复三次。
结果解读:与全长Ppt1p相比,截短突变体对两种底物的基础活性均提升2倍,且对32P-MBP的活性仍可被AA激活12倍(图3A);而哺乳动物PP5截短C端后活性大幅提升,且不再被脂质激活,序列比对显示Ppt1p与PP5的C端区域存在差异(图3B),提示Ppt1p的C端区域对活性的调控机制与PP5不同,其自抑制作用较弱。
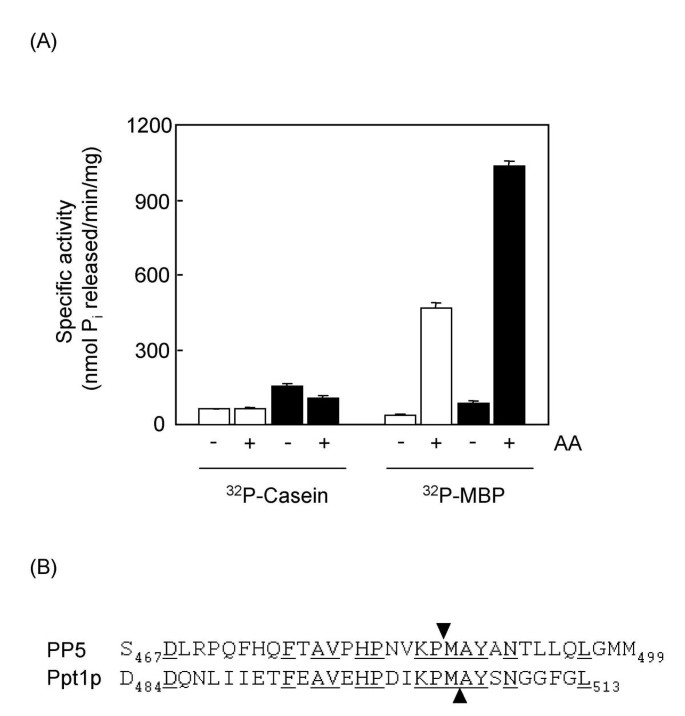
实验所用关键产品:PCR试剂(Sigma)、蛋白纯化试剂(Sigma)等。
3.4 HA-Ppt1p的细胞表达模式与定位分析
实验目的:确定Ppt1p在酵母细胞中的表达时序和亚细胞定位,明确其在酵母细胞中的功能定位。
方法细节:通过两步基因替换法构建表达HA标记Ppt1p的酵母菌株WHT4-1;收集不同生长阶段的酵母细胞,通过免疫印迹检测HA-Ppt1p的蛋白表达水平,Northern blot检测PPT1 mRNA的表达水平;取对数生长早期的细胞,通过间接免疫荧光结合DAPI核染色分析Ppt1p的亚细胞定位,同时表达Spc42p-EGFP作为对照验证免疫荧光方法的可靠性,每个实验重复四次。
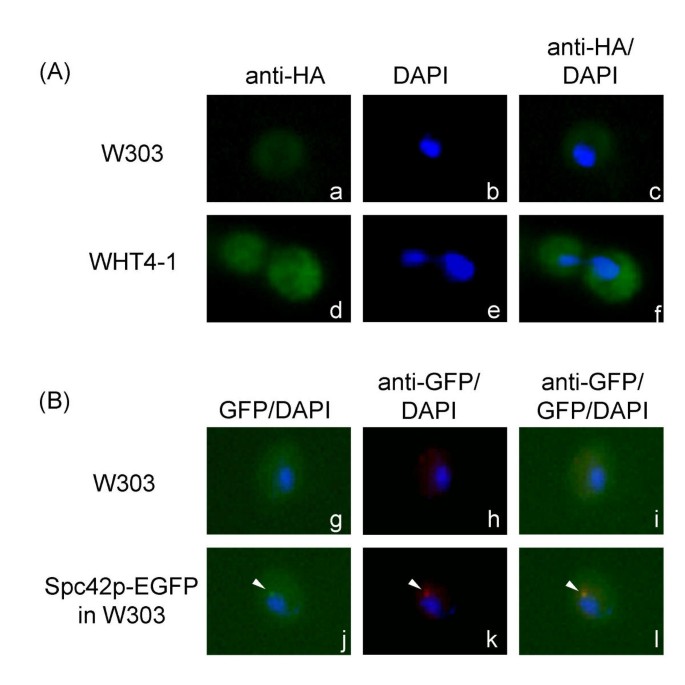
结果解读:免疫印迹和Northern blot结果显示,Ppt1p的蛋白和mRNA水平在对数生长早期达到峰值,进入稳定期后显著下降(图4A、B、C),提示Ppt1p的表达与细胞增殖速率正相关;间接免疫荧光显示Ppt1p分布在细胞核和细胞质中,且与细胞周期无关(图5A);对照实验中Spc42p-EGFP的定位结果与已知的纺锤体极体定位一致,验证了免疫荧光方法的可靠性(图5B)。
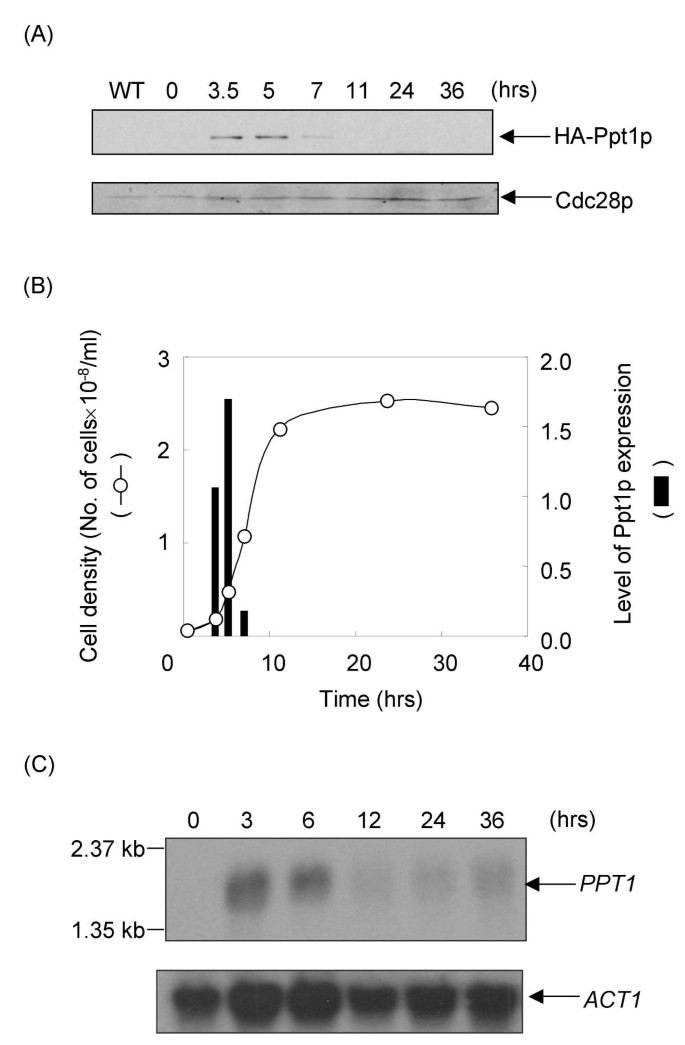
实验所用关键产品:抗HA单克隆抗体(Roche Molecular Biochemicals)、抗Cdc28p抗体(Santa Cruz Biotechnology)、DAPI染色剂(Sigma)、荧光显微镜(Olympus BX60)等。
4. Biomarker研究及发现成果解析
本研究中Ppt1p作为酿酒酵母细胞生长状态的功能性Biomarker,其表达水平与细胞增殖速率密切相关,通过系统的实验验证明确了其作为细胞生长状态标记物的特异性和可靠性。
Biomarker定位:Ppt1p属于细胞功能状态类Biomarker,筛选逻辑为基于PP5亚家族与细胞增殖的关联假设,通过生长曲线结合蛋白和mRNA表达分析筛选得到,验证逻辑为“细胞生长阶段分析→免疫印迹验证→Northern blot验证→重复实验确认”的完整链条。
研究过程详述:Biomarker来源为酿酒酵母细胞的内源性蛋白,验证方法包括免疫印迹(检测蛋白表达水平)、Northern blot(检测mRNA表达水平),特异性表现为仅在对数生长早期高表达,稳定期表达水平显著降低,样本量为四次独立实验(n=4),统计学结果显示对数早期与稳定期的表达差异具有显著趋势(文献未明确提供该数据,基于图表趋势推测)。
核心成果提炼:Ppt1p作为细胞生长状态的标记物,其表达水平与酵母细胞增殖速率正相关,首次发现其TPR结构域和C端区域的自抑制作用弱于哺乳动物PP5,且定位于细胞核和细胞质,提示其可能在多个亚细胞区域参与细胞信号调控;创新性在于首次系统表征酵母PP5同源物的特性,揭示了PP5亚家族调控机制的进化差异,为PP5的功能研究提供了酵母模型,同时Ppt1p可作为酵母细胞快速生长状态的特异性标记物,用于细胞增殖相关的研究。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。