Expression of epidermal growth factor, transforming growth factor-β1 and adiponectin in nipple aspirate fluid and plasma of pre and post-menopausal women
绝经前和绝经后妇女乳头抽吸液和血浆中表皮生长因子、转化生长因子-β1和脂联素的表达
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2013 | 起止号: | 2013 Apr 15;1(1):18 |
| doi: | 10.1186/2050-7771-1-18 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Expression of epidermal growth factor, transforming growth factor-β1 and adiponectin in nipple aspirate fluid and plasma of pre and post-menopausal women;发表期刊:Biomarker Research;影响因子:未公开;研究领域:乳腺肿瘤预防生物标志物研究。
乳腺肿瘤是女性高发恶性肿瘤,预防研究中需寻找能反映乳腺微环境的生物标志物。乳头抽吸液(nipple aspirate fluid, NAF)因富含蛋白质且直接源于乳腺导管系统,被认为更贴近乳腺局部微环境,其产生曾被证实与乳腺癌风险 doubling 相关(Petrakis 等),是乳腺肿瘤预防的潜在生物标志物来源。但现有研究多聚焦 NAF 与肿瘤的关联,健康女性 NAF 与血浆中特定蛋白的相关性、绝经状态及身体质量指数(body mass index, BMI)对生物标志物的修饰作用尚未明确——这一空白限制了 NAF 作为乳腺风险评估工具的临床转化。本研究通过收集 43 名健康绝经前与绝经后女性的匹配 NAF 和血浆样本,比较表皮生长因子(epidermal growth factor, EGF)、转化生长因子-β1(transforming growth factor-β1, TGF-β1)、脂联素的水平差异,旨在阐明 NAF 与血浆生物标志物的独立性及绝经状态、BMI 的影响,为乳腺肿瘤风险的多维度评估提供生物学依据。
2. 文献综述解析
文献综述围绕“NAF 作为乳腺微环境生物标志物的潜力”展开核心评述:作者首先回顾 NAF 的生物学特性——NAF 由乳腺导管上皮细胞分泌,成分反映乳腺局部代谢与免疫状态(Malatesta 等);接着梳理 NAF 与乳腺癌风险的关联:Petrakis 等发现“能产生 NAF 的女性乳腺癌风险增加 2 倍”,推动 NAF 成为乳腺风险标志物的研究热点,但现有研究多针对肿瘤患者,健康女性 NAF 与血浆生物标志物的对比研究极少;最后指出现有研究的局限性:未纳入匹配血浆样本、未考虑绝经状态(激素水平变化)和 BMI(代谢状态)对生物标志物的影响。
现有研究的关键结论包括:① NAF 是乳腺局部微环境的“窗口”,但其与循环系统(血浆)的物质交换机制不明;② 仅少数研究用 NAF 筛查乳腺风险标志物(Sauter 等),但缺乏血浆数据验证其特异性;技术方法上,已有研究采用 ELISA 检测 NAF 蛋白,但未对 NAF 总蛋白进行归一化(忽略样本浓度差异);局限性集中在“样本量小”“未控制混杂因素”。本研究的创新价值在于:首次在健康人群中分析匹配 NAF 与血浆样本的三种生物标志物水平,系统探讨绝经状态和 BMI 的修饰作用,明确 NAF 生物标志物的“局部特异性”——这补充了 NAF 作为独立风险评估工具的理论基础。
3. 研究思路总结与详细解析
3.1 整体研究框架
研究目标:比较健康绝经前与绝经后女性 NAF 和血浆中 EGF、TGF-β1、脂联素的水平差异,评估绝经状态和 BMI 的修饰作用;核心科学问题:NAF 与血浆生物标志物是否相关?绝经状态、BMI 如何影响两者的表达?技术路线遵循“招募对象→样本收集→生物标志物检测→统计分析”的闭环逻辑:① 招募 43 名健康女性(16 名绝经前、27 名绝经后);② 收集基线匹配 NAF 和血浆;③ ELISA 定量检测生物标志物;④ 用线性回归(控制 BMI)比较组间差异,Spearman 相关分析相关性。
3.2 研究对象招募与样本收集
实验目的:获取健康绝经前与绝经后女性的匹配 NAF 和血浆样本,确保人群同质性。
方法细节:纳入标准为“18-65 岁、无恶性肿瘤史、未怀孕/哺乳、无严重代谢疾病”的健康女性;NAF 收集采用“乳腺按摩+Medela 吸乳器”,样本立即用磷酸盐缓冲液(PBS)1:10 稀释;血浆收集用肝素抗凝管,离心分离后与 NAF 共同存储于-80℃。
结果解读:共纳入 16 名绝经前(平均年龄 44.5 岁,BMI 28.3 kg/m²)、27 名绝经后女性(平均年龄 58.2 岁,BMI 26.1 kg/m²);NAF 体积差异大(3-50 μL),总蛋白浓度范围 13-101 mg/mL(提示需归一化处理)。
实验所用关键产品:Medela 乳腺吸乳器、肝素钠抗凝管(未提及具体品牌)。
3.3 生物标志物定量检测
实验目的:精准测量 NAF 和血浆中 EGF、TGF-β1、脂联素的水平,消除样本浓度差异的干扰。
方法细节:采用 R&D Systems 的 ELISA 试剂盒检测,NAF 样本根据蛋白浓度稀释(EGF 1:100-400、TGF-β1 1:20-40、脂联素 1:3-20),血浆样本按试剂盒说明书稀释(脂联素 1:200);每样本设复孔(变异系数 CV<10%),确保检测稳定性。
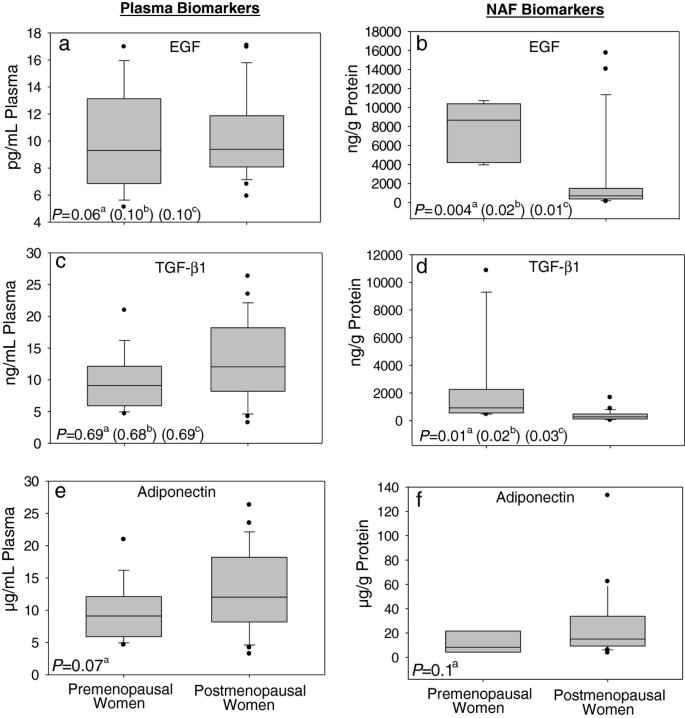
结果解读:最终获得 33 对 EGF、35 对 TGF-β1、28 对脂联素的匹配数据;NAF 生物标志物水平经“总蛋白浓度归一化”后,绝经前女性 NAF 中 EGF(均值 12.6 pg/mg 总蛋白)、TGF-β1(均值 45.2 pg/mg 总蛋白)显著高于绝经后(EGF 均值 5.8 pg/mg 总蛋白,TGF-β1 均值 22.1 pg/mg 总蛋白),血浆中无此差异(P>0.05)。
实验所用关键产品:R&D Systems 的 EGF(货号未提及)、TGF-β1(货号未提及)、脂联素 ELISA 试剂盒(货号未提及)。
3.4 统计分析与结果验证
实验目的:分析 NAF 与血浆生物标志物的相关性,验证绝经状态、BMI 的修饰作用。
方法细节:用线性回归模型控制 BMI,比较绝经前与绝经后生物标志物的差异;Spearman 相关系数分析 NAF 与血浆、生物标志物与 BMI 的关联;P<0.05 为统计学显著。
结果解读:① NAF 与血浆生物标志物无相关性(Spearman 系数均<0.3,P>0.05);② 绝经前女性 NAF 中 EGF(P=0.004)、TGF-β1(P=0.01)显著高于绝经后,血浆中无此差异;③ 绝经后女性血浆中 EGF(P=0.003)、TGF-β1(P<0.001)、脂联素(P=0.05)均与 BMI 呈负相关,但 NAF 生物标志物与 BMI 无关联(P>0.05)。
4. Biomarker 研究及发现成果解析
4.1 Biomarker 定位与筛选逻辑
本研究的生物标志物为“NAF/血浆中的 EGF、TGF-β1、脂联素”,筛选逻辑基于“生物标志物与乳腺风险的关联”:EGF 促进乳腺上皮细胞增殖(Foley 等)、TGF-β1 调控细胞凋亡与侵袭(Muraoka-Cook 等)、脂联素参与代谢与炎症(Chen 等)——三者均是乳腺肿瘤发生的关键调控因子。验证路径遵循“临床样本收集→ELISA 定量→统计关联分析”,确保生物标志物的“临床相关性”与“检测可靠性”。
4.2 研究过程与核心数据
Biomarker 来源为“健康女性的 NAF 和血浆”(NAF 反映局部,血浆反映系统);验证方法采用 ELISA(灵敏度:EGF 3.9-250 pg/mL、TGF-β1 31.2-2000 pg/mL、脂联素 3.9-250 ng/mL),NAF 样本经总蛋白归一化(消除体积差异);关键数据包括:
- 相关性:NAF 与血浆 EGF、TGF-β1、脂联素无显著相关(Spearman 系数分别为 0.12、0.21、0.09,P>0.05);
- 绝经状态影响:绝经前女性 NAF 中 EGF(P=0.004)、TGF-β1(P=0.01)显著高于绝经后,血浆中无差异;
- BMI 影响:绝经后女性血浆 EGF(r=-0.45,P=0.003)、TGF-β1(r=-0.52,P<0.001)、脂联素(r=-0.38,P=0.05)与 BMI 负相关,NAF 中无关联。
4.3 成果与创新价值
本研究的核心成果为:NAF 生物标志物具有“局部特异性”——其水平不受循环系统(血浆)影响,且绝经状态、BMI 对 NAF 与血浆生物标志物的调控机制不同。具体包括:
1. 生物标志物独立性:NAF 与血浆中 EGF、TGF-β1、脂联素无相关性,提示 NAF 能提供血浆之外的“乳腺局部风险信息”;
2. 绝经状态的修饰作用:绝经前女性 NAF 中促增殖因子(EGF、TGF-β1)水平更高,可能与雌激素水平相关(Chatterton 等),而血浆中无此差异——这解释了“绝经后女性乳腺癌风险升高但 NAF 生物标志物下降”的矛盾;
3. BMI 的代谢调控差异:绝经后女性血浆生物标志物与 BMI 负相关(符合“脂联素与 BMI 负相关”的领域共识),但 NAF 中无关联——提示 BMI 对乳腺局部的影响可能通过“非循环途径”(如脂肪组织局部分泌)实现。
这些发现的创新性在于:首次在健康人群中证明“NAF 生物标志物的局部特异性”,为乳腺肿瘤风险的“局部+系统”双维度评估提供了实验依据——未来可通过联合检测 NAF 与血浆生物标志物,提高乳腺风险预测的准确性。
本研究的局限性为样本量小(43 例),但已通过“匹配样本”“归一化处理”控制了部分混杂;未来需扩大样本量,验证激素水平(如雌激素)对 NAF 生物标志物的调控机制,推动 NAF 成为乳腺肿瘤预防的“非侵入性筛查工具”。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。