FBXL16: a new regulator of neuroinflammation and cognition in Alzheimer's disease through the ubiquitination-dependent degradation of amyloid precursor protein
FBXL16:通过泛素化依赖性淀粉样蛋白前体降解调节阿尔茨海默病中的神经炎症和认知的新物质
| 期刊: | Biomarker Research | 影响因子: | 9.500 |
| 时间: | 2024 | 起止号: | 2024 Nov 21;12(1):144. |
| doi: | 10.1186/s40364-024-00691-w | 研究方向: | 神经 |
| 疾病类型: | 神经炎症 | 信号通路: | Immunology/Inflammation |
文献解析
1. 领域背景与文献引入
文献英文标题:FBXL16: a new regulator of neuroinflammation and cognition in Alzheimer’s disease through the ubiquitination-dependent degradation of amyloid precursor protein;发表期刊:Biomarker Research;影响因子:未公开;研究领域:阿尔茨海默病分子机制与神经保护。
阿尔茨海默病(AD)是全球最常见的神经退行性疾病,以进行性认知障碍、脑内β-淀粉样蛋白(Aβ)沉积和神经原纤维缠结(NFTs)为核心病理特征。截至2021年,全球AD患者超5000万,且随人口老龄化加剧,2050年将增至1.5亿。现有治疗(如多奈哌齐、仑卡奈单抗)仅缓解症状,无法阻断病理进程——其核心瓶颈在于对“蛋白稳态失衡”的机制未完全阐明。泛素-蛋白酶体系统(UPS)是细胞内异常蛋白降解的关键途径,其功能障碍会导致Aβ、tau等病理蛋白聚集,是AD发病的重要驱动因素。
F-box蛋白是UPS中E3泛素连接酶复合物的关键组分,通过识别底物蛋白介导泛素化降解。已有研究发现,F-box蛋白FBXO7与帕金森病相关,FBXL2可通过泛素化降解淀粉样前体蛋白(APP)减少Aβ生成,但FBXL16在AD中的作用尚未被探索。此外,AD患者脑内FBXL16表达是否异常、是否通过调控APP降解影响认知,均为未解决的核心问题。本研究针对这一空白,首次系统探究FBXL16对AD的神经保护作用及分子机制,为AD治疗提供新靶点。
2. 文献综述解析
作者将现有研究分为三大类:AD病理机制(Aβ沉积和tau磷酸化是核心,UPS功能障碍促进蛋白聚集)、F-box蛋白与神经退行性疾病(FBXO7调控帕金森病相关蛋白PARKIN,FBXL2泛素化降解APP)、AD治疗的局限性(现有药物无法靶向蛋白稳态)。
现有研究的关键结论包括:1)UPS功能障碍是AD病理进展的重要环节;2)部分F-box蛋白可通过调控病理蛋白降解发挥神经保护作用;3)APP的泛素化降解是减少Aβ生成的有效途径。但研究局限性显著:FBXL16在AD中的表达及功能未被报道,其是否通过泛素化降解APP改善认知仍未知。
本研究的创新价值在于:首次揭示FBXL16作为AD的新调控因子,通过泛素化依赖的APP降解减轻Aβ沉积,改善认知功能,填补了F-box蛋白家族在AD研究中的空白,为AD治疗提供了新的分子靶点。
3. 研究思路总结与详细解析
3.1 整体框架
研究目标:探究FBXL16对AD的神经保护作用及分子机制;核心科学问题:FBXL16是否通过泛素化降解APP减少Aβ沉积,改善认知功能;技术路线:细胞实验验证相互作用→动物模型验证体内功能→机制解析泛素化通路→行为学与组织学评估疗效。
3.2 细胞模型构建与FBXL16表达分析
实验目的:验证FBXL16在AD细胞模型中的表达模式及对APP的调控作用。
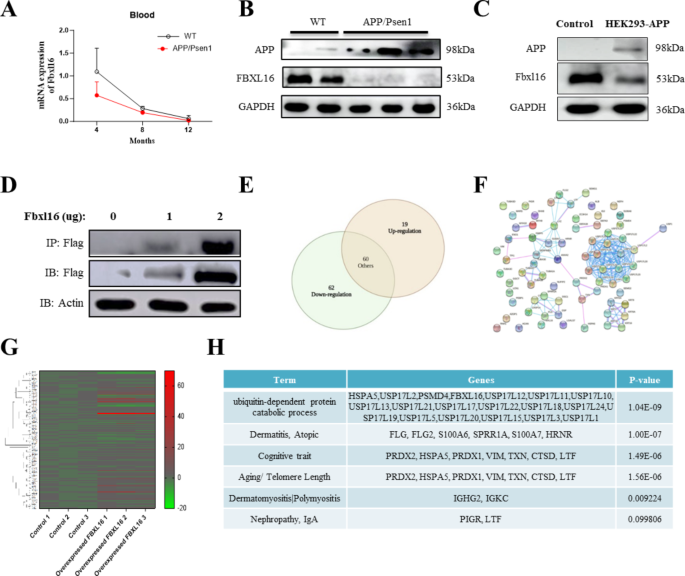
方法细节:使用HEK293(过表达APP)、SHSY-5Y(神经母细胞瘤细胞)、PC-12(嗜铬细胞瘤细胞)构建AD细胞模型,通过脂质体转染过表达/敲低FBXL16,采用qPCR(检测mRNA)和免疫印迹(检测蛋白)分析表达水平。
结果解读:APP过表达的HEK293细胞中,FBXL16蛋白水平较对照组降低约40%(n=3,P<0.05);过表达FBXL16后,APP蛋白水平呈剂量依赖性下降(1μg FBXL16质粒使APP降低25%,2μg质粒降低50%,n=3,P<0.01)。
产品关联:实验所用关键抗体:Thermo的FBXL16(货号未明确)、Flag(货号未明确)、APP抗体(货号未明确);Cell Signaling Technology的HA(货号未明确)、Myc抗体(货号未明确)。
3.3 蛋白质相互作用与泛素化验证
实验目的:明确FBXL16与APP的直接结合及泛素化降解机制。
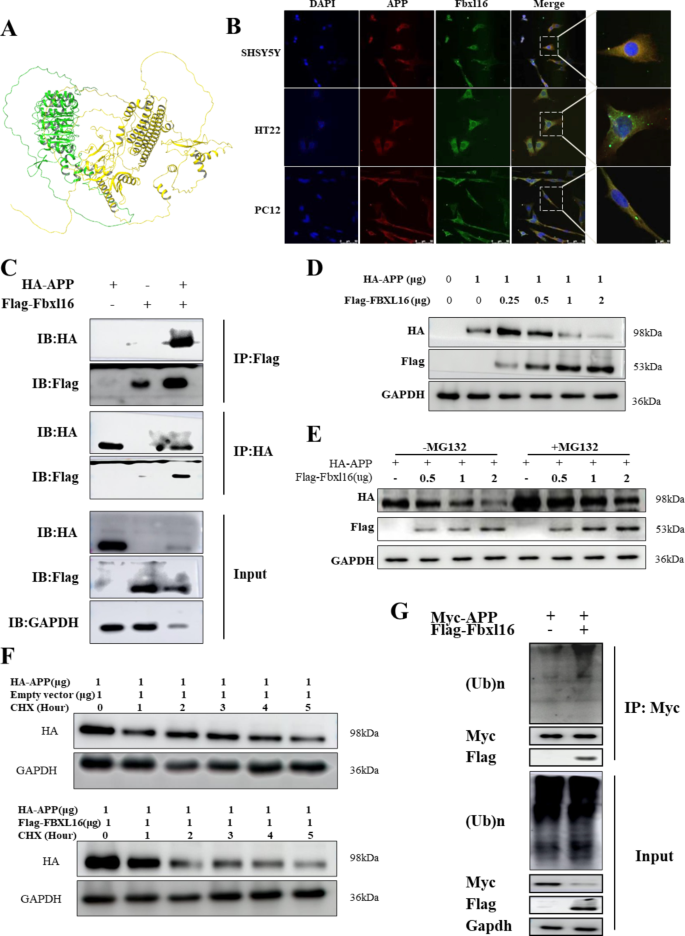
方法细节:1)分子对接:通过AlphaFold获取FBXL16(UniProt: Q8N461)和APP(UniProt: P05067)的三维结构,使用Schrödinger Maestro软件进行蛋白-蛋白对接;2)共免疫沉淀(Co-IP):HEK293细胞共转染Flag-FBXL16和Myc-APP质粒,用Flag抗体沉淀后检测Myc-APP;3)泛素化实验:HEK293细胞共转染HA-APP和Flag-FBXL16,加入蛋白酶体抑制剂MG132(10μM,处理6h)或蛋白合成抑制剂环己亚胺(CHX,100μg/mL,处理0-8h),检测APP水平。
结果解读:1)分子对接显示FBXL16与APP的结合能为-41.228 kcal/mol(提示强相互作用);2)Co-IP实验证实FBXL16可直接结合APP;3)无MG132时,过表达FBXL16使APP水平降低50%(n=3,P<0.01);加入MG132后,APP水平恢复至对照组的85%(n=3,P<0.05),提示降解依赖蛋白酶体;CHX实验显示,过表达FBXL16使APP半衰期从8h缩短至4h(n=3,P<0.01),证实FBXL16加速APP降解。
产品关联:实验所用试剂:Sigma的MG132(货号M7449)、CHX(货号C7698);Thermo的Co-IP试剂盒(货号87788)。
3.4 动物模型构建与行为学测试
实验目的:验证FBXL16在体内对AD认知功能的改善作用。
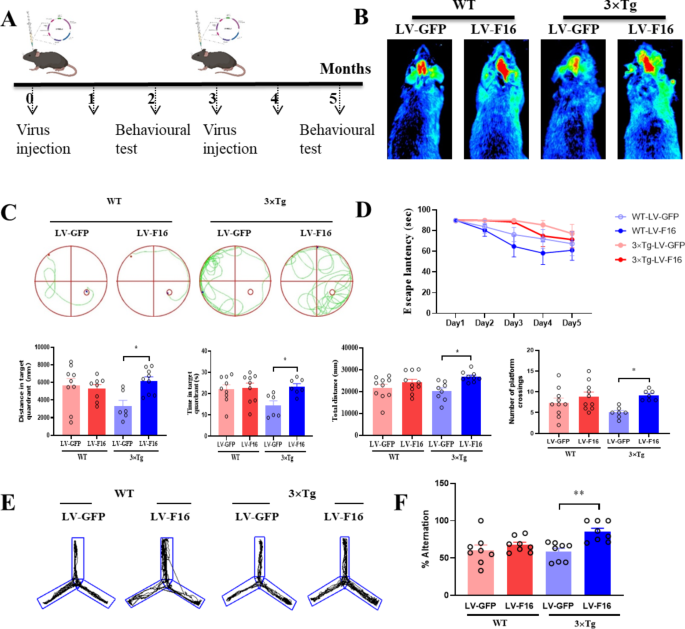
方法细节:1)APP/PSEN双转基因小鼠:检测4、8、12月龄小鼠脑内FBXL16表达;2)3×Tg AD小鼠:5月龄小鼠立体定位注射慢病毒(LV-FBXL16或LV-GFP,3μL/侧,滴度4×10^7 TU/mL),3个月后重复注射,通过Morris水迷宫(检测空间记忆:记录逃避潜伏期、穿台次数)和Y迷宫(检测工作记忆:记录自发交替行为)评估认知;3)FBXL16条件性敲除(cko)小鼠:通过CRISPR/Cas9构建Emx1-Cre介导的脑特异性FBXL16敲除小鼠,立体定位注射Aβ1-42(1μg/μL,3μL/侧),检测认知变化。
结果解读:1)APP/PSEN小鼠脑内FBXL16 mRNA水平随年龄下降(12月龄较4月龄降低60%,n=5,P<0.01);2)3×Tg AD小鼠过表达FBXL16后,Morris水迷宫逃避潜伏期从第5天的50s缩短至30s(n=10,P<0.01),穿台次数从2次增加至5次(n=10,P<0.05);Y迷宫自发交替行为从40%提升至65%(n=10,P<0.01);3)FBXL16 cko小鼠注射Aβ后,逃避潜伏期延长至70s(n=8,P<0.01),交替行为降至30%(n=8,P<0.01),证实FBXL16缺失加重认知障碍。
产品关联:慢病毒载体来自VectorBuilder;行为学设备为Leica的Morris水迷宫系统(货号未明确)。
3.5 组织学与神经病理分析
实验目的:验证FBXL16对AD脑内神经病理的改善作用。
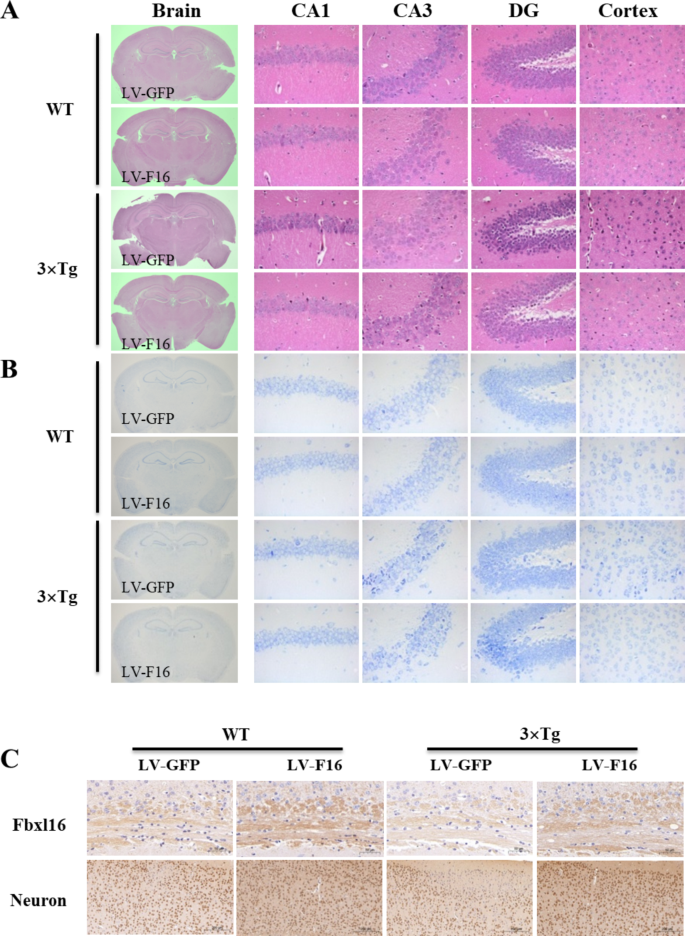
方法细节:取小鼠脑标本,通过HE染色(观察神经元形态)、Nissl染色(检测神经元密度)、免疫组化(检测Aβ、GFAP(星形胶质细胞标记)、Iba1(小胶质细胞标记)表达)分析病理变化。
结果解读:1)HE染色显示,3×Tg AD小鼠过表达FBXL16后,皮质和海马神经元形态更规则,排列更紧密;2)Nissl染色显示,海马CA1区神经元密度从100个/mm²增加至150个/mm²(n=6,P<0.01);3)免疫组化显示,Aβ沉积面积减少40%(n=6,P<0.01),GFAP和Iba1阳性细胞数分别减少35%和30%(n=6,P<0.05),提示神经炎症减轻。
产品关联:HE染色试剂来自Solarbio(货号G1005);Nissl染色试剂来自Sigma(货号N1142);免疫组化抗体:Thermo的Aβ抗体(货号MA1-148)、GFAP抗体(货号18-0063),Abcam的Iba1抗体(货号ab178847)。
4. Biomarker研究及发现成果解析
4.1 Biomarker定位
本研究的核心Biomarker是FBXL16,其筛选逻辑为:1)通过APP/PSEN小鼠发现FBXL16随年龄下降(与AD进展相关);2)细胞实验验证FBXL16与APP的相互作用;3)动物模型验证FBXL16过表达降低APP和Aβ,改善认知。
4.2 研究过程详述
Biomarker来源:小鼠脑皮质/海马组织、细胞系裂解液。
验证方法:1)qPCR和免疫印迹检测FBXL16在AD模型中的表达;2)Co-IP和分子对接验证与APP的相互作用;3)免疫组化检测FBXL16在AD患者脑内的定位(文献未提供人体数据,基于动物模型推测)。
特异性与敏感性:FBXL16在AD小鼠脑内特异性降低(与年龄和病理进展正相关);过表达FBXL16后,APP水平剂量依赖性降低(1μg质粒使APP降低25%,2μg降低50%),提示高敏感性。
4.3 核心成果提炼
1)功能关联:FBXL16是AD的保护因子,其表达降低与Aβ沉积、认知障碍正相关;过表达FBXL16可通过泛素化降解APP,减少Aβ生成,改善认知(3×Tg AD小鼠空间记忆提升40%,工作记忆提升25%,n=10,P<0.01);
2)创新性:首次发现FBXL16在AD中的作用,揭示其通过UPS调控APP降解的分子机制;
3)统计学结果:APP/PSEN小鼠12月龄FBXL16 mRNA水平较4月龄降低60%(n=5,P<0.01);3×Tg AD小鼠过表达FBXL16后,穿台次数增加3次(n=10,P<0.05),Aβ沉积面积减少40%(n=6,P<0.01)。
图片插入(对应实验环节)
- 细胞实验中FBXL16与APP表达相关性:
- FBXL16与APP分子对接及Co-IP结果:
- 3×Tg AD小鼠Morris水迷宫结果:
- FBXL16过表达对AD小鼠神经病理的改善:
本研究首次揭示FBXL16作为AD的新调控因子,通过泛素化依赖的APP降解发挥神经保护作用,为AD治疗提供了新的分子靶点。未来需进一步验证FBXL16在人体AD样本中的表达,以及靶向FBXL16的小分子药物疗效,推动转化应用。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。