Myeloid-derived suppressor cells: key immunosuppressive regulators and therapeutic targets in hematological malignancies
髓系来源的抑制细胞:血液系统恶性肿瘤的关键免疫抑制调节因子和治疗靶点
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2023 | 起止号: | 2023 Mar 29;11(1):34 |
| doi: | 10.1186/s40364-023-00475-8 | 研究方向: | 细胞生物学、肿瘤、免疫/内分泌 |
文献解析
1. 领域背景与文献引入
文献英文标题:Myeloid-derived suppressor cells: key immunosuppressive regulators and therapeutic targets in hematological malignancies;发表期刊:Biomarker Research;影响因子:未公开;研究领域:血液系统恶性肿瘤中的免疫抑制调控与靶向治疗。
髓源性抑制细胞(MDSCs)是一类起源于造血干细胞的未成熟髓细胞群体,其研究可追溯至1970年代——科学家在肿瘤小鼠中发现一类能抑制T细胞功能的“免疫抑制髓细胞”,2007年国际共识正式将其命名为MDSCs。生理状态下,MDSCs在健康人外周血中数量极低;但在癌症、感染、慢性炎症等病理条件下,MDSCs通过“扩增-激活”两步模型大量累积,通过精氨酸酶1(ARG1)、诱导型一氧化氮合酶(iNOS)、活性氧(ROS)等途径抑制T细胞、NK细胞功能,促进调节性T细胞(Treg)扩增,是肿瘤免疫逃逸的核心驱动因素之一。
血液系统恶性肿瘤(如淋巴瘤、白血病、多发性骨髓瘤)的发生发展高度依赖免疫抑制性肿瘤微环境(TME),MDSCs作为TME中最关键的免疫抑制细胞,其表型异质性、功能机制及靶向策略是当前研究热点。然而,MDSCs的亚群分类不统一、不同肿瘤中作用机制差异大、缺乏特异性靶向标志物等问题,限制了其临床转化。在此背景下,本文系统总结了MDSCs在血液肿瘤中的生物学功能、表型特征、免疫抑制机制及治疗策略,为解决上述问题提供了全景式参考。
2. 文献综述解析
核心评述逻辑
作者以“MDSCs的基础生物学-疾病特异性作用-治疗应用”为核心逻辑,将现有研究分为三大板块:(1)MDSCs的表型分类与免疫抑制机制;(2)MDSCs在淋巴瘤、白血病、多发性骨髓瘤等血液肿瘤中的具体作用;(3)针对MDSCs的靶向治疗策略及临床进展。
现有研究关键结论
- MDSCs的表型与功能:MDSCs主要分为多形核MDSCs(PMN-MDSCs)、单核MDSCs(M-MDSCs)及早期MDSCs(e-MDSCs)等亚群。小鼠中以GR-1⁺CD11b⁺为通用表型;人类中PMN-MDSCs表型为CD11b⁺CD14⁻CD15⁺HLA-DRlowCD66b⁺,M-MDSCs为CD11b⁺CD14⁺HLA-DRlow/-。MDSCs通过消耗精氨酸(ARG1)、产生一氧化氮(iNOS)、ROS等途径抑制T细胞激活,还可通过PD-L1、TIGIT等免疫检查点增强抑制效果。
- MDSCs在血液肿瘤中的作用:(1)淋巴瘤:弥漫大B细胞淋巴瘤(DLBCL)患者外周血M-MDSCs比例与总生存期(OS)负相关(样本量n=58,HR=2.1,P=0.008);(2)白血病:急性髓系白血病(AML)患者MDSCs通过VISTA通路抑制PD-1⁺CD8⁺T细胞;(3)多发性骨髓瘤:MDSCs通过AMPK通路促进肿瘤细胞存活,诱导piRNA-823增强肿瘤干细胞特性;(4)骨髓增生异常综合征(MDS):高风险患者MDSCs的IL-10/IL-12、TGF-β/TNF-α比值显著升高,免疫抑制更强。
- 治疗策略:(1)耗竭MDSCs:化疗药物(如5-氟尿嘧啶)、CD33单抗(如BI 836858)通过抗体依赖性细胞毒性(ADCC)减少MDSCs;(2)诱导分化:全反式维甲酸(ATRA)可诱导MDSCs分化为成熟髓细胞;(3)阻断招募:PI3K抑制剂(如idelalisib)抑制MDSCs向TME迁移;(4)抑制功能:PDE5抑制剂(如他达拉非)降低ARG1、iNOS表达,恢复T细胞活性。
现有研究局限性与本文创新点
现有研究的局限性:(1)MDSCs的异质性导致表型定义不统一(如部分研究将PMN-MDSCs与中性粒细胞混淆);(2)不同肿瘤中机制差异大(如淋巴瘤依赖M-MDSCs,白血病依赖PMN-MDSCs);(3)单一靶向治疗疗效有限,联合免疫检查点抑制剂(ICIs)的临床数据不足。
本文创新价值:(1)首次系统总结了血液肿瘤中MDSCs的异质性,明确了不同肿瘤类型的优势亚群;(2)整合了MDSCs靶向治疗的最新进展,尤其是联合ICIs、CAR-T等免疫治疗的策略,为临床转化提供了新方向;(3)强调了MDSCs在造血干细胞移植(HSCT)中的双重作用——预防移植物抗宿主病(GVHD)同时保留移植物抗白血病(GVL)效应,拓展了其临床应用场景。
3. 研究思路总结与详细解析
整体框架
本文作为综述性研究,以“基础理论-疾病特异性作用-治疗应用”为整体框架:
1. 基础理论:阐述MDSCs的起源、亚群分类及“扩增-激活”两步模型;
2. 疾病作用:分述MDSCs在淋巴瘤、白血病、多发性骨髓瘤等肿瘤中的具体机制;
3. 治疗应用:总结四类靶向策略的作用机制与临床数据。
分步骤解析
3.1 MDSCs的表型与生物学功能解析
综述目的:明确MDSCs的起源、亚群及免疫抑制机制。
方法细节:综合1970年代至今的经典研究及最新文献,总结MDSCs的来源(造血干细胞分化受阻)、亚群分类(PMN-MDSCs、M-MDSCs等)、表型标志物(小鼠与人类的差异),以及“两步模型”的调控因子——生长因子(如G-CSF、GM-CSF)介导扩增,促炎细胞因子(如IL-6、IFN-γ)介导激活。
结果解读:MDSCs在病理状态下通过STAT3、NF-κB等信号通路扩增,获得免疫抑制功能;不同亚群的功能存在差异——PMN-MDSCs主要通过ROS抑制T细胞,M-MDSCs通过ARG1和iNOS发挥作用。
图片关联:
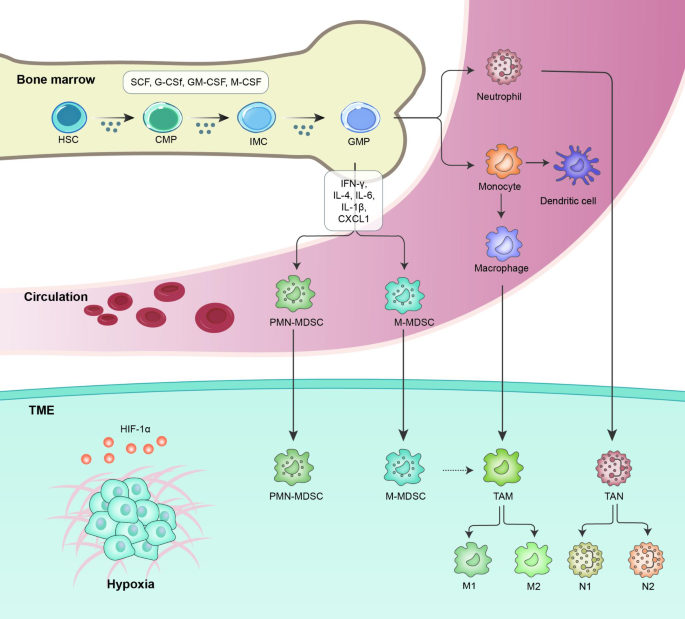
(展示MDSCs的分化与积累过程)
产品关联:文献未提及具体实验产品,领域常规使用流式细胞仪(如BD FACSCanto)检测表型,ELISA试剂盒(如R&D Systems)检测ARG1、iNOS等细胞因子。
3.2 不同血液肿瘤中MDSCs的作用机制解析
综述目的:探讨MDSCs在不同血液肿瘤中的特异性作用。
方法细节:按肿瘤类型分类,整合临床样本分析、动物模型研究及机制实验结果。例如:(1)DLBCL:通过流式细胞术检测58例患者外周血M-MDSCs比例;(2)AML:通过细胞系实验验证VISTA通路的作用;(3)多发性骨髓瘤:通过小鼠模型研究piRNA-823的功能。
结果解读:
- 淋巴瘤:DLBCL患者M-MDSCs比例显著高于健康对照(P<0.05),且与IPI评分正相关,机制为通过IL-10抑制T细胞;
- 白血病:AML患者MDSCs通过VISTA抑制PD-1⁺CD8⁺T细胞,CML患者MDSCs通过Akt/mTOR通路扩增;
- 多发性骨髓瘤:MDSCs通过AMPK通路促进肿瘤细胞存活,诱导piRNA-823增强肿瘤干细胞自我更新;
- MDS:高风险患者MDSCs的TGF-β/TNF-α比值显著升高(P<0.01),与原始细胞比例正相关。
图片关联:
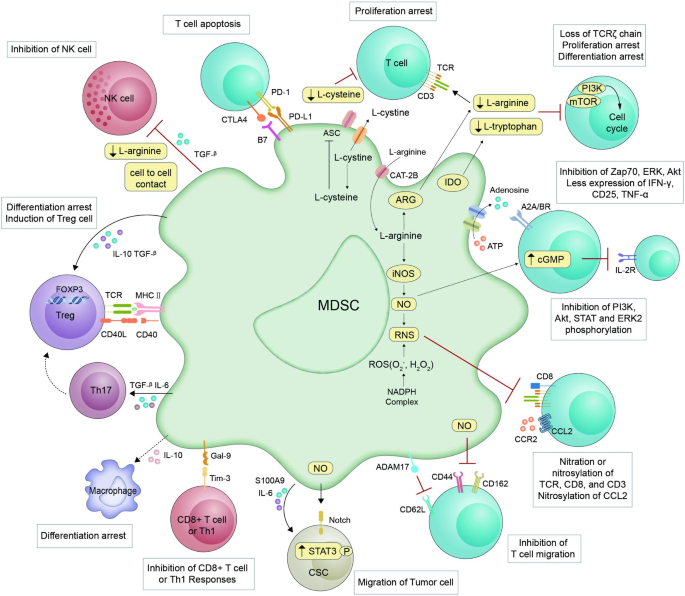
(展示MDSCs的免疫抑制机制)
产品关联:文献中提到的关键产品包括CD33单抗BI 836858、ATRA;未明确的产品如PI3K抑制剂idelalisib,领域常规使用。
3.3 针对MDSCs的治疗策略解析
综述目的:总结MDSCs靶向治疗的研究进展及临床潜力。
方法细节:将治疗策略分为四类,分别综述其机制与临床数据:
1. 耗竭MDSCs:CD33单抗BI 836858通过ADCC效应减少MDSCs,在MDS患者中降低ROS水平(文献未明确具体数据);
2. 诱导分化:ATRA可诱导MDSCs分化为成熟髓细胞,恢复T细胞功能;
3. 阻断招募:PI3K抑制剂idelalisib抑制MDSCs向TME迁移;
4. 抑制功能:PDE5抑制剂他达拉非降低ARG1、iNOS表达,恢复T细胞活性。
结果解读:
- 化疗药物(如5-氟尿嘧啶)可选择性耗竭MDSCs,在淋巴瘤小鼠模型中增强DC疫苗的疗效;
- IL-13诱导的MDSCs通过ARG1和PD-L1增强抑制效果,可预防HSCT后的GVHD(文献未明确具体数据)。
图片关联:
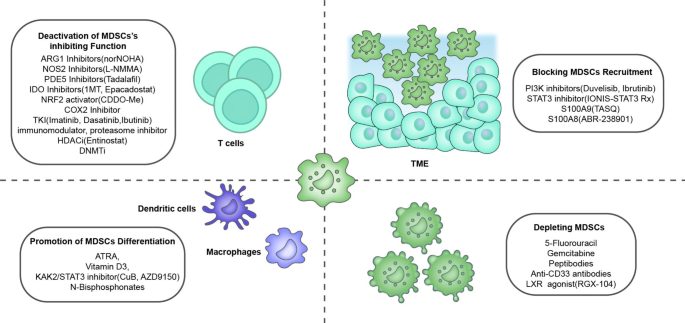
(展示MDSCs的治疗策略)
产品关联:文献中提到的关键产品包括BI 836858(CD33单抗)、ATRA、他达拉非;未明确的产品如idelalisib,领域常规使用。
4. Biomarker研究及发现成果解析
核心信息段
本文重点讨论了MDSCs相关的Biomarker,包括表型标志物、功能标志物及预后标志物,这些Biomarker为血液肿瘤的诊断、预后评估及靶向治疗提供了依据。
Biomarker定位与筛选逻辑
作者通过“临床样本关联-机制验证-临床验证”的逻辑筛选Biomarker:
1. 表型标志物:M-MDSCs(CD14⁺HLA-DRlow/-)通过DLBCL患者样本分析发现与OS负相关,机制研究证实其通过IL-10抑制T细胞;
2. 功能标志物:ARG1、iNOS通过ELISA检测DLBCL患者血清,发现与M-MDSCs比例正相关;
3. 治疗靶点标志物:CD33通过AML细胞系研究发现高表达,临床实验证实CD33单抗的疗效。
研究过程详述
- 表型Biomarker:
- M-MDSCs(CD14⁺HLA-DRlow/-):通过流式细胞术检测58例DLBCL患者外周血,新诊断患者比例显著高于健康对照(P<0.05),且与IPI评分正相关(HR=2.1,P=0.008);
- PMN-MDSCs(CD11b⁺CD15⁺CD33int):通过流式细胞术检测123例MDS患者,高风险患者水平显著高于低风险患者(P<0.01),与原始细胞比例正相关。
- 功能Biomarker:
- ARG1、iNOS:通过ELISA检测DLBCL患者血清(n=32),结果显示M-MDSCs比例与ARG1、iNOS浓度正相关(P<0.05);
- PD-L1:通过免疫组化(IHC)检测AML患者骨髓样本(n=49),发现MDSCs的PD-L1表达与CD8⁺T细胞浸润负相关(P<0.01)。
- 治疗靶点Biomarker:
- CD33:通过AML细胞系研究发现其高表达,临床实验证实CD33单抗BI 836858可减少MDSCs(文献未明确具体数据)。
核心成果提炼
- 预后Biomarker:M-MDSCs(CD14⁺HLA-DRlow/-)作为DLBCL的预后标志物,与OS负相关(HR=2.1,P=0.008);
- 疾病进展Biomarker:PMN-MDSCs(CD11b⁺CD15⁺CD33int)作为MDS的疾病进展标志物,高风险患者水平显著升高(P<0.01);
- 治疗靶点Biomarker:CD33作为MDSCs的治疗靶点,AML细胞系高表达,CD33单抗BI 836858可通过ADCC效应减少MDSCs;
- 功能Biomarker:ARG1、iNOS作为MDSCs的免疫抑制功能标志物,与DLBCL患者M-MDSCs比例正相关(P<0.05)。
总结:本文系统总结了MDSCs在血液肿瘤中的研究进展,明确了其作为免疫抑制关键细胞的作用,为血液肿瘤的免疫治疗提供了新的靶点与策略。未来研究需进一步解决MDSCs的异质性问题,开发更特异的Biomarker,并开展更多联合治疗的临床实验,推动MDSCs靶向治疗的临床转化。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。