Development and validation of a novel bioassay to determine glucocorticoid sensitivity
开发和验证一种测定糖皮质激素敏感性的新型生物测定方法
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2016 | 起止号: | 2016;4:26 |
| doi: | 10.1186/s40364-016-0079-y | 研究方向: | 免疫/内分泌 |
文献解析
1. 领域背景与文献引入
文献英文标题:Development and validation of a novel bioassay to determine glucocorticoid sensitivity;发表期刊:Biomarker Research;影响因子:未公开;研究领域:炎症性疾病生物标志物、糖皮质激素敏感性检测。
半个多世纪以来,糖皮质激素一直是哮喘、类风湿关节炎、炎症性肠病等几乎所有非感染性炎症疾病的一线初始治疗药物,其通过结合细胞质糖皮质激素受体,调控靶基因转录,抑制核因子κB等促炎转录因子活性,发挥强效抗炎作用。然而,患者对糖皮质激素的应答存在显著异质性,约30%的患者为无应答者,这类患者不仅面临疾病未控制的进展风险,还因长期大剂量用药承受严重的不良反应,如骨质疏松、糖尿病、心血管疾病风险升高等。目前临床缺乏可在治疗前预测糖皮质激素应答的生物标志物,现有金标准检测方法——地塞米松抑制淋巴细胞增殖实验(DILPA)虽能有效预测临床应答,但依赖放射性同位素标记和专业设备,健康安全标准严格,难以在常规临床实验室推广应用。因此,开发一种非放射性、操作简便、可临床转化的糖皮质激素敏感性检测方法,实现患者分层治疗,具有迫切的临床需求。本研究针对这一核心问题,开发并验证了新型非放射性生物分析方法BLISS,为糖皮质激素敏感性的临床检测提供了可行方案。
2. 文献综述解析
作者围绕糖皮质激素敏感性检测的技术路线与临床转化潜力展开综述,按现有检测方法的技术特性和应用场景分类,系统梳理了金标准方法、替代技术的优缺点,明确了当前领域的核心痛点与研究空白。
作者首先阐述了金标准DILPA的临床价值,该方法通过检测地塞米松对植物血凝素诱导的淋巴细胞增殖的抑制作用,可在多种炎症性疾病中预测糖皮质激素临床应答,其结果与患者临床敏感性直接相关,且健康人群中的检测结果稳定,不受内源性皮质醇水平影响。但DILPA的局限性也十分突出,需使用氚化胸腺嘧啶核苷等放射性同位素,配套设备昂贵,仅少数研究机构可开展,临床转化难度大。随后作者介绍了基于溴脱氧尿苷(BrdU)的细胞增殖检测替代技术,包括化学发光法和流式细胞术,其中化学发光法需专用发光检测仪,流式细胞术可实现单细胞水平分析,但依赖专业设备与人员,通量较低,难以满足临床常规检测需求。通过对比现有技术的不足,作者凸显了本研究的创新价值:首次建立了基于BrdU比色法的标准化糖皮质激素敏感性检测方法(BLISS),无需放射性设备,仅需常规细胞培养与ELISA读板仪,操作流程简便,可在具备细胞培养条件的任意实验室推广应用,填补了非放射性、临床可及的糖皮质激素敏感性检测技术的空白。
3. 研究思路总结与详细解析
本研究以开发可临床转化的糖皮质激素敏感性检测方法为核心目标,以替代金标准DILPA为科学问题,构建了“方法优化→头对头对比→统计验证→临床潜力评估”的完整研究闭环,通过在101名健康受试者中开展实验,验证了BLISS方法的准确性与可行性。
3.1 研究对象与样本制备
实验目的是获取高活性的外周血单个核细胞(PBMC),为后续两种检测方法提供合格的实验材料。方法细节:研究经NHS健康研究管理局伦理批准,招募101名健康受试者,签署书面知情同意书后采集20mL EDTA抗凝外周血,采用Ficoll密度梯度离心法结合Leucosep离心管分离PBMC,台盼蓝染色排除死细胞,通过血细胞计数板手动计数细胞密度。结果解读:最终所有样本均成功分离出合格PBMC,其中BLISS实验仅1例因植物血凝素刺激孔增殖过低出现技术失败,DILPA实验无技术失败样本,确保了后续对比实验的样本量与数据可靠性。产品关联:实验所用关键产品:Ficoll-Paque Plus(VWR International)、Leucosep离心管(Greiner Bio-One International)。
3.2 金标准DILPA实验流程
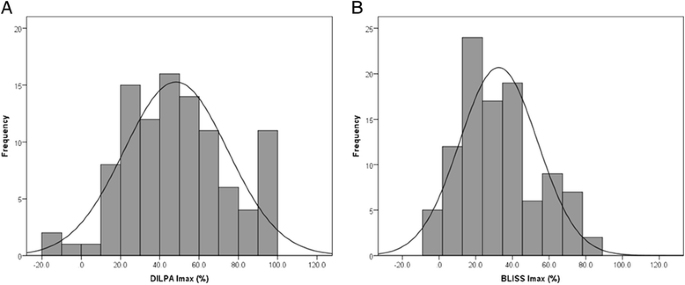
实验目的是提供糖皮质激素敏感性的参考标准数据,作为BLISS方法的验证基准。方法细节:将PBMC以2×10^6/mL的密度接种于96孔板,每孔加入20μg/mL植物血凝素,同时设置含1×10^-6 M地塞米松(糖皮质激素)与不含地塞米松的对照孔,在37℃、5%CO₂条件下培养42h后,加入185kBq/mL氚化胸腺嘧啶核苷,继续培养6h;随后使用细胞收集器将细胞转移至玻璃纤维滤纸,通过β闪烁计数器检测放射性强度,计算最大增殖抑制率(Imax),公式为Imax=(1-糖皮质激素存在下的增殖/无糖皮质激素的增殖)×100%。结果解读:101例健康受试者的DILPA Imax值呈正态分布,均值为48.2%(标准差26.3%,n=101),符合健康人群中糖皮质激素敏感性的已知分布特征,为BLISS的验证提供了可靠的基准数据。产品关联:实验所用关键产品:RPMI培养基(Thermo Fisher Scientific)、胎牛血清(Thermo Fisher Scientific)、植物血凝素(Sigma-Aldrich)、地塞米松(Sigma-Aldrich)、β闪烁计数器(Wallac)。
3.3 BLISS实验方法优化与标准化
实验目的是建立稳定、可重复的非放射性糖皮质激素敏感性检测流程,确保实验结果的一致性与可靠性。方法细节:作者对细胞接种密度、培养时间、BrdU孵育浓度与时间等参数进行优化,最终确定标准化流程:PBMC接种与培养条件与DILPA完全一致,培养42h后加入10μM BrdU孵育6h,随后将细胞转移至平底96孔板,离心后弃上清,干燥固定细胞,加入抗BrdU-过氧化物酶抗体孵育90min,洗涤后加入底物显色,通过ELISA读板仪检测370nm吸光度(参考波长492nm),并按相同公式计算Imax。结果解读:BLISS的Imax值同样呈正态分布,均值为32.5%(标准差21.2%,n=100),与DILPA的分布存在显著差异(n=100,P<0.001),提示需通过统计模型校准以实现与金标准的对比。
3.4 统计分析与方法学验证
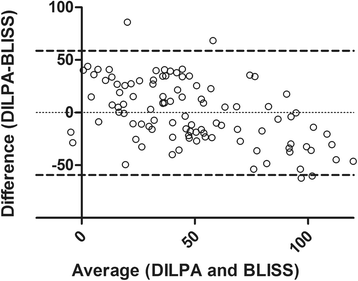
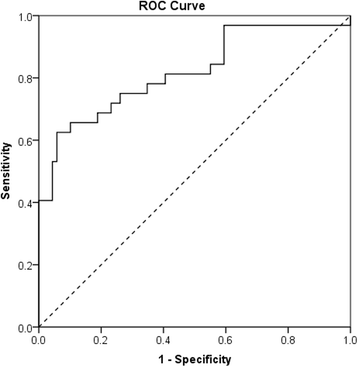
实验目的是验证BLISS与DILPA的一致性,评估BLISS检测糖皮质激素抵抗的准确性。方法细节:首先采用逆回归模型对BLISS的Imax数据进行校准,模型为BLISS Imax=6.8+(0.53×DILPA Imax);随后进行Bland-Altman一致性分析,评估两种方法的结果差异;绘制受试者工作特征(ROC)曲线,计算曲线下面积(AUROC)、敏感性与特异性,其中DILPA的糖皮质激素抵抗阈值为Imax<60%,通过逆回归模型转换为BLISS的阈值38.7%。结果解读:校准后Bland-Altman分析显示,两种方法的偏差为-0.2%,95%一致性界限为-59.2%至58.7%,提示整体一致性良好;ROC曲线的AUROC为0.82(95%置信区间0.73-0.92,n=100,P<0.001),以38.7%为阈值,BLISS识别糖皮质激素抵抗者的敏感性为83%(95%置信区间71-90%),特异性为69%(95%置信区间50-83%),表明BLISS可准确识别金标准定义的糖皮质激素抵抗个体。
产品关联:文献未提及具体统计分析软件,领域常规使用SPSS、R等专业统计软件。
4. Biomarker研究及发现成果解析
本研究将淋巴细胞糖皮质激素敏感性(以Imax值量化)作为预测糖皮质激素临床应答的生物标志物,通过BLISS方法实现了非放射性检测,验证了该生物标志物检测方法的准确性与临床转化潜力。
Biomarker定位:本研究涉及的生物标志物为淋巴细胞糖皮质激素敏感性(以Imax值表示),属于功能型生物标志物,其筛选与验证逻辑为:基于金标准DILPA已证实的淋巴细胞敏感性与临床糖皮质激素应答的相关性,开发BLISS方法替代DILPA,通过健康人群的头对头对比验证检测准确性,为后续临床患者队列验证奠定基础。
研究过程详述:该生物标志物的来源为健康受试者的外周血淋巴细胞,验证方法为与金标准DILPA对比,通过统计分析评估检测性能。具体数据显示,校准后的BLISS方法与DILPA的AUROC为0.82(95%置信区间0.73-0.92,n=100,P<0.001),以38.7%为Imax阈值,BLISS识别糖皮质激素抵抗者的敏感性为83%(95%置信区间71-90%),特异性为69%(95%置信区间50-83%);初步在10例急性重症酒精性肝炎患者中验证显示,BLISS的Imax值与临床应答评估的Lille评分呈显著负相关(相关系数-0.74,n=10,P=0.02),提示其具有临床应用潜力。
核心成果提炼:该生物标志物检测方法的核心功能关联在于可在治疗前预测患者的糖皮质激素应答情况,避免无应答者暴露于不必要的激素治疗与不良反应;创新性在于首次建立了非放射性、操作简便的标准化检测流程,解决了金标准方法难以临床转化的痛点;目前已在健康人群中完成方法学验证,后续需在炎症性疾病患者队列中开展前瞻性验证,以明确其作为预后或疗效预测生物标志物的临床价值,暂无风险比(HR)等预后数据。推测:若在患者队列中验证成功,BLISS可作为临床常规生物标志物,用于炎症性疾病患者的糖皮质激素治疗分层,优化个体化治疗方案。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。