1. 领域背景与文献引入
文献英文标题:Gut microbial metabolite butyrate boosts p53-expressing telomerase-specific oncolytic adenovirus efficacy by enhancing infectivity and activating MHC-I/cGAS-STING;发表期刊:Cancer Immunology, Immunotherapy;影响因子:未公开;研究领域:肿瘤免疫治疗(结直肠癌方向)。
领域共识:结直肠癌是全球发病率排名第三、癌症相关死亡率排名第二的恶性肿瘤,其发生发展与肠道菌群紊乱密切相关。肠道菌群通过代谢产物调控肠道免疫微环境,其中短链脂肪酸丁酸作为组蛋白去乙酰化酶抑制剂,已被证实具有抗炎、诱导肿瘤细胞凋亡、调节免疫应答等功能,是肿瘤免疫治疗领域的研究热点之一。溶瘤病毒治疗作为新型肿瘤免疫治疗策略,可选择性杀伤肿瘤细胞并诱导免疫原性细胞死亡,目前已有多款溶瘤病毒获批进入临床应用,其中端粒酶特异性溶瘤腺病毒因肿瘤靶向性良好得到广泛关注,该团队研发的二代溶瘤腺病毒OBP-702携带p53抑癌基因,在多种实体瘤中显示出较强的抗肿瘤活性,但如何进一步提高其在结直肠癌中的治疗响应率仍是领域未解决的核心问题。现有研究尚未明确肠道微生物代谢物与溶瘤腺病毒的协同作用机制,本研究针对这一研究空白,探索丁酸与OBP-702联合治疗结直肠癌的效果及分子机制,为结直肠癌的免疫联合治疗提供新的策略与理论依据。
2. 文献综述解析
本研究文献综述部分按“肠道菌群代谢物的免疫调控功能”“溶瘤病毒治疗的研究进展”两个核心维度展开,系统梳理了领域内现有研究的关键结论与局限性。
现有研究证实,肠道菌群代谢产物丁酸可通过抑制组蛋白去乙酰化酶活性,上调肿瘤细胞表面主要组织相容性复合体I类(MHC-I)分子表达,进而促进CD8+T细胞的抗原识别与杀伤效应,该调控过程依赖cGAS-STING通路的激活,提示丁酸与免疫治疗药物联合具有潜在的协同增效作用,但目前丁酸与溶瘤病毒的联合应用研究较为缺乏。在溶瘤病毒研究领域,第一代端粒酶特异性溶瘤腺病毒OBP-301已进入食管癌治疗的二期临床试验,二代产品OBP-702通过插入p53基因进一步增强了抗肿瘤活性,可诱导免疫原性细胞死亡、促进树突状细胞活化、招募CD8+T细胞浸润,在“冷肿瘤”胰腺癌中也显示出免疫激活效果,但现有研究未关注肠道微环境成分对溶瘤病毒感染效率及免疫激活效应的调控作用。现有研究的局限性主要体现为两方面:一是丁酸对溶瘤腺病毒感染肿瘤细胞的直接调控作用尚未被阐明,二是两者联合的免疫协同机制缺乏系统的体内外验证。本研究的创新价值在于首次揭示了丁酸通过双重机制增强OBP-702的抗结直肠癌效应,既在直接层面上调病毒受体表达增强感染性,又在间接层面激活免疫通路促进抗肿瘤免疫应答,填补了肠道代谢物与溶瘤病毒联合治疗的机制空白,为临床转化提供了实验依据。
3. 研究思路总结与详细解析
本研究的核心目标是验证丁酸与OBP-702联合治疗结直肠癌的协同效应,并阐明其潜在的作用机制,核心科学问题包括丁酸如何直接增强溶瘤腺病毒对肿瘤细胞的杀伤效率,以及丁酸如何通过调控免疫微环境间接增强抗肿瘤免疫应答,整体技术路线遵循“体外细胞功能验证→分子机制探索→体内临床前模型验证”的闭环逻辑,先在免疫缺陷模型中验证直接协同效应,再在免疫健全模型中验证免疫协同效应,实验设计严谨,逻辑链条完整。
3.1 丁酸与OBP-702的直接协同杀伤效应验证
实验目的为明确丁酸和OBP-702联合对结直肠癌细胞的直接杀伤作用,评估两者的协同效应。方法细节方面,研究采用多种人源(SW48、HCT116、RKO)和鼠源(CT26、MC38)结直肠癌细胞系,先以不同浓度丁酸(0、1、2、3 mM)预处理细胞2小时,再加入不同感染复数的OBP-702处理72小时,采用XTT法检测细胞活力,通过CalcuSyn软件计算联合指数(CI)判定协同效应;采用免疫印迹法检测自噬相关蛋白p62、凋亡相关蛋白剪切型PARP的表达水平,明确联合杀伤的细胞死亡方式;体内实验采用免疫缺陷BALB/c裸鼠构建CT26和HCT116皮下移植瘤模型,丁酸以1 mM浓度加入饮用水中持续口服,OBP-702以5×10^8 PFU的剂量瘤内注射,每周3次,定期监测肿瘤体积并统计完全缓解率。
结果解读显示,细胞活力检测证实联合治疗在所有测试的结直肠癌细胞系中均呈现协同杀伤效应(CI<1),免疫印迹结果显示联合处理组的HCT116和RKO细胞中p62表达下调、剪切型PARP表达上调,提示联合处理可增强肿瘤细胞的自噬和凋亡水平。体内免疫缺陷小鼠模型中,联合治疗组的CT26和HCT116肿瘤生长抑制效果显著优于丁酸单药组和OBP-702单药组,其中HCT116模型中联合治疗组的完全缓解率达60%(n=5),显著高于OBP-702单药组的20%(n=5)和丁酸单药组的0%(n=5),差异具有统计学意义(P<0.05)。该部分实验结果对应原文图1,具体如下:
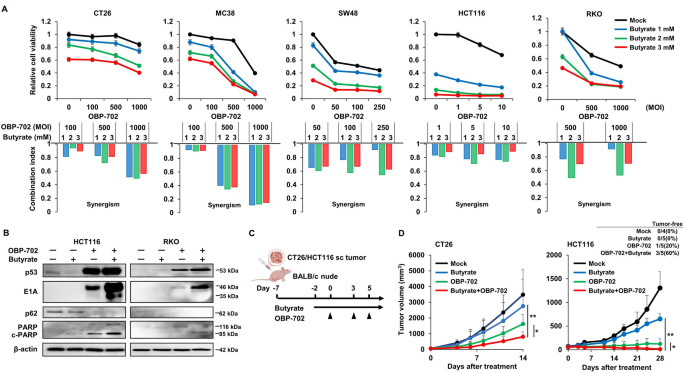
实验所用关键产品:Sigma-Aldrich的丁酸(货号B103500)、Roche的细胞增殖试剂盒II(XTT)、Cell Signaling Technology的p53抗体(货号18032)、p62抗体(货号5114)、PARP抗体(货号9542),BD Pharmingen的E1A抗体(货号554155),Santa Cruz Biotechnology的柯萨奇病毒和腺病毒受体(CAR)抗体(货号18979),Sigma-Aldrich的β-肌动蛋白抗体(货号A-5441)。
3.2 丁酸增强OBP-702感染性的机制探索
实验目的为阐明丁酸增强溶瘤腺病毒抗肿瘤效果的直接分子机制,明确其作用靶点。方法细节方面,研究采用表达绿色荧光蛋白(GFP)的复制缺陷型腺病毒Ad-GFP作为指示病毒,联合丁酸处理结直肠癌细胞后,通过荧光显微镜检测GFP荧光强度,评估病毒感染效率;体内实验采用HCT116皮下移植瘤模型,口服丁酸预处理2天后瘤内注射Ad-GFP,2天后获取肿瘤组织制备冰冻切片,通过荧光显微镜检测GFP表达水平;采用流式细胞术检测丁酸处理后细胞表面CAR、整合素αvβ3、αvβ5的表达水平,筛选丁酸调控的病毒感染相关受体;采用抗CAR抗体预处理细胞,阻断CAR与病毒的结合,验证CAR在丁酸增强感染性中的关键作用;通过免疫印迹法检测病毒E1A蛋白和p53蛋白的表达时程,区分丁酸对病毒感染初始阶段和复制阶段的调控效应。
结果解读显示,体外实验中丁酸处理可显著提升多种结直肠癌细胞中Ad-GFP的感染效率,GFP荧光强度较对照组显著升高(P<0.05,n=3-4);体内实验中口服丁酸组的肿瘤组织GFP荧光强度较对照组升高约1.5倍(P<0.05,n=6);流式细胞术检测结果显示,丁酸处理可显著上调细胞表面CAR、αvβ3、αvβ5的平均荧光强度(P<0.05,n=3);抗CAR抗体预处理可完全阻断丁酸对Ad-GFP感染的增强作用,证实CAR是丁酸增强病毒感染的关键靶点;免疫印迹结果显示,丁酸处理组的病毒E1A蛋白表达在感染后2小时即显著升高,早于病毒复制的起始时间,且后续检测显示病毒复制效率无显著变化,提示丁酸通过增强病毒的初始感染性而非促进病毒复制提升疗效。该部分实验结果对应原文图2,具体如下:
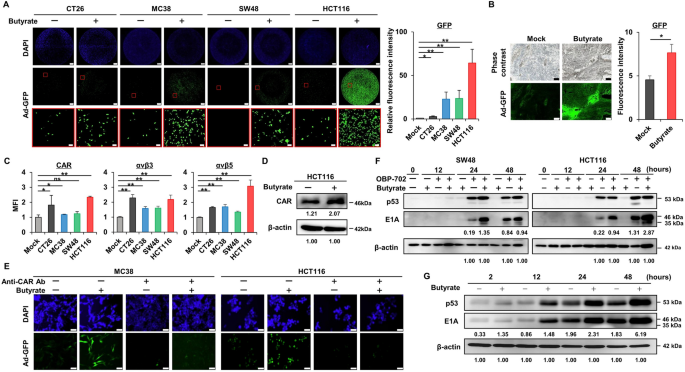
实验所用关键产品:Cell Signaling Technology的CAR抗体(货号D3W3G),Bioss antibodies的αvβ3抗体(货号bs-1310R)、αvβ5抗体(货号bs-1356R),BD Biosciences的流式细胞仪FACS Array、BD FACS Aria及FlowJo分析软件。
3.3 丁酸的免疫调节效应验证
实验目的为探索丁酸对全身及肿瘤微环境的免疫调控作用,明确联合治疗的间接免疫协同机制。方法细节方面,研究采用免疫健全BALB/c小鼠构建CT26皮下移植瘤模型,丁酸以1 mM浓度加入饮用水中持续口服,定期监测肿瘤体积和小鼠体重,评估丁酸单药的抗肿瘤活性和安全性;采用气相色谱-质谱联用(GC-MS)技术检测口服丁酸14天后小鼠回盲部粪便、门静脉血和肿瘤组织中的丁酸浓度,明确丁酸的体内分布特征;采用免疫组化(IHC)和流式细胞术检测回盲部、脾脏和肿瘤组织中CD8+T细胞的浸润水平,评估丁酸对免疫细胞的招募效应;通过细胞因子阵列和酶联免疫吸附实验(ELISA)检测丁酸处理后CT26细胞上清中的细胞因子和趋化因子表达变化,筛选丁酸调控的免疫相关分泌因子;采用流式细胞术检测细胞系和小鼠各组织中MHC-I及其关键调控因子NLRC5的表达水平,明确丁酸调控MHC-I的组织特异性。
结果解读显示,免疫健全小鼠中丁酸单药可显著抑制CT26肿瘤生长(P<0.05,n=3),且无明显体重下降、腹泻等不良反应,安全性良好;口服丁酸14天后,小鼠回盲部、门静脉血和肿瘤组织中的丁酸浓度均显著升高,其中肿瘤组织中丁酸浓度可达0.8 mM(n=5),证实口服丁酸可有效富集于肿瘤组织;丁酸处理后,小鼠回盲部、脾脏和肿瘤组织中的CD8+T细胞数量均显著增加(P<0.01,n=3),提示丁酸具有全身免疫激活效应;体外细胞实验显示丁酸可显著上调CT26细胞CXCL10的分泌水平,较对照组升高约3.2倍(P<0.01,n=3),CXCL10是招募CD8+T细胞浸润的关键趋化因子;流式检测结果显示丁酸可选择性上调肿瘤组织中NLRC5和MHC-I的表达水平,其中MHC-I的平均荧光强度较对照组升高2.1倍(P<0.01,n=3),而对回肠、肝脏、皮肤等正常组织的MHC-I表达无显著影响,提示丁酸的免疫激活具有肿瘤选择性,可降低自身免疫风险。该部分实验结果对应原文图3,具体如下:
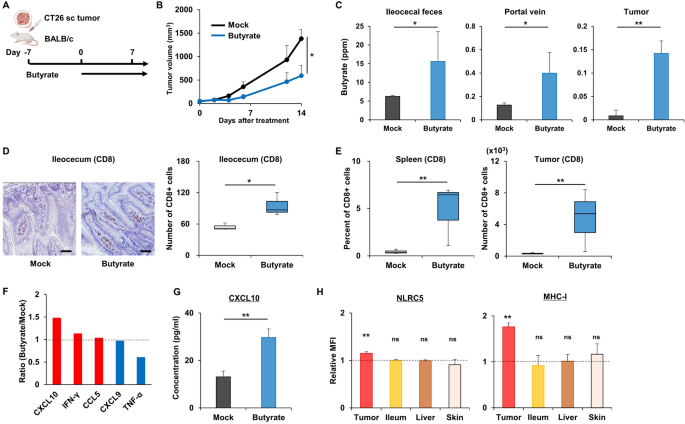
实验所用关键产品:Abcam的CD8a抗体(货号YTS169.4)、CXCL10 ELISA试剂盒(货号ab260067),Bio X Cell的MHC-I抗体(货号BE0077),Affinity Bioscience的NLRC5抗体(货号DF13672),BioLegend的IFN-γ抗体(货号XMG1.2)、颗粒酶B抗体(货号QA18A28),岛津的GCMS-QP2020 NX气相色谱-质谱联用仪。
4. Biomarker研究及发现成果
本研究涉及的生物标志物主要包括病毒感染效率相关标志物、免疫激活相关标志物及治疗响应预测标志物三大类,筛选与验证遵循“分子机制靶点筛选→细胞水平功能验证→体内组织水平验证”的完整逻辑链条,所有标志物均经过多维度实验验证,具有潜在的临床转化价值。
病毒感染效率相关标志物为CAR、整合素αvβ3和αvβ5,三者均为腺病毒感染细胞的关键受体,筛选基于腺病毒感染的已知分子机制,通过流式细胞术在多种结直肠癌细胞系中验证丁酸对其的上调作用,其中CAR的上调效应最为显著,丁酸处理后细胞表面CAR的平均荧光强度较对照组升高约1.8倍(n=3,P<0.05),体内肿瘤组织中也验证了丁酸对CAR的上调作用,功能阻断实验证实CAR是丁酸增强病毒感染的核心靶点,可作为联合治疗前病毒感染敏感性的预测标志物。免疫激活相关标志物包括MHC-I、NLRC5、CXCL10和CD8+T细胞,其中NLRC5是MHC-I表达的关键转录调控因子,丁酸通过激活cGAS-STING通路上调NLRC5的表达,进而选择性上调肿瘤细胞表面MHC-I的表达,肿瘤组织中MHC-I的表达水平较对照组升高2.1倍(n=3,P<0.01),且仅在肿瘤组织中上调,特异性良好;CXCL10是丁酸诱导肿瘤细胞分泌的关键趋化因子,细胞上清中CXCL10浓度较对照组升高3.2倍(n=3,P<0.01),可有效招募CD8+T细胞浸润至肿瘤微环境,丁酸处理后肿瘤组织中CD8+T细胞的比例较对照组升高1.7倍(n=3,P<0.01),上述标志物可用于评估联合治疗的免疫激活程度。治疗响应预测标志物为肿瘤组织中的丁酸浓度,口服1 mM丁酸后肿瘤组织中丁酸浓度可达0.8 mM(n=5),当浓度达到0.5 mM以上时可观察到显著的病毒感染增强效应和免疫激活效应,可作为治疗过程中疗效预测的参考指标。
本研究的核心成果在于首次鉴定出丁酸可作为OBP-702溶瘤病毒治疗的有效增敏剂,其调控的CAR、MHC-I、CXCL10等生物标志物可用于联合治疗的患者筛选和疗效监测,创新性地揭示了肠道微生物代谢物通过直接调控病毒感染和间接调控抗肿瘤免疫的双重协同机制,为结直肠癌的溶瘤病毒联合治疗提供了全新的靶点和策略,所有结果均经过体内外多模型验证,统计学差异显著,具有良好的临床转化潜力。
