
(图片来源:Lu ShaoJi/盖蒂图片社)
终末期肝病患者的肝脏损伤程度已超出该器官本就极强的再生能力修复或代偿的极限,一旦进入这一不可逆阶段,唯一的治疗方案为器官移植,但供体肝脏需求极高、供应极其有限。
目前学界正在开展大量前沿研究,目标是最终实现可植入完整人工肝脏的工程化构建,但当前实验室构建的肝脏结构最大尺寸仍存在限制,尚无法为患者提供治疗获益。来自哈佛大学维斯研究所、波士顿大学与麻省理工学院的研究团队另辟蹊径,攻克这一核心难题。
“我们提出了一种设想:是否可以先植入小型肝脏结构,待其植活后诱导其在体内扩增?”维斯研究所核心成员、波士顿大学William Fairfield Warren杰出生物医学工程教授、生物设计中心主任Christopher Chen医学博士/哲学博士表示,“充分生长的功能性‘附属肝脏’可即刻减轻损伤肝脏的代谢负担,帮助患者桥接至获得供体肝脏的移植窗口期。”
Chen与该研究所副研究员Sangeeta Bhatia医学博士/哲学博士共同主导了这项研究,Bhatia是麻省理工学院科赫综合癌症研究所健康科学与技术、电气工程与计算机科学双聘教授,同时为霍华德·休斯医学研究所研究员。Chen同时也是维斯研究所3D器官工程计划的牵头人,以及近期获得ARPA-H PRINT项目资助的ImPLANT项目负责人,该项目聚焦于维斯研究所及合作机构的全器官肝脏工程化研究。
该项目由Amy Stoddard博士(2025年毕业于麻省理工学院)牵头,她在博士研究阶段及后续博士后工作中开发了这套整合组织工程与合成生物学工具的遗传策略,研究团队将其命名为“通过合成生物学触发的生物工程按需增生”(bioengineered on-demand outgrowth via synthetic biology triggering, BOOST)。通过特异性重编程原代肝细胞与支持性成纤维细胞的基因表达,科学家成功在小型工程化肝脏结构植入小鼠体内后,精准开启其组织生长程序。
研究团队在发表于《科学·进展》(Science Advances)、题为《植入式工程化肝脏组织生长的合成调控》的论文中表示:“我们以工程化肝脏组织为概念验证应用,整合合成生物学与组织工程工具,构建出可在植入体内(in vivo)后按需扩增的肝脏组织。”他们在论文中总结道:“本研究探索了一种非传统细胞疗法规模化策略的初步路径:先构建小型结构,再诱导其原位(in situ)生长……这套被我们命名为BOOST的策略具备多项核心优势,包括无需大量细胞原材料,同时规避了构建可快速灌注、能在植活期存活的结构这一极高难度挑战。”
作者在文中写道:“器官移植目前是终末期器官衰竭患者唯一的治愈性疗法,但由于可供移植的器官稀缺,大量患者无法获得这一治疗机会。”尽管目前工程化组织细胞疗法领域已取得重大进展,有望成为替代治疗方案或移植桥接方案,但研究人员也指出:“将这些结构放大至具有治疗价值的尺寸,仍是临床转化的核心障碍。”
为解决当前构建过程中存在的诸多挑战,Chen及其团队转换研究视角,提出是否可以先植入小型结构,待其在宿主植活后再诱导其原位扩增。
要实现植入的小型肝脏结构在受者体内原位生长,研究人员首先需要确定可实现这一目标的相关调控信号。他们指出:“实现这种原位规模化扩增的关键第一步,是在结构植活后成功调控工程化结构内的细胞生长。”已知肝脏生长受可溶性生长因子(growth factor, GF)调控,因此Stoddard对一系列候选因子进行了筛选,以确定加入培养的人原代肝细胞(hepatocyte, HEP)后,促生长效应最强的因子。
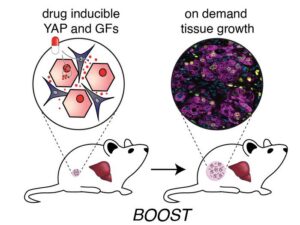
(图片说明:遗传“BOOST”策略整合组织工程与合成生物学工具,实现体内肝脏按需生长。通过特异性重编程原代肝细胞与支持性成纤维细胞的基因表达,小型工程化肝脏结构植入受者体内后,加入诱导剂(图示为药丸)即可开启组织生长程序,结构内的肝细胞将持续增殖,直至达到目标尺寸后停止提供诱导信号。在小鼠模型中,BOOST策略可实现稳定、健康的肝脏生长。[来源:哈佛大学维斯研究所])
Stoddard表示:“我们最终筛选出4种生长因子:肝细胞生长因子(HGF)、转化生长因子α(TGFα)、WNT2与RSPO3,可强效诱导培养皿中稀疏分布的原代肝细胞生长。但当我们测试这些因子是否能在由密集排列的原代肝细胞与成纤维细胞构成的3D肝脏组织中发挥相同效应时,却发现其并无作用。这让我们提出假设:人原代肝细胞中一定存在其他机制,在高密度条件下抑制细胞增殖。”
研究团队聚焦于Yes相关蛋白(YAP),这是一种感知机械信号的蛋白,已知在低密度条件下可从细胞质转移至细胞核,促进细胞增殖相关基因的表达;但在高密度条件下,细胞受到挤压,YAP在细胞质中被降解,从而阻止靶基因激活、限制增殖。
Stoddard指出:“重要的是,当我们在原代肝细胞中过表达不可降解版本的YAP时,该蛋白在高密度条件下也可进入细胞核参与基因调控,我们成功打破了原代肝细胞的密度检查点。有意思的是,我们发现原代肝细胞需要同时接受YAP与生长因子的刺激,才能在致密3D肝脏组织中生长。”
为实现活体生物、最终在人类患者中安全诱导并调控原代肝细胞增殖的目标,研究人员利用合成生物学工具,在工程化3D肝脏组织内的原代肝细胞与成纤维细胞中,局部安装了这些信号通路的调控元件。他们表示:“我们开发了一套合成生物学工具包,可局部调控工程化肝脏组织内的生长因子与YAP信号,甚至在植入后仍可实现增殖的按需调控。”
研究团队改造了成纤维细胞系,使其分别分泌4种生长因子中的一种,同时改造原代肝细胞使其表达不可降解的YAP蛋白,且所有蛋白的表达都可被多西环素(doxycycline, DOX)诱导。时间梯度实验显示,持续7天的多西环素处理,可使工程化细胞构成的3D肝脏组织在培养皿中实现尺寸与细胞数量的稳定扩增;撤除多西环素后,原代肝细胞恢复至非增殖状态。
但Stoddard也指出:“当我们对比BOOST改造、多西环素诱导的3D肝脏组织中的单细胞基因表达,与未改造或BOOST改造但未诱导的3D肝脏组织细胞的基因表达时,我们发现这种扩增存在权衡:高增殖率对应着原代肝细胞的功能状态降低。我们认为这是多种生物学场景中普遍存在的天然权衡,未来有望解决这一问题,因为肝脏本身也存在内源性的功能重塑信号可以利用。”
BOOST改造的3D肝脏组织生长的验证性实验,是观察其植入活体小鼠后,接受同样7天全身性多西环素处理时是否会发生相似扩增。实验显示,植入组织的增殖水平大幅提升500%,仅工程化原代肝细胞的数量就实现翻倍,且组织已完成血管化,可满足扩增组织的代谢需求。小鼠对植入组织的耐受性良好,未观察到免疫细胞浸润、成纤维细胞炎症导致的纤维化,也无肿瘤生长迹象。
Stoddard表示:“这些结果让我们格外振奋,在我们的研究之前,一直需要损伤宿主肝脏才能触发肝细胞植活与增殖,而我们摆脱了这一依赖,在完全健康的宿主体内实现了植入肝脏组织的按需生长。”
未来,研究团队将探索BOOST扩增的肝脏组织在肝损伤场景下挽救宿主功能的能力。Bhatia指出:“我们的BOOST策略为未来实现实体器官细胞疗法的非手术调控奠定了基础,可根据患者与临床医生的需求调整治疗方案。除治疗肝病外,BOOST的理念还可应用于其他受限于组织规模化挑战的工程化组织疗法,例如用于治疗重症疾病的工程化心脏或胰腺组织。”
作者在论文中总结道:“本研究是一项令人振奋的概念验证,证明通过生长实现组织规模化是可行的……该研究为未来的‘智能’组织疗法奠定了基础,这类疗法可根据患者需求调整尺寸,从而为大量此前无法治愈的疾病提供治疗方案。”
专业注释
- BOOST策略:合成生物学介导的植入后组织可控扩增技术
- YAP蛋白:感知机械信号、调控细胞增殖的核心功能蛋白
- 多西环素诱导系统:常用的外源基因可控表达调控工具
