The proneural transcription factor Atoh1 promotes odontogenic differentiation in human dental pulp stem cells (DPSCs).
促神经转录因子 Atoh1 促进人类牙髓干细胞 (DPSC) 的成牙分化
| 期刊: | BMC Molecular and Cell Biology | 影响因子: | 2.700 |
| 时间: | 2025 | 起止号: | 2025 Jan 20; 26(1):5 |
| doi: | 10.1186/s12860-025-00530-2 | 种属: | Human |
| 研究方向: | 神经科学 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Ectopic expression of the proneural transcription factor Atoh1 promotes odontogenic differentiation of human dental pulp stem cells through BMP/Wnt signaling and metabolic remodeling;发表期刊:BMC Oral Health;影响因子:未公开;研究领域:牙髓干细胞成牙分化与牙组织再生
牙组织再生是口腔医学领域的重要研究方向,随着干细胞技术与基因治疗的发展,利用转录因子精准调控牙髓干细胞(DPSC)的成牙分化命运,成为实现牙-牙髓复合体功能性再生的潜在策略。领域发展的关键节点包括2000年左右人DPSC的成功分离鉴定,以及后续骨形态发生蛋白(BMP)、Wnt等核心信号通路在牙发育与修复中调控机制的阐明;当前研究热点聚焦于筛选高效的转录因子或信号分子,解决现有再生策略中存在的分化效率低、再生组织功能不完善等问题;未解决的核心问题包括缺乏特异性调控DPSC成牙分化的关键转录因子,以及对成牙分化过程中的代谢调控机制认识不足。针对这一研究空白,本研究探索了经典前神经转录因子Atoh1在DPSC成牙分化中的调控作用,旨在揭示其跨界调控细胞命运的新机制,为基因介导的牙组织再生提供新的靶点与策略。
2. 文献综述解析
作者以转录因子的功能多样性为核心评述逻辑,首先梳理牙发育与修复中信号通路及转录因子的调控网络,再聚焦Atoh1的已知功能域,结合其与成牙分化核心信号通路的关联,提出研究假设。
现有研究表明,牙发育与修复依赖时空精准调控的基因网络,BMP、Wnt等信号通路通过激活Runx2、Osterix等转录因子,调控干细胞的功能与组织更新,这些研究为牙组织工程提供了理论基础;技术方法上,多采用基因操作结合细胞模型的方式,能有效解析信号通路与转录因子的调控关系,但多数研究聚焦于Atoh1在神经、听觉或肠道组织中的功能,缺乏其在牙髓干细胞及牙组织再生领域的研究,且对成牙分化过程中的代谢调控机制探索较少。本研究通过对比现有研究的空白,首次发现Atoh1在DPSC中异位表达具有成牙分化调控功能,揭示了其通过BMP/Wnt信号通路及代谢重编程介导成牙分化的新机制,填补了Atoh1在牙组织再生领域的研究空白,为基因治疗介导的牙-牙髓复合体再生提供了新的学术依据。
3. 研究思路总结与详细解析
本研究的核心目标是明确Atoh1异位表达对人DPSC成牙分化的调控作用及分子机制,核心科学问题为Atoh1如何通过信号通路及代谢重编程介导DPSC的成牙分化命运决定,技术路线遵循“假设构建→细胞模型建立→表型检测→机制解析→结论验证”的完整闭环。
3.1 牙髓干细胞分离培养与Atoh1异位表达模型构建
该环节的核心目标是获取高活性的人DPSC,并建立Atoh1稳定异位表达的细胞模型。方法上,从无龋第三磨牙中分离牙髓组织,采用5mg/ml胶原酶37℃消化90分钟,获得细胞后接种于含10%胎牛血清的Advanced DMEM培养基培养;通过复制缺陷型腺病毒载体(Adv-Atoh1)感染DPSC,以空载体(Adv-Null)为对照,感染复数为100,感染2小时后更换培养基继续培养。结果显示,实时荧光定量聚合酶链反应(qPCR)检测发现Adv-Atoh1处理组Atoh1表达水平较对照组升高约3000倍(n=6,P<0.001),蛋白质免疫印迹(Western blotting)结果显示处理组可检测到Atoh1蛋白条带,对照组无明显信号,表明成功建立Atoh1异位表达的DPSC模型。实验所用关键产品:Thermo Fisher Scientific的Advanced DMEM培养基、TrypLE消化液;Proteintech的Atoh1抗体(货号21215-1-AP);Qiagen的RNA提取试剂盒;Bio-Rad的iScript cDNA合成试剂盒、SYBR Green qPCR混合液;Pierce Biotechnology的SuperSignal化学发光底物。
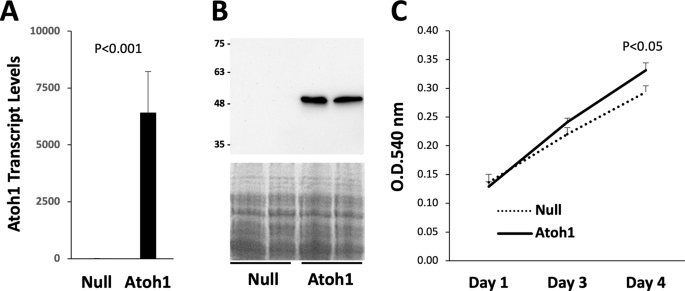
3.2 Atoh1对牙髓干细胞增殖能力的调控
该环节旨在检测Atoh1异位表达对DPSC增殖的影响。方法上,将处理后的DPSC以6000细胞/孔接种于24孔板,采用MTT法在感染后1、3、4天检测细胞增殖:加入0.125mg/ml MTT溶液37℃孵育20分钟,用二甲基亚砜(DMSO)溶解甲瓒结晶后在540nm波长下检测吸光度。结果显示,感染后4天,Adv-Atoh1处理组细胞增殖率显著高于对照组(n=3,P<0.05),表明Atoh1异位表达可显著促进DPSC的增殖活性。
3.3 Atoh1对牙髓干细胞成牙分化表型的诱导
该环节的核心目标是明确Atoh1异位表达对DPSC成牙分化的特异性诱导作用。方法上,将处理后的DPSC接种于成牙分化培养基,培养至7、14天时提取RNA,qPCR检测成牙分化关键转录因子的表达;培养20天后采用茜素红染色检测细胞外基质矿化情况,提取染色结晶后在450nm波长下定量分析。结果显示,处理组Osterix表达水平在第7天升高3倍(n=6,P<0.001),第14天升高8倍(n=6,P<0.005);Runx2和Dlx5表达无显著变化(n=3或6,P>0.05);茜素红染色结果显示处理组细胞外基质矿化程度显著高于对照组(n=3,P<0.05),表明Atoh1可特异性诱导DPSC向成牙细胞方向分化。
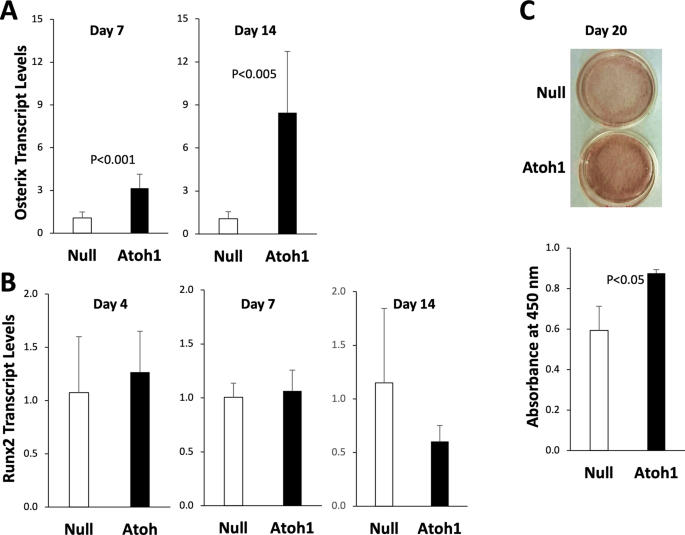
3.4 Atoh1对成牙分化相关基质蛋白表达的调控
该环节旨在解析Atoh1对DPSC成牙分化过程中基质蛋白表达的影响。方法上,在成牙分化培养第7、14天提取RNA,qPCR检测I型胶原、碱性磷酸酶及小整合素结合配体N端糖蛋白(SIBLINGs)家族蛋白的表达。结果显示,处理组I型胶原(Col1A1)表达在第7天显著升高(n=6,P<0.005),第14天持续升高(n=6,P<0.01);碱性磷酸酶(ALP)表达在第4天略有升高,第7天显著降低(n=3或6,P<0.05);SIBLINGs家族中,骨涎蛋白(BSP)升高4倍(n=6,P<0.001),牙本质基质蛋白1(DMP1)升高2倍(n=6,P<0.05),牙本质涎磷蛋白(DSPP)升高4倍(n=6,P<0.005),骨桥蛋白(OPN)升高15倍(n=6,P<0.001),表明Atoh1可显著促进成牙分化相关基质蛋白的表达,为矿化基质形成奠定基础。
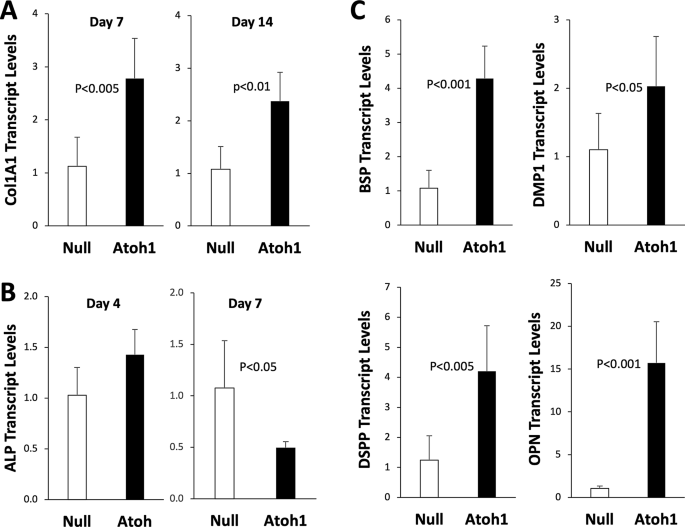
3.5 Atoh1介导成牙分化的信号通路与代谢机制解析
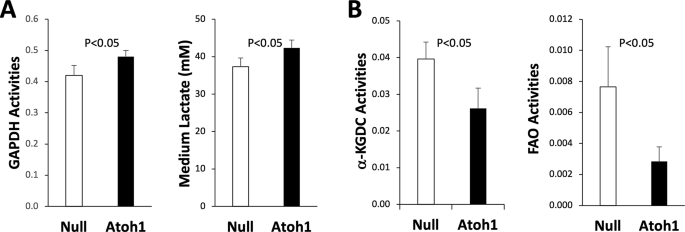
该环节的核心目标是揭示Atoh1调控DPSC成牙分化的分子机制。方法上,在成牙分化培养第7、14天提取RNA,qPCR检测信号分子的表达;培养第10天提取细胞蛋白,检测糖酵解及线粒体代谢相关酶的活性,同时检测培养基中乳酸含量。结果显示,信号通路方面,处理组BMP2在第7天显著升高(n=6,P<0.001),BMP7在第14天显著升高(n=6,P<0.01);Wnt信号通路的负调控因子sFRP2及靶基因Axin2表达显著升高(n=3或6,P<0.005、P<0.01);血管内皮生长因子A(VEGF-A)和缺氧诱导因子1α(HIF1α)表达显著降低(n=3或6,P<0.005、P<0.05)。代谢方面,处理组糖酵解关键酶甘油醛-3-磷酸脱氢酶(GAPDH)活性显著升高(n=3,P<0.05),培养基乳酸含量显著升高(n=3,P<0.05);线粒体代谢相关的α-酮戊二酸脱氢酶复合体(α-KGDC)及脂肪酸氧化(FAO)活性显著降低(n=3,P<0.05),表明Atoh1通过激活BMP/Wnt信号通路,同时调控糖酵解增强、线粒体代谢减弱的代谢重编程,介导DPSC的成牙分化。
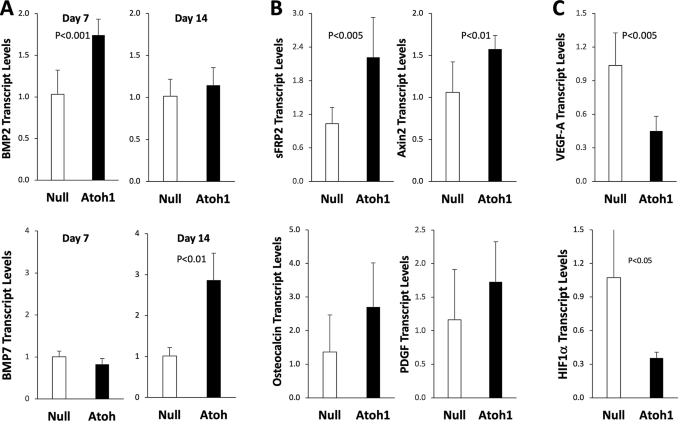
4. Biomarker研究及发现成果解析
本研究中,Atoh1作为功能性调控Biomarker,其异位表达可作为DPSC成牙分化的关键靶点;同时,Osterix、BMP2、BMP7及糖酵解相关指标(GAPDH活性、乳酸含量)可作为Atoh1介导成牙分化的特征性Biomarker。筛选与验证逻辑为:首先通过文献调研提出Atoh1调控成牙分化的假设,然后通过细胞模型验证Atoh1异位表达对成牙分化的诱导作用,再通过信号通路及代谢检测验证下游特征性Biomarker的变化。
Biomarker来源为人DPSC细胞及培养上清;验证方法采用qPCR检测基因表达、蛋白质免疫印迹检测蛋白表达、酶活性检测及代谢物含量检测;特异性与敏感性方面,Atoh1异位表达后,Osterix表达水平升高8倍(n=6,P<0.005),BMP2表达显著升高(n=6,P<0.001),GAPDH活性及乳酸含量均显著升高(n=3,P<0.05),具有显著的统计学差异。核心成果提炼:Atoh1作为前神经转录因子,在DPSC中异位表达具有新的成牙分化调控功能,其通过激活BMP/Wnt信号通路及代谢重编程介导成牙分化;该发现的创新性在于首次揭示了Atoh1跨界调控细胞命运的新机制,为牙组织再生提供了新的基因治疗靶点;统计学结果显示,各检测指标均具有显著差异(P<0.05或P<0.01),样本量为n=3或6,数据可靠性较高。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。