IGFBP7 inhibits cell proliferation by suppressing AKT activity and cell cycle progression in thyroid carcinoma
IGFBP7 通过抑制甲状腺癌细胞中的 AKT 活性和细胞周期进程来抑制细胞增殖
| 期刊: | Cell and Bioscience | 影响因子: | 6.100 |
| 时间: | 2019 | 起止号: | 2019 Jun 6:9:44. |
| doi: | 10.1186/s13578-019-0310-2 | 研究方向: | 免疫、细胞生物学 |
| 疾病类型: | 甲状腺癌 | 细胞类型: | 肿瘤细胞 |
| 信号通路: | PI3K/Akt | ||
文献解析
1. 领域背景与文献引入
文献英文标题:IGFBP7 inhibits cell proliferation by suppressing AKT activity and cell cycle progression in thyroid carcinoma;发表期刊:Cell Bioscience;影响因子:5.51(2019年);研究领域:甲状腺癌分子生物学、肿瘤抑制因子与信号通路研究。
甲状腺癌是全球发病率增长最快的内分泌恶性肿瘤,2018年全球新发病例达56.7万,女性发病率为男性的3倍。根据病理特征可分为乳头状甲状腺癌(PTC)、滤泡状甲状腺癌(FTC)和未分化甲状腺癌(ATC),其中PTC占比超80%,预后相对良好,但约20-30%患者会出现复发;ATC恶性程度极高,5年生存率不足10%,且对常规化疗存在耐药性。目前临床缺乏有效区分甲状腺癌亚型的特异性生物标志物,导致部分患者接受过度治疗,因此亟需探索甲状腺癌发生发展的分子机制,寻找可用于亚型诊断和靶向治疗的新靶点。胰岛素样生长因子(IGF)通路在细胞增殖、分化过程中发挥关键调控作用,其家族成员胰岛素样生长因子结合蛋白7(IGFBP7)已被证实为多种肿瘤的分泌型抑癌因子,在乳腺癌、肺癌等肿瘤组织中低表达与不良预后相关,但IGFBP7在甲状腺癌不同亚型中的表达模式及功能机制尚未明确,本研究针对这一临床与基础研究空白展开系统探究。
2. 文献综述解析
本文综述部分围绕“甲状腺癌临床需求-IGF通路研究现状-IGFBP7泛肿瘤研究-甲状腺癌研究空白”的逻辑展开,先梳理甲状腺癌的流行病学特征、分型差异及未满足的临床需求,再总结IGF通路及IGFBP7在泛肿瘤领域的抑癌作用,最后聚焦甲状腺癌领域的研究缺口,明确本研究的科学必要性。
现有研究中,甲状腺癌的分子机制研究主要集中在BRAF、RAS基因突变或RET/PTC重排激活丝裂原活化蛋白激酶(MAPK)信号通路,约70%患者存在此类突变;同时磷脂酰肌醇3-激酶/蛋白激酶B(PI3K/AKT)通路在低分化甲状腺癌中过度激活,但现有研究多聚焦于胞内分子,缺乏针对分泌型生物标志物的系统分析。在泛肿瘤领域,IGFBP7被证实为分泌型抑癌因子,在乳腺癌、肺癌等多种肿瘤组织中低表达,过表达可抑制肿瘤细胞增殖、锚定非依赖性生长及体内肿瘤生长,但其作用机制在不同肿瘤中存在差异,且未在甲状腺癌不同亚型中进行系统分析。本研究的创新价值在于,首次明确IGFBP7在甲状腺癌不同亚型中的表达差异,揭示其在FTC和ATC中特异性低表达的模式,同时阐明其通过抑制AKT活性、调控细胞周期进程发挥抑癌作用的机制,弥补了甲状腺癌分泌型生物标志物研究的空白,为亚型诊断和靶向治疗提供新方向。
3. 研究思路总结与详细解析
本研究以“IGFBP7在甲状腺癌不同亚型中的表达模式-功能验证-机制解析”为核心逻辑,通过临床样本明确表达差异,利用细胞系和动物模型验证其抑癌功能,最终揭示其通过AKT-细胞周期轴调控增殖的分子机制,形成完整的“临床-基础-机制”研究闭环。
3.1 临床样本中IGFBP7表达模式分析
实验目的是明确IGFBP7在不同甲状腺病变及癌亚型中的表达差异,为后续功能研究提供临床依据。研究收集了中山大学附属第一医院2005-2010年的112例石蜡包埋样本,包括18例甲状腺腺瘤、63例PTC、15例FTC、16例ATC,采用免疫组化(IHC)染色检测IGFBP7表达,由两位对样本病理信息盲法的研究者根据阳性细胞比例和染色强度评分。结果显示,正常甲状腺组织、甲状腺腺瘤及经典PTC中IGFBP7阳性表达率较高,分别为腺瘤66.7%、PTC65.0%,而FTC中仅13.4%、ATC中仅12.5%的样本检测到IGFBP7表达;进一步分析PTC亚型发现,经典PTC(CPTC)中IGFBP7染色强度显著高于滤泡亚型PTC(FVPTC),后者几乎无阳性表达(n=112,P<0.01)。这一结果提示IGFBP7表达与甲状腺癌分化程度相关,在低分化的FTC和ATC中特异性缺失。
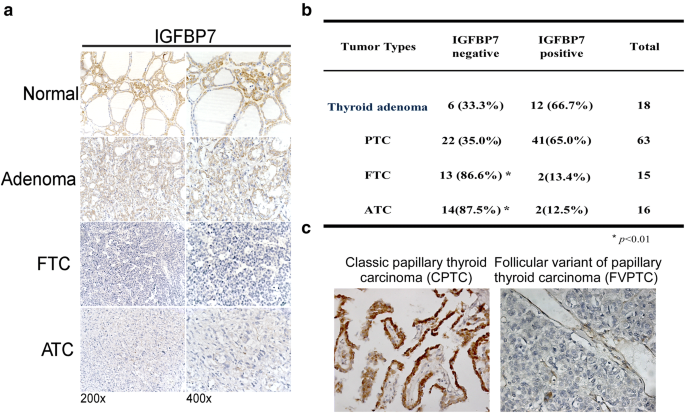
文献未提及具体实验产品,领域常规使用免疫组化试剂盒、抗IGFBP7单克隆抗体、病理图像分析系统等。
3.2 甲状腺癌细胞系中IGFBP7的增殖调控功能验证
实验目的是在细胞水平验证IGFBP7对甲状腺癌细胞增殖的调控作用。研究选择无内源性IGFBP7表达的ATC细胞系ARO、FRO,通过逆转录病毒转导过表达IGFBP7;选择中等表达IGFBP7的FTC细胞系WRO,同时进行过表达和shRNA沉默(两种特异性shRNA)处理,采用蛋白质免疫印迹(Western blot)验证表达效率。随后通过细胞计数、MTT、软琼脂克隆形成、平板克隆形成实验检测增殖能力:过表达IGFBP7的ARO、FRO、WRO细胞在接种3-5天后汇合度仅约20%,而对照组细胞汇合度达80-90%;沉默IGFBP7的WRO细胞数较对照组增加2倍以上(n=3,P<0.01);软琼脂实验中,过表达IGFBP7的细胞形成的克隆数量更少、体积更小,而沉默组克隆数量更多、体积更大;MTT和细胞计数实验结果一致,证实过表达IGFBP7显著抑制甲状腺癌细胞增殖,沉默则促进增殖(n=3,P<0.05或P<0.01)。
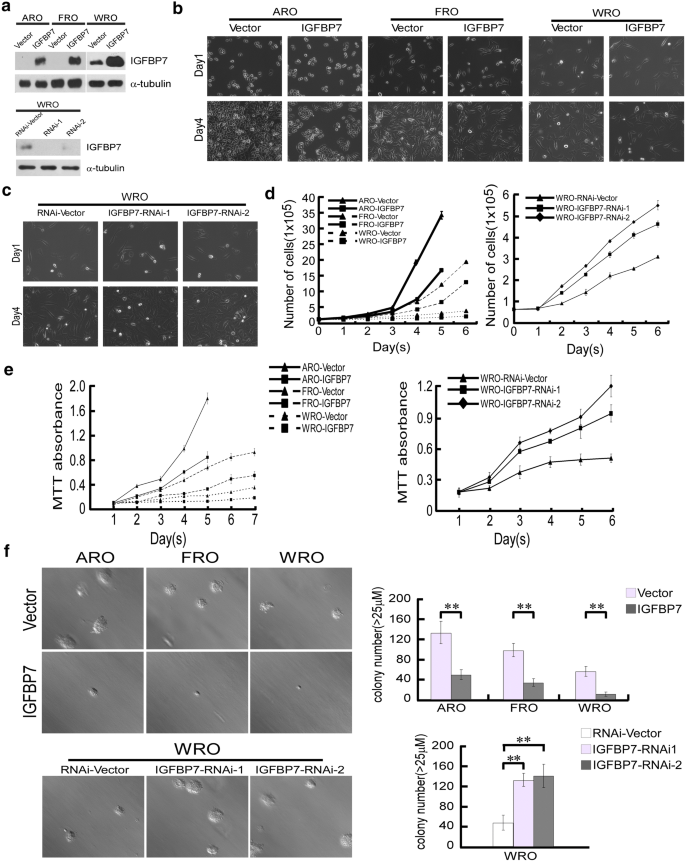
文献未提及具体实验产品,领域常规使用细胞培养试剂、MTT试剂、逆转录病毒载体、Western blot抗体等。
3.3 体内甲状腺肿瘤生长的抑制作用验证
实验目的是在体内水平验证IGFBP7对甲状腺癌肿瘤生长的调控作用。研究将过表达/沉默IGFBP7的ARO、FRO、WRO细胞分别皮下接种于BALB/C裸鼠背部,每2天测量肿瘤体积,实验终点处死小鼠并取瘤称重,同时进行HE染色和Ki67免疫组化检测增殖活性。结果显示,过表达IGFBP7的ARO、FRO、WRO细胞形成的肿瘤生长速度显著慢于对照组,终点肿瘤体积和重量均显著降低(n=5,P<0.05);其中WRO过表达组5只裸鼠中仅2只形成可检测的肿瘤,而对照组5只均成瘤;沉默IGFBP7的WRO细胞形成的肿瘤生长速度显著加快,体积和重量高于对照组(n=5,P<0.05);Ki67免疫组化结果显示,过表达IGFBP7的肿瘤组织中Ki67阳性细胞比例显著降低,沉默组则显著升高,进一步证实IGFBP7在体内抑制甲状腺癌增殖。
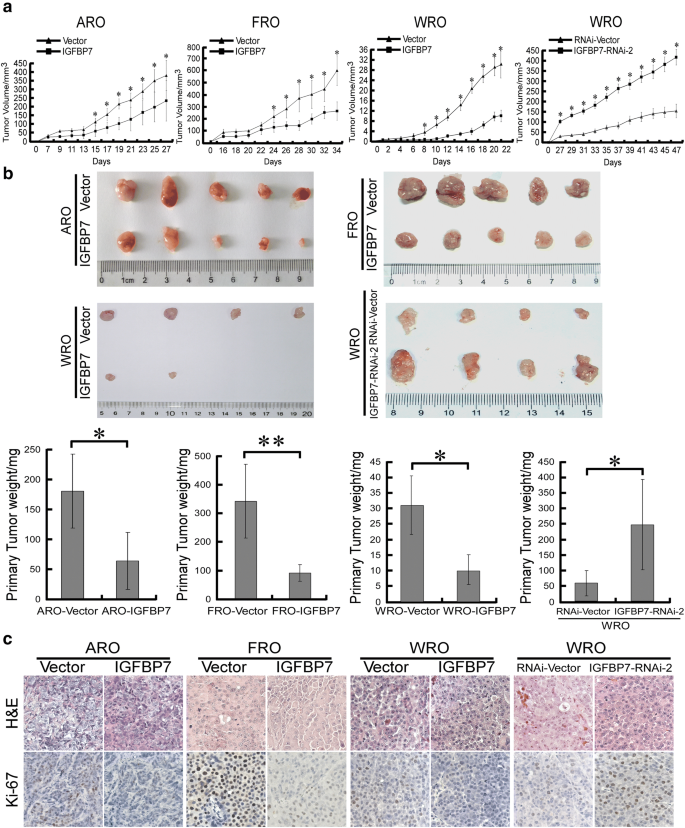
文献未提及具体实验产品,领域常规使用裸鼠模型、Ki67单克隆抗体、病理染色试剂盒等。
3.4 IGFBP7调控细胞周期进程的机制解析
实验目的是揭示IGFBP7抑制甲状腺癌细胞增殖的细胞周期机制。研究采用Western blot检测细胞周期调控蛋白的表达,结果显示过表达IGFBP7显著上调细胞周期依赖性激酶抑制剂p21和p27的表达,同时降低视网膜母细胞瘤蛋白(Rb)的磷酸化水平,而CDK2和Cyclin E的表达无显著变化;沉默IGFBP7则得到相反结果。为进一步验证细胞周期阻滞效应,采用5-溴-2-脱氧尿苷(BrdU)掺入实验和流式细胞术分析细胞周期分布:血清饥饿同步化后,过表达IGFBP7的ARO、FRO、WRO细胞中BrdU阳性率分别为10.6%、21.2%、7.7%,显著低于对照组的44.4%、34.0%、16.0%(n=3,P<0.01);流式细胞术结果显示,过表达IGFBP7的细胞中G0/G1期比例显著增加,S期比例显著降低,沉默IGFBP7则促进细胞从G1期进入S期,证实IGFBP7通过诱导G1/S期阻滞抑制细胞增殖。
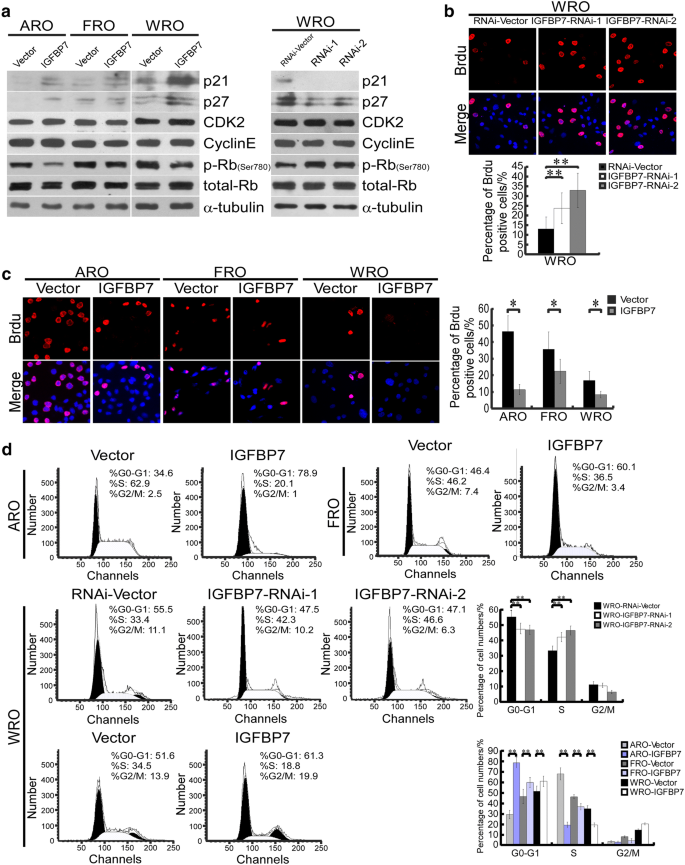
文献未提及具体实验产品,领域常规使用Western blot抗体、BrdU检测试剂盒、流式细胞仪等。
3.5 IGFBP7抑制AKT通路活性的机制验证
实验目的是明确IGFBP7调控细胞周期的上游信号通路。基于AKT通路在细胞周期调控中的关键作用,研究采用Western blot检测AKT的磷酸化水平,结果显示过表达IGFBP7显著降低AKT在Ser473和Thr308位点的磷酸化水平,沉默IGFBP7则显著增强该位点的磷酸化(n=3,P<0.01);进一步采用AKT激酶活性实验检测其激酶功能,结果显示过表达IGFBP7显著抑制AKT激酶活性,表现为其底物GSK3β的磷酸化水平降低,沉默IGFBP7则增强AKT激酶活性(n=3,P<0.01)。这一结果证实IGFBP7通过抑制AKT的磷酸化激活及激酶活性,进而调控细胞周期进程。
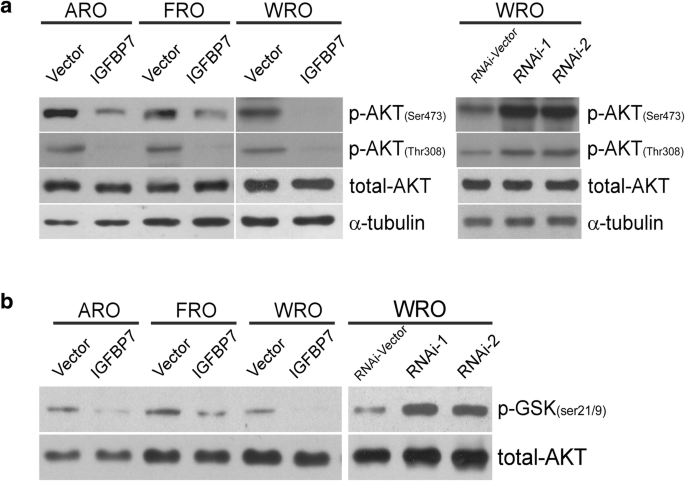
实验所用关键产品:Cell Signaling的AKT激酶活性检测试剂盒(货号9840)。
4. Biomarker研究及发现成果解析
本研究将IGFBP7定位为甲状腺癌亚型区分的潜在分泌型生物标志物,通过临床-基础-机制的系统研究,明确其表达模式、功能及机制,为甲状腺癌的诊断和治疗提供新靶点。
Biomarker定位:IGFBP7属于分泌型肿瘤抑制性生物标志物,其筛选与验证逻辑为:首先通过112例临床样本免疫组化筛选,明确其在FTC和ATC中特异性低表达的模式;随后通过细胞系和动物模型验证其抑癌功能;最后解析其通过AKT-细胞周期轴发挥作用的机制,形成完整的验证链条。研究过程中,IGFBP7的来源为临床甲状腺组织样本及甲状腺癌细胞系,验证方法包括免疫组化、Western blot、细胞增殖实验、体内肿瘤模型、激酶活性实验等;特异性方面,IGFBP7在FTC和ATC中的阳性率仅为13.4%和12.5%,与正常甲状腺、腺瘤、经典PTC的高阳性率(66.7%、65.0%)存在显著统计学差异(P<0.01);敏感性方面,其可有效区分低分化甲状腺癌(FTC、ATC)与高分化/良性病变。核心成果方面,IGFBP7作为甲状腺癌的潜在生物标志物,可用于区分不同分化程度的甲状腺癌亚型,尤其是FTC和ATC;功能上,其通过抑制AKT的磷酸化激活及激酶活性,上调细胞周期抑制剂p21和p27的表达,诱导G1/S期阻滞,从而抑制甲状腺癌细胞增殖;创新性在于首次系统揭示IGFBP7在甲状腺癌不同亚型中的表达模式,明确其作为分泌型生物标志物的诊断潜力,同时阐明其通过AKT-细胞周期轴发挥抑癌作用的机制。统计学结果方面,临床样本分析中FTC/ATC与PTC/腺瘤的IGFBP7阳性率差异具有显著统计学意义(P<0.01);细胞实验中增殖指标的差异均具有统计学意义(P<0.05或P<0.01,n=3);体内实验中肿瘤重量的差异具有统计学意义(P<0.05,n=5)。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。