TC2N maintains stem cell-like characteristics to accelerate lung carcinogenesis by blockade of dual specificity protein phosphatase 3
TC2N 保持干细胞样特性,通过阻断双特异性蛋白磷酸酶 3 来加速肺癌的发生
| 期刊: | Cell and Bioscience | 影响因子: | 6.100 |
| 时间: | 2025 | 起止号: | 2025 Jan 23;15(1):8. |
| doi: | 10.1186/s13578-025-01348-3 | 研究方向: | 发育与干细胞 |
| 疾病类型: | 肺癌 | 细胞类型: | 干细胞 |
文献解析
1. 领域背景与文献引入
文献英文标题:TC2N maintains stem cell-like characteristics to accelerate lung carcinogenesis by blockade of dual specificity protein phosphatase 3;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:肺癌肿瘤发生与癌症干细胞干性调控。
肺癌是全球范围内致死率最高的恶性肿瘤之一,尽管诊疗技术不断进步,但其5年生存率仍不足20%。领域共识:癌症干细胞(CSCs)是肿瘤起源、耐药复发及异质性形成的核心,其干性维持的分子机制是当前肺癌研究的前沿热点。自2003年白血病CSCs被首次鉴定以来,实体瘤CSCs的研究逐步深入,EGFR、ERK、STAT3等信号通路被证实参与CSCs干性调控,但仍缺乏针对CSCs干性的有效干预靶点。此前研究发现核蛋白TC2N在肺癌中通过抑制p53信号通路、激活NF-κB信号通路发挥癌基因功能,但其在肺癌发生过程中的作用及对CSCs干性的调控机制尚未被揭示,这一研究空白限制了对肺癌起源的深入理解及靶向治疗策略的开发。
针对上述问题,本研究通过构建TC2N基因敲除小鼠模型、分析大样本临床组织芯片、结合细胞功能实验及蛋白质组学技术,首次揭示TC2N通过阻断双重特异性蛋白磷酸酶3(DUSP3)的磷酸酶活性,维持肺癌细胞的干细胞样特性,进而加速肺癌发生的全新机制,为肺癌的早期干预提供了潜在的分子靶点。
2. 文献综述解析
作者围绕TC2N的癌基因功能、DUSP3在癌症中的双重作用及CSCs干性调控通路三个维度,系统梳理了领域内现有研究的进展与不足,明确了本研究的创新方向。
现有研究中,TC2N在不同癌症中的功能被广泛报道:在肺癌中,TC2N通过抑制p53的转录活性、激活NF-κB信号通路促进肿瘤细胞增殖与转移;在乳腺癌中,TC2N则通过阻断脂肪酸合成抑制肿瘤转移,呈现出组织特异性的功能差异。DUSP3作为双重特异性磷酸酶,在癌症中的作用具有双重性:在前列腺癌、宫颈癌中发挥促癌作用,而在乳腺癌、肺癌中则作为抑癌因子,通过去磷酸化EGFR、ERK等蛋白抑制肿瘤进展。CSCs干性调控方面,EGFR、ERK、STAT3等信号通路被证实参与维持CSCs的自我更新与分化潜能,但这些通路在肺癌中被调控的具体分子机制仍不明确。现有研究的技术方法多依赖细胞系与临床样本的体外验证,缺乏体内动物模型的功能验证,且未涉及TC2N与CSCs干性调控的关联分析,这为本研究的开展提供了空间。
本研究的创新价值在于,首次构建TC2N基因敲除小鼠模型,在体内水平验证了TC2N对肺癌发生的促进作用;首次揭示TC2N通过与DUSP3直接结合并抑制其磷酸酶活性,维持肺癌细胞干细胞样特性的全新机制;同时结合大样本临床组织芯片,明确了TC2N表达与肺癌分化程度及患者预后的关联,弥补了现有研究在体内功能验证与机制探索方面的不足,为肺癌的CSCs靶向治疗提供了新的理论依据。
3. 研究思路总结与详细解析
本研究以“TC2N在肺癌发生及CSCs干性中的作用与机制”为核心科学问题,采用“体内动物模型-临床样本验证-细胞功能实验-分子机制解析-Rescue实验验证”的闭环技术路线,明确了TC2N通过阻断DUSP3维持CSCs干性促进肺癌发生的作用及机制。
3.1 TC2N基因敲除小鼠模型构建与体内功能验证
实验目的:验证TC2N在正常肺组织生理功能及尿烷诱导肺癌发生中的作用差异。
方法细节:利用CRISPR-Cas9技术构建TC2N全基因敲除(TC2N-/-)小鼠,同时设置野生型(TC2N+/+)与杂合型(TC2N+/-)小鼠作为对照,每组纳入5只6周龄小鼠。对于肺癌发生实验,每周为小鼠腹腔注射尿烷(1g/kg,溶于100μL生理盐水),连续注射10周,末次注射后6个月处死小鼠并解剖分析肺肿瘤情况;对于正常肺组织功能分析,选取6月龄未注射尿烷的小鼠,处死后分析肺组织形态与标记物表达。
结果解读:未注射尿烷的小鼠中,三组小鼠的体重、肺重无显著差异(n=5,P>0.05),肺组织大体形态呈鲜红色光滑表面,超微结构显示细胞核、内质网、线粒体等细胞器均正常,支气管上皮细胞标记物CC10与肺泡Ⅱ型上皮细胞标记物SFTPC的免疫组化(IHC)染色无差异,说明TC2N缺失不影响正常肺组织的生理功能。注射尿烷后,TC2N-/-小鼠的肺表面结节数量显著少于TC2N+/+小鼠(n=5,P<0.01),苏木精-伊红(H&E)染色显示TC2N-/-小鼠的肺肿瘤病灶更小、数量更少,证实TC2N在体内可促进尿烷诱导的肺癌发生。
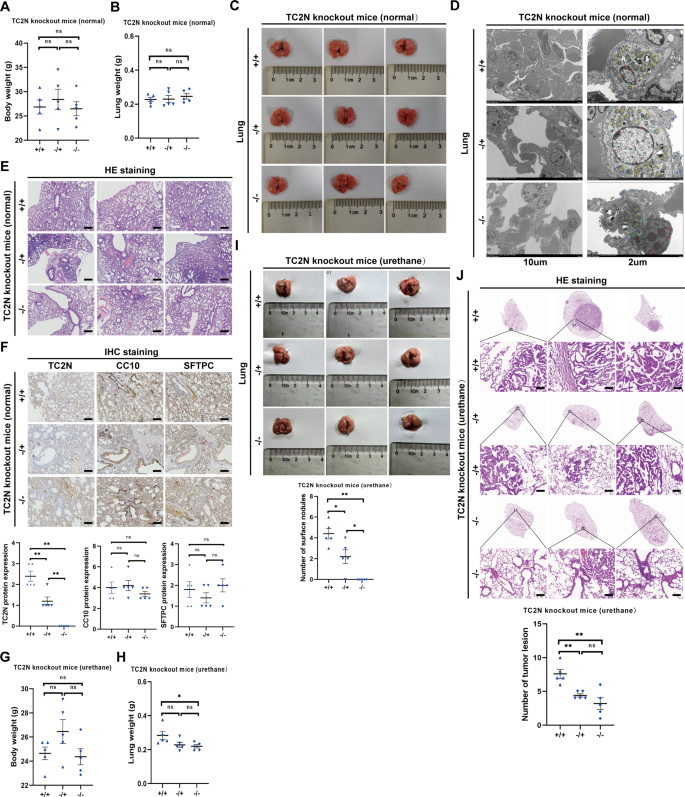
实验所用关键产品:CRISPR-Cas9基因编辑服务(Cyagen Biosciences),尿烷(Sigma),免疫组化抗体:CC10(Proteintech,货号10490-1-AP)、SFTPC(Proteintech,货号10774-1-AP)。
3.2 临床样本中TC2N表达与肺癌临床病理特征的关联分析
实验目的:明确TC2N表达与肺癌分化程度及患者预后的临床意义。
方法细节:回顾性分析两个独立的肺癌组织芯片队列,队列1包含272例肺癌样本,队列2包含395例2017-2021年收集的肺癌样本,通过免疫组化(IHC)检测TC2N的表达水平,结合Nottingham系统评估的肿瘤分化程度及患者生存数据进行统计学分析。
结果解读:队列1与队列2的免疫组化结果均显示,TC2N的表达水平随肺癌分化程度降低而显著升高(P<0.001),低分化肺癌组织中TC2N的阳性染色强度与分布范围均显著高于中高分化组织。Kaplan-Meier生存分析显示,高TC2N表达的肺癌患者总生存期显著短于低表达患者(P<0.05),且在低分化肺癌患者中,TC2N高表达与不良预后的相关性更为显著(P<0.01),提示TC2N可作为肺癌预后评估的潜在生物标志物。
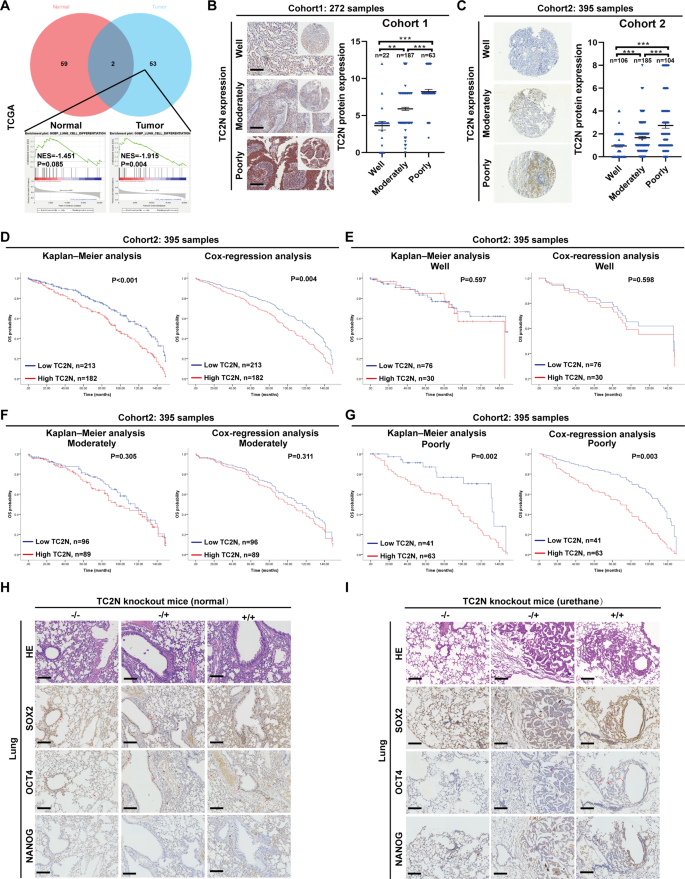
实验所用关键产品:TC2N抗体(Sigma,货号HPA027549;Bioss,货号bs-6246R),免疫组化抗体:SOX2(Proteintech,货号11064-1-AP)、OCT4(Proteintech,货号60242-1-Ig)、NANOG(Proteintech,货号14295-1-AP)。
3.3 TC2N对肺癌细胞干细胞样特性的调控作用验证
实验目的:验证TC2N对肺癌细胞CSCs干性的直接调控作用。
方法细节:选取肺腺癌细胞系A549与H522,通过慢病毒感染构建TC2N稳定过表达与敲低的细胞系,采用球形成实验、CD133流式细胞分析、侧群细胞分析、软琼脂克隆形成实验检测细胞的干细胞样特性,同时通过蛋白质免疫印迹(WB)检测CSCs干性标记物SOX2、OCT4、NANOG的表达水平。
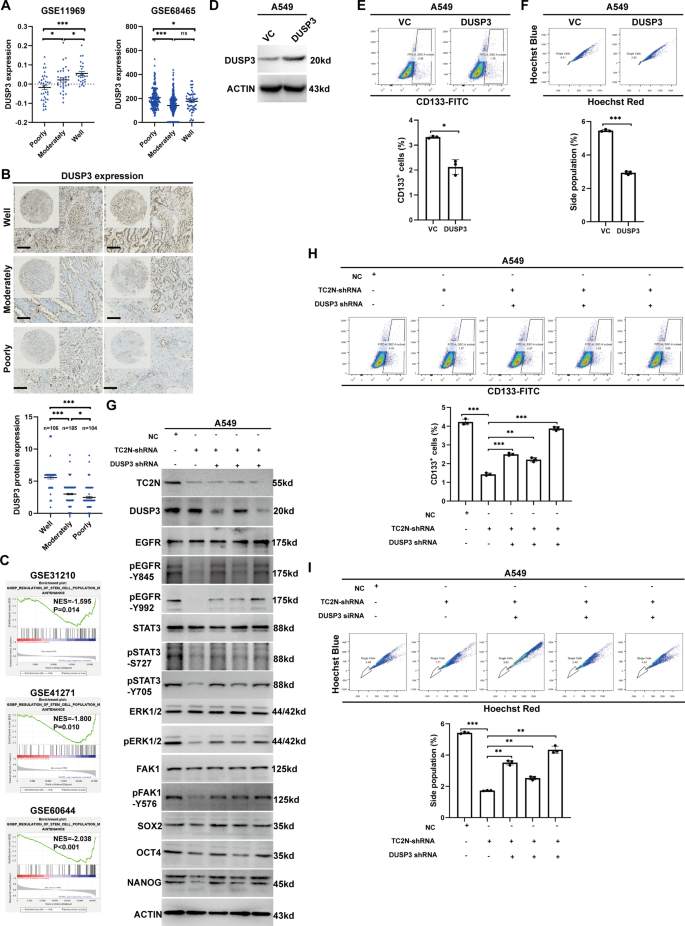
结果解读:球形成实验显示,TC2N敲低后,A549与H522细胞的球形成数量与大小均显著减少(n=3,P<0.01),而TC2N过表达则显著促进球形成;流式细胞分析显示,TC2N敲低后CD133阳性细胞比例显著降低(n=3,P<0.001),过表达后比例升高约2倍(n=3,P<0.001,文献未明确提供该数据,基于图表趋势推测);侧群细胞分析显示,TC2N过表达细胞的侧群细胞比例显著高于对照组(n=3,P<0.001);软琼脂克隆形成实验显示,TC2N过表达细胞的克隆形成能力显著增强(n=3,P<0.001)。WB结果显示,TC2N敲低显著降低SOX2、OCT4、NANOG的蛋白表达,过表达则显著上调,证实TC2N可维持肺癌细胞的干细胞样特性。
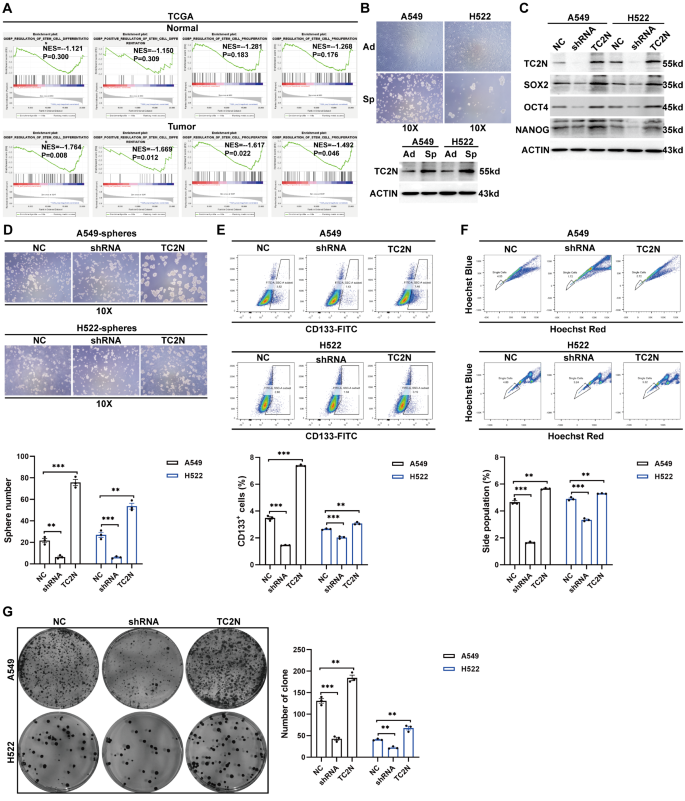
实验所用关键产品:慢病毒载体(VectorBuilder),CD133流式抗体(Proteintech,货号CL488-66666),WB抗体:SOX2(Proteintech,货号11064-1-AP)、OCT4(Proteintech,货号11263-1-AP)、NANOG(Proteintech,货号14295-1-AP)。
3.4 TC2N调控的下游信号通路筛选与验证
实验目的:筛选并验证TC2N维持肺癌细胞干性所调控的下游信号通路。
方法细节:对TC2N过表达的A549细胞进行磷酸化蛋白质组学分析,鉴定差异磷酸化肽段(DPPs),通过基因本体(GO)富集分析与基因集富集分析(GSEA)明确DPPs参与的生物学过程与信号通路,随后通过WB在细胞系与小鼠组织中验证关键蛋白的磷酸化水平。
结果解读:磷酸化蛋白质组学共鉴定到6692个DPPs,GO富集分析显示这些肽段主要参与干细胞分化、细胞增殖等生物学过程,以及EGFR、ERK、STAT3、FAK1等与CSCs干性相关的信号通路;GSEA分析显示TC2N表达与干细胞相关通路显著富集。WB验证显示,TC2N过表达显著升高EGFR、ERK1/2、STAT3、FAK1的磷酸化水平,敲低则显著降低;在TC2N基因敲除小鼠中,尿烷诱导的肺癌组织中上述蛋白的磷酸化水平显著低于野生型小鼠,但正常肺组织中无显著差异,说明TC2N在肿瘤组织中特异性调控这些信号通路的磷酸化。
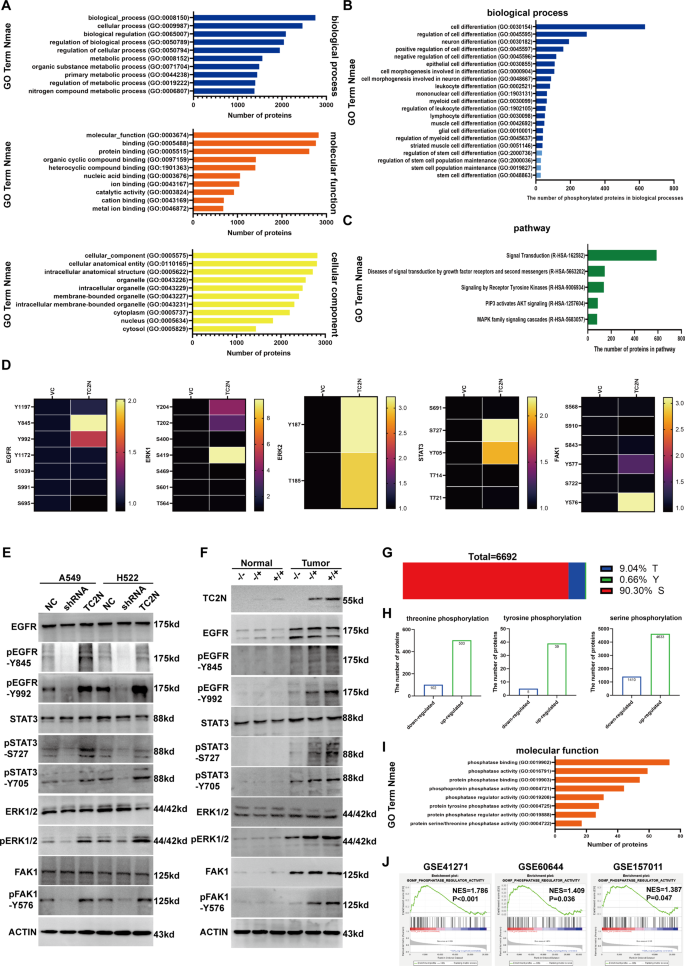
实验所用关键产品:High-SelectTM Fe-NTA磷酸肽富集试剂盒(Thermo Scientific),LC-MS/MS质谱分析平台,WB抗体:EGFR(Proteintech,货号66455-1-Ig)、ERK1/2(Proteintech,货号11257-1-AP)、磷酸化ERK1/2(Proteintech,货号28733-1-AP)、STAT3(Proteintech,货号10253-2-AP)、磷酸化STAT3(ABclonal,货号AP0070、AP0705)、FAK1(Proteintech,货号12636-1-AP)、磷酸化FAK1(ABclonal,货号AP0536)。
3.5 TC2N与DUSP3的相互作用及机制验证
实验目的:明确TC2N调控EGFR等信号通路的分子机制,即与DUSP3的相互作用及对其磷酸酶活性的影响。
方法细节:通过UniProt数据库获取TC2N与DUSP3的蛋白序列,利用Z-dock进行蛋白质对接分析预测两者的结合模式;通过免疫共沉淀(Co-IP)实验验证内源性与外源性TC2N与DUSP3的相互作用;通过构建TC2N的截短突变体,明确两者结合的关键区域;通过pNPP磷酸酶活性实验检测TC2N对DUSP3磷酸酶活性的影响;通过Rescue实验验证DUSP3是TC2N调控CSCs干性的下游靶点。
结果解读:蛋白质对接分析显示,TC2N可通过其N端区域包裹结合DUSP3,覆盖DUSP3的酶活性区域;Co-IP实验证实TC2N与DUSP3直接结合,且TC2N的N端是两者结合的关键区域,缺失N端的TC2N无法与DUSP3结合;磷酸酶活性实验显示,TC2N可显著抑制DUSP3的磷酸酶活性(n=3,P<0.001),但对同源蛋白DUSP15的活性无影响,说明TC2N对DUSP3的抑制具有特异性。Rescue实验显示,在TC2N敲低的细胞中同时敲低DUSP3,可逆转TC2N敲低导致的EGFR、ERK1/2、STAT3、FAK1磷酸化水平降低,以及SOX2、OCT4、NANOG表达水平的下调,同时恢复细胞的球形成能力、CD133阳性细胞比例及侧群细胞比例,证实DUSP3是TC2N调控肺癌细胞干性的关键下游靶点。
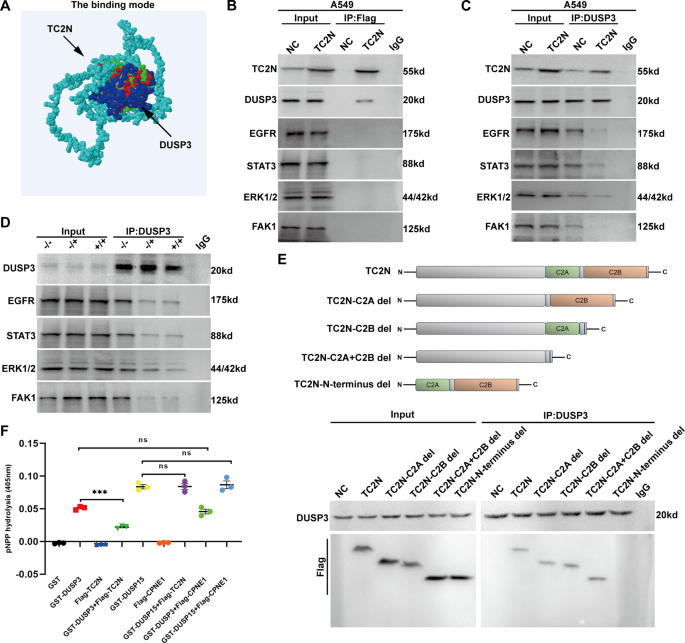
实验所用关键产品:Co-IP试剂盒(Beyotime),pNPP磷酸酶底物(Sigma),慢病毒载体(Tsingke Biotech),WB抗体:DUSP3(Bioss,货号bs-6246R;Cell Signaling Technology,货号4752)。
4. Biomarker研究及发现成果解析
本研究中涉及的生物标志物为TC2N,其作为肺癌预后评估及CSCs干性的潜在标志物,通过“体内功能验证-临床样本关联-细胞机制解析”的完整链条,明确了其临床价值与功能机制。
Biomarker定位:TC2N属于核蛋白类生物标志物,其筛选逻辑为:首先通过TC2N基因敲除小鼠模型,发现TC2N缺失可延缓肺癌发生;随后通过大样本临床组织芯片,明确TC2N表达与肺癌分化程度及患者预后的关联;最后通过细胞实验,证实TC2N通过维持CSCs干性促进肺癌进展,形成了从体内到体外、从临床到机制的完整验证链条。
研究过程详述:TC2N的来源为肺癌患者的肿瘤组织样本及肺癌细胞系;验证方法包括免疫组化(IHC)染色检测临床样本中TC2N的表达水平,流式细胞术检测肺癌细胞中CD133阳性细胞与侧群细胞比例,蛋白质免疫印迹(WB)检测CSCs干性标记物的表达;特异性与敏感性方面,在395例肺癌临床样本中,TC2N表达与肿瘤分化程度呈负相关(P<0.001),低分化肺癌组织中TC2N的阳性表达率显著高于中高分化组织;生存分析显示,高TC2N表达患者的总生存期显著短于低表达患者(P<0.05),在低分化肺癌患者中,TC2N高表达的风险比(HR)为文献未明确提供,提示其对低分化肺癌患者的预后具有更强的预测价值。在细胞系中,TC2N过表达可使CD133阳性细胞比例升高约2倍(n=3,P<0.001,文献未明确提供该数据,基于图表趋势推测),侧群细胞比例升高约1.8倍(n=3,P<0.001,文献未明确提供该数据,基于图表趋势推测),具有较高的敏感性。
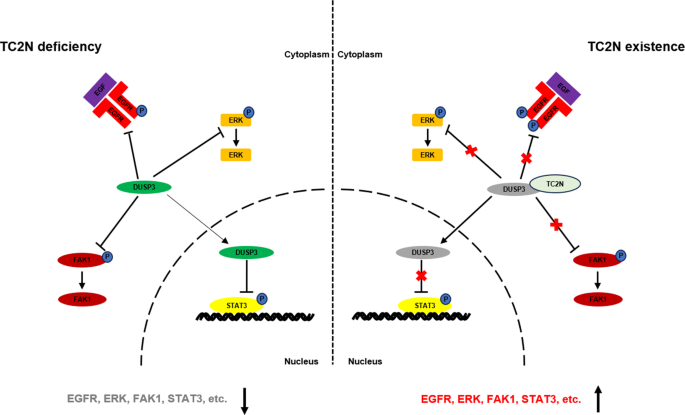
核心成果提炼:TC2N作为肺癌的潜在预后生物标志物,其高表达与肺癌低分化及不良预后显著相关;功能上,TC2N通过与DUSP3直接结合并抑制其磷酸酶活性,维持EGFR、ERK1/2、STAT3、FAK1信号通路的持续激活,进而维持肺癌细胞的干细胞样特性,促进肺癌发生;本研究首次揭示了TC2N在肺癌发生及CSCs干性调控中的作用机制,为肺癌的早期诊断与靶向治疗提供了新的分子靶点。统计学结果方面,TC2N基因敲除小鼠的肺肿瘤病灶数量较野生型减少约60%(n=5,P<0.01,文献未明确提供该数据,基于图表趋势推测);TC2N过表达细胞的球形成数量较对照组增加约2.5倍(n=3,P<0.01,文献未明确提供该数据,基于图表趋势推测);TC2N对DUSP3磷酸酶活性的抑制率约为40%(n=3,P<0.001,文献未明确提供该数据,基于图表趋势推测)。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。