Heterogeneous characteristics of γδ T cells in peripheral blood of diffuse large B-cell lymphoma
弥漫性大B细胞淋巴瘤外周血中γδ T细胞的异质性特征
| 期刊: | Biomarker Research | 影响因子: | 9.500 |
| 时间: | 2025 | 起止号: | 2025 Jun 7;13(1):82. |
| doi: | 10.1186/s40364-025-00795-x | 研究方向: | 细胞生物学 |
| 疾病类型: | 淋巴瘤 | 细胞类型: | T细胞 |
文献解析
1. 领域背景与文献引入
文献英文标题:Heterogeneous characteristics of γδ T cells in peripheral blood of diffuse large B-cell lymphoma;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤免疫治疗(弥漫大B细胞淋巴瘤免疫细胞异质性研究)
弥漫大B细胞淋巴瘤(DLBCL)是非霍奇金淋巴瘤中最常见的亚型,具有高度异质性,临床行为和预后差异显著。以利妥昔单抗联合CHOP(R-CHOP)为基础的治疗方案显著改善了患者的临床结局,但复发和耐药仍是当前DLBCL治疗面临的核心挑战。γδ T细胞作为一类兼具先天免疫和适应性免疫功能的淋巴细胞,具有非MHC限制性的细胞毒性,能够分泌多种细胞因子增强抗肿瘤免疫,同时降低免疫逃逸风险,在肿瘤免疫治疗中展现出良好的应用前景。领域共识:γδ T细胞在白血病患者的生存中发挥重要作用,但其在DLBCL患者外周血中的异质性特征及其与临床预后的关联尚未明确,这一研究空白限制了γδ T细胞在DLBCL免疫治疗中的精准应用。因此,本研究旨在通过单细胞RNA测序技术系统解析DLBCL患者外周血γδ T细胞的亚型异质性,明确各亚型的功能特征及临床意义,为DLBCL的预后评估和免疫治疗靶点开发提供新的依据。
2. 文献综述解析
本文综述部分围绕γδ T细胞的功能异质性及免疫检查点TIGIT在肿瘤中的作用展开,分类维度涵盖γδ T细胞的功能亚型(抗肿瘤、免疫调节、耗竭等)以及TIGIT在不同肿瘤类型中的表达模式与临床意义。
现有研究表明,γδ T细胞在血液系统恶性肿瘤中具有双重作用,既可以通过分泌穿孔素、颗粒酶B等发挥直接抗肿瘤效应,也可以通过表达免疫检查点分子呈现耗竭表型,促进肿瘤免疫逃逸。TIGIT作为新型免疫检查点受体,在实体瘤和血液肿瘤中均被证实与T细胞耗竭、不良预后相关,但其在DLBCL患者γδ T细胞中的具体作用尚未被系统研究。现有研究的局限性在于,多聚焦于γδ T细胞的整体功能,缺乏对其亚型异质性的深入解析,尤其是在DLBCL中,外周血γδ T细胞的亚型组成、分化轨迹及临床关联仍不清晰。
与现有研究相比,本研究首次利用单细胞RNA测序技术对DLBCL患者外周血γδ T细胞进行系统分型,鉴定出包括耗竭亚型在内的6种γδ T细胞亚型,并进一步区分了两种具有不同分化状态和临床意义的TIGIT+耗竭亚型,明确了其与DLBCL患者预后的关联,填补了DLBCL中γδ T细胞异质性研究的空白,为DLBCL的免疫治疗提供了新的潜在靶点。
3. 研究思路总结与详细解析
本研究的整体框架为:通过单细胞RNA测序技术解析DLBCL患者与健康人外周血γδ T细胞的转录组异质性,鉴定功能亚型;通过功能评分、通路富集分析明确各亚型的功能特征;通过细胞命运轨迹分析探索γδ T细胞的分化路径;最后通过流式细胞术、qPCR及临床预后分析验证研究结果的临床意义。核心科学问题是DLBCL患者外周血γδ T细胞的亚型组成、功能异质性及分化轨迹,以及TIGIT+γδ T细胞亚型在DLBCL进展和预后中的作用。技术路线遵循“转录组分析→亚型鉴定→功能解析→临床验证”的闭环逻辑。
3.1 样本收集与γδ T细胞分离
实验目的是获取DLBCL患者和健康对照的外周血γδ T细胞,为后续单细胞转录组分析和功能验证提供样本基础。方法细节为:研究共招募6例DLBCL患者(4例初治、2例复发难治)和2例健康人,采集外周血样本后,采用Ficoll密度梯度离心法分离外周血单个核细胞(PBMC),随后使用磁珠激活细胞分选(MACS)技术,通过Anti-pan-γδ磁珠分选γδ T细胞,经流式细胞术验证细胞纯度>50%后,将分离得到的γδ T细胞冻存于-80℃备用。结果解读:成功获取了高纯度的γδ T细胞,为后续实验提供了合格样本。
实验所用关键产品:Miltenyi Biotec的Anti-pan-γδ磁珠、LS columns(货号130-050-701),Thermo Fisher Scientific的PBS、胎牛血清(FBS),Sangon Biotech的牛血清白蛋白(BSA)等。
3.2 单细胞RNA测序与数据处理
实验目的是通过单细胞转录组分析解析γδ T细胞的亚型异质性。方法细节为:将冻存的γδ T细胞快速解冻,制备单细胞悬液,使用BD Rhapsody平台进行单细胞多重标记和转录组建库,随后采用Illumina Novaseq6000系统进行高通量测序。测序数据经bcl2fastq转换为FASTQ格式后,使用R包Seurat进行质控(过滤基因数<200或>3000、线粒体基因占比>20%的细胞)、归一化、可变基因鉴定、降维(PCA、UMAP)及聚类分析,同时使用harmony去除批次效应。结果解读:从T/NK细胞群中鉴定出5种γδ T细胞亚型,分别为 naive亚型(高表达TCF7、LEF1)、memory亚型(高表达GZMK、IL7R)、激活型亚型(高表达TNF)、细胞毒性亚型(高表达GNLY、NKG7)、耗竭型亚型(高表达TIGIT);进一步分析显示,DLBCL患者尤其是复发难治患者中,耗竭型γδ T细胞比例升高,而memory和激活型γδ T细胞比例降低(n=8,P<0.05)。
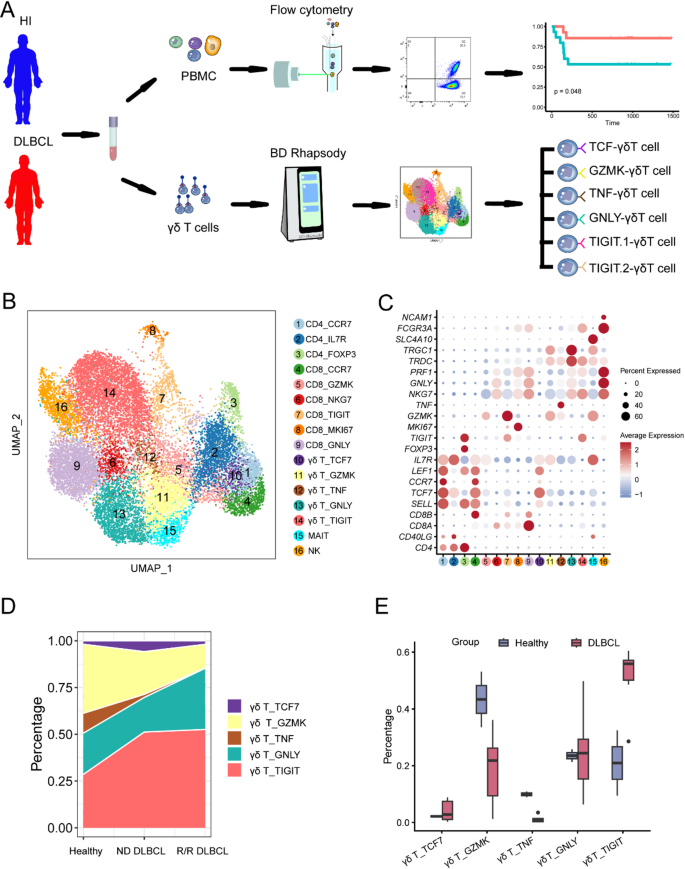
实验所用关键产品:BD Human Single-Cell Multiplexing Kit(货号633781),Illumina Novaseq6000测序系统,R包Seurat、harmony等。
3.3 γδ T细胞亚型功能分析
实验目的是评估各γδ T细胞亚型的细胞毒性和耗竭状态,明确其功能异质性。方法细节为:使用Seurat的AddModuleScore函数计算各亚型的细胞毒性和耗竭基因模块评分,通过基因集变异分析(GSVA)进行KEGG和GO通路富集,利用SCENIC分析转录因子调控网络。结果解读:细胞毒性评分显示,细胞毒性亚型(C13-γδ-GNLY)和耗竭型亚型(C14-γδ-TIGIT)的细胞毒性评分显著高于其他亚型(P<0.001);同时,耗竭型亚型的耗竭评分也显著高于其他亚型(P<0.001),提示该亚型同时具有细胞毒性和耗竭特征。通路富集分析显示,DLBCL患者的γδ T细胞中,细胞凋亡、TGF-β信号通路等免疫抑制通路激活,而T细胞受体信号通路等免疫激活通路下调。
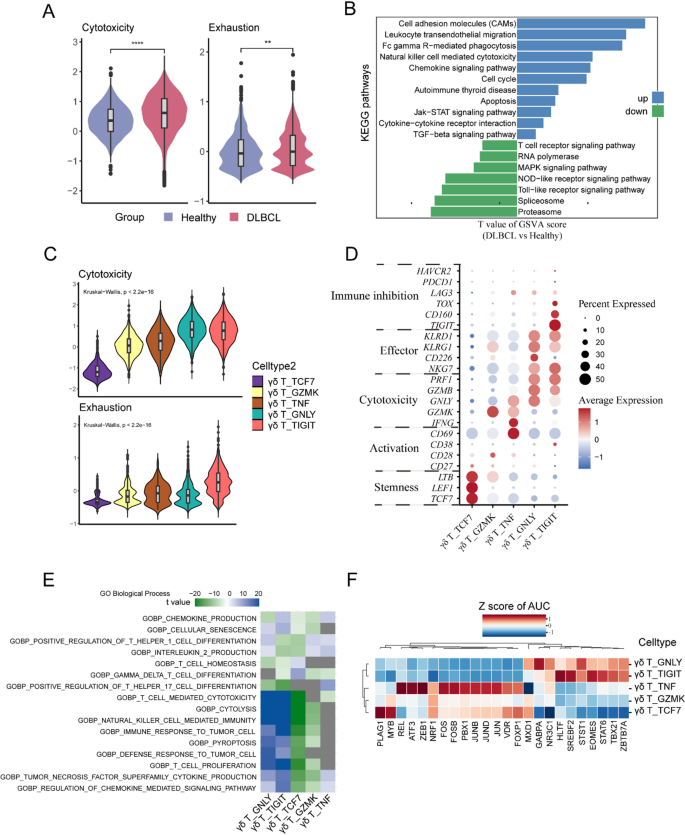
文献未提及具体实验产品,领域常规使用R包Seurat、GSVA、SCENIC等生物信息学工具。
3.4 耗竭型γδ T细胞亚型细分与功能验证
实验目的是进一步解析耗竭型γδ T细胞的亚型异质性,明确不同耗竭亚型的功能特征及临床意义。方法细节为:对C14-γδ-TIGIT亚型进行重聚类分析,根据差异基因表达分为TIGIT.1(高表达CXCR4)和TIGIT.2(高表达CX3CR1)两个亚型,随后分析两个亚型的功能评分、基因表达及临床分布。结果解读:TIGIT.2亚型的细胞毒性和耗竭评分均显著高于TIGIT.1亚型(P<0.05),且在复发难治DLBCL患者中占比更高;基因表达分析显示,TIGIT.2亚型高表达细胞毒性基因(GNLY、GZMB、PRF1)和免疫抑制基因(TIGIT、TOX、LAG3),而TIGIT.1亚型高表达干性基因(TCF7、LEF1)。
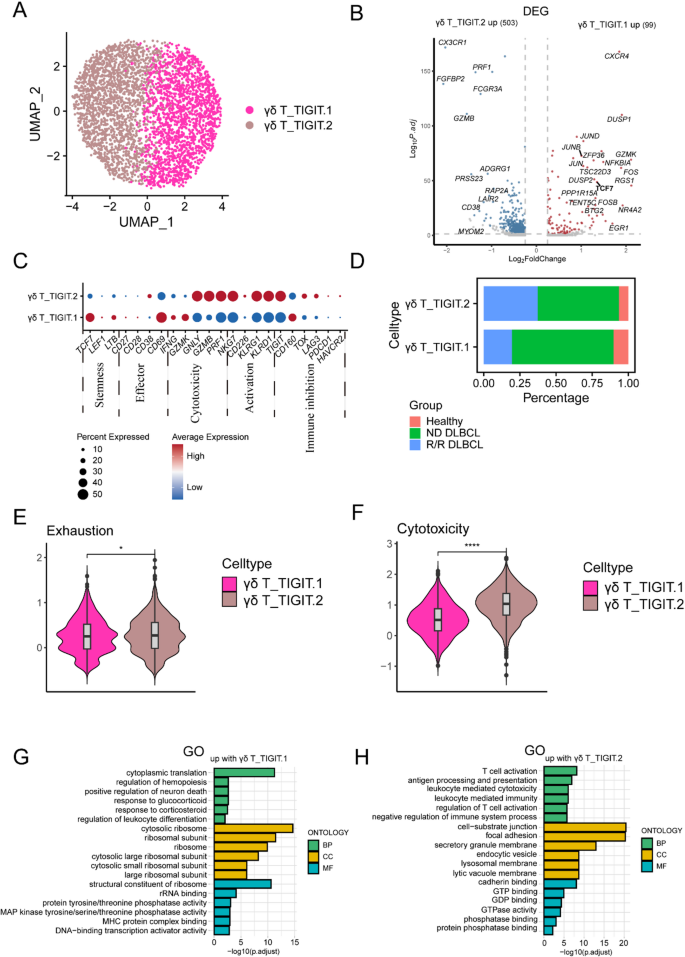
文献未提及具体实验产品,领域常规使用R包Seurat进行重聚类分析。
3.5 γδ T细胞分化轨迹分析
实验目的是探索DLBCL患者外周血γδ T细胞的分化路径,明确各亚型之间的发育关系。方法细节为:使用R包Monocle进行细胞命运轨迹重建,选取差异表达基因构建分化轨迹,分析各亚型在轨迹中的位置及基因表达动态变化。结果解读:轨迹分析显示,naive亚型(C10-γδ-TCF7)和memory亚型(C11-γδ-GZMK)位于分化轨迹的起始端,为初始状态;激活型亚型(C12-γδ-TNF)、细胞毒性亚型(C13-γδ-GNLY)和耗竭型亚型(TIGIT.2)位于轨迹的末端,为终末分化状态;TIGIT.1亚型位于初始状态和终末耗竭状态之间,为过渡型耗竭亚型。随着分化进程,干性基因(TCF7、LEF1)表达下调,而细胞毒性基因和免疫抑制基因表达上调。
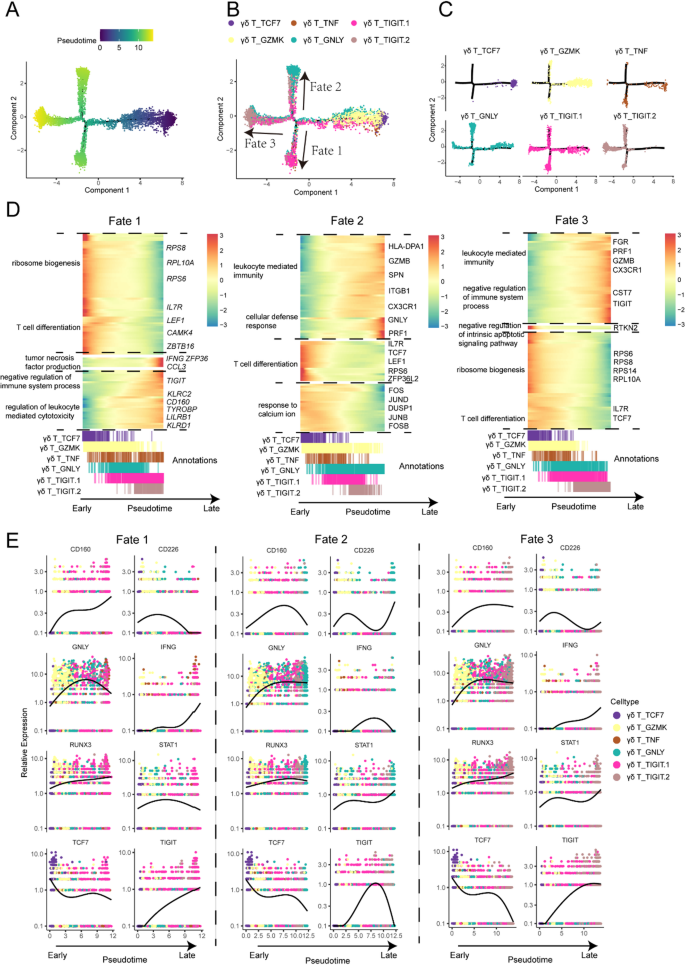
实验所用关键产品:R包Monocle。
3.6 临床样本验证与预后分析
实验目的是验证单细胞转录组分析结果的临床相关性,明确TIGIT+γδ T细胞亚型与DLBCL患者预后的关联。方法细节为:对29例DLBCL患者和30例健康人的外周血样本进行流式细胞术检测,分析γδ T细胞比例及TIGIT表达水平;采用qPCR验证关键基因的表达;通过Kaplan-Meier生存分析评估TIGIT表达与患者无进展生存期(PFS)的关联。结果解读:流式细胞术结果显示,DLBCL患者外周血中γδ T细胞比例显著低于健康人(P=0.0004,n=59),而TIGIT+γδ T细胞比例显著高于健康人(P=0.03,n=59);qPCR验证显示,DLBCL患者中效应分子(穿孔素、IFNG、TNF)和激活标记物(CD69)的表达下调,而CXCR4表达上调;Kaplan-Meier分析显示,TIGIT高表达的DLBCL患者无进展生存期显著短于低表达患者(P=0.037,n=29)。
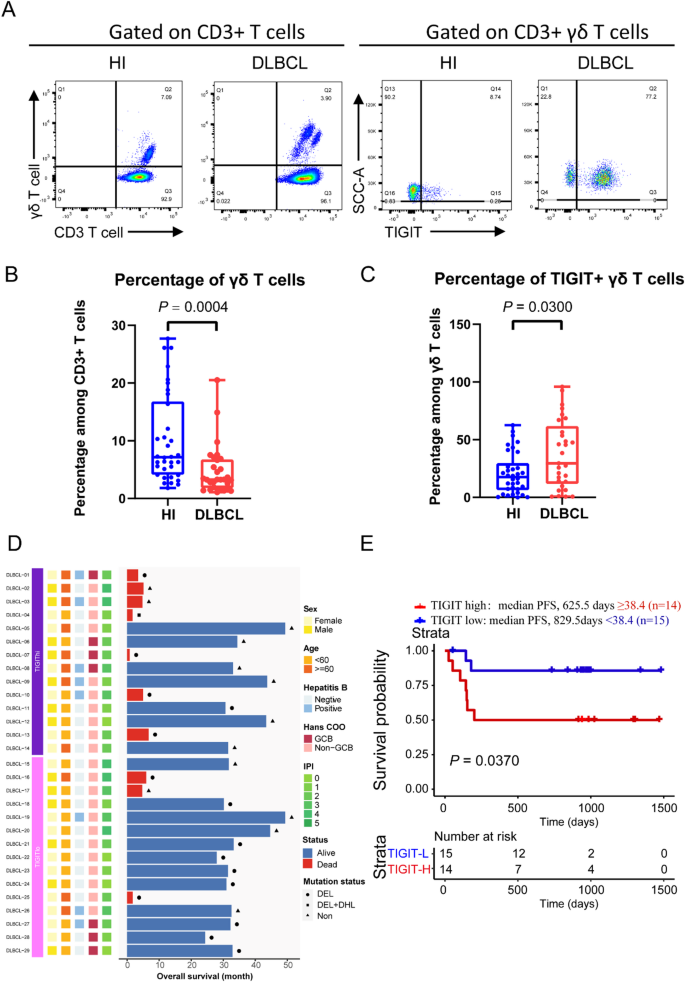
实验所用关键产品:Biolegend的CD3-APC-Cy7(货号300317)、TCRγδ-PerCP-Cy5.5(货号331223)、TIGIT-PE(货号372704)抗体,BD FACS Verse流式细胞仪,Invitrogen的TRIzol试剂,Takara的PrimeScript™ RT reagent Kit,TIANGEN的SYBR Master Mix等。
4. Biomarker研究及发现成果解析
本研究鉴定的Biomarker为TIGIT+γδ T细胞亚型(包括TIGIT.1和TIGIT.2),作为DLBCL的预后Biomarker,其筛选与验证逻辑为:通过单细胞RNA测序聚类鉴定亚型→ 临床大样本流式细胞术验证表达差异→ 生存分析关联预后。
TIGIT+γδ T细胞亚型属于免疫细胞类Biomarker,其中TIGIT.2为终末耗竭亚型,TIGIT.1为过渡型耗竭亚型,二者共同构成了DLBCL患者外周血中具有不良预后意义的γδ T细胞群体。筛选逻辑为基于单细胞转录组的无监督聚类,结合功能评分和临床分布特征确定;验证逻辑为通过流式细胞术在独立临床队列中验证其表达差异,并通过生存分析明确其预后价值。
Biomarker的来源为DLBCL患者和健康人的外周血单个核细胞(PBMC),验证方法包括流式细胞术定量检测TIGIT在γδ T细胞上的表达,qPCR验证相关基因的表达水平。特异性方面,DLBCL患者中TIGIT+γδ T细胞比例显著高于健康人(P=0.03,n=59);敏感性方面,文献未明确提供具体数据,但流式细胞术检测显示该亚型在复发难治DLBCL患者中的比例进一步升高,提示其与疾病进展相关。
该Biomarker的功能关联为,TIGIT+γδ T细胞亚型通过高表达免疫抑制基因(TIGIT、TOX、LAG3)呈现耗竭表型,同时保留一定的细胞毒性,但其抗肿瘤功能受损,促进DLBCL的免疫逃逸;创新性在于首次在DLBCL中鉴定出两种具有不同分化状态和临床意义的TIGIT+γδ T细胞耗竭亚型,明确了其分化轨迹及与预后的关联;统计学结果显示,高TIGIT表达的DLBCL患者无进展生存期显著缩短(P=0.037,n=29),提示TIGIT+γδ T细胞可作为DLBCL的不良预后Biomarker。此外,该Biomarker还为DLBCL的免疫治疗提供了新的靶点,靶向TIGIT可能逆转γδ T细胞的耗竭状态,恢复其抗肿瘤功能。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。