Genome editing of the HIV co-receptors CCR5 and CXCR4 by CRISPR-Cas9 protects CD4(+) T cells from HIV-1 infection.
利用 CRISPR-Cas9 对 HIV 辅助受体 CCR5 和 CXCR4 进行基因组编辑,可以保护 CD4(+) T 细胞免受 HIV-1 感染。
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2017 | 起止号: | 2017 Sep 9; 7:47 |
| doi: | 10.1186/s13578-017-0174-2 | 靶点: | CCR5、CD4、CXCR4、CAS9 |
| 研究方向: | 细胞生物学 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Genome editing of the HIV co-receptors CCR5 and CXCR4 by CRISPR-Cas9 protects CD4+ T cells from HIV-1 infection;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:HIV-1感染基因治疗、CRISPR-Cas9基因编辑。
艾滋病(Acquired Immune Deficiency Syndrome, AIDS)由人类免疫缺陷病毒1型(Human Immunodeficiency Virus type 1, HIV-1)感染引起,自1981年首次报道以来已成为全球重大公共卫生问题。HIV-1主要靶向人体CD4+T淋巴细胞,通过病毒表面蛋白gp120结合细胞表面CD4受体,再辅助结合趋化因子受体CCR5或CXCR4实现细胞入侵,最终导致免疫系统衰竭。领域发展关键节点包括:1996年发现CCR5基因32碱基对缺失(CCR5Δ32)的纯合子个体天然抵抗HIV-1感染;2007年“柏林病人”通过移植CCR5Δ32供体的造血干细胞实现HIV-1治愈,开创了基因治疗HIV的先河;2013年CRISPR-Cas9基因编辑技术问世,以其高效、简便的优势迅速成为HIV基因治疗的核心工具。当前研究热点聚焦于利用基因编辑技术敲除HIV共受体以阻断病毒入侵,但现有研究多针对单一共受体,而HIV-1在感染后期可能发生共受体切换(从CCR5嗜性转为CXCR4嗜性),单一共受体编辑可能导致病毒逃逸,同时缺乏多种sgRNA组合的有效性与系统性安全性评估,这是领域未解决的核心问题。
针对上述研究空白,本研究设计两种靶向CXCR4和CCR5的sgRNA组合,构建可同时表达两种sgRNA及Cas9的慢病毒载体,在多种细胞系及原代CD4+T细胞中实现双共受体同时编辑,系统评估其抗HIV-1感染的效果、编辑特异性及细胞毒性,为HIV-1的功能性治愈提供更全面、可靠的实验依据。
2. 文献综述解析
作者按基因编辑技术发展时间线(锌指核酸酶→转录激活因子样效应物核酸酶→CRISPR-Cas9)及共受体靶向策略(单一共受体→双共受体)的维度,对HIV基因治疗领域的现有研究进行分类评述,明确现有研究的优势、局限及本研究的创新定位。
早期研究主要利用锌指核酸酶(Zinc Finger Nucleases, ZFN)敲除CCR5,例如Perez等通过ZFN实现原代CD4+T细胞中50%的CCR5稳定敲除,编辑细胞在体内外均表现出显著的HIV-1抗性,但ZFN存在设计复杂、成本高昂、编辑效率有限的局限;转录激活因子样效应物核酸酶(Transcription Activator-Like Effector Nucleases, TALEN)虽也能实现CCR5编辑,但同样面临技术门槛高的问题。CRISPR-Cas9技术问世后,多个研究团队利用其高效敲除CCR5或CXCR4,例如Wang等构建的慢病毒CRISPR系统实现了原代CD4+T细胞中高效的CCR5敲除,且未检测到明显脱靶效应;作者团队此前也报道了CRISPR-Cas9敲除CXCR4可保护CD4+T细胞免受HIV-1感染,但这些研究均聚焦于单一共受体编辑。同时,临床研究发现单一CCR5编辑存在病毒逃逸风险,如“埃森病人”接受CCR5Δ32干细胞移植后,HIV-1突变为CXCR4嗜性毒株导致治疗失败;仅有的一项双共受体CRISPR编辑研究仅测试了一种sgRNA组合,缺乏多组合的有效性与安全性对比验证。
本研究的核心创新点在于设计两种不同的CXCR4与CCR5 sgRNA组合,构建单载体CRISPR-Cas9系统,首次系统对比了双共受体编辑在多种细胞模型中的效果,证明双编辑细胞对单一嗜性及双嗜性HIV-1的抗性均显著优于单一编辑细胞,同时全面评估了系统的脱靶效应与细胞毒性,填补了双共受体编辑多组合评估的研究空白,为临床转化提供了更充分的实验依据。
3. 研究思路总结与详细解析
本研究的整体目标是构建高效、安全的双靶向CRISPR-Cas9系统,同时敲除HIV共受体CCR5和CXCR4,验证其在细胞系及原代CD4+T细胞中的抗HIV-1效果,核心科学问题是双共受体同时编辑能否有效阻断不同嗜性HIV-1的感染且无明显副作用,技术路线遵循“载体构建→细胞系验证→原代细胞验证→安全性评估”的闭环逻辑。
3.1 双靶向CRISPR-Cas9载体构建
实验目的:构建可同时表达CXCR4和CCR5 sgRNA及Cas9的慢病毒载体,实现两种共受体的同步基因组编辑。
方法细节:基于作者团队前期筛选的2种高效CXCR4 sgRNA,将其与U6启动子扩增后,插入已含CCR5 sgRNA的lenti-sgR5-Cas9载体中,构建两种重组慢病毒载体lenti-X4R5-Cas9-#1和lenti-X4R5-Cas9-#2,载体携带嘌呤霉素筛选标记以富集编辑细胞。
结果解读:载体构建示意图(
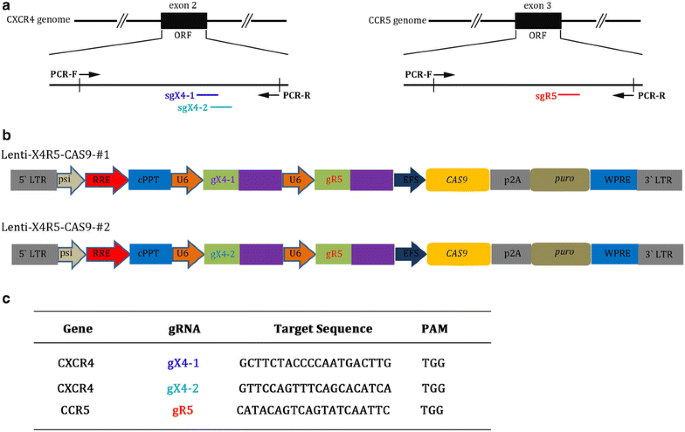
)清晰展示了sgRNA的靶向位点及载体结构,T7核酸内切酶I(T7E1)检测显示,在TZM-bl细胞中,lenti-X4R5-Cas9-#1对CXCR4和CCR5的插入/缺失(indel)突变率分别为20.35%和15.90%,lenti-X4R5-Cas9-#2的突变率分别为40.57%和32.95%(n=3,P<0.05),DNA测序进一步验证了编辑的特异性。
产品关联:文献未提及具体实验产品,领域常规使用慢病毒载体构建试剂盒、PCR扩增试剂、T7核酸内切酶等。
3.2 TZM-bl细胞系中编辑效率与抗HIV效果验证
实验目的:验证双靶向CRISPR系统在上皮来源CD4+细胞系中的编辑效率及对不同嗜性HIV-1的抗性。
方法细节:将两种lenti-X4R5-Cas9载体通过脂质体转染TZM-bl细胞,转染后用1μg/ml嘌呤霉素处理24h以富集编辑细胞,采用T7E1检测基因组水平的indel率,流式细胞术检测细胞表面CXCR4和CCR5的表达水平;随后分别用CXCR4嗜性HIV-1NL4-3或CCR5嗜性HIV-1YU-2感染细胞,感染72h后通过荧光素酶报告实验检测病毒感染水平。
结果解读:T7E1实验结果显示两种载体均能有效编辑CXCR4和CCR5基因(
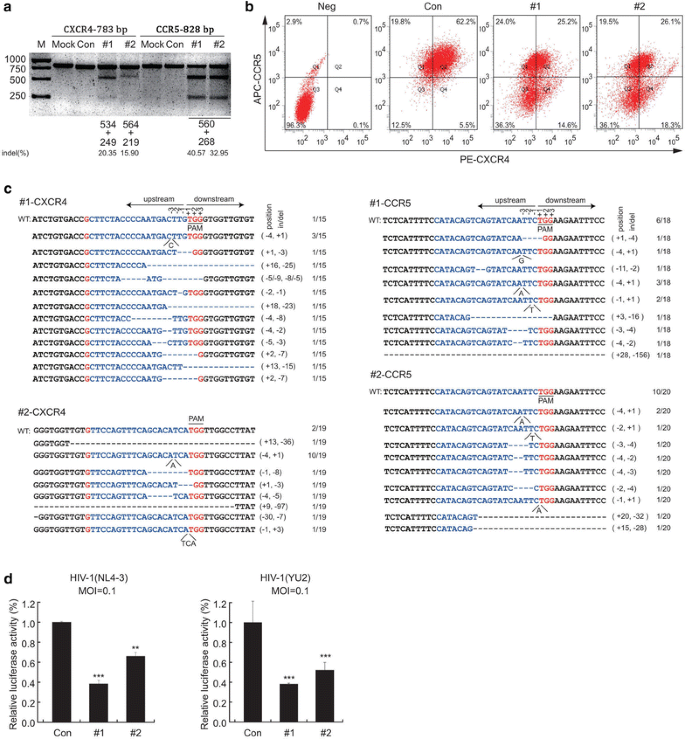
a);流式细胞术结果显示,编辑细胞表面CXCR4和CCR5的表达水平较对照组显著下调(

b);HIV-1感染实验显示,双编辑细胞对两种嗜性HIV-1的抗性均显著高于对照组,其中lenti-X4R5-Cas9-#2处理组的病毒抑制效果更显著(n=3,P<0.01)(

d)。
产品关联:实验所用关键产品:PEI转染试剂(Sigma)、嘌呤霉素(Sigma)、PE标记抗CXCR4抗体、APC标记抗CCR5抗体(Biolegend)、T7核酸内切酶I(NEB)。
3.3 Jurkat T细胞系中编辑效率、抗HIV效果及选择性优势分析
实验目的:验证双靶向CRISPR系统在T细胞系中的编辑效率、抗HIV效果,以及编辑细胞在HIV-1感染过程中的选择性优势。
方法细节:将包装好的X4R5-Cas9慢病毒以感染复数(Multiplicity of Infection, MOI)=40转染Jurkat T细胞,转染后用嘌呤霉素筛选富集编辑细胞;采用T7E1及DNA测序检测基因组编辑效率,流式细胞术检测细胞表面CXCR4表达(Jurkat细胞CCR5表达水平低,仅检测CXCR4),Western blot检测细胞内CXCR4和CCR5的总蛋白水平;分别用HIV-1NL4-3或YU-2感染细胞,在感染后1、3、5天检测细胞上清中HIV-1 p24抗原水平;同时将编辑细胞与未编辑细胞混合,用1:1的HIV-1NL4-3和YU-2混合毒株感染,培养18天,定期提取细胞基因组DNA检测indel率变化,评估编辑细胞的选择性优势。
结果解读:T7E1及DNA测序验证Jurkat细胞中CXCR4和CCR5基因均被有效编辑(
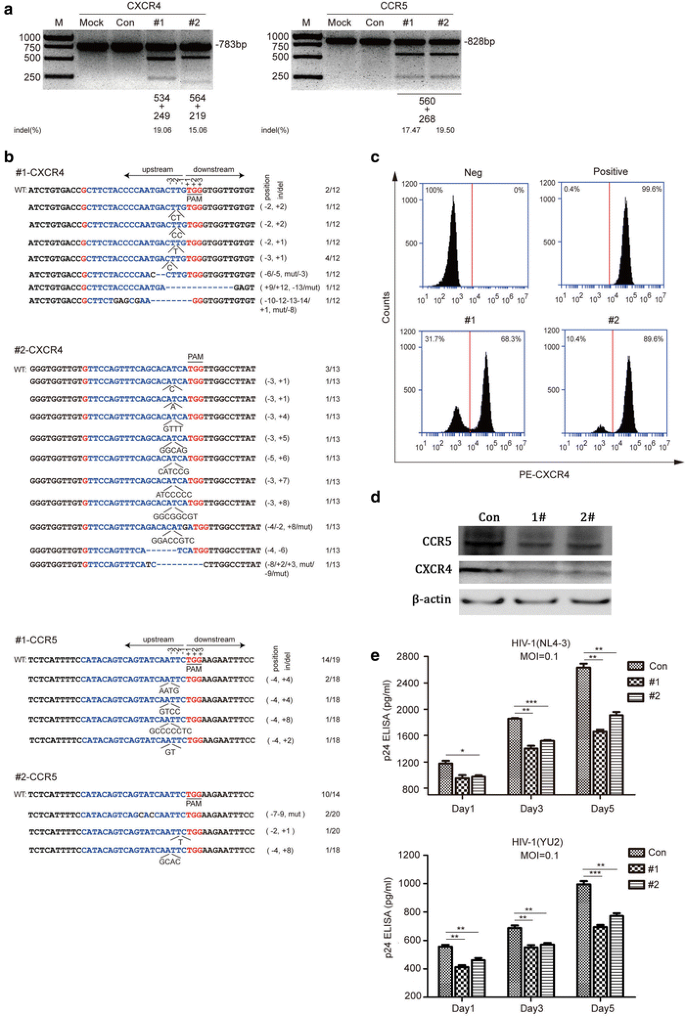
a、b);流式细胞术及Western blot结果显示,编辑细胞的CXCR4和CCR5表达水平显著下调(

c、d);p24抗原检测显示,编辑细胞的病毒复制水平显著低于对照组(

e);选择性优势实验显示,感染18天后,编辑细胞的indel率较感染前显著升高,说明编辑细胞在HIV-1感染过程中逐渐富集,具有明显的生存优势(
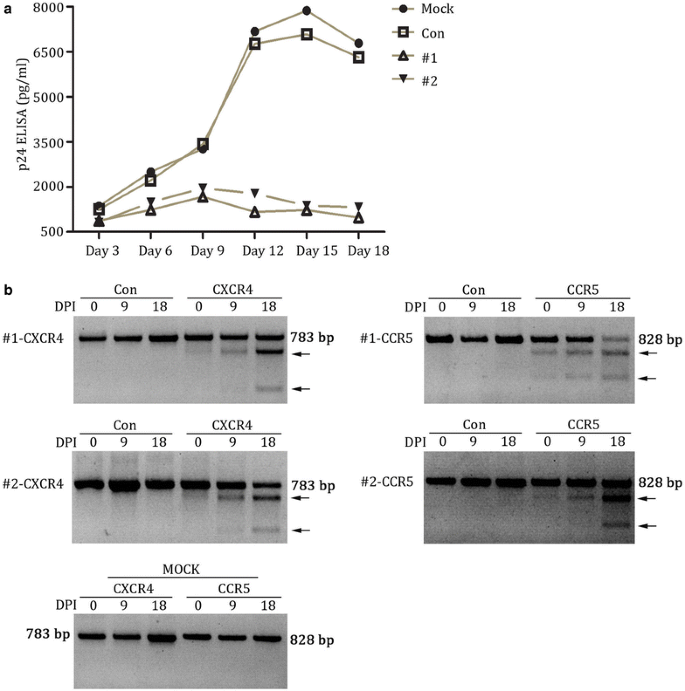
a、b)。
产品关联:文献未提及具体实验产品,领域常规使用慢病毒包装试剂盒、Western blot抗体、p24 ELISA试剂盒等。
3.4 原代CD4+T细胞中编辑效率与抗HIV效果验证
实验目的:验证双靶向CRISPR系统在原代CD4+T细胞中的编辑效率及对不同嗜性HIV-1的抗性,对比单一共受体编辑与双共受体编辑的效果差异。
方法细节:从健康供者的外周血单个核细胞(Peripheral Blood Mononuclear Cells, PBMC)中分离富集原代CD4+T细胞,通过电穿孔将lenti-X4R5-Cas9载体转染细胞;采用T7E1及深度测序检测基因组indel率;分别用HIV-1NL4-3、YU-2或两者混合毒株感染细胞,在感染后1、3、5、7天检测细胞上清中p24抗原水平,同时设置单一CCR5编辑组、单一CXCR4编辑组及未编辑对照组作为对比。
结果解读:T7E1及深度测序结果显示,原代CD4+T细胞中CXCR4和CCR5基因被有效编辑(
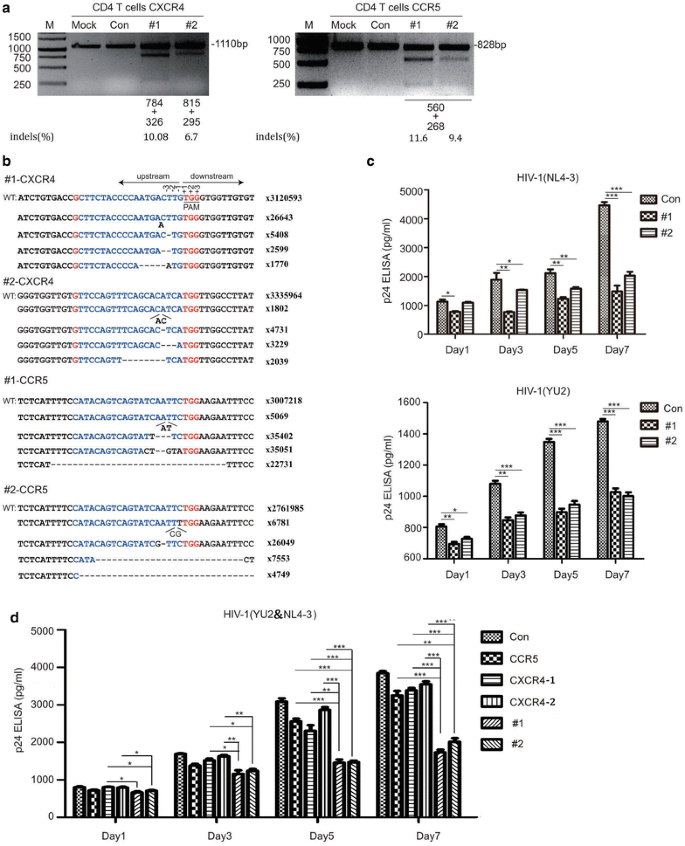
a、b);p24抗原检测显示,双共受体编辑细胞对单一嗜性及双嗜性HIV-1的抗性均显著高于对照组及单一共受体编辑组,其中双编辑组在感染第7天的p24水平较对照组降低约70%(n=3,P<0.001)(

c、d)。
产品关联:实验所用关键产品:人CD4+T细胞分离试剂盒(Miltenyi Biotech)、Lonza 4D-Nucleofector电转系统、p24 ELISA试剂盒。
3.5 脱靶效应与细胞毒性评估
实验目的:系统评估双靶向CRISPR系统的编辑特异性(脱靶效应)及对原代CD4+T细胞的毒性(凋亡水平)。
方法细节:利用在线工具(http://crispr.mit.edu)预测CXCR4和CCR5 sgRNA的潜在脱靶位点,从编辑后的原代CD4+T细胞中提取基因组DNA,通过PCR扩增潜在脱靶位点的片段,采用T7E1及DNA测序检测突变情况;同时在转染后1、3、5天,用Annexin V/7-氨基放线菌素D(7-Aminoactinomycin D, 7-AAD)染色编辑细胞,通过流式细胞术检测细胞早期凋亡率,评估细胞毒性。
结果解读:脱靶分析结果显示,所有预测的潜在脱靶位点均未检测到非特异性突变,证明该系统具有高度的编辑特异性(
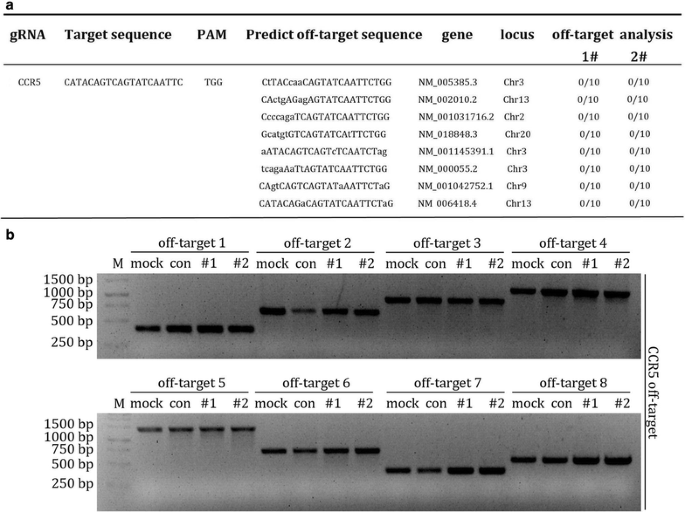
a、b);凋亡检测结果显示,编辑细胞的早期凋亡率与未编辑对照组无显著差异(n=3,P>0.05),说明双共受体编辑对原代CD4+T细胞无明显细胞毒性(
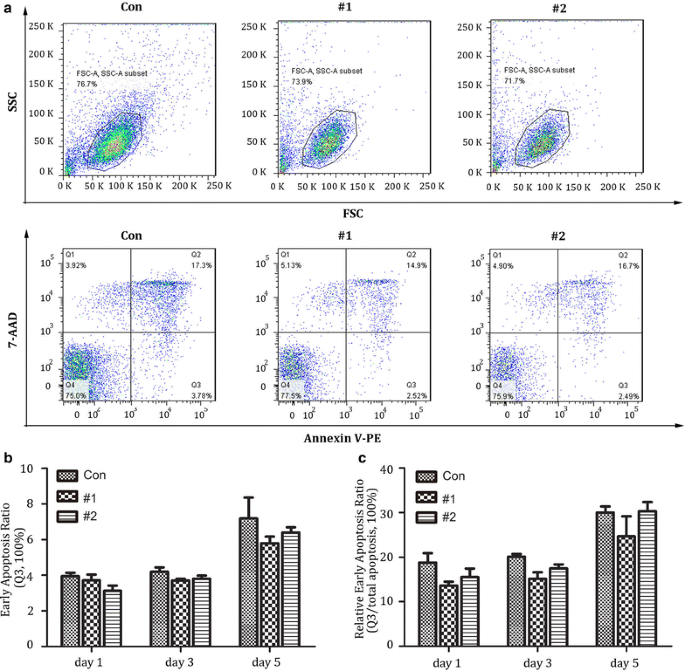
a、b、c)。
产品关联:实验所用关键产品:Annexin V凋亡检测试剂盒(BD Pharmingen)、流式细胞仪(BD Aria III)。
4. Biomarker研究及发现成果解析
本研究中的功能性生物标志物为CCR5和CXCR4基因的indel突变(基因组水平)及细胞表面蛋白表达下调(蛋白水平),其作为HIV-1感染抗性标志物的筛选与验证逻辑为:基于HIV-1入侵细胞的共受体依赖机制,设计sgRNA靶向CCR5和CXCR4编码区,通过CRISPR-Cas9诱导基因功能缺失突变,经细胞系及原代细胞的编辑效率验证、抗HIV效果验证、特异性及安全性验证,明确其作为抗HIV生物标志物的价值。
该Biomarker的基因组水平突变来源于CRISPR-Cas9诱导的CCR5和CXCR4基因indel,蛋白水平标志物为细胞表面CXCR4和CCR4表达下调;验证方法包括T7E1、深度测序检测基因组突变率,流式细胞术检测蛋白表达水平,HIV-1感染实验验证抗性功能;特异性数据显示,该系统的编辑特异性为100%(所有预测脱靶位点均无突变),敏感性方面,双编辑细胞对HIV-1的抑制率显著高于单一编辑组,其中对双嗜性HIV-1的抑制率在感染第7天可达约70%(n=3,P<0.001)。
该Biomarker的核心功能关联为:CCR5和CXCR4双基因编辑可使CD4+T细胞同时抵抗CCR5嗜性、CXCR4嗜性及双嗜性HIV-1的感染,且编辑细胞在HIV-1感染过程中具有选择性生存优势;创新性在于首次系统验证了两种不同sgRNA组合的双共受体编辑效果,证明双编辑的抗HIV效果显著优于单一编辑,同时全面证实了系统的高特异性与低细胞毒性;统计学结果显示,双编辑组的p24水平较对照组降低约70%(n=3,P<0.001),早期凋亡率与对照组无显著差异(P>0.05)。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。