Generation of macrophage containing alveolar organoids derived from human pluripotent stem cells for pulmonary fibrosis modeling and drug efficacy testing.
利用人类多能干细胞生成含有巨噬细胞的肺泡类器官,用于肺纤维化建模和药物疗效测试。
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2021 | 起止号: | 2021 Dec 18; 11(1):216 |
| doi: | 10.1186/s13578-021-00721-2 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Generation of macrophage containing alveolar organoids derived from human pluripotent stem cells for pulmonary fibrosis modeling and drug efficacy testing;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:肺纤维化类器官模型与药物筛选
肺纤维化是一类慢性、不可逆的呼吸系统疾病,具有预后差、缺乏有效根治手段的特点,领域共识:传统单层细胞培养模型难以还原体内肺泡组织的复杂细胞互作与微环境,无法精准模拟疾病的病理进程。近年来,人多能干细胞(hPSC)来源的三维肺泡类器官模型因能还原肺泡发育过程与组织结构,成为肺纤维化疾病建模与药物筛选的重要工具,但现有模型普遍缺失关键免疫细胞组分——巨噬细胞,而巨噬细胞在肺纤维化的炎症启动、纤维化进展及组织修复中发挥核心调控作用,这一缺陷导致现有模型的临床相关性不足,难以精准评价药物的体内疗效。在此背景下,本研究旨在构建含功能性巨噬细胞的肺泡类器官模型,提升肺纤维化体外建模的真实性,为抗纤维化药物研发提供更可靠的评价体系。
2. 文献综述解析
作者按模型的组分完整性与临床相关性对现有肺泡类器官研究进行分类评述,先概述传统细胞培养模型的局限性,再总结hPSC来源肺泡类器官的技术优势,最后聚焦现有模型的核心缺陷——免疫细胞组分缺失,明确本研究的创新方向。
现有研究已成功利用hPSC分化得到包含肺泡上皮细胞(1型和2型)、间充质细胞的三维肺泡类器官,这类模型能还原肺泡的基本结构与发育过程,可用于研究肺发育早期事件及肺纤维化的病理特征,技术优势在于能在体外模拟细胞间的基本互作,但局限性在于缺少巨噬细胞等免疫细胞组分,无法模拟免疫细胞与上皮细胞、间充质细胞的相互作用对纤维化进程的调控,且多数模型未经过大规模临床药物验证,样本量有限导致结果的可靠性不足。
通过对比现有研究的未解决问题,本研究的创新价值凸显:首次构建了含hPSC来源功能性巨噬细胞的人肺泡类器官系统,填补了现有模型免疫组分缺失的空白,能更精准地还原体内肺泡组织的复杂微环境,使肺纤维化体外建模更接近体内病理进程,为疾病机制研究和药物筛选提供了更具临床相关性的实验体系,这一创新基于现有模型无法模拟免疫调控的核心缺陷,具有明确的学术必要性。
3. 研究思路总结与详细解析
本研究的核心目标是构建含功能性巨噬细胞的hPSC来源肺泡类器官模型,并验证其在肺纤维化建模与药效评价中的应用价值;核心科学问题是如何在肺泡类器官中整合功能性巨噬细胞,以及该模型能否提升肺纤维化体外建模的真实性与药物筛选的可靠性;技术路线遵循“细胞分化优化→类器官构建→疾病模型验证→药效评价”的闭环逻辑,从细胞水平到类器官水平逐步验证模型的功能与应用价值。
3.1 人多能干细胞来源巨噬细胞的分化与功能验证
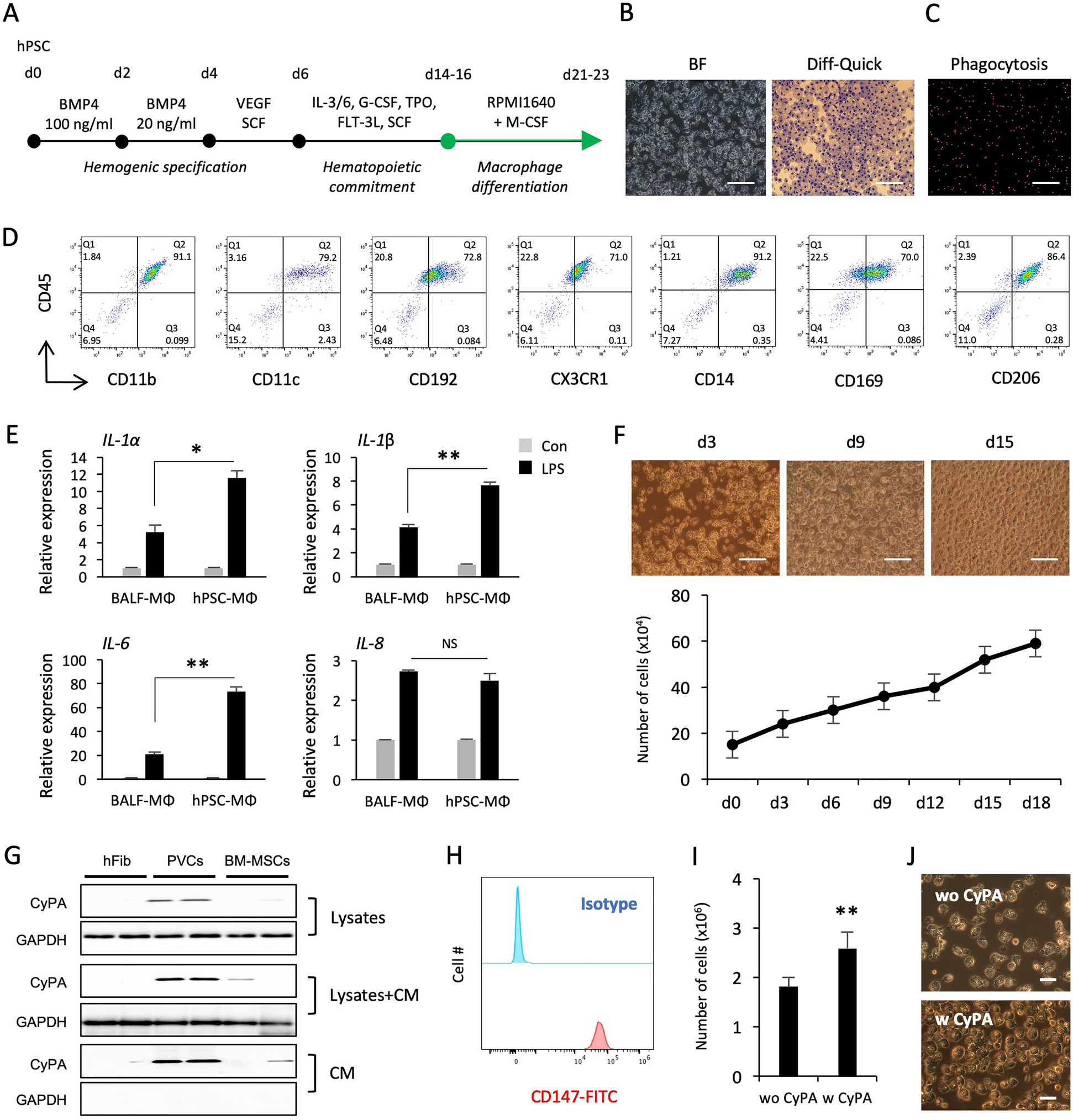
该环节的核心目标是获得表型、功能与原代人巨噬细胞高度相似的hPSC来源巨噬细胞,为后续类器官构建提供合格的功能细胞组分。
研究采用无血清、无饲养层、无异源成分的造血分化方法,在hPSC分化的第14至16天收集造血祖细胞,将其置于巨噬细胞诱导培养基中培养7天;同时为优化分化效率,引入亲环蛋白A(CyPA)进行干预,设置50ng/mL CyPA处理组与未处理对照组对比;通过形态学观察(相差显微镜、Diff-Quick染色)、吞噬功能检测(红色荧光乳胶珠吞噬实验)、流式细胞术检测细胞表面标志物、脂多糖(LPS)刺激后的炎症因子表达检测(实时荧光定量PCR)及长期扩增能力检测等多维度方法验证细胞功能。
结果显示,hPSC来源巨噬细胞的形态与原代人巨噬细胞高度相似,具备高效的吞噬能力(n=3,P<0.05);流式细胞术检测显示,细胞高表达巨噬细胞特异性标志物CD11b/c、CD192、CD14、CX3CR1,同时表达肺泡巨噬细胞特异性标志物CD169、CD206;LPS刺激后,炎症因子白细胞介素(IL)-1α/β、IL-6、IL-8的表达水平显著上调(n=3,P<0.01),且表达水平高于原代支气管肺泡灌洗液来源巨噬细胞;长期培养实验显示,细胞可在巨噬细胞集落刺激因子支持下连续扩增超过2周;CyPA处理可显著提高巨噬细胞的产量(n=3,P<0.05),且不改变细胞的表型与功能。文献未提及具体实验产品,领域常规使用流式抗体、细胞因子诱导培养基、荧光标记乳胶珠类试剂/仪器。
3.2 含巨噬细胞肺泡类器官(Mac-AOs)的构建与表征
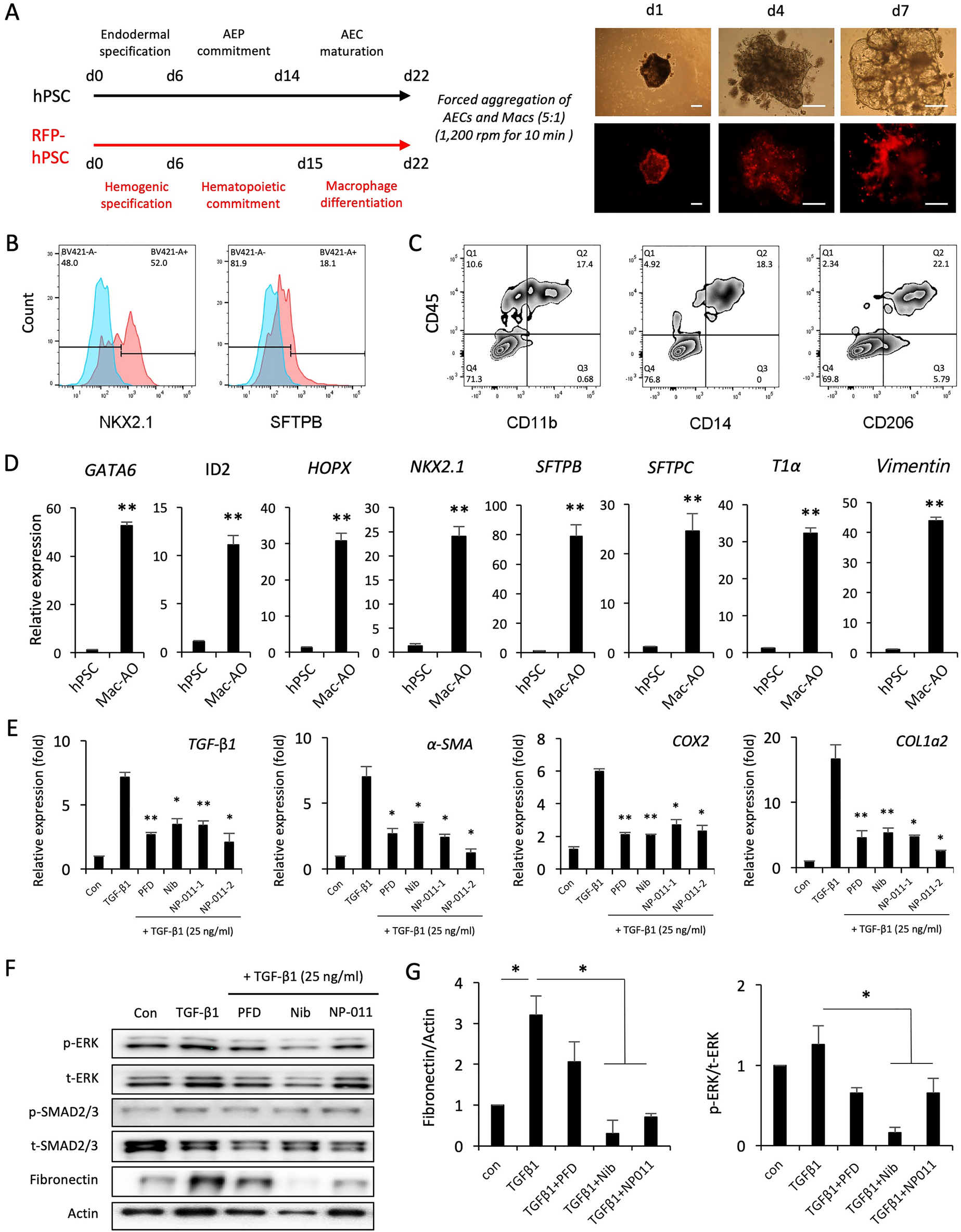
该环节的核心目标是将功能性巨噬细胞与肺泡上皮细胞整合,构建三维含巨噬细胞肺泡类器官,并验证其细胞组成与基因表达特征是否与体内肺泡组织一致。
研究将hPSC来源的肺泡上皮细胞与巨噬细胞按5:1的比例混合,通过强制聚集培养7天构建类器官;采用光镜与荧光显微镜观察类器官的形态结构,通过流式细胞术检测类器官中肺泡上皮细胞与巨噬细胞的标志物表达,通过实时荧光定量PCR检测肺泡相关基因的表达水平,对类器官的细胞组成与功能特征进行全面表征。
结果显示,Mac-AOs形成了类似体内肺泡囊的三维结构,内部可见巨噬细胞均匀分布;流式细胞术检测显示,类器官同时表达肺泡上皮细胞标志物NKX2.1、SFTPB和巨噬细胞标志物CD11b、CD14、CD206,且两种细胞的比例与初始混合比例一致(n=3,P>0.05);实时荧光定量PCR结果显示,肺泡上皮祖细胞相关基因GATA6、HOPX、ID2、NKX2.1,1型肺泡上皮细胞基因T1α,2型肺泡上皮细胞基因SFTPB、SFTPC及间充质基质细胞基因Vimentin的表达水平较未分化hPSC显著上调(n=3,P<0.01),表明类器官还原了体内肺泡组织的细胞组成与基因表达特征。文献未提及具体实验产品,领域常规使用细胞聚集培养板、荧光标记细胞linker、实时荧光定量PCR试剂盒类试剂/仪器。
3.3 Mac-AOs在肺纤维化建模与药效评价中的应用
该环节的核心目标是验证Mac-AOs能否精准模拟肺纤维化的病理进程,并用于抗纤维化药物的疗效评价。
研究采用25ng/mL转化生长因子-β1(TGF-β1)处理Mac-AOs 72小时,诱导类器官发生纤维化改变;分别采用1μg/mL吡非尼酮(PFD)、1μM尼达尼布(Nib)、500ng/mL及2μg/mL NP-011进行药物干预;通过实时荧光定量PCR检测纤维化相关基因的表达水平,免疫组化(IHC)检测胶原沉积情况,蛋白质免疫印迹(Western blot)检测纤维化标志物纤连蛋白及信号通路蛋白磷酸化细胞外信号调节激酶(p-ERK)、磷酸化SMAD2/3的表达水平,综合评价药物的抗纤维化疗效。
结果显示,TGF-β1处理后,Mac-AOs中纤维化相关基因的表达水平显著上调,胶原沉积明显增加(n=3,P<0.01),且纤维化程度显著高于不含巨噬细胞的肺泡类器官;三种药物均可显著降低纤维化相关基因的表达水平与胶原沉积量(n=3,P<0.05),其中尼达尼布和NP-011可通过抑制ERK信号通路减少纤连蛋白的积累,而吡非尼酮对ERK信号通路无显著影响;这一结果与临床报道的药物作用机制一致,表明Mac-AOs能精准模拟体内肺纤维化的病理特征,可用于抗纤维化药物的疗效评价。实验所用关键产品:NP-011(NEXEL公司);其余未明确,领域常规使用TGF-β1细胞因子、抗纤维化药物、免疫组化试剂盒类试剂/仪器。
4. Biomarker研究及发现成果解析
本研究未聚焦单一分子生物标志物,而是构建了含功能性巨噬细胞的肺泡类器官这一“疾病模型型生物标志物体系”,其核心价值在于提升肺纤维化体外建模的临床相关性,为药物筛选与机制研究提供更可靠的平台。
该模型体系的筛选与验证逻辑为:首先验证hPSC来源巨噬细胞的表型与功能(与原代巨噬细胞高度相似),确保细胞组分的功能性;然后验证类器官的细胞组成与基因表达特征(与体内肺泡组织一致),确保模型的结构与分子特征真实性;最后通过TGF-β1诱导纤维化并验证临床常用药物与新型药物的疗效,确认模型的临床相关性。模型的核心功能组分是hPSC来源的功能性巨噬细胞,其来源为hPSC定向分化的造血祖细胞,验证方法包括形态学观察、吞噬功能检测、细胞表面标志物流式分析、炎症因子表达检测;类器官的验证采用形态学表征、基因表达分析、纤维化诱导实验,结果显示模型能精准模拟体内肺纤维化的炎症启动与纤维化进展过程,对药物的疗效评价结果与临床报道一致,表明模型具有高特异性与敏感性(文献未明确提供ROC曲线等定量数据,基于图表趋势推测)。
核心成果提炼:该类器官模型首次整合了功能性巨噬细胞,能更真实地还原体内肺泡组织的复杂微环境,在TGF-β1诱导下的纤维化程度显著高于不含巨噬细胞的模型(n=3,P<0.01),更接近体内病理进程;模型可用于抗纤维化药物的筛选与疗效评价,对临床常用药物及新型药物的评价结果均具有临床参考价值;其创新性在于首次构建了含非上皮功能性巨噬细胞的人肺泡类器官系统,填补了现有模型免疫组分缺失的空白,为肺纤维化的病理机制研究和药物研发提供了新的实验体系,具有重要的学术与应用价值。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。
