Dysregulated bile acid receptor-mediated signaling and IL-17A induction are implicated in diet-associated hepatic health and cognitive function.
胆汁酸受体介导的信号传导失调和 IL-17A 诱导与饮食相关的肝脏健康和认知功能有关。
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2020 | 起止号: | 2020 Nov 6; 8(1):59 |
| doi: | 10.1186/s40364-020-00239-8 | 靶点: | IL-17、IL-17A |
| 研究方向: | 信号转导 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Dysregulated bile acid receptor-mediated signaling and IL-17A induction are implicated in diet-associated hepatic health and cognitive function;发表期刊:Biomarker Research;影响因子:未公开;研究领域:代谢综合征、肠道-肝轴、肠道-脑轴、神经可塑性。
非酒精性脂肪性肝病(NAFLD)是全球范围内代谢综合征的核心表现之一,其与认知功能下降的关联已被多项临床研究证实——NAFLD患者常存在精神运动速度减慢、学习能力受损等认知障碍(领域共识)。肠道微生态(肠道菌群及其代谢产物)作为“肠道-肝轴”“肠道-脑轴”的关键调控者,通过短链脂肪酸(SCFA)、胆汁酸等代谢产物影响肝脏代谢与脑功能:一方面,肠道菌群失调可诱导肝脏脂质沉积与炎症;另一方面,其代谢产物可通过血脑屏障调控小胶质细胞激活与神经可塑性(领域共识)。
当前研究存在三大空白:① 饮食诱导的NAFLD对神经可塑性的具体影响及机制尚不明确;② 胆汁酸受体(如法尼酯X受体FXR、Takeda G蛋白偶联受体5 TGR5)介导的信号通路在“饮食-肝-脑”交互中的作用未被系统解析;③ 益生元(如菊粉)对NAFLD与认知功能的联合干预效果及机制缺乏研究。本研究针对上述空白,以高糖、高脂、高胆固醇(FPC)饮食建立NAFLD模型,探讨菊粉干预对肝脏健康、认知功能的改善作用,并揭示胆汁酸信号与IL-17A炎症的介导机制,为代谢相关认知障碍的防治提供新靶点。
2. 文献综述解析
作者对领域现有研究的评述逻辑围绕“NAFLD-认知关联→肠道微生态调控→胆汁酸信号作用→菊粉干预现状”展开:
现有研究的核心结论与局限
- NAFLD与认知的关联:临床研究证实NAFLD患者认知功能下降,但饮食(如高糖高脂)诱导的NAFLD对神经可塑性的影响及机制未明;
- 肠道微生态的作用:肠道菌群失调(如Erysipelotrichaceae增加)可通过代谢产物诱导肝脏炎症,但菌群与脑功能的直接关联缺乏实验验证;
- 胆汁酸受体的功能:FXR与TGR5作为胆汁酸的核心受体,不仅调控肝脏脂质代谢,还参与脑小胶质细胞激活,但饮食对其系统信号的影响未被研究;
- 菊粉的干预现状:菊粉可通过发酵产生SCFA改善代谢综合征,但长期摄入对肝脏(如是否诱导胆汁淤积)与脑功能的联合影响存在争议。
本研究的创新价值
作者通过FPC饮食模型(模拟人类“快餐饮食”),首次系统探讨了菊粉对NAFLD与认知功能的同时干预效果,并揭示:① 饮食通过改变肠道菌群与胆汁酸信号,诱导IL-17A炎症,进而同时损伤肝脏与脑功能;② 菊粉通过调节肠道菌群(如增加Barnesiella、减少Allobaculum)、恢复胆汁酸受体信号(FXR/TGR5)、降低IL-17A水平,实现对肝脏与认知的双重保护。
3. 研究思路总结与详细解析
整体框架
研究目标:明确FPC饮食诱导的NAFLD对神经可塑性的影响及菊粉的干预机制;核心科学问题:饮食如何通过肠道菌群、胆汁酸信号、IL-17A介导“肝-脑”联合损伤;技术路线:动物模型构建→ 肝/脑病理与炎症检测→ 神经可塑性评估→ 肠道菌群测序→ 胆汁酸信号解析→ 代谢组学分析→ 多组学相关性验证。
3.1 动物实验设计
实验目的:建立饮食诱导的NAFLD模型,评估菊粉的干预效果。
方法细节:C57BL/6小鼠自断奶(3周龄)起分为三组:① 健康对照饮食(CD)组;② FPC饮食(高糖+高脂+高胆固醇)组;③ FPC+6%菊粉组(3月龄时开始补充菊粉)。8月龄时处死小鼠,收集肝、脑、盲肠样本。
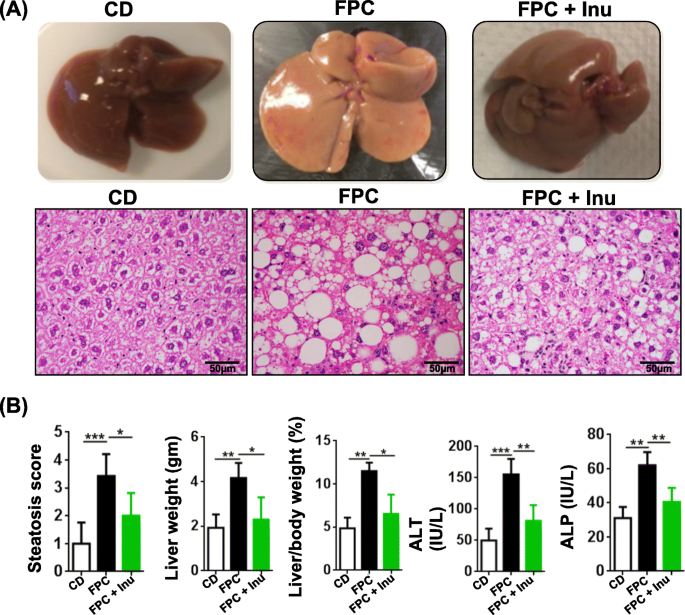
结果解读:FPC组小鼠出现显著肝脂肪变(H&E染色显示脂肪变等级3级,n=4,P<0.01)、血清ALT/ALP升高(ALT升高2.1倍,ALP升高1.8倍,n=4,P<0.05),并伴随认知障碍(开放场实验显示探索距离增加30%,n=13-16,P<0.05);菊粉组上述表型均显著改善。
3.2 肝脂肪变与炎症分析
实验目的:解析FPC饮食对肝脏代谢与炎症的影响及菊粉的干预机制。
方法细节:① 肝组织H&E染色评估脂肪变;② 血清ALT/ALP检测肝功能;③ qPCR检测脂代谢基因(Acc1、Scd1、Fasn)与炎症基因(Il6、Il1β);④ Western blot检测FASN、CD36、IL-17A、TNFα蛋白。
结果解读:FPC组脂代谢基因(Acc1 mRNA升高2.5倍,Fasn mRNA升高3倍,n=4,P<0.01)与炎症因子(IL-17A蛋白升高3倍,TNFα蛋白升高2.2倍,n=4,P<0.01)显著升高;菊粉组上述指标均降低(Acc1 mRNA降低40%,IL-17A蛋白降低50%,n=4,P<0.05)。
实验所用关键产品:脂肪酸合成酶(FASN)抗体(Cell Signaling Technology)、CD36抗体(Bioss Antibodies)、白细胞介素-17A(IL-17A)抗体(eBiosciences)、肿瘤坏死因子α(TNFα)抗体(Bioss Antibodies)。
3.3 神经可塑性与认知功能检测
实验目的:评估FPC饮食对神经可塑性的影响及菊粉的干预效果。
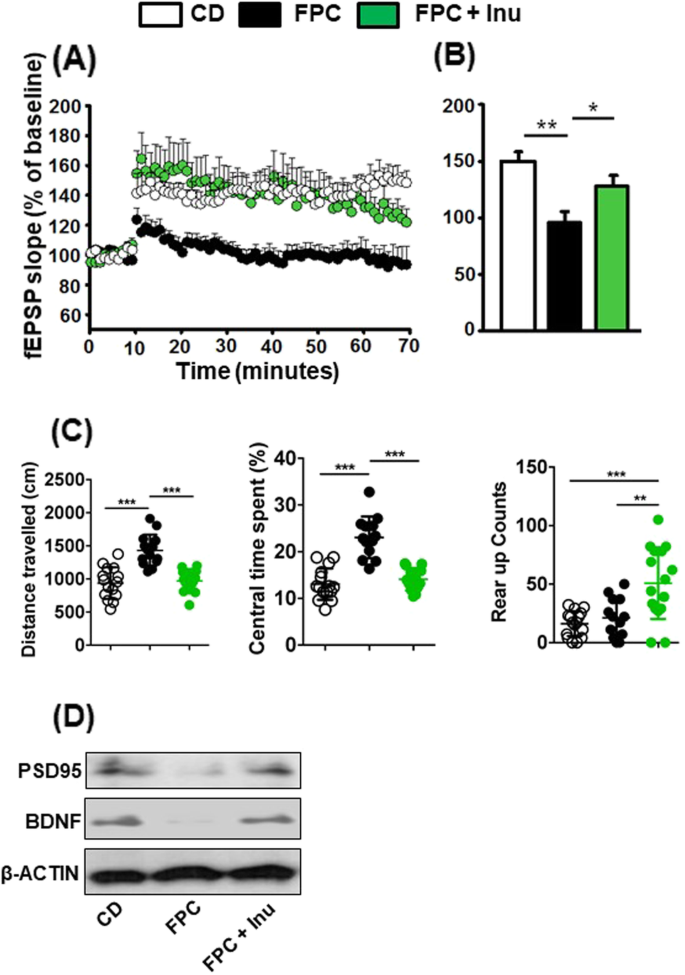
方法细节:① 海马脑片电生理记录长时程增强(LTP);② 开放场实验检测探索行为;③ Western blot检测突触后密度蛋白95(PSD-95)、脑源性神经营养因子(BDNF)蛋白。
结果解读:FPC组海马LTP振幅降低40%(n=3,P<0.05),PSD-95(降低50%,n=4,P<0.01)与BDNF(降低45%,n=4,P<0.01)蛋白水平显著下降;菊粉组LTP恢复至CD组水平,PSD-95与BDNF蛋白升高(分别增加60%、55%,n=4,P<0.05)。
实验所用关键产品:PSD-95抗体(Cell Signaling Technology)、BDNF抗体(Millipore Sigma)。
3.4 肠道菌群组成分析
实验目的:解析饮食与菊粉对肠道菌群的影响。
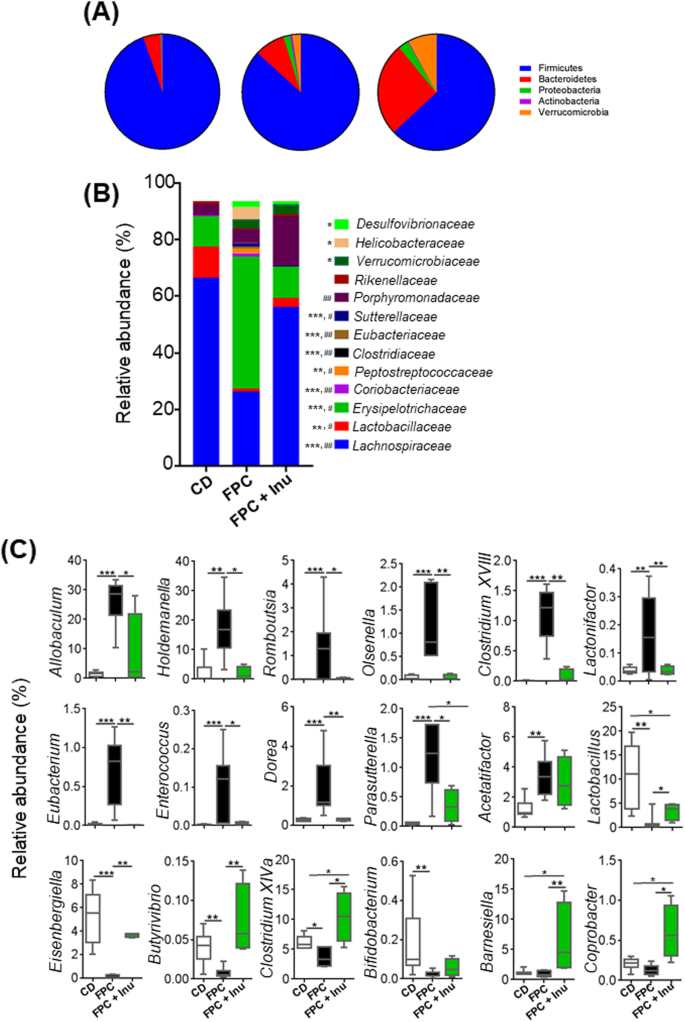
方法细节:盲肠样本提取DNA,16S rRNA测序(V4区)分析菌群组成。
结果解读:FPC组菌群多样性降低,Coriobacteriaceae(与胆固醇代谢相关)、Erysipelotrichaceae(与炎症相关)、Allobaculum(与肥胖相关)丰度显著增加(Allobaculum相对丰度增加3倍,n=7,P<0.01);菊粉组上述菌群丰度降低,同时增加Lachnospiraceae(产SCFA)、Barnesiella(免疫调节)丰度(Barnesiella增加2倍,n=4,P<0.05)。
3.5 胆汁酸受体信号解析
实验目的:探讨饮食与菊粉对胆汁酸信号的系统影响。
方法细节:① qPCR检测肝与小胶质细胞中FXR、TGR5及下游基因(Shp、Nos1、Dio2);② Western blot检测FXR、TGR5蛋白。
结果解读:FPC组肝组织FXR mRNA降低40%(n=4,P<0.05)、TGR5蛋白降低50%(n=4,P<0.01),小胶质细胞中Shp(FXR下游基因)mRNA降低35%(n=4,P<0.05);菊粉组恢复FXR/TGR5信号(FXR mRNA增加50%,TGR5蛋白增加60%,n=4,P<0.05)。
实验所用关键产品:FXR抗体(Santa Cruz Biotechnology)、TGR5抗体(Lifespan Biosciences)。
3.6 代谢组学分析
实验目的:解析饮食与菊粉对肠道代谢物的影响。
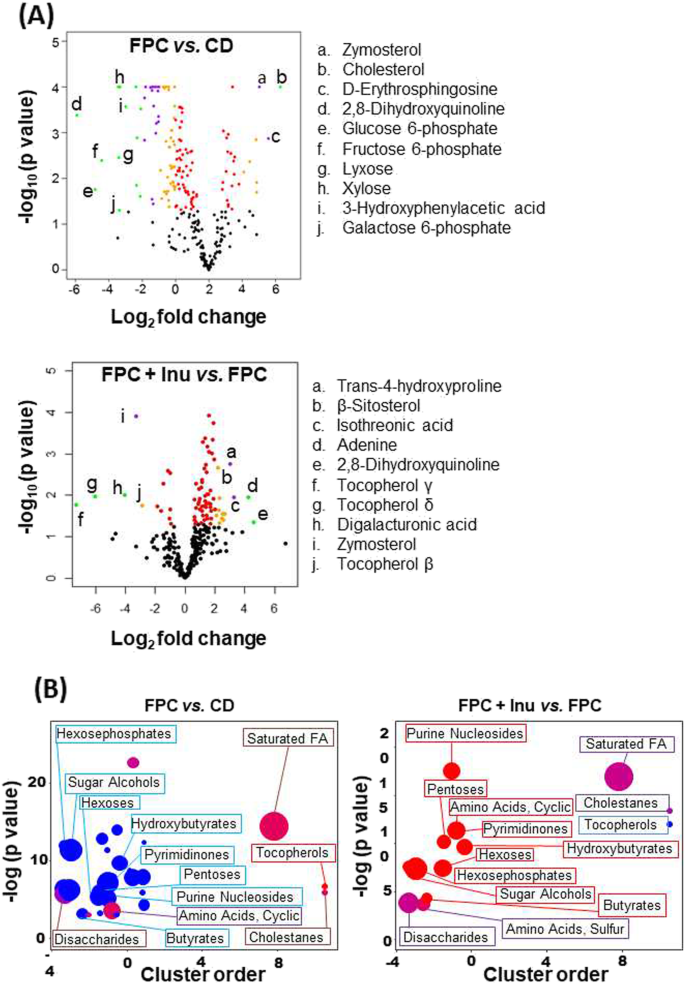
方法细节:盲肠样本通过气相色谱-飞行时间质谱(GC-TOF-MS)检测代谢物。
结果解读:共鉴定273种代谢物,FPC组与CD组相比,104种代谢物显著变化:① 胆固醇前体zymosterol升高3.2倍(n=7,P<0.001);② 具有改善葡萄糖耐受作用的2,8-二羟基喹啉降低60%(n=7,P<0.001);菊粉组反转上述变化(zymosterol降低50%,2,8-二羟基喹啉增加2.5倍,n=4,P<0.01)。
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
本研究识别的核心Biomarker涵盖炎症因子(IL-17A、RORγt)、胆汁酸受体(FXR、TGR5)、肠道菌群(Allobaculum、Barnesiella)、代谢物(zymosterol、2,8-二羟基喹啉)。筛选验证逻辑:① 炎症因子通过qPCR(mRNA)与Western blot(蛋白)在肝/脑组织中验证;② 胆汁酸受体通过qPCR与Western blot在肝/小胶质细胞中验证;③ 肠道菌群通过16S rRNA测序筛选,结合Spearman相关性验证;④ 代谢物通过GC-TOF-MS筛选,结合通路分析验证。
核心Biomarker的功能关联
IL-17A与RORγt:作为肝/脑炎症的核心Biomarker,FPC组肝组织IL-17A蛋白升高3倍(n=4,P<0.01)、RORγt(IL-17A转录因子)mRNA升高2.5倍(n=4,P<0.01),且与肝脂肪变等级(r=0.85,P<0.01)、认知障碍(r=0.78,P<0.05)正相关;菊粉组显著降低其水平,提示IL-17A是“肝-脑”联合损伤的关键介质。
FXR与TGR5:作为胆汁酸信号的核心Biomarker,FPC组FXR/TGR5水平降低,与肝脂代谢基因(Fasn,r=-0.82,P<0.01)、小胶质细胞炎症(Il1β,r=-0.75,P<0.05)负相关;菊粉组恢复其水平,证实胆汁酸受体信号是菊粉干预的关键靶点。
肠道菌群Biomarker:① Allobaculum:FPC组丰度增加3倍,与zymosterol(r=0.88,P<0.01)、IL-17A(r=0.79,P<0.05)正相关,提示其参与胆固醇代谢与炎症;② Barnesiella:菊粉组丰度增加2倍,与2,8-二羟基喹啉(r=0.81,P<0.01)、BDNF(r=0.76,P<0.05)正相关,提示其具有免疫调节与神经保护作用。
代谢物Biomarker:① zymosterol:与肝脂肪变(r=0.90,P<0.001)、认知障碍(r=0.83,P<0.01)正相关,是胆固醇代谢紊乱的标志;② 2,8-二羟基喹啉:与葡萄糖耐受(r=0.85,P<0.01)、神经可塑性(BDNF,r=0.78,P<0.05)正相关,是菊粉改善认知的关键代谢物。
创新性成果
本研究首次证实:① IL-17A是饮食诱导“肝-脑”联合损伤的共同介质;② FXR/TGR5作为胆汁酸受体,是连接“肠道菌群-肝-脑”的关键信号节点;③ zymosterol与2,8-二羟基喹啉可作为饮食相关认知障碍的潜在 Biomarker。这些发现为代谢综合征患者的饮食干预(如菊粉补充)提供了精准靶点,也为“肝-脑”联合疾病的机制研究提供了新视角。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。