Intracellular Ca(2+) is not essential for SHH signaling but is promoted by Shh ligand in embryonic fibroblasts.
| 期刊: | BMC Molecular and Cell Biology | 影响因子: | 2.700 |
| 时间: | 2026 | 起止号: | 2026 Jan 18; 27(1):7 |
| doi: | 10.1186/s12860-026-00567-x | ||
文献解析
1. 领域背景与文献
文献英文标题:Intracellular Ca²⁺ is not essential for SHH signaling but is promoted by Shh ligand in embryonic fibroblasts;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:细胞生物学,音猬因子信号通路调控。
领域共识,音猬因子(Sonic Hedgehog)信号通路是调控胚胎发育、细胞增殖与分化的核心信号轴之一,自20世纪90年代被首次克隆以来,其核心传导机制已被逐步阐明:音猬因子配体与细胞膜上的补丁受体(Patched)结合后,可解除补丁受体对平滑化蛋白(Smoothened)的抑制作用,进而激活下游胶质瘤相关癌基因同源物转录因子,调控下游靶基因表达,参与器官发生、组织稳态维持等多个生理过程,通路异常可导致神经管畸形、髓母细胞瘤、基底细胞癌等多种疾病。
当前领域研究热点包括音猬因子通路的表观遗传调控、与其他信号通路的交叉对话、小分子靶向药物开发等,但长期存在一个核心争议问题:钙离子信号与音猬因子通路的互作机制尚未明确,现有研究结论存在明显分歧,部分研究认为钙离子是音猬因子通路激活的必需元件,部分研究则认为音猬因子通路可调控细胞内钙离子振荡,但缺乏直接的细胞水平验证,且细胞内、外钙离子对音猬因子通路的差异化调控作用尚未被系统解析。本研究针对上述研究空白,通过精准操纵细胞内、外钙离子浓度,结合不同的音猬因子通路激活方式,明确二者的互作模式,为领域内的争议提供直接实验证据,完善音猬因子通路的调控网络。
2. 文献综述解析
作者以“钙离子与音猬因子通路的互作关系”为核心分类维度,对现有研究进行系统梳理,从双向调控的角度整合现有结论,明确现有研究的优势与局限性,凸显本研究的创新价值。
现有研究可分为四类核心结论:第一类支持音猬因子通路可调控细胞内钙离子浓度,包括2006年研究发现音猬因子可通过升高细胞内钙离子浓度激活胞外调节蛋白激酶通路,促进大鼠胃黏膜细胞增殖,2019年研究发现音猬因子可增强海马星形胶质细胞的钙离子振荡;第二类支持特定浓度的钙离子是音猬因子通路传导的必需元件,2007年研究发现钙/蛋白激酶C通路与表皮生长因子受体共同参与音猬因子诱导的小鼠胚胎干细胞增殖过程,2011年研究发现发育脊髓中的钙离子峰活性可解码音猬因子信号;第三类支持钙通道功能异常可破坏音猬因子通路基因的表达,2023年研究发现神经细胞初级纤毛上的瞬时受体电位通道C3介导的钙离子内流,对音猬因子通路依赖的神经发生至关重要,2018年研究发现电压门控钙通道介导的钙离子振荡可通过音猬因子依赖的缝隙连接网络调控羽毛间充质细胞运动;第四类支持细胞内钙离子振荡可调控音猬因子通路传导,多项研究在不同细胞模型中验证了二者的正相关关系。
现有研究的优势在于覆盖了发育组织、干细胞、肿瘤细胞等多种生理病理模型,为二者的互作提供了多维度的初步证据;局限性在于现有研究多同时耗竭细胞内、外钙离子,或通过敲低钙通道的方式间接验证,无法区分细胞内、外钙离子对音猬因子通路的独立调控作用,且未在不同音猬因子通路激活方式下进行一致性验证,导致研究结论存在明显争议。本研究的创新价值在于首次采用特异性螯合细胞内钙离子、梯度调控细胞外钙离子浓度的策略,同时结合三种不同的音猬因子通路激活方式(全长音猬因子配体、N端音猬因子片段、平滑化蛋白激动剂)进行平行验证,直接明确了细胞内、外钙离子对音猬因子通路的差异化调控作用,解决了领域内长期存在的争议,为音猬因子通路的调控机制研究提供了新的实验依据。
3. 研究思路总结与详细解析
本研究的核心目标是明确钙离子与音猬因子信号通路的双向互作机制,核心科学问题为“细胞内钙离子是否为音猬因子信号传导的必需元件、细胞外钙离子对音猬因子通路的调控作用及机制如何”,技术路线遵循“提出假设→梯度干预→多方法验证→机制解析”的闭环逻辑:首先假设细胞内、外钙离子对音猬因子通路的调控作用存在差异,随后通过特异性螯合剂耗竭细胞内钙离子、梯度添加外源性钙离子操纵胞外钙浓度,结合三种音猬因子通路激活方式,以胶质瘤相关癌基因同源物1蛋白水平为通路活性的核心读数验证调控作用,进一步通过钙成像、钙库操纵性钙内流实验解析钙离子流动的具体分子机制,最终明确二者的互作模式。
3.1 音猬因子通路激活与钙离子干预体系构建
实验目的是构建稳定的音猬因子通路激活模型及钙离子浓度操纵体系,明确不同钙环境下音猬因子通路的活性变化。方法细节:采用小鼠胚胎成纤维细胞NIH/3T3作为研究模型,通过三种方式激活音猬因子通路:一是使用HEK293T细胞制备的全长音猬因子配体条件培养基(配体具有N端棕榈酰化、C端胆固醇化双脂修饰),二是N端音猬因子片段条件培养基(仅具有N端棕榈酰化修饰),三是100 nmol/L平滑化蛋白激动剂;采用10~50 nmol/L钙离子特异性螯合剂处理细胞螯合细胞内钙离子,梯度添加0.3~10 mmol/L外源氯化钙调控细胞外钙离子浓度,处理24小时后通过免疫印迹检测胶质瘤相关癌基因同源物1蛋白水平作为通路活性的读数,同时采用ATP检测试剂盒评估细胞活性,排除钙离子干预的细胞毒性影响。
结果解读:免疫印迹结果显示,三种激活方式诱导的胶质瘤相关癌基因同源物1蛋白上调均不受10~50 nmol/L钙离子螯合剂处理的影响(n=3,P>0.05),而6 mmol/L细胞外钙离子可显著抑制三种激活方式诱导的胶质瘤相关癌基因同源物1上调(n=3,P<0.01),且细胞活性无显著变化(n=3,P>0.05),说明细胞内钙离子螯合不影响音猬因子通路传导,而高浓度细胞外钙离子可抑制通路活性。对应实验结果图1:
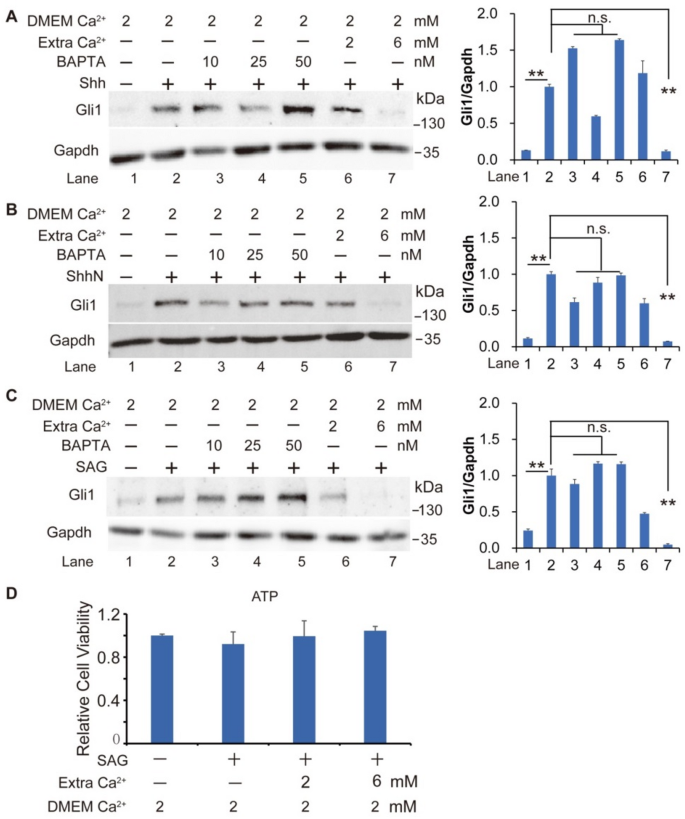
进一步的梯度浓度实验显示,全长音猬因子配体激活的通路对胞外钙离子更敏感,0.3 mmol/L胞外钙离子即可显著抑制胶质瘤相关癌基因同源物1表达,而平滑化蛋白激动剂激活的通路需3 mmol/L胞外钙离子才达到类似抑制效果(n=3,P<0.01),对应实验结果图2:
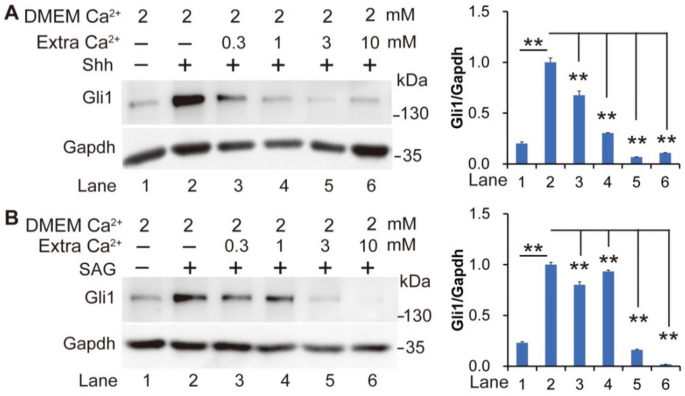
产品关联:实验所用关键产品:Cell Signaling Technology的胶质瘤相关癌基因同源物1抗体(货号#2643)、Servicebio的甘油醛-3-磷酸脱氢酶抗体(货号#AC22027016)、MCE的钙离子特异性螯合剂(货号#HY-100545)、Promega的CellTiter-Glo细胞活力检测试剂盒(货号#G7572)。
3.2 不同音猬因子激活方式下的细胞内钙离子水平检测
实验目的是明确音猬因子通路激活对细胞内钙离子水平的调控作用,区分全长音猬因子配体与平滑化蛋白激动剂的作用差异。方法细节:采用Fluo-8 AM钙探针对NIH/3T3细胞进行染色,分别在钙离子螯合剂处理耗竭胞内钙、不同浓度胞外钙的条件下,检测全长音猬因子配体或平滑化蛋白激动剂处理后的细胞内钙离子荧光强度;采用毒胡萝卜素处理耗尽内质网钙库,构建钙库操纵性钙内流实验模型,检测钙离子的重内流水平,每组实验重复5次以上。
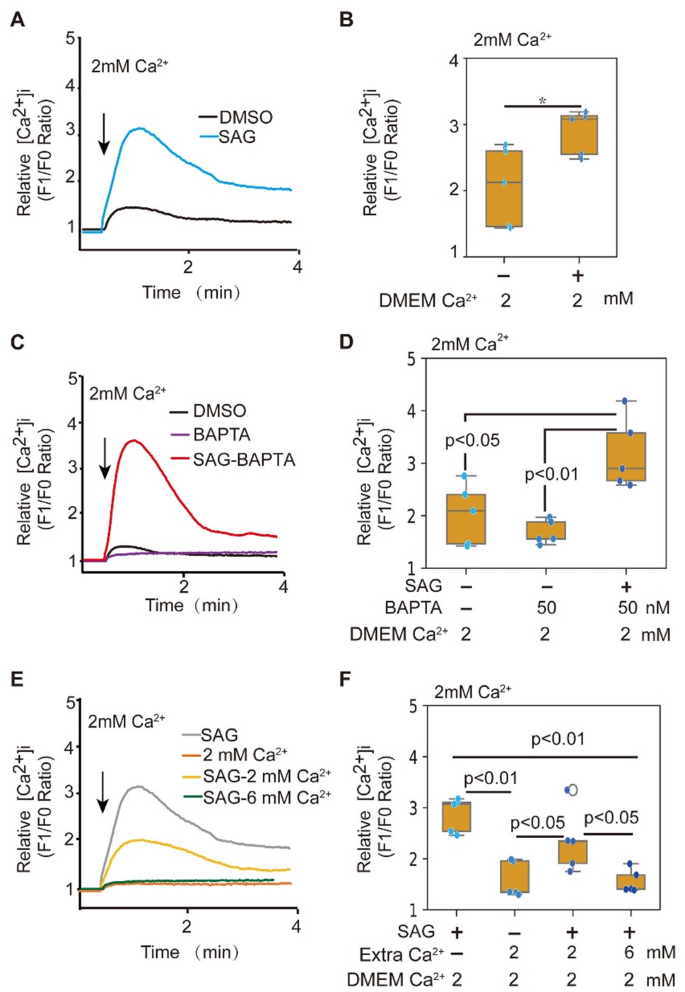
结果解读:在钙离子螯合剂存在的条件下,全长音猬因子配体仍可显著升高细胞内钙离子水平(n>5,P<0.05),而平滑化蛋白激动剂无此作用;在2 mmol/L胞外钙离子条件下,平滑化蛋白激动剂可显著升高胞内钙水平,而全长音猬因子配体需6 mmol/L胞外钙离子才达到类似效果(n>5,P<0.05),说明二者升高胞内钙离子的来源存在差异。对应实验结果图3:
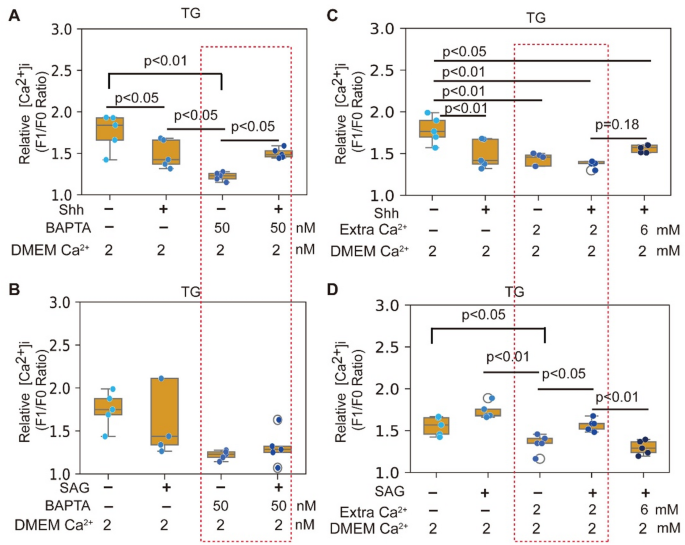
产品关联:实验所用关键产品:Abcam的Fluo-8 AM钙探针(货号#ab142773)、源叶生物的毒胡萝卜素(货号#B26241)。
3.3 钙库操纵性钙内流的调控机制解析
实验目的是明确音猬因子通路激活调控钙离子流动的具体分子机制。方法细节:在钙库操纵性钙内流模型中,先通过毒胡萝卜素处理耗尽内质网钙库,再添加2 mmol/L氯化钙诱导钙内流,分别检测全长音猬因子配体或平滑化蛋白激动剂处理、联合钙离子螯合剂或高浓度胞外钙条件下的钙内流水平,采用共聚焦显微镜实时记录钙离子荧光强度变化。
结果解读:正常生理钙浓度条件下,全长音猬因子配体处理不影响钙内流水平,但钙离子螯合剂耗竭胞内钙后,音猬因子诱导的钙内流水平升高约78%(n>5,P<0.05),2 mmol/L胞外钙离子条件下升高约40%,6 mmol/L胞外钙离子条件下钙内流被完全抑制;而平滑化蛋白激动剂处理可直接促进钙库操纵性钙内流介导的钙内流(n>5,P<0.05),该效应在钙离子螯合剂或2 mmol/L胞外钙离子条件下仍存在,6 mmol/L胞外钙离子条件下被抑制。对应实验结果图4:
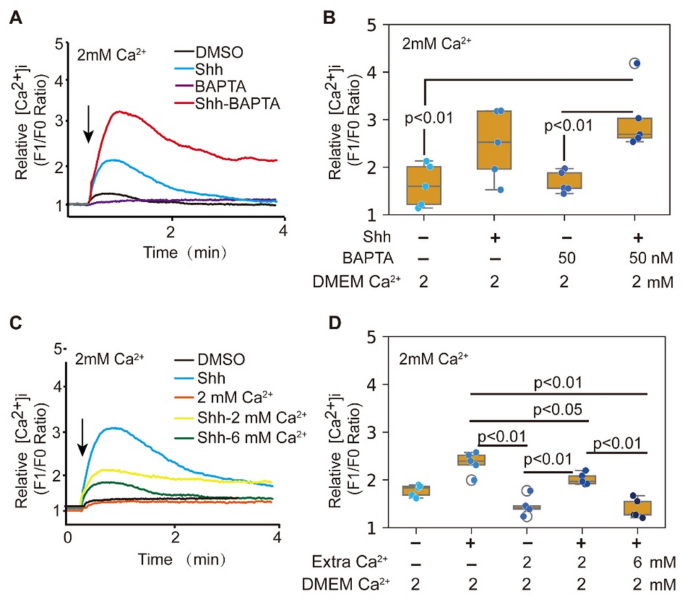
对应实验结果图5:
上述结果说明全长音猬因子配体主要通过促进胞内钙库释放钙离子升高胞浆钙水平,而平滑化蛋白激动剂主要通过促进胞外钙离子内流升高胞浆钙水平,二者均依赖钙库操纵性钙内流通路,且高浓度胞外钙离子可抑制该效应。
产品关联:文献未提及钙成像相关仪器信息,领域常规使用共聚焦激光扫描显微镜进行钙成像检测。
本研究存在一定局限性,仅采用钙离子螯合剂处理的方式耗竭胞内钙,无法将胞内钙降至极低水平,推测:若细胞内钙离子浓度被完全耗竭,可能会影响音猬因子信号通路的传导,需进一步通过基因编辑敲除钙通道、无钙培养基联合螯合剂处理等方式验证。
4. Biomarker 研究及发现成果
本研究未涉及临床疾病相关的诊断、预后生物标志物开发,主要以胶质瘤相关癌基因同源物1作为音猬因子信号通路活性的分子标志物,明确其在不同钙环境下的表达规律,同时初步探索了钙内流水平作为音猬因子通路激活功能性标志物的可行性。
Biomarker定位:胶质瘤相关癌基因同源物1是音猬因子通路下游的核心靶基因,属于通路活性的特异性标志物,其筛选验证逻辑为“基于领域共识选择标志物→免疫印迹定量检测验证特异性→不同干预条件下的一致性验证”。研究过程详述:胶质瘤相关癌基因同源物1的检测样本为NIH/3T3细胞总蛋白,验证方法为免疫印迹,以甘油醛-3-磷酸脱氢酶为内参进行灰度定量,在三种音猬因子激活方式下,胶质瘤相关癌基因同源物1的表达上调均具有统计学显著性(n=3,P<0.01),且在钙离子螯合剂处理组与对照组无显著差异(n=3,P>0.05),在6 mmol/L胞外钙组较对照组下调超过60%(n=3,P<0.01),具有良好的稳定性与特异性。
核心成果提炼:本研究明确了胶质瘤相关癌基因同源物1作为音猬因子通路活性标志物在钙干预研究中的稳定性,证实胞内钙离子螯合不影响其表达上调,而高浓度胞外钙可显著抑制其表达,为后续音猬因子通路与钙离子互作研究提供了稳定的读数指标;此外本研究发现全长音猬因子配体诱导的钙内流水平可作为音猬因子通路激活的功能性标志物,在胞内钙低水平条件下其升高幅度可达78%(n>5,P<0.05),具有较好的指示性。本研究未涉及临床样本验证,上述标志物的临床应用价值需进一步探索。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。
