Expression spectrum of TE-driven transcripts in human adult tissues
TE驱动转录本在人类成人组织中的表达谱
| 期刊: | Genome Biology | 影响因子: | 9.400 |
| 时间: | 2026 | 起止号: | 2026 Jan 27;27(1) |
| doi: | 10.1186/s13059-025-03898-8 | ||
文献解析
1. 领域背景与文献
文献英文标题:Transposable elements drive widespread transcription and enhance protein diversity in human adult tissues;发表期刊:BMC Genomics;影响因子:未公开;研究领域:基因组学与转录调控(转座子功能与人类转录组多样性)
转座子是真核生物基因组的重要组成部分,曾被视为“垃圾DNA”,但随着组学技术发展,其在基因组进化、染色质结构调控、基因表达调控中的关键作用逐渐被揭示。领域发展关键节点:早期研究发现转座子可通过插入突变影响基因功能,后续证实其作为增强子、CTCF结合位点参与染色质拓扑结构维持,在胚胎发育、干细胞、免疫细胞等场景中被重新激活,参与细胞稳态和适应性反应。当前研究热点包括转座子在早期发育中的调控机制、转座子与疾病的关联、转座子的进化贡献等。未解决的核心问题:现有研究多聚焦于早期发育或特定细胞类型,成年组织中转座子对转录组的调控作用尚未系统解析,转座子作为替代启动子对蛋白质异构体多样性的影响研究不足,人类特异性转座子的功能及进化意义有待深入阐明。
本研究针对上述空白,系统分析人类47种成年组织的17329个转录组样本,旨在揭示转座子在成年组织中作为启动子驱动转录的广泛作用,解析其在组织特异性、性别特异性调控中的机制及对蛋白质多样性的贡献,填补该领域研究空白。
2. 文献综述解析
作者对领域内现有研究按转座子的功能类型(增强子、CTCF结合位点、替代启动子)、研究场景(胚胎发育、干细胞、免疫细胞、疾病状态)、进化贡献(基因组结构重塑、新基因产生)三个维度分类评述,系统梳理转座子的已知功能,同时指出成年组织研究缺失等关键局限性。
现有研究的关键结论包括:转座子是基因组遗传变异的重要来源,可通过促进基因组重排、引入新型调控序列推动进化;作为增强子参与组织特异性基因调控,在小鼠基因组中短散在核元件(SINE)携带近30%的CTCF结合位点,维持染色质拓扑关联域的进化保守性;在应激、干细胞、免疫细胞中被重新激活,参与细胞稳态和适应性反应;作为替代启动子驱动基因转录,产生新的转录本和蛋白质异构体,如在人类胎盘发育中长末端重复序列(LTR)调控印记基因表达,在气道上皮细胞中Alu元件驱动IL33的特定异构体表达与慢性阻塞性肺疾病相关。现有研究的技术方法优势在于利用ChIP-seq、RNA-seq等组学技术结合生物信息学分析,高效解析转座子的调控功能;但存在局限性,多数研究集中在早期发育阶段或特定细胞类型,缺乏对成年组织中转座子驱动转录的系统分析,对转座子调控蛋白质多样性的机制研究不够深入,人类特异性转座子的功能研究较为零散。
通过对比现有研究的未解决问题,本研究的创新价值凸显:首次系统解析人类47种成年组织中转座子驱动的转录组特征,揭示其在管家基因功能维持和组织特异性调控中的双重作用;阐明性别差异表达的转座子驱动转录本的调控机制,明确性激素受体的关键调控作用;深入解析转座子驱动的替代转录起始对蛋白质异构体多样性的贡献,包括蛋白长度、结构和亚细胞定位的改变;鉴定人类特异性转座子驱动的转录本,并解析其在代谢和环境适应中的功能,为转座子在人类进化中的作用提供新证据。
3. 研究思路总结与详细解析
本研究的整体研究目标是揭示转座子在人类成年组织中作为启动子驱动转录的广泛功能,解析其对转录组多样性和蛋白质多样性的贡献;核心科学问题包括转座子在成年组织中如何调控基因转录、是否参与组织特异性和性别特异性调控、如何通过替代转录起始影响蛋白质异构体多样性;技术路线遵循“定义与鉴定→表达模式分析→调控机制解析→功能与进化意义阐释”的闭环逻辑,整合基因组注释、转录组数据、进化分析、分子实验验证等多维度研究方法。
3.1 转座子驱动转录本的鉴定与成年组织表达模式分析
实验目的:系统鉴定人类基因组中转座子驱动的转录本,并全面分析其在人类成年组织中的表达特征、组织分布和转座子亚家族偏好性。
方法细节:整合UCSC数据库的RepeatMasker转座子注释(hg38版本)和GENCODE v26的转录本注释,定义转录起始位点(TSS)位于转座子基因组坐标范围内的转录本为转座子驱动转录本(排除仅含转座子片段但不由转座子启动的转录本);利用GTEx V8数据集的17329个人类成年组织样本,过滤低表达转录本(在某组织中CPM≤1的样本占比≥50%的转录本),采用TMM方法归一化后计算RPKM值,分析转座子驱动转录本在不同组织、性别中的表达水平、数量分布,通过Log富集比(LER)分析转座子亚家族的富集情况。
结果解读:研究发现21%的人类基因包含转座子驱动的TSS,其中包括5330个蛋白编码基因和2673个非编码基因;男性和女性组织中分别有4743和4482个蛋白编码基因的转座子驱动转录本表达(RPKM>0.1,n=16651);平均每个组织表达约3000个蛋白编码和400个长链非编码RNA的转座子驱动转录本;多数转座子驱动转录本表达水平较低,约65%的蛋白编码、80%的长链非编码RNA转座子驱动转录本RPKM<1(n=16651),且男性组织中表达的长链非编码RNA转座子驱动转录本数量多于女性,其中睾丸组织的数量最多(856个);蛋白编码基因的转座子驱动TSS近半数来自短散在核元件,长链非编码RNA的则近半数来自长末端重复序列;MER52A、LFSINE、LTR12C等转座子亚家族显著富集于转座子驱动的TSS;同时鉴定到组织特异性的转座子驱动转录本,与对应组织的生物学功能显著关联,提示转座子在进化中被驯化作为替代启动子参与组织特异性调控。
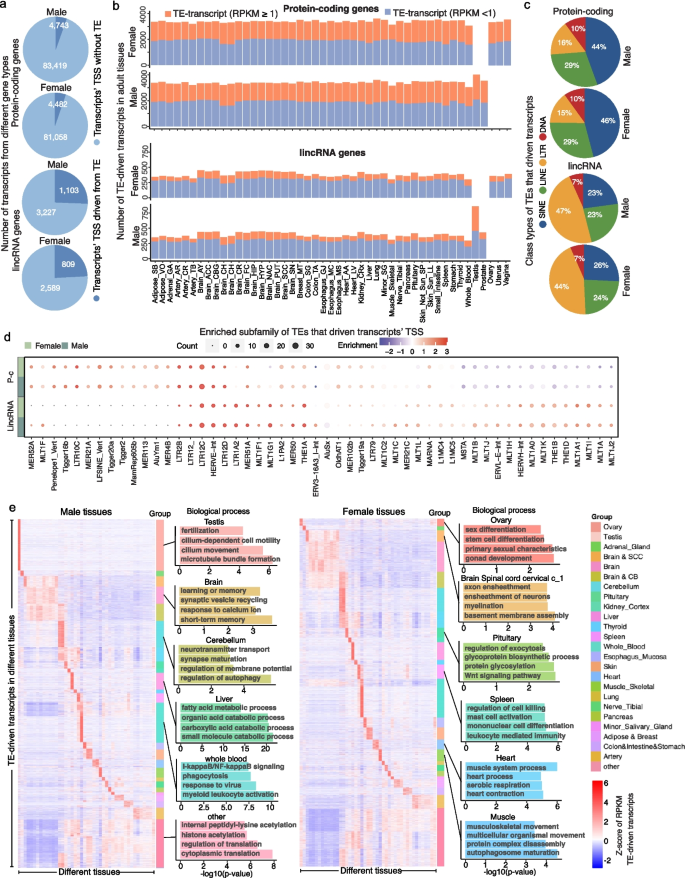
产品关联:文献未提及具体实验产品,领域常规使用的试剂/仪器包括RNA-seq建库试剂盒、基因组注释数据库(UCSC、GENCODE)、生物信息学分析工具(Bedtools、R语言的clusterProfiler包等)。
3.2 性别差异表达转座子驱动转录本的分析
实验目的:解析人类组织中转座子驱动转录本的性别差异表达模式,明确其调控机制及功能意义。
方法细节:对除性器官外的组织进行差异表达分析,采用Wilcox检验比较同一组织中女性与男性样本的转录本表达水平,通过p.adjust函数进行FDR校正,筛选显著差异表达的转座子驱动转录本(FDR<0.01,|log2(倍数变化)|>log2(1.5),在女性或男性组中平均RPKM≥0.1);利用ToppFun工具进行基因本体(GO)富集分析,采用FIMO方法分析转录因子结合基序,结合ENCODE数据库的ESR1 ChIP-seq数据和人类乳腺组织RNA-seq数据验证调控机制。
结果解读:多数组织中转座子驱动转录本的性别差异表达不显著,仅约9%的蛋白编码、11%的长链非编码RNA转座子驱动转录本存在显著性别差异(n=16651);乳腺组织中差异表达最为显著,共鉴定到312个蛋白编码、83个长链非编码RNA转座子驱动转录本,多数在女性组织中高表达,富集于乳腺发育相关的生物学过程(如血管生成、乳腺肿瘤通路,FDR<0.01);转座子亚家族分析显示,MIRb、L2b亚家族显著贡献于女性高表达的蛋白编码转录本,HERV15-int、LTR12C亚家族与长链非编码RNA的性别差异表达相关;近50%的女性高表达转座子驱动转录本的启动子区域含有ESR1结合基序,而男性高表达的则与AR结合基序相关,提示性激素受体直接调控性别差异表达的转座子驱动转录本。
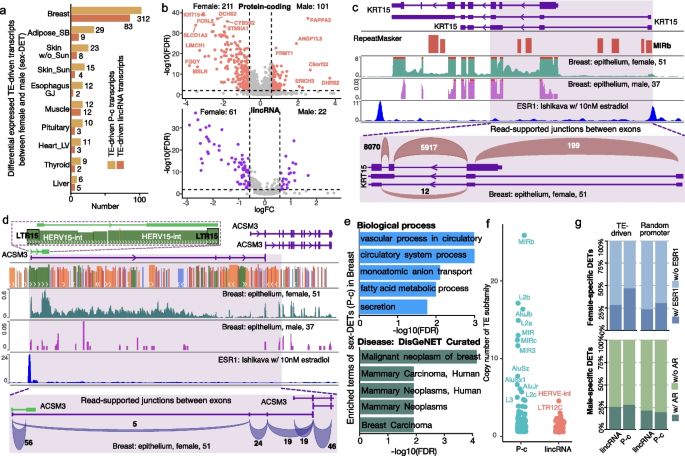
产品关联:文献未提及具体实验产品,领域常规使用的试剂/仪器包括ChIP-seq试剂盒、转录因子结合基序分析工具(FIMO)、基因组可视化工具(IGV、WashU Epigenome Browser)。
3.3 转座子驱动转录本对宿主基因表达的贡献分析
实验目的:评估转座子驱动转录本对宿主基因总表达的贡献程度,解析高贡献度基因的组织分布和功能特征。
方法细节:计算转座子驱动转录本在宿主基因总表达中的贡献度(贡献度=转座子驱动转录本的RPKM总和/宿主基因所有转录本的RPKM总和),筛选贡献度≥50%的基因,分析其在不同组织、性别的分布特征,通过GO富集分析解析其功能;结合AlphaFold数据库预测转座子驱动转录本编码蛋白与非转座子驱动转录本编码蛋白的结构差异。
结果解读:约30%的转座子驱动转录本在至少一种组织中贡献宿主基因表达的50%以上(女性1300个、男性1619个,n=16651);这些基因呈现两种分布模式,一类为广泛表达于所有组织的管家基因,富集于受体信号通路、脂质代谢、干扰素调控等核心生物学过程,另一类为组织特异性基因,如男性睾丸中富集大量特异性基因,女性肝脏中存在23个组织特异性基因,提示其参与性别特异性代谢过程;以NPIPA5基因为例,其长散在核元件驱动的转录本占该基因总表达的90%以上(n=16651),编码的蛋白含有新型21氨基酸的N端肽段,与非转座子驱动转录本的蛋白结构存在明显差异,表明转座子插入可重塑基因表达模式和蛋白结构。
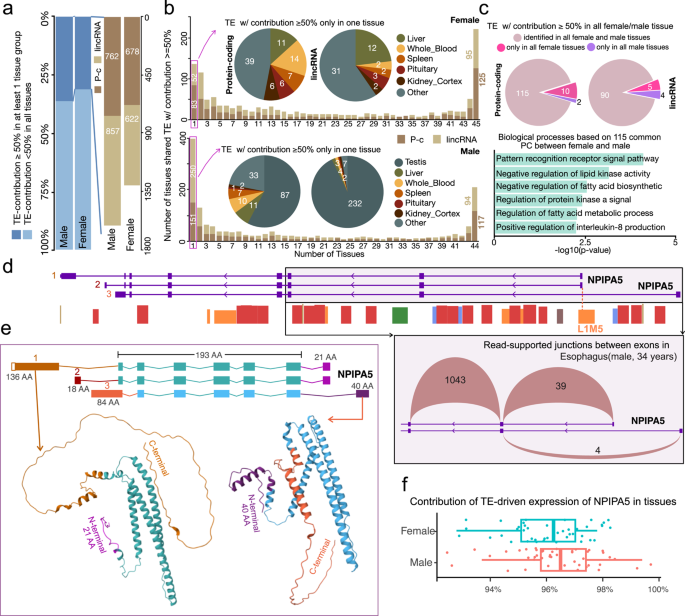
产品关联:文献未提及具体实验产品,领域常规使用的试剂/仪器包括蛋白结构预测工具(AlphaFold)、生物信息学分析软件(R语言)。
3.4 转座子驱动转录本对蛋白质异构体多样性的贡献分析
实验目的:系统解析转座子驱动的替代转录起始对蛋白质异构体多样性的影响,包括蛋白长度、结构、亚细胞定位及组织表达特征。
方法细节:根据GENCODE v26的注释将转座子驱动的蛋白编码转录本分为蛋白编码、保留内含子、加工转录本、无义介导降解四类,分析不同类别中转座子亚家族的分布;比较转座子驱动与非转座子驱动转录本编码的蛋白长度差异,结合UniProt数据库和AlphaFold分析蛋白结构与亚细胞定位差异;采用RT-qPCR方法在前列腺癌Du145、非小细胞肺癌H1299、三阴性乳腺癌MDA-MB231细胞系中验证转座子驱动转录本的表达。
结果解读:约40%的转座子驱动转录本编码蛋白产物,其余60%为非翻译转录本(n=16651);约66%的转座子驱动蛋白编码转录本(来自1009个基因)编码的蛋白长度与非转座子驱动转录本不同,其中379个基因的转座子驱动转录本贡献其总表达的50%以上(n=16651);这些基因呈现组织特异性和性别特异性分布,男性特异性基因数量多于女性,其中31个为睾丸特异性基因;以WNT2B基因为例,其MIR和Arthur1b驱动的转录本分别编码299氨基酸和372氨基酸的蛋白,亚细胞定位分别为细胞核、细胞核和线粒体,而非转座子驱动转录本编码391氨基酸的蛋白定位于内质网,且转座子驱动转录本在多数组织中占主导表达,在多种癌细胞系中MIR驱动的异构体为主要表达形式(n=3,P<0.05,文献未明确提供具体P值,基于图表趋势推测)。
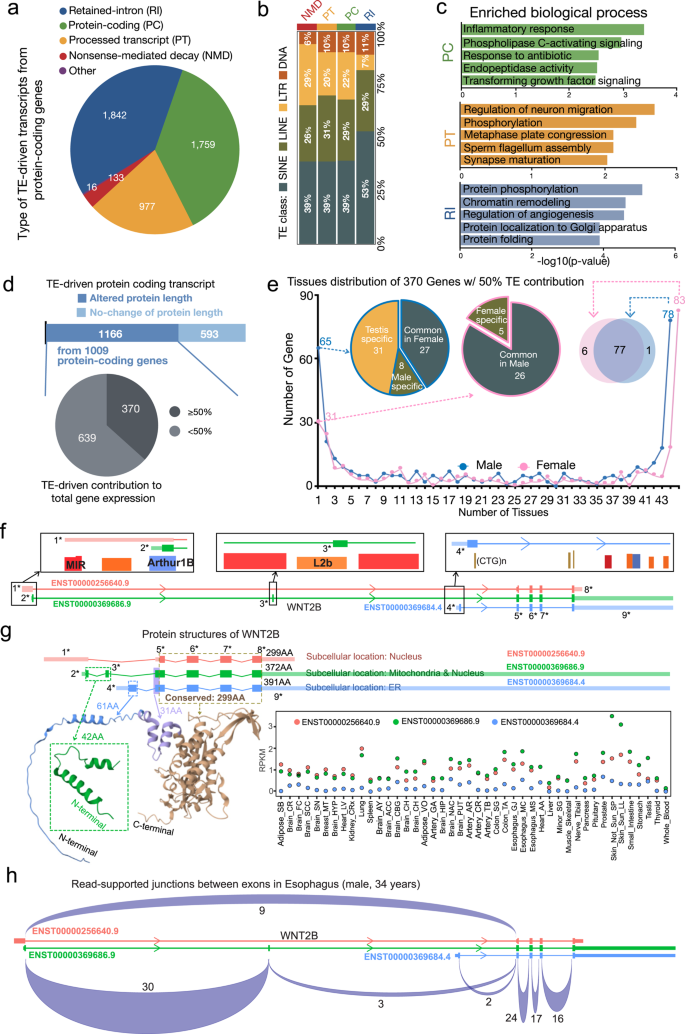
产品关联:实验所用关键产品:Monarch Total RNA Miniprep Kit(NEB #T2010)、iScript™ Reverse Transcription Supermix(BioRad)、PowerUp™ SYBR™ Green Master Mix(Thermo Fisher)。
3.5 转座子驱动转录本的进化保守性与人类特异性分析
实验目的:解析转座子驱动转录本的进化保守性,鉴定人类特异性转座子驱动的转录本并解析其功能意义。
方法细节:利用Dfam v3.8数据库获取转座子亚家族的分类信息,通过TimeTree 5数据库计算其进化插入时间;采用liftOver工具将人类转座子比对到黑猩猩、小鼠、鸡基因组,将转座子分为四物种共有、人与黑猩猩和小鼠共有、人与黑猩猩共有、人类特异性四个进化组;通过LER分析不同进化组中转座子亚家族的富集情况,采用clusterProfiler包进行GO富集分析解析不同进化组基因的功能。
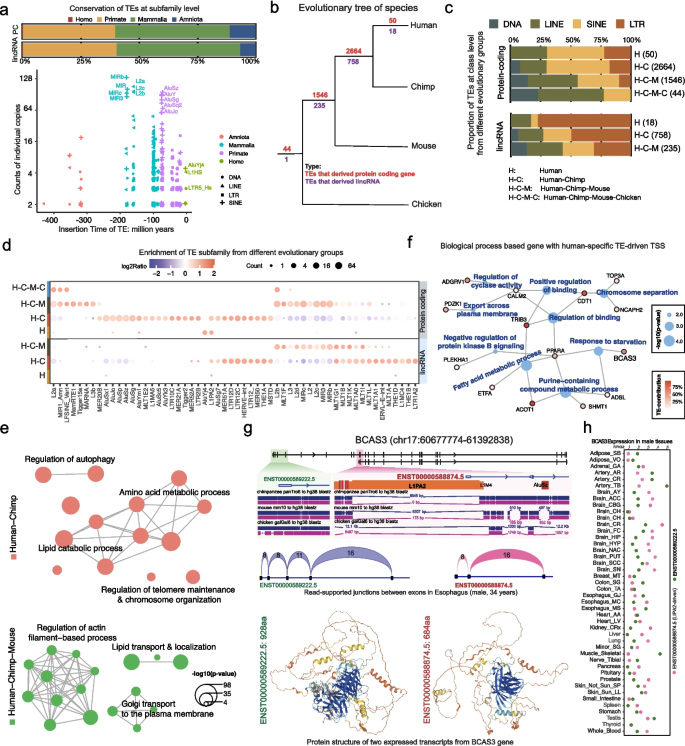
结果解读:多数转座子驱动转录本的转座子在哺乳动物或灵长类中保守,插入时间多在2亿年内;共鉴定到68个人类特异性转座子驱动的转录本,其中50个来自蛋白编码基因(主要为长散在核元件和短散在核元件),18个来自长链非编码RNA(主要为长末端重复序列);L1PA2作为人类特异性转座子亚家族,显著贡献于蛋白编码和长链非编码RNA的转录;人类特异性转座子驱动的基因富集于脂肪酸代谢、嘌呤代谢、染色体分离、饥饿应答等生物学过程(FDR<0.01),以BCAS3基因为例,其L1PA2驱动的转录本为人类特异性,编码截短型蛋白(缺失N端244氨基酸),在多数组织中占主导表达。
产品关联:文献未提及具体实验产品,领域常规使用的试剂/仪器包括基因组比对工具(liftOver)、进化分析数据库(Dfam、TimeTree)。
4. Biomarker研究及发现成果解析
本研究中涉及的Biomarker为调控性转录组分子,即转座子驱动的转录本,包括组织特异性转录本、性别差异表达转录本、人类特异性转录本三类,其筛选与验证遵循“基因组注释鉴定→转录组数据表达验证→功能与进化分析”的完整逻辑链条。
Biomarker定位:组织特异性转座子驱动转录本的筛选逻辑为基于GTEx转录组数据鉴定仅在单一组织中高表达的转座子驱动转录本,验证其与组织功能的关联;性别差异表达转录本的筛选逻辑为通过差异表达分析鉴定乳腺组织中女性与男性表达显著差异的转座子驱动转录本,结合ChIP-seq验证性激素受体的调控作用;人类特异性转座子驱动转录本的筛选逻辑为通过跨物种基因组比对鉴定仅在人类基因组中存在的转座子驱动转录本,分析其进化保守性与功能。
研究过程详述:这些Biomarker的来源为人类47种成年组织的转录组样本(GTEx数据集,n=16651),验证方法包括RNA-seq表达谱分析(RPKM定量)、差异表达分析(FDR<0.01,|log2(倍数变化)|>log2(1.5))、ChIP-seq验证转录因子结合位点、跨物种基因组比对验证进化保守性、RT-qPCR验证细胞系表达;组织特异性转座子驱动转录本的组织特异性显著,如睾丸中319个特异性转录本,女性肝脏中23个特异性转录本;性别差异表达转录本在乳腺组织中女性与男性的表达倍数变化>1.5(FDR<0.01,n=16651),近50%的女性高表达转录本的启动子区域含有ESR1结合基序;人类特异性转座子驱动转录本仅在人类基因组中存在,其驱动的基因富集于特定代谢和应激应答通路。
核心成果提炼:组织特异性转座子驱动转录本参与维持组织的独特生物学功能,如睾丸中的特异性转录本可能参与生殖细胞发育,女性肝脏中的参与性别特异性代谢过程;性别差异表达转录本受性激素受体调控,参与乳腺发育与相关疾病的潜在调控,为乳腺疾病的研究提供新的调控靶点;转座子驱动的转录本作为一类新型调控分子,显著增强了蛋白质异构体的多样性,通过改变蛋白长度、结构和亚细胞定位影响蛋白功能,如WNT2B的不同异构体具有不同的亚细胞定位,提示其可能参与不同的细胞信号通路;人类特异性转座子驱动的转录本参与脂肪酸代谢、饥饿应答等过程,为人类适应环境的进化机制提供了分子证据,其作为人类特有的转录调控元件,可能是人类物种特异性性状形成的重要基础。所有成果均基于实验数据,其中差异表达分析的统计学显著性为FDR<0.01,转座子贡献度分析中≥50%的基因占比约30%(n=16651)。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。