TRAIL (DR5) receptor and the modulation of TRAIL pathway in PLWHIV: key mechanisms in the progression of HIV disease
TRAIL (DR5) 受体及 TRAIL 通路在 HIV 感染者中的调控:HIV 疾病进展的关键机制
| 期刊: | BMC Molecular and Cell Biology | 影响因子: | |
| 时间: | 2025 | 起止号: | 2025 Jun 1;26(1):17 |
| doi: | 10.1186/s12860-025-00541-z | 靶点: | TRAIL |
| 研究方向: | 信号转导、炎症/感染、微生物学 | 疾病类型: | HIV |
文献解析
1. 领域背景与文献引入
文献英文标题:TRAIL (DR5) receptor and the modulation of TRAIL pathway in PLWHIV: key mechanisms in the progression of HIV disease;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:HIV感染与免疫细胞凋亡机制。
人类免疫缺陷病毒(HIV)感染的核心特征是CD4⁺T细胞进行性耗竭,最终导致获得性免疫缺陷综合征(AIDS)。领域共识:传统研究认为Fas死亡通路是介导HIV感染者CD4⁺T细胞凋亡的主要途径,通过旁观者效应导致未感染细胞的非特异性死亡,且该通路的激活与免疫激活状态密切相关。然而,肿瘤坏死因子相关凋亡诱导配体(TRAIL)通路在HIV感染中的作用研究相对匮乏,尤其是在未接受抗逆转录病毒治疗(ART)的早期感染者中,TRAIL通路受体的表达特征、与免疫激活标志物的关联及其在疾病进展中的调控机制尚未明确。针对这一研究空白,本研究聚焦未接受ART的HIV感染者(PLWHIV),系统分析Fas和TRAIL通路在CD3⁺CD4⁺T细胞及CD14⁺CD4⁺单核细胞中的激活状态,探讨其与免疫激活标志物、炎症细胞因子及HIV共受体的关联,为明确HIV疾病进展的关键机制提供新的实验依据。
2. 文献综述解析
作者对领域内现有研究的分类维度主要围绕死亡通路类型(Fas通路、TRAIL通路)、免疫激活状态、细胞亚群特征及疾病进展阶段展开。现有研究中,Fas通路的相关报道较为充分,多项研究证实HIV感染者的免疫细胞中Fas配体(FasL)及Fas受体表达上调,介导未感染CD4⁺T细胞的旁观者凋亡,且其表达水平与病毒载量、免疫激活程度正相关,但此类研究多聚焦于全T细胞群体,对CD14⁺CD4⁺单核细胞等亚群的分析不足,且样本量较小导致部分结论的统计学效力有限。TRAIL通路的研究则相对零散,部分体外实验及动物模型显示TRAIL受体在HIV感染的免疫细胞中表达升高,但其在临床样本中的表达特征、与疾病进展的关联及功能活性尚未得到系统验证,尤其是在未接受ART的早期感染者中,TRAIL通路与免疫激活标志物的调控关系仍不明确。
通过对比现有研究的局限性,本研究的创新价值凸显:首次在未接受ART的PLWHIV中同时分析Fas和TRAIL通路在CD3⁺CD4⁺T细胞及CD14⁺CD4⁺单核细胞中的表达差异,结合免疫激活标志物、炎症细胞因子及HIV共受体的检测,系统揭示TRAIL通路受体DR5与疾病进展的关联,明确其作为HIV疾病进展潜在生物标志物的学术价值,同时补充了TRAIL通路在单核细胞中非经典凋亡机制的实验证据。
3. 研究思路总结与详细解析
本研究的整体研究目标是分析HIV感染对Fas和TRAIL通路受体/配体表达、免疫激活标志物及炎症细胞因子的影响,明确其与HIV疾病进展的关联;核心科学问题为TRAIL通路在HIV早期感染中的激活机制及其与免疫激活状态的调控关系;技术路线遵循“临床样本招募→细胞与分子水平检测→统计分析关联→功能实验验证”的闭环逻辑,确保研究结论的严谨性与可靠性。
3.1 研究对象招募与样本采集
实验目的是获取基线特征匹配的研究样本,排除混杂因素对实验结果的干扰。方法细节为招募14名未接受ART的男性PLWHIV(纳入标准:年龄>18岁、CD4⁺T细胞计数>350细胞/µL、无其他病毒感染及自身免疫疾病),同时招募14名年龄、性别匹配的健康对照;采集外周血样本,分离外周血单个核细胞(PBMC)并冻存,分离血清用于细胞因子检测。结果解读显示两组研究对象的生化指标无显著差异,PLWHIV的病毒载量均值为25563拷贝/mL(n=14),CD4⁺T细胞计数中位数为470细胞/µL(n=14),确保样本的同质性与研究的可比性。实验所用关键产品:PBMC分离采用Axis-Shield的Lymphoprep,细胞培养试剂来自GIBCO™ Invitrogen,流式细胞术检测所用抗体来自BioLegend、BD、R&D Systems、Abcam等品牌。
3.2 Fas与TRAIL通路受体/配体表达检测
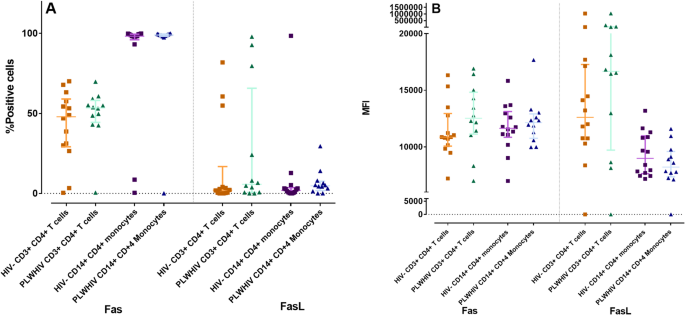
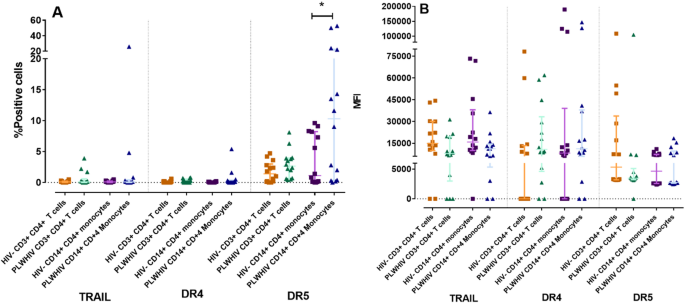
实验目的是分析两种死亡通路在目标免疫细胞中的表达差异,明确HIV感染对通路激活的影响。方法细节为采用流式细胞术检测CD3⁺CD4⁺T细胞及CD14⁺CD4⁺单核细胞中Fas、FasL、DR4、DR5、TRAIL的表达水平,通过平均荧光强度(MFI)及阳性细胞百分比量化表达差异。结果解读显示,PLWHIV的CD14⁺CD4⁺单核细胞中DR5的表达显著高于健康对照(n=14,P<0.05),CD3⁺CD4⁺T细胞中DR5表达呈升高趋势;Fas及FasL在两组细胞中的表达无显著统计学差异;TRAIL在两组细胞中的表达均极低,且PLWHIV中的MFI低于健康对照。
3.3 HIV共受体与免疫激活标志物检测
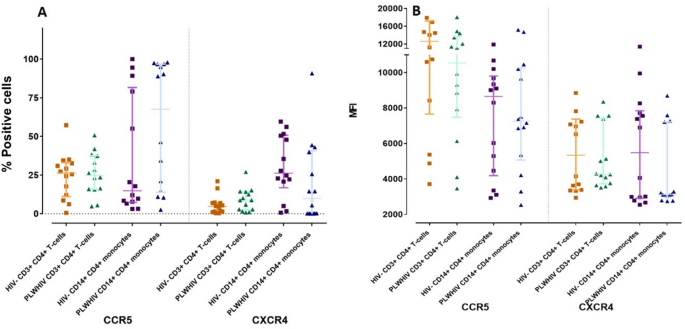
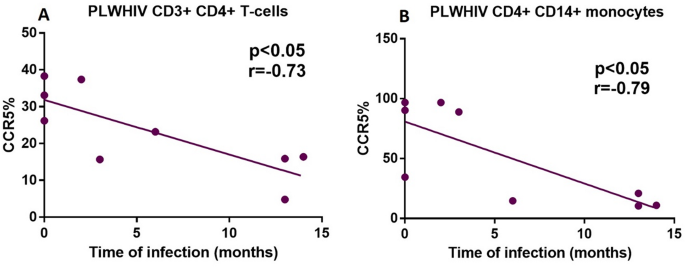
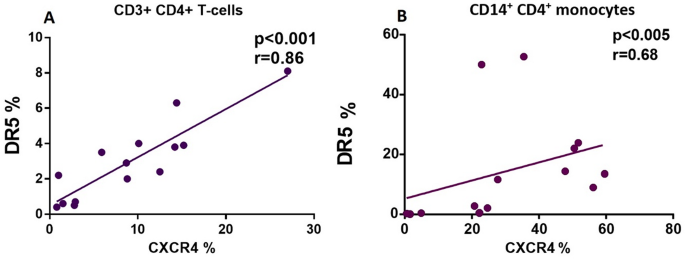
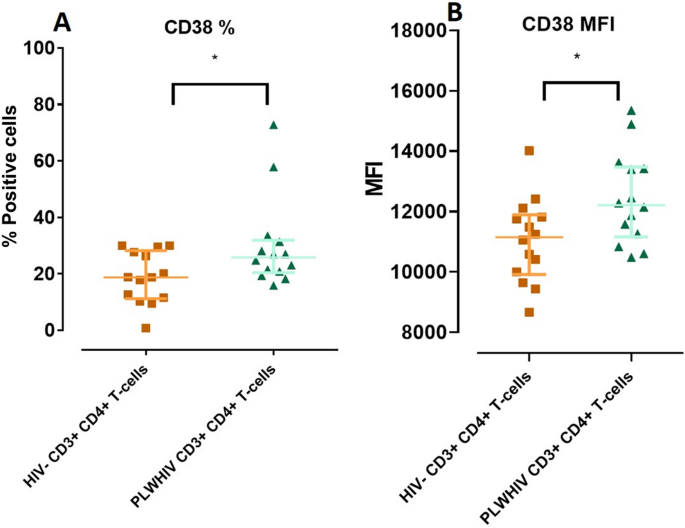
实验目的是分析HIV共受体CXCR4、CCR5与死亡通路的关联,明确免疫激活标志物在PLWHIV中的表达特征。方法细节为采用流式细胞术检测CD3⁺CD4⁺T细胞及CD14⁺CD4⁺单核细胞中CXCR4、CCR5的表达,同时检测免疫激活标志物CD25、CD69、CD38(T细胞)及CD80、CD86、HLA-DR(单核细胞)的表达。结果解读显示,PLWHIV的CD3⁺CD4⁺T细胞中CD38的表达显著升高(n=14,P<0.05);CXCR4与DR5的表达呈正相关(CD3⁺CD4⁺T细胞:r=0.86,n=14,P<0.001;CD14⁺CD4⁺单核细胞:r=0.68,n=14,P<0.005);CCR5的表达与感染时间呈负相关(CD3⁺CD4⁺T细胞:r=-0.73,n=14,P<0.05;CD14⁺CD4⁺单核细胞:r=-0.79,n=14,P<0.05)。
3.4 血清炎症细胞因子检测
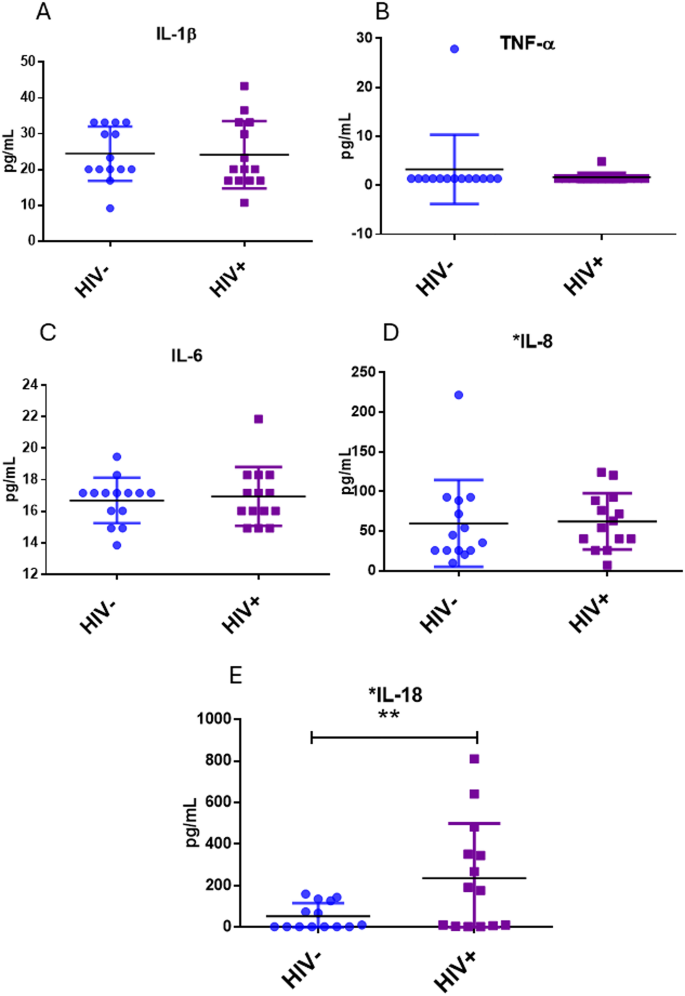
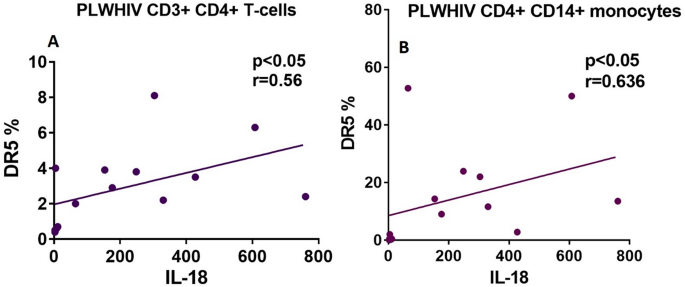
实验目的是分析PLWHIV的炎症状态,明确炎症细胞因子与死亡通路的关联。方法细节为采用BioLegend的LEGENDplex多重免疫分析试剂盒检测血清中IL-1β、IL-6、IL-8、TNF-α、IL-18的水平。结果解读显示,PLWHIV的血清IL-18水平显著高于健康对照(n=14,P<0.05),其余细胞因子水平无显著差异;IL-18水平与DR5的表达呈正相关(CD3⁺CD4⁺T细胞:r=0.56,n=14,P<0.05;CD14⁺CD4⁺单核细胞:r=0.636,n=14,P<0.05)。
3.5 凋亡诱导与抑制功能实验
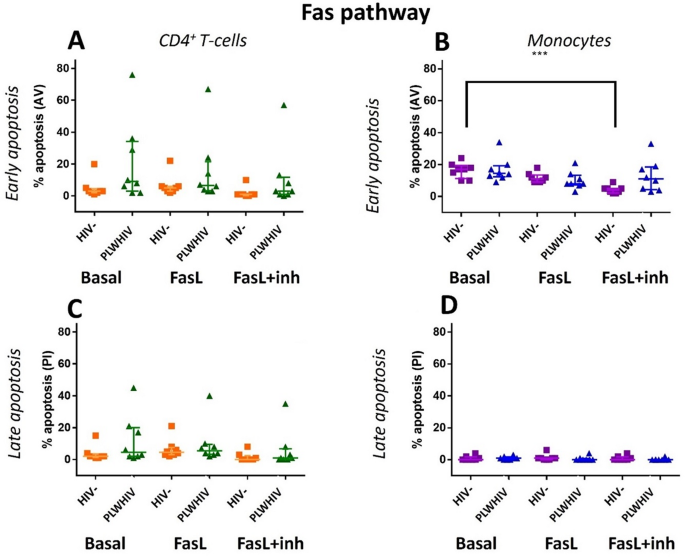
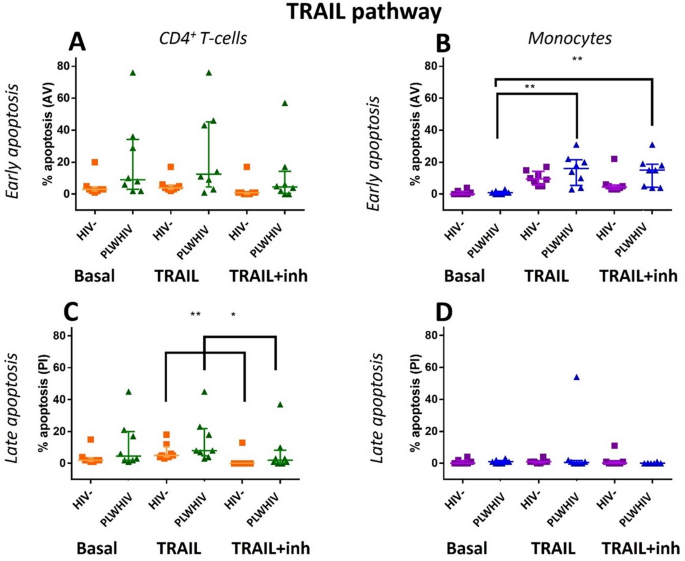
实验目的是验证Fas和TRAIL通路的功能活性,明确其介导细胞凋亡的机制。方法细节为用重组FasL和TRAIL处理PBMC,同时加入caspase8抑制剂,采用Annexin V/PI染色法检测细胞早期及晚期凋亡情况。结果解读显示,PLWHIV的CD14⁺CD4⁺单核细胞在TRAIL处理后早期凋亡显著增加(n=14,P<0.05),且该效应不受caspase8抑制剂的影响;Fas通路处理后,两组细胞的凋亡水平无显著差异。
4. Biomarker研究及发现成果
Biomarker定位与筛选逻辑
本研究聚焦的核心生物标志物为TRAIL通路受体DR5,其筛选与验证逻辑遵循“临床样本表达差异分析→关联疾病进展指标→功能实验验证”的完整链条:首先通过流式细胞术检测发现PLWHIV的CD14⁺CD4⁺单核细胞中DR5表达显著升高,随后分析其与感染时间、免疫激活标志物及炎症细胞因子的关联,明确其与疾病进展的正相关关系,最后通过凋亡功能实验验证其介导的非经典凋亡机制,全面验证其作为HIV疾病进展生物标志物的潜力。
研究过程详述
DR5的检测样本为PLWHIV的CD3⁺CD4⁺T细胞及CD14⁺CD4⁺单核细胞表面蛋白,采用流式细胞术进行定量检测。特异性方面,PLWHIV的CD14⁺CD4⁺单核细胞中DR5阳性细胞百分比及MFI均显著高于健康对照(n=14,P<0.05);敏感性方面,DR5的表达与感染时间呈正相关(CD14⁺CD4⁺单核细胞:r=0.88,n=14,P<0.005),与免疫激活标志物CD38、炎症细胞因子IL-18及HIV共受体CXCR4的表达均呈正相关,提示其可反映HIV感染的免疫激活状态与疾病进展程度。
核心成果提炼
本研究明确DR5可作为HIV早期感染的潜在疾病进展生物标志物,其表达与感染时间正相关(r=0.88,n=14,P<0.005),且与免疫激活、炎症反应及HIV共受体调控密切相关;首次发现TRAIL通路介导CD14⁺CD4⁺单核细胞的早期凋亡不依赖caspase8,提示存在非经典的细胞死亡机制(如坏死性凋亡);同时补充了未接受ART的PLWHIV中IL-18与DR5的调控关系,为HIV疾病进展的免疫机制研究提供新的实验依据。这些成果为后续开发以TRAIL通路为靶点的HIV治疗策略及疾病进展监测标志物奠定了基础。# 《TRAIL(DR5)受体及TRAIL通路在HIV感染者中的调控:HIV疾病进展的关键机制》-文献解析
1. 领域背景与文献引入
文献英文标题:TRAIL (DR5) receptor and the modulation of TRAIL pathway in PLWHIV: key mechanisms in the progression of HIV disease;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:HIV感染与免疫细胞凋亡机制。
人类免疫缺陷病毒(HIV)感染的核心特征是CD4⁺T细胞进行性耗竭,最终导致获得性免疫缺陷综合征(AIDS)。领域共识:传统研究认为Fas死亡通路是介导HIV感染者CD4⁺T细胞凋亡的主要途径,通过旁观者效应导致未感染细胞的非特异性死亡,且该通路的激活与免疫激活状态密切相关。然而,肿瘤坏死因子相关凋亡诱导配体(TRAIL)通路在HIV感染中的作用研究相对匮乏,尤其是在未接受抗逆转录病毒治疗(ART)的HIV感染者中,其与免疫激活、疾病进展的关联及功能机制尚未明确。针对这一研究空白,本研究聚焦未接受ART的HIV感染者(PLWHIV),系统分析Fas和TRAIL通路在CD3⁺CD4⁺T细胞及CD14⁺CD4⁺单核细胞中的激活状态,探讨其与免疫激活标志物、炎症细胞因子及HIV共受体的关联,为明确HIV疾病进展的关键机制提供新的实验依据。
2. 文献综述解析
作者对领域内现有研究的分类维度主要围绕死亡通路类型(Fas通路、TRAIL通路)、免疫激活状态、细胞亚群特征及疾病进展阶段展开。现有研究中,Fas通路的相关报道较为充分,多项研究证实HIV感染者的免疫细胞中Fas配体(FasL)及Fas受体表达上调,介导未感染CD4⁺T细胞的旁观者凋亡,且其表达水平与病毒载量、免疫激活程度正相关,但此类研究多聚焦于全T细胞群体,对CD14⁺CD4⁺单核细胞等亚群的分析不足,且样本量较小导致部分结论的统计学效力有限。TRAIL通路的研究则相对零散,部分体外实验及动物模型显示TRAIL受体在HIV感染的免疫细胞中表达升高,但其在临床样本中的表达特征、与疾病进展的关联及功能活性尚未得到系统验证,尤其是在未接受ART的早期感染者中,TRAIL通路与免疫激活标志物的调控关系仍不明确。
通过对比现有研究的局限性,本研究的创新价值凸显:首次在未接受ART的PLWHIV中同时分析Fas和TRAIL通路在CD3⁺CD4⁺T细胞及CD14⁺CD4⁺单核细胞中的表达差异,结合免疫激活标志物、炎症细胞因子及HIV共受体的检测,系统揭示TRAIL通路受体DR5与疾病进展的关联,明确其作为HIV疾病进展潜在生物标志物的学术价值,同时补充了TRAIL通路在单核细胞中非经典凋亡机制的实验证据。
3. 研究思路总结与详细解析
本研究的整体研究目标是分析HIV感染对Fas和TRAIL通路受体/配体表达、免疫激活标志物及炎症细胞因子的影响,明确其与HIV疾病进展的关联;核心科学问题为TRAIL通路在HIV早期感染中的激活机制及其与免疫激活状态的调控关系;技术路线遵循“临床样本招募→细胞与分子水平检测→统计分析关联→功能实验验证”的闭环逻辑,确保研究结论的严谨性与可靠性。
3.1 研究对象招募与样本采集
实验目的是获取基线特征匹配的研究样本,排除混杂因素对实验结果的干扰。方法细节为招募14名未接受ART的男性PLWHIV(纳入标准:年龄>18岁、CD4⁺T细胞计数>350细胞/µL、无其他病毒感染及自身免疫疾病),同时招募14名年龄、性别匹配的健康对照;采集外周血样本,分离外周血单个核细胞(PBMC)并冻存,分离血清用于细胞因子检测。结果解读显示两组研究对象的生化指标无显著差异,PLWHIV的病毒载量均值为25563拷贝/mL(n=14),CD4⁺T细胞计数中位数为470细胞/µL(n=14),确保样本的同质性与研究的可比性。实验所用关键产品:PBMC分离采用Axis-Shield的Lymphoprep,细胞培养试剂来自GIBCO™ Invitrogen,流式细胞术检测所用抗体来自BioLegend、BD、R&D Systems、Abcam等品牌。
3.2 Fas与TRAIL通路受体/配体表达检测
实验目的是分析两种死亡通路在目标免疫细胞中的表达差异,明确HIV感染对通路激活的影响。方法细节为采用流式细胞术检测CD3⁺CD4⁺T细胞及CD14⁺CD4⁺单核细胞中Fas、FasL、DR4、DR5、TRAIL的表达水平,通过平均荧光强度(MFI)及阳性细胞百分比量化表达差异。结果解读显示,PLWHIV的CD14⁺CD4⁺单核细胞中DR5的表达显著高于健康对照(n=14,P<0.05),CD3⁺CD4⁺T细胞中DR5表达呈升高趋势;Fas及FasL在两组细胞中的表达无显著统计学差异;TRAIL在两组细胞中的表达均极低,且PLWHIV中的MFI低于健康对照。


3.3 HIV共受体与免疫激活标志物检测
实验目的是分析HIV共受体CXCR4、CCR5与死亡通路的关联,明确免疫激活标志物在PLWHIV中的表达特征。方法细节为采用流式细胞术检测CD3⁺CD4⁺T细胞及CD14⁺CD4⁺单核细胞中CXCR4、CCR5的表达,同时检测免疫激活标志物CD25、CD69、CD38(T细胞)及CD80、CD86、HLA-DR(单核细胞)的表达。结果解读显示,PLWHIV的CD3⁺CD4⁺T细胞中CD38的表达显著升高(n=14,P<0.05);CXCR4与DR5的表达呈正相关(CD3⁺CD4⁺T细胞:r=0.86,n=14,P<0.001;CD14⁺CD4⁺单核细胞:r=0.68,n=14,P<0.005);CCR5的表达与感染时间呈负相关(CD3⁺CD4⁺T细胞:r=-0.73,n=14,P<0.05;CD14⁺CD4⁺单核细胞:r=-0.79,n=14,P<0.05)。




3.4 血清炎症细胞因子检测
实验目的是分析PLWHIV的炎症状态,明确炎症细胞因子与死亡通路的关联。方法细节为采用BioLegend的LEGENDplex多重免疫分析试剂盒检测血清中IL-1β、IL-6、IL-8、TNF-α、IL-18的水平。结果解读显示,PLWHIV的血清IL-18水平显著高于健康对照(n=14,P<0.05),其余细胞因子水平无显著差异;IL-18水平与DR5的表达呈正相关(CD3⁺CD4⁺T细胞:r=0.56,n=14,P<0.05;CD14⁺CD4⁺单核细胞:r=0.636,n=14,P<0.05)。


3.5 凋亡诱导与抑制功能实验
实验目的是验证Fas和TRAIL通路的功能活性,明确其介导细胞凋亡的机制。方法细节为用重组FasL和TRAIL处理PBMC,同时加入caspase8抑制剂,采用Annexin V/PI染色法检测细胞早期及晚期凋亡情况。结果解读显示,PLWHIV的CD14⁺CD4⁺单核细胞在TRAIL处理后早期凋亡显著增加(n=14,P<0.05),且该效应不受caspase8抑制剂的影响;Fas通路处理后,两组细胞的凋亡水平无显著差异。


4. Biomarker研究及发现成果
Biomarker定位与筛选逻辑
本研究聚焦的核心生物标志物为TRAIL通路受体DR5,其筛选与验证逻辑遵循“临床样本表达差异分析→关联疾病进展指标→功能实验验证”的完整链条:首先通过流式细胞术检测发现PLWHIV的CD14⁺CD4⁺单核细胞中DR5表达显著升高,随后分析其与感染时间、免疫激活标志物及炎症细胞因子的关联,明确其与疾病进展的正相关关系,最后通过凋亡功能实验验证其介导的非经典凋亡机制,全面验证其作为HIV疾病进展生物标志物的潜力。
研究过程详述
DR5的检测样本为PLWHIV的CD3⁺CD4⁺T细胞及CD14⁺CD4⁺单核细胞表面蛋白,采用流式细胞术进行定量检测。特异性方面,PLWHIV的CD14⁺CD4⁺单核细胞中DR5阳性细胞百分比及MFI均显著高于健康对照(n=14,P<0.05);敏感性方面,DR5的表达与感染时间呈正相关(CD14⁺CD4⁺单核细胞:r=0.88,n=14,P<0.005),与免疫激活标志物CD38、炎症细胞因子IL-18及HIV共受体CXCR4的表达均呈正相关,提示其可反映HIV感染的免疫激活状态与疾病进展程度。
核心成果提炼
本研究明确DR5可作为HIV早期感染的潜在疾病进展生物标志物,其表达与感染时间正相关(r=0.88,n=14,P<0.005),且与免疫激活、炎症反应及HIV共受体调控密切相关;首次发现TRAIL通路介导CD14⁺CD4⁺单核细胞的早期凋亡不依赖caspase8,提示存在非经典的细胞死亡机制(如坏死性凋亡);同时补充了未接受ART的PLWHIV中IL-18与DR5的调控关系,为HIV疾病进展的免疫机制研究提供新的实验依据。这些成果为后续开发以TRAIL通路为靶点的HIV治疗策略及疾病进展监测标志物奠定了基础。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。