Stromal Senp1 promotes mouse early folliculogenesis by regulating BMP4 expression
基质Senp1通过调节BMP4表达促进小鼠早期卵泡发生
| 期刊: | Cell and Bioscience | 影响因子: | 6.100 |
| 时间: | 2017 | 起止号: | 2017 Jul 25:7:36. |
| doi: | 10.1186/s13578-017-0163-5 | 种属: | Mouse |
| 研究方向: | 信号转导 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Stromal Senp1 promotes mouse early folliculogenesis by regulating BMP4 expression;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:生殖生物学(卵巢早期卵泡发生调控)
哺乳动物卵泡发生是卵巢卵泡从原始状态发育至成熟排卵的复杂生理过程,小鼠卵巢发育主要分为生殖囊泡破裂与原始卵泡形成、原始卵泡激活发育、排卵或凋亡三个关键阶段。领域共识:现有研究明确原始卵泡库的大小决定了成年雌性的生殖寿命,卵母细胞与周围体细胞(颗粒细胞、基质细胞等)的双向信号通讯是卵泡激活和发育的核心驱动力,骨形态发生蛋白(BMP)家族等基质来源的生长因子在原始卵泡向初级卵泡转化过程中发挥关键作用。近年来,小泛素样修饰(SUMO)化在卵母细胞减数分裂中的功能逐渐被揭示,但基质细胞中SUMO化修饰调控因子对卵泡发生的作用及分子机制尚未明确,这一空白限制了对卵巢早衰等生殖疾病发病机制的理解。
结合领域现状,本研究聚焦基质细胞中的SUMO特异性蛋白酶SENP1,旨在明确其在小鼠早期卵泡发生中的调控功能及分子机制,为卵巢早衰的病理研究提供新的实验模型和潜在靶点。
2. 文献综述解析
作者以卵泡发生的基本生理过程为基础,系统梳理了卵母细胞与体细胞互作的研究进展,聚焦SUMO化修饰在生殖系统中的功能研究现状,明确了基质细胞SUMO化调控机制的研究空白,为自身研究的开展奠定了逻辑基础。
现有研究已清晰界定小鼠卵巢发育的阶段特征,证实卵母细胞与颗粒细胞、基质细胞的信号通讯是卵泡激活和发育的核心驱动力,BMP4等基质来源的生长因子在原始卵泡向初级卵泡转化过程中发挥关键作用。同时,SUMO化修饰在卵母细胞减数分裂的纺锤体组装、染色体分离等过程中的功能已被报道,但针对基质细胞中SUMO化调控因子的研究仍处于空白状态,现有研究无法解释基质细胞如何通过蛋白修饰调控卵母细胞发育的分子机制,也缺乏相关的动物模型验证。
本研究的创新价值在于首次将SUMO化调控因子的研究范围从卵母细胞拓展至基质细胞,通过构建基质细胞特异性敲除模型,揭示了SENP1通过调控BMP4表达参与基质-卵母细胞通讯的新机制,填补了基质细胞蛋白修饰调控早期卵泡发生的研究空白,为卵巢早衰的发病机制研究提供了新的视角。
3. 研究思路总结与详细解析
本研究的整体目标是明确基质细胞SENP1在小鼠早期卵泡发生中的功能及分子机制,核心科学问题为基质细胞SENP1如何通过调控下游分子影响卵母细胞发育与卵泡形成,技术路线遵循“模型构建→表型观察→机制解析→功能验证”的闭环逻辑,通过体内动物实验与体外细胞实验相结合的方式,系统验证了SENP1-BMP4轴的调控作用。
3.1 基质细胞特异性SENP1敲除小鼠模型构建与验证
实验目的:构建SM22α阳性基质细胞特异性敲除SENP1的小鼠模型,验证SENP1在目标细胞中的敲除效率,为后续表型分析提供实验基础。方法细节:采用Cre-loxP条件性基因敲除技术,将携带loxP位点的SENP1 flox/flox小鼠与SM22α启动子驱动的Cre工具鼠交配,获得基质细胞特异性SENP1敲除(SENP1-smKO)小鼠;通过SM22α-Cre与mG/mT报告小鼠交配,验证SM22α阳性细胞在卵巢基质中的定位;从WT和SENP1-smKO小鼠卵巢中分离SM22α阳性细胞,采用实时荧光定量PCR(qRT-PCR)和蛋白质免疫印迹(Western blot)分别检测SENP1的mRNA和蛋白表达水平。结果解读:报告小鼠实验显示SM22α阳性细胞主要分布于卵巢基质区域;qRT-PCR结果显示SENP1-smKO小鼠SM22α阳性细胞中SENP1 mRNA水平较WT下调约70%(n=3,P<0.05),Western blot结果显示蛋白水平下调约65%(n=3,P<0.05),证实SENP1在基质细胞中被特异性敲除。
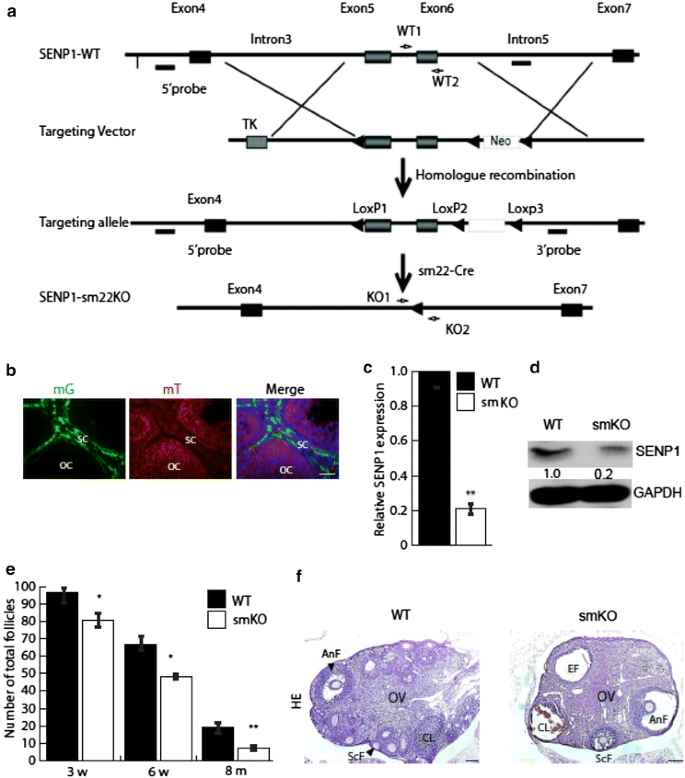
产品关联:文献未提及具体实验产品,领域常规使用Cre-loxP系统构建条件性敲除小鼠,qRT-PCR常用SYBR Green荧光定量试剂盒,Western blot常用抗SENP1单克隆抗体、GAPDH内参抗体等。
3.2 卵巢发育表型的多阶段分析
实验目的:观察SENP1敲除对小鼠不同年龄段卵巢卵泡发育的影响,明确其在早期卵泡发生及生殖寿命维持中的作用。方法细节:选取3周、6周、8个月龄的WT和SENP1-smKO小鼠,取卵巢组织进行苏木精-伊红(H&E)染色,统计原始卵泡、初级卵泡、次级卵泡等不同阶段的卵泡数量;对新生(D0)、出生后3天(D3)、7天(D7)的小鼠卵巢进行免疫荧光染色,采用卵母细胞标志物VASA和基质细胞标志物SM22α观察卵母细胞形态及卵泡结构。结果解读:H&E染色统计显示,SENP1-smKO小鼠各年龄段卵巢的总卵泡数量均显著低于WT小鼠,8月龄时WT小鼠卵巢仍可见各发育阶段卵泡及黄体,而SENP1-smKO小鼠卵巢几乎无发育中卵泡,呈现卵巢早衰表型(n=5,P<0.01);D3和D7时SENP1-smKO小鼠的卵母细胞体积较WT小约25%(n=5,P<0.05),初级和次级卵泡数量分别减少约40%和50%(n=5,P<0.01),表明早期卵泡发生过程受阻。
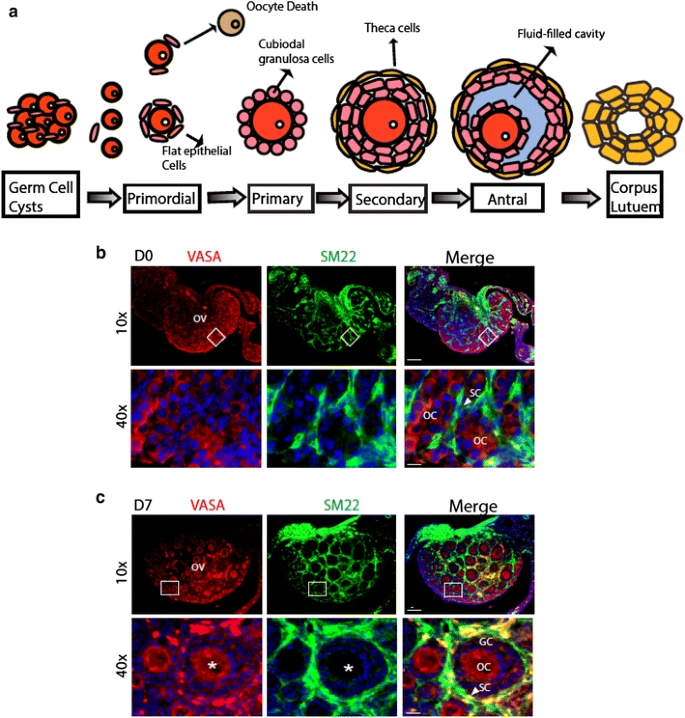
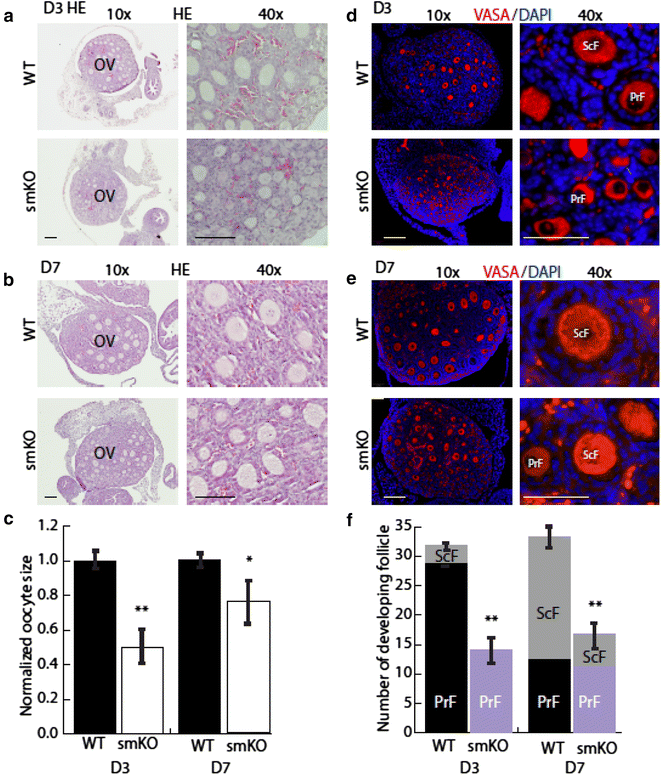
产品关联:文献未提及具体实验产品,领域常规使用H&E染色试剂盒,免疫荧光实验常用抗VASA多克隆抗体、抗SM22α单克隆抗体及荧光二抗等。
3.3 基质细胞形态与BMP4表达的分子解析
实验目的:探究SENP1敲除对基质细胞组织形态及BMP家族基因表达的影响,筛选下游调控分子。方法细节:对WT和SENP1-smKO小鼠D0、D3卵巢进行SM22α免疫荧光染色,观察基质细胞的分布形态;分离培养人卵巢SM22α阳性基质细胞,采用siRNA敲低SENP1表达,通过qRT-PCR检测BMP2、BMP4、BMP6的mRNA水平,Western blot检测BMP4的蛋白表达水平。结果解读:免疫荧光结果显示,WT小鼠卵巢中SM22α阳性基质细胞紧密包裹卵泡,分布均匀,而SENP1-smKO小鼠的基质细胞分布紊乱,无法形成完整的卵泡包裹结构;人基质细胞中SENP1敲低后,BMP4的mRNA水平下调约60%(n=3,P<0.05),蛋白水平下调约50%(n=3,P<0.05),而BMP2、BMP6的表达无显著变化,表明SENP1特异性调控基质细胞中BMP4的表达。
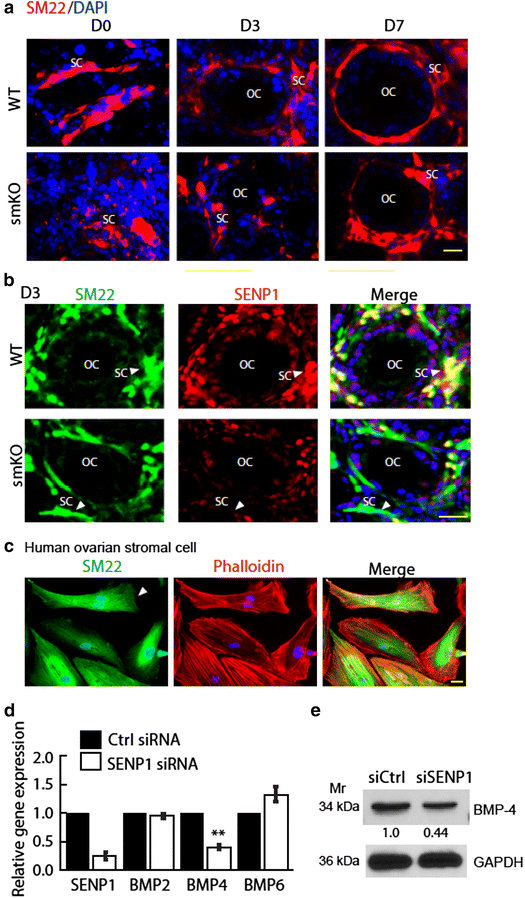
产品关联:文献未提及具体实验产品,领域常规使用siRNA转染试剂、qRT-PCR引物、抗BMP4单克隆抗体等。
3.4 卵母细胞BMP4受体表达的验证
实验目的:验证SENP1敲除对卵母细胞上BMP4受体表达的影响,明确基质-卵母细胞通讯的调控机制。方法细节:取WT和SENP1-smKO小鼠D7卵巢组织,进行BMP4与BMPR1A、BMPR1B、BMPR2的免疫荧光共染色,观察受体在卵母细胞上的表达水平。结果解读:免疫荧光结果显示,WT小鼠卵母细胞上高表达BMPR1B和BMPR2,而SENP1-smKO小鼠卵母细胞上的BMPR1B表达下调约45%(n=5,P<0.05),BMPR2表达下调约50%(n=5,P<0.05),BMPR1A的表达无显著变化,表明基质细胞SENP1缺失通过下调BMP4的表达,间接影响卵母细胞上BMP4受体的表达,破坏了基质-卵母细胞的信号通讯。
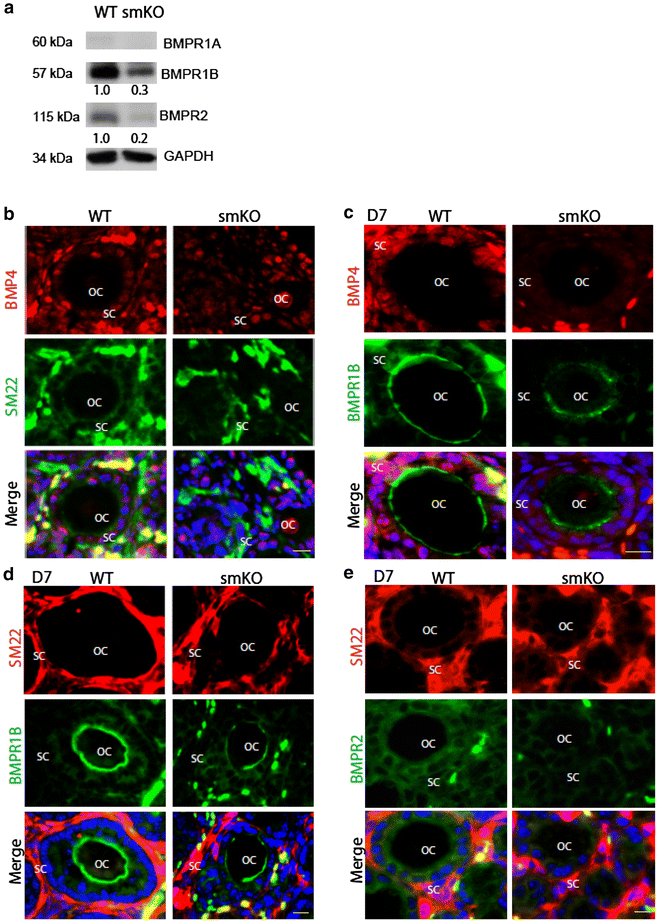
产品关联:文献未提及具体实验产品,领域常规使用抗BMPR1B、抗BMPR2单克隆抗体及荧光共染色试剂等。
4. Biomarker研究及发现成果解析
本研究中涉及的功能调控分子包括基质细胞中的SENP1及其下游靶分子BMP4,二者共同构成调控早期卵泡发生的关键轴,其筛选与验证遵循“体内表型锁定→体外细胞验证→分子机制解析”的完整逻辑链条。
Biomarker定位:SENP1属于SUMO特异性蛋白酶家族,作为功能调控型Biomarker,其表达于SM22α阳性卵巢基质细胞;BMP4属于TGF-β超家族成员,作为效应型Biomarker,由基质细胞分泌。二者的筛选逻辑为:通过SENP1基质特异性敲除小鼠的卵巢早衰表型,锁定SENP1为核心调控因子,再通过体外细胞实验筛选其下游调控的生长因子,最终验证BMP4的关键作用,验证过程涵盖动物模型、细胞系及分子水平的多维度验证。
研究过程详述:SENP1的来源为小鼠卵巢SM22α阳性基质细胞,通过条件性敲除模型验证其功能;BMP4的来源为卵巢基质细胞,在人卵巢基质细胞中通过siRNA敲低SENP1后,qRT-PCR和Western blot验证其表达显著下调;特异性方面,SENP1仅调控BMP4的表达,对BMP2、BMP6等其他BMP家族成员无显著影响;敏感性方面,SENP1敲除后,小鼠卵巢中BMP4的表达水平下调约50%,卵母细胞上BMPR1B和BMPR2的表达水平分别下调约45%和50%(n=5,P<0.05)。
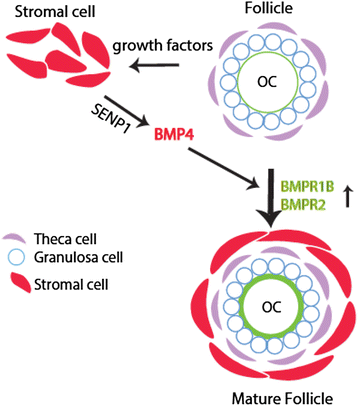
核心成果提炼:SENP1通过维持基质细胞中BMP4的表达,促进卵母细胞上BMP4受体的表达,进而调控早期卵泡发生,其缺失会导致生殖囊泡破裂不完全、卵泡数量减少,最终引发卵巢早衰;该研究首次揭示了基质细胞中SUMO化修饰调控因子在早期卵泡发生中的功能,构建的SENP1-smKO小鼠可作为人类卵巢早衰的实验模型;统计学结果显示,8月龄SENP1-smKO小鼠的总卵泡数量仅为WT小鼠的20%左右(n=5,P<0.01),D7时初级卵泡数量减少约40%(n=5,P<0.01)。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。