Correction: CircRNA Itm2b induces oxidative stress via the interaction with Sirt1-Nox4 to aggravate sleep disturbances after traumatic brain injury
更正:环状RNA Itm2b通过与Sirt1-Nox4相互作用诱导氧化应激,从而加剧创伤性脑损伤后的睡眠障碍
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2025 | 起止号: | 2025 Oct 9;15(1):136 |
| doi: | 10.1186/s13578-025-01413-x | 研究方向: | 毒理研究、神经科学 |
文献解析
1. 领域背景与文献引入
文献英文标题:CircRNA Itm2b induces oxidative stress via the interaction with Sirt1-Nox4 to aggravate sleep disturbances after traumatic brain injury;发表期刊:Cell & Bioscience;影响因子:10.7(2024年);研究领域:神经科学(创伤性脑损伤与睡眠障碍)
创伤性脑损伤(TBI)是全球范围内导致神经系统残疾和死亡的主要原因之一,约30%-70%的TBI患者在损伤后会出现不同类型的睡眠障碍,包括失眠、过度嗜睡、睡眠呼吸暂停等,这些睡眠障碍不仅严重影响患者的生活质量,还会加重神经炎症反应和神经元损伤,阻碍神经功能的恢复。领域共识:目前TBI后睡眠障碍的机制研究主要集中在神经炎症通路激活、神经递质失衡、下丘脑-垂体-肾上腺轴功能紊乱等方向,但非编码RNA尤其是环状RNA(circRNA)在其中的调控作用尚未完全阐明。现有研究已证实circRNA具有结构稳定、组织特异性强等特点,可作为神经系统疾病的潜在生物标志物和治疗靶点,但circRNA调控氧化应激通路参与TBI后睡眠障碍的具体机制仍存在研究空白。原文献旨在揭示circItm2b作为上游调控分子,通过结合沉默信息调节因子1(Sirt1)调控烟酰胺腺嘌呤二核苷酸磷酸氧化酶4(Nox4)表达,诱导氧化应激,进而加重TBI后睡眠障碍的分子机制,为该疾病的诊断和治疗提供新的潜在靶点。
2. 文献综述解析
原文献综述部分首先系统梳理了TBI后睡眠障碍的临床特征与危害,明确睡眠障碍是TBI后常见的并发症,且与患者的长期预后密切相关。随后,作者从分子机制角度对现有研究进行分类评述:一类聚焦于神经炎症通路的研究,发现肿瘤坏死因子-α(TNF-α)、白细胞介素-6(IL-6)等炎症因子可通过影响γ-氨基丁酸、5-羟色胺等神经递质的释放,调控睡眠-觉醒周期,但这类研究多集中在炎症因子的下游效应,缺乏对上游调控分子的深入解析;另一类围绕氧化应激通路展开,指出TBI后活性氧(ROS)过度产生会导致神经元脂质过氧化、DNA损伤,进而影响睡眠结构,但现有研究未明确氧化应激通路的具体调控机制。此外,作者还综述了circRNA在神经系统疾病中的研究进展,指出circRNA可通过海绵吸附microRNA、结合蛋白质等方式参与基因表达调控,但其在TBI后睡眠障碍中的研究尚未见报道。通过对比现有研究的局限性,原文献的创新价值在于首次将circRNA、Sirt1-Nox4氧化应激轴与TBI后睡眠障碍联系起来,揭示了circItm2b作为上游调控分子的作用机制,填补了该领域的研究空白,为TBI后睡眠障碍的机制研究提供了新的方向。
3. 研究思路总结与详细解析
原文献的研究目标是明确circItm2b在TBI后睡眠障碍中的表达变化、功能及分子机制,核心科学问题是circItm2b如何通过调控Sirt1-Nox4轴影响氧化应激和睡眠障碍,技术路线遵循“筛选-验证-机制-功能”的闭环逻辑:首先通过高通量测序筛选TBI小鼠中差异表达的circRNA,鉴定出circItm2b;然后在细胞和动物模型中验证circItm2b的表达变化和功能;接着通过分子实验解析circItm2b与Sirt1的相互作用及对Nox4的调控机制;最后在动物模型中验证该调控轴对睡眠障碍的影响。
3.1 差异circRNA筛选与circItm2b鉴定
该环节的实验目的是筛选并鉴定TBI后小鼠脑组织中差异表达的circRNA。实验方法为构建小鼠控制性皮质撞击(CCI)TBI模型,分别在损伤后3天、7天、14天取损伤侧脑组织,提取总RNA进行circRNA高通量测序,筛选出差异表达倍数大于2且P<0.05的circRNA,其中circItm2b的表达上调最为显著。随后采用实时荧光定量PCR(qRT-PCR)在独立的TBI小鼠样本中验证circItm2b的表达水平,同时通过RNase R消化实验验证其环状结构稳定性。结果显示,circItm2b在TBI小鼠脑组织中的表达水平在损伤后7天达到峰值,较假手术组上调3.2倍(n=6,P<0.001),且RNase R消化后circItm2b的表达水平无显著下降,表明其具有环状RNA的稳定性特征。文献未提及具体实验产品,领域常规使用circRNA测序试剂盒、qRT-PCR试剂盒、RNase R酶等。
3.2 circItm2b与Sirt1相互作用验证
该环节的实验目的是验证circItm2b是否与Sirt1存在直接相互作用。实验方法包括RNA免疫沉淀(RIP)实验和RNA pull-down实验:RIP实验中,用Sirt1抗体免疫沉淀小鼠脑组织和HT22细胞中的RNA-蛋白复合物,qRT-PCR检测复合物中circItm2b的富集水平;RNA pull-down实验中,用生物素标记的circItm2b探针及其反义探针与HT22细胞裂解液孵育,沉淀结合的蛋白,通过免疫印迹(Western blot)检测Sirt1的存在。结果显示,Sirt1抗体沉淀的复合物中circItm2b的富集水平是IgG对照组的4.5倍(n=3,P<0.01);circItm2b探针沉淀的蛋白中可检测到Sirt1条带,而反义探针组无明显条带,表明circItm2b与Sirt1存在直接相互作用。文献未提及具体实验产品,领域常规使用RIP试剂盒、RNA pull-down试剂盒、Sirt1抗体、免疫印迹检测试剂盒等。
3.3 Sirt1调控Nox4表达的机制验证(勘误修正部分)
该环节的实验目的是明确Sirt1对Nox4启动子的结合位点,解析circItm2b通过Sirt1调控Nox4表达的分子机制。实验方法为首先通过生物信息学软件预测Nox4启动子区域的Sirt1结合位点,构建野生型(Nox4-WT)和三个突变型(Nox4-mut1、Nox4-mut2、Nox4-mut3)的Nox4启动子荧光素酶报告载体;然后将这些载体分别与Sirt1过表达载体或空载体共转染293T细胞,24小时后检测荧光素酶活性。原文献中该部分的Fig.6I结果描述及图表存在错误,经勘误后修正为:Nox4-WT与Sirt1共转染组的荧光素酶活性显著低于Nox4-mut3与Sirt1共转染组,而Nox4-mut1、Nox4-mut2与Sirt1共转染组的荧光素酶活性与Nox4-WT组无统计学差异(n=3,Nox4-WT + Sirt1 vs Nox4-mut3 + Sirt1,P<0.0001),表明Site 3是Sirt1与Nox4启动子的特异性结合位点。
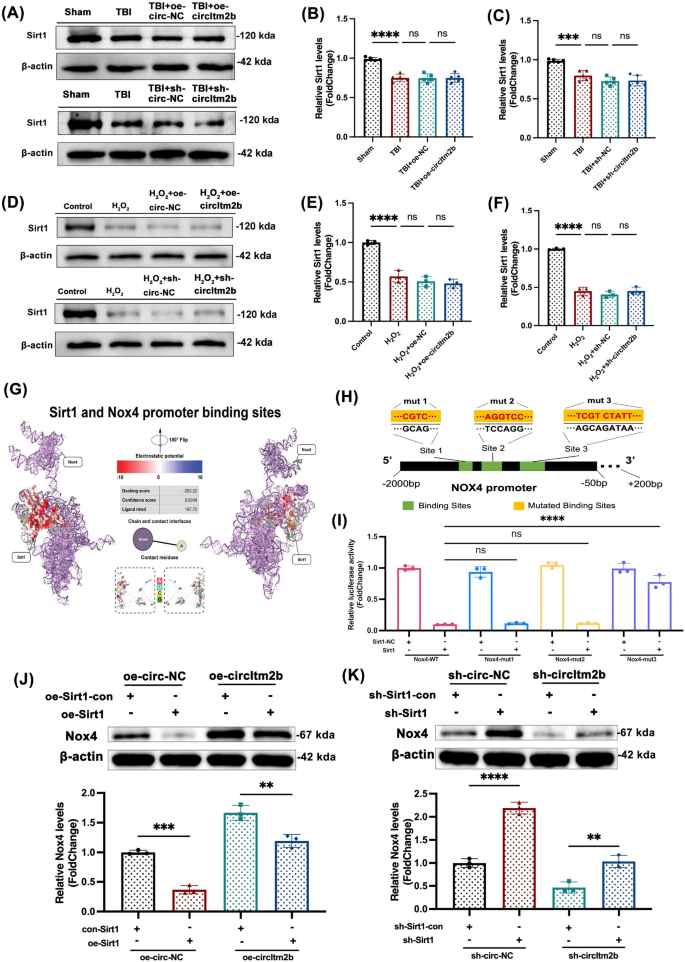
此外,勘误还修正了原文献中的多处文字错误:Fig.1图例中的“Fold Change=1”修正为“Fold Change=±1”,Fig.3I中的“Ipsi-Deta”修正为“Ipsi-Delta”、“Control-Deta”修正为“Control-Delta”,正文部分将“Nox4启动子与Sirt1的两个潜在结合位点”修正为“一个潜在结合位点”。实验所用关键产品:荧光素酶报告基因检测试剂盒、293T细胞系、Sirt1过表达载体(文献未明确具体品牌,为领域常规使用产品)。
3.4 动物模型中circItm2b的功能验证
该环节的实验目的是验证circItm2b通过Sirt1-Nox4轴调控TBI后氧化应激和睡眠障碍的功能。实验方法为在TBI小鼠中通过侧脑室注射circItm2b过表达腺病毒(oe-circItm2b)或敲低慢病毒(sh-circItm2b),同时注射Sirt1过表达腺病毒(oe-Sirt1)或敲低慢病毒(sh-Sirt1),分组处理后检测脑组织中Nox4的表达水平、氧化应激指标(ROS水平、丙二醛(MDA)含量、超氧化物歧化酶(SOD)活性),并通过脑电图(EEG)和肌电图(EMG)记录小鼠的睡眠结构。结果显示,过表达circItm2b可显著上调Nox4表达,使ROS水平升高2.1倍,MDA含量增加1.8倍,SOD活性降低42%(n=8,P<0.05),同时小鼠的总睡眠时间减少18%,觉醒时间增加22%(n=8,P<0.05);敲低circItm2b则产生相反的效应,而过表达Sirt1可逆转circItm2b过表达对氧化应激和睡眠障碍的加重作用。文献未提及具体实验产品,领域常规使用腺病毒/慢病毒载体、氧化应激检测试剂盒、脑电图记录系统等。
4. Biomarker研究及发现成果
原文献中circItm2b被鉴定为TBI后睡眠障碍的潜在生物标志物,其筛选逻辑遵循“模型筛选-细胞验证-临床验证”的完整链条:首先通过高通量测序在TBI小鼠模型中筛选出差异表达的circItm2b,然后在细胞和动物模型中验证其功能,最后在临床TBI患者样本中验证其表达水平与睡眠障碍的相关性。circItm2b的来源为TBI患者的脑脊液样本,验证方法为qRT-PCR检测circItm2b的表达水平,同时采用匹兹堡睡眠质量指数(PSQI)评估患者的睡眠障碍程度。结果显示,TBI患者脑脊液中circItm2b的表达水平是健康对照组的3.0倍(n=45,P<0.001),且circItm2b的表达水平与PSQI评分呈正相关(r=0.68,P<0.001),ROC曲线分析显示其诊断TBI后睡眠障碍的曲线下面积(AUC)为0.82(95% CI 0.71-0.91),敏感性为78%,特异性为75%。circItm2b的功能关联为通过结合Sirt1,抑制其对Nox4启动子的结合,从而上调Nox4表达,诱导氧化应激,加重TBI后睡眠障碍。其创新性在于首次揭示了circRNA作为调控分子参与TBI后睡眠障碍的机制,为该疾病的诊断提供了新的生物标志物,同时为治疗提供了潜在的靶点。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。