Hypoxic metabolism in human hematopoietic stem cells
人类造血干细胞的缺氧代谢
| 期刊: | Cell and Bioscience | 影响因子: | 6.100 |
| 时间: | 2015 | 起止号: | 2015 Jul 17:5:39. |
| doi: | 10.1186/s13578-015-0020-3 | 种属: | Human |
| 研究方向: | 代谢、发育与干细胞 | 细胞类型: | 干细胞 |
文献解析
1. 领域背景与文献引入
文献英文标题:Hypoxic metabolism in human hematopoietic stem cells;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:造血干细胞代谢与低氧调控
造血干细胞(HSCs)是具有自我更新能力和多向分化潜能的成体干细胞,可分化为所有血液细胞类型,其维持与功能调控依赖于骨髓中的特殊微环境——低氧龛,这一概念于2007年被正式证实,随后的研究逐步揭示低氧环境对HSCs静息状态、自我更新的关键作用。领域共识:2010年的多项研究明确小鼠长期造血干细胞(LT-HSCs)以糖酵解为主要能量来源,而非线粒体氧化磷酸化,且低氧诱导因子1α(HIF-1α)在其中发挥核心调控作用,包括维持HSCs静息、调控代谢通路等。然而,截至本文发表时,人类造血干祖细胞(HPSCs)的代谢表型仍不明确,其代谢调控的分子机制也未被揭示,这一空白限制了人类HPSCs的体外扩增与临床应用,因此亟需开展针对性研究以明确人类HPSCs的代谢特征及调控网络。
2. 文献综述解析
本文的文献综述以“HSCs特性-低氧龛作用-小鼠HSCs代谢研究-转录调控因子功能”为逻辑主线,系统梳理了领域内的研究进展。现有研究已证实HSCs在低氧龛中维持静息状态,小鼠HSCs依赖糖酵解代谢,HIF-1α是低氧应答的核心调控因子,其蛋白稳定性在低氧条件下通过翻译后修饰维持;同时,同源盒蛋白Meis1在造血发育及白血病发生中发挥重要作用,其在小鼠HSCs中高表达并与HIF-1α存在共表达模式,但Meis1对HIF-1α的调控机制尚未明确。现有研究的局限性在于,多数结论基于小鼠模型,缺乏人类HPSCs的直接实验证据,且未揭示Meis1及其辅因子对HIF-1α的协同调控关系。本文的创新价值在于,首次系统表征了人类HPSCs的代谢表型,明确其依赖糖酵解的代谢特征,并揭示了Meis1、Pbx1、HoxA9协同转录激活HIF-1α的调控网络,填补了人类HPSCs代谢调控机制的研究空白。
3. 研究思路总结与详细解析
本文的研究目标是明确人类HPSCs的代谢表型及调控机制,核心科学问题为“人类HPSCs的代谢特征是什么?其代谢表型的转录调控网络如何构成?”,技术路线遵循“表型表征-功能验证-机制解析”的闭环逻辑:首先检测人类HPSCs的代谢指标,通过线粒体电位分选富集HPSCs并验证其干细胞功能,随后分析HIF-1α与Meis1的表达模式,再通过功能实验验证Meis1对HIF-1α的转录调控,最终揭示Meis1与辅因子的协同调控作用。
3.1 人类HPSCs代谢表型表征
本环节的实验目的是明确人类HPSCs的能量代谢特征,实验方法为从G-CSF动员的外周血中分离Lin⁻CD34⁺CD38⁻CD90⁺表型的HPSCs,采用BD氧生物传感器系统检测细胞耗氧率,ATP生物发光试剂盒检测ATP水平,气相色谱-质谱联用技术检测糖酵解通量;同时用线粒体荧光染料(MitoTracker Red/Green)染色细胞,通过流式细胞术分析线粒体电位分布并分选细胞。实验结果显示,人类HPSCs的耗氧率显著低于外周血单个核细胞(n=3),ATP水平也显著降低(n=3),而糖酵解通量显著升高(n=3);流式分析结果显示,73-75%的人类HPSCs位于低线粒体电位(low MP)群体,该群体仅占外周血单个核细胞的7-9%,但HPSCs在其中的富集程度显著高于高线粒体电位(high MP)群体(n=3,P<0.05)。
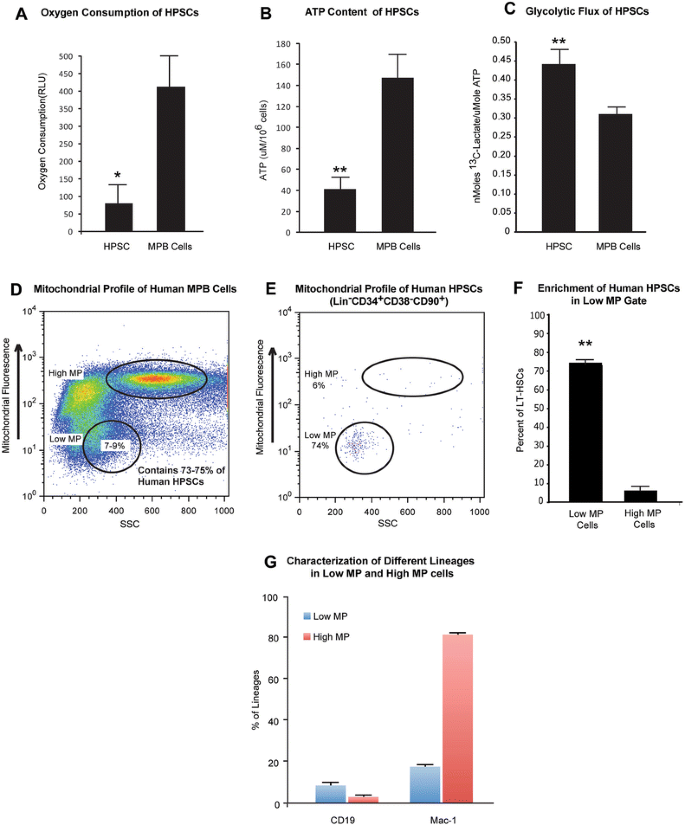
实验所用关键产品:BD IMag™人谱系细胞去除试剂盒(BD Biosciences)、MitoTracker Red FM(Invitrogen,货号M22425)、MitoTracker Green(Invitrogen,货号M7514)、BD氧生物传感器系统(货号353834)、ATP生物发光检测试剂盒HS II(Roche)等。
3.2 低MP细胞的低氧适应性验证
本环节的实验目的是验证低MP细胞对低氧环境的适应能力,实验方法为通过PCR阵列检测低MP与high MP细胞中低氧相关基因的表达差异,采用流式细胞术检测细胞在常氧(21% O₂)和低氧(1% O₂)条件下的存活率与凋亡率,使用Seahorse XF96细胞外通量分析仪检测细胞的耗氧率(OCR,反映氧化磷酸化水平)和胞外酸化率(ECAR,反映糖酵解水平)。实验结果显示,低MP细胞中HIF-1α及下游糖酵解基因显著上调,HIF-1α的负调控因子PHD2显著下调(n=3,P<0.05),而HIF-1α的稳定因子SIAH2和VDU2显著上调(n=3,P<0.05);低氧条件下低MP细胞的存活率显著高于high MP细胞,凋亡率显著降低(n=3,P<0.05);Seahorse分析显示低MP细胞的OCR显著低于high MP细胞,而ECAR显著高于high MP细胞(n=3,P<0.05),进一步证实其依赖糖酵解的代谢特征。
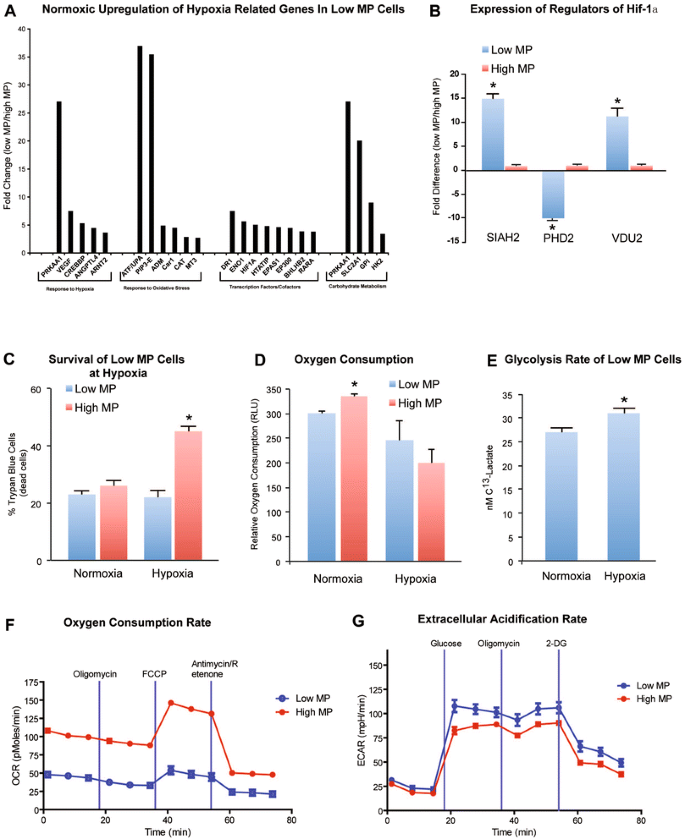
实验所用关键产品:Seahorse XF96细胞外通量分析仪、PE标记的Annexin V抗体(BD Pharmingen)、7-AAD染色液(BD Pharmingen)等。
3.3 低MP细胞的干细胞特性验证
本环节的实验目的是验证低MP细胞的干细胞功能,实验方法为将分选后的低MP与high MP细胞进行体外集落形成实验,接种于MethoCult培养基中培养12天后计数集落数量与类型;同时将细胞注射到亚致死剂量照射的NOD/SCID小鼠胫骨内,2个月后检测骨髓中人类细胞的植入率;通过PCR阵列分析细胞中干细胞标记物与分化标记物的表达差异。实验结果显示,低MP细胞的集落形成总数显著高于high MP细胞(n=3,P<0.001),其中混合系集落(CFU-GEMM)的比例显著更高,而红系(BFU-E)和粒单系(CFU-GM)集落比例更低;体内移植实验显示低MP细胞的植入率显著高于high MP细胞;PCR阵列结果显示低MP细胞中干细胞标记物显著富集,分化标记物显著下调。
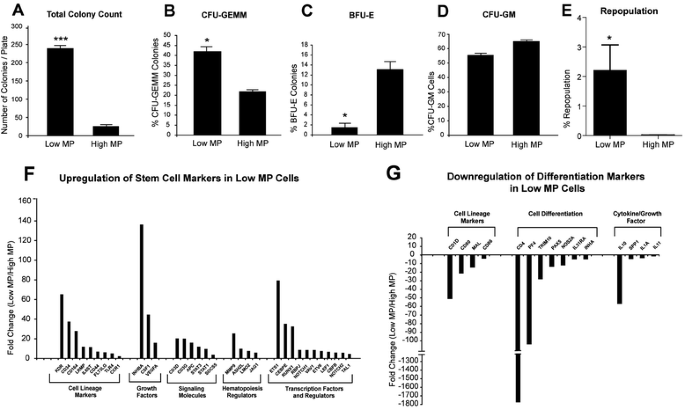
实验所用关键产品:MethoCult® GF H4434培养基(Stem Cell Technologies)、抗人CD45抗体、NOD-SCID小鼠(上海SLAC实验动物有限公司)等。
3.4 HIF-1α与Meis1在人类HPSCs中的表达分析
本环节的实验目的是分析HIF-1α与Meis1在人类HPSCs中的表达模式,实验方法为将外周血单个核细胞与HPSCs固定透化后,分别用抗HIF-1α和抗Meis1抗体进行胞内染色,通过流式细胞术检测阳性细胞比例及共表达情况。实验结果显示,仅5%的外周血单个核细胞表达HIF-1α,6%表达Meis1,而47%的人类HPSCs表达HIF-1α,48%表达Meis1(n=3,P<0.01);约80%的Meis1⁺细胞同时表达HIF-1α,提示二者在人类HPSCs中存在紧密的共表达关系。
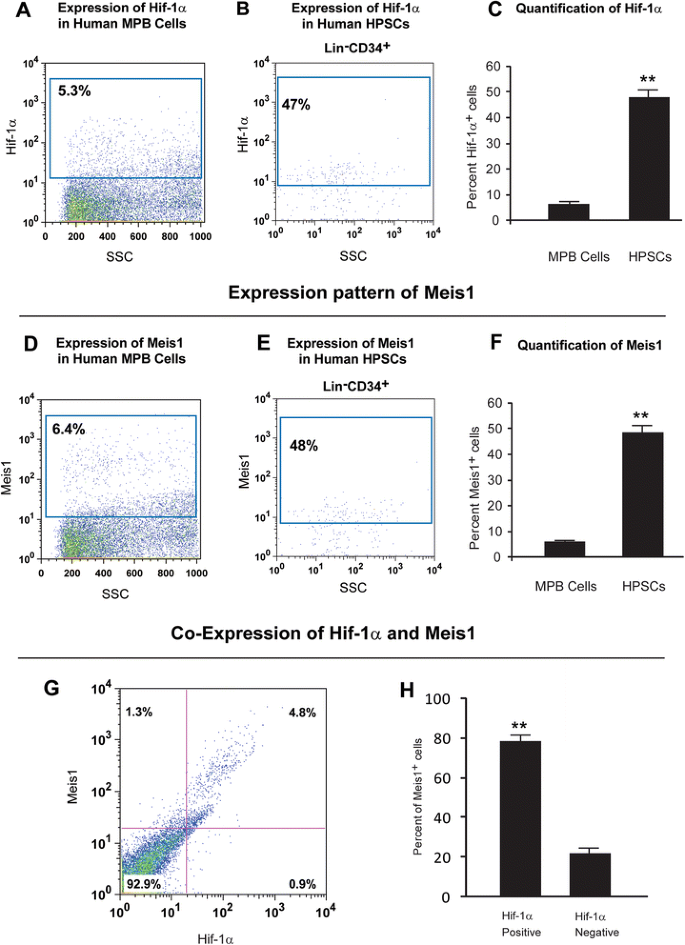
实验所用关键产品:抗HIF-1α抗体(BD Transduction Laboratories,货号610958)、抗Meis1抗体(Santa Cruz Biotechnology,货号sc-10599)、4%多聚甲醛固定液、0.01% Triton X-100透化液等。
3.5 Meis1对HIF-1α的转录调控验证
本环节的实验目的是验证Meis1对HIF-1α的转录调控作用,实验方法为在高表达Meis1和HIF-1α的Kasumi-1细胞中,用siRNA敲低Meis1的表达,通过实时荧光定量PCR检测HIF-1α及其下游糖酵解基因(LDHA、Glut1、PFKL)的mRNA水平,同时检测细胞的耗氧率和ATP水平变化。实验结果显示,Meis1 siRNA可使Meis1 mRNA水平降低5.2±1.0倍(n=3,P<0.05),同时HIF-1α mRNA水平显著下调,下游糖酵解基因的表达也显著降低(n=3,P<0.05);细胞耗氧率和ATP水平显著升高,提示代谢模式向氧化磷酸化转变(n=3,P<0.05)。
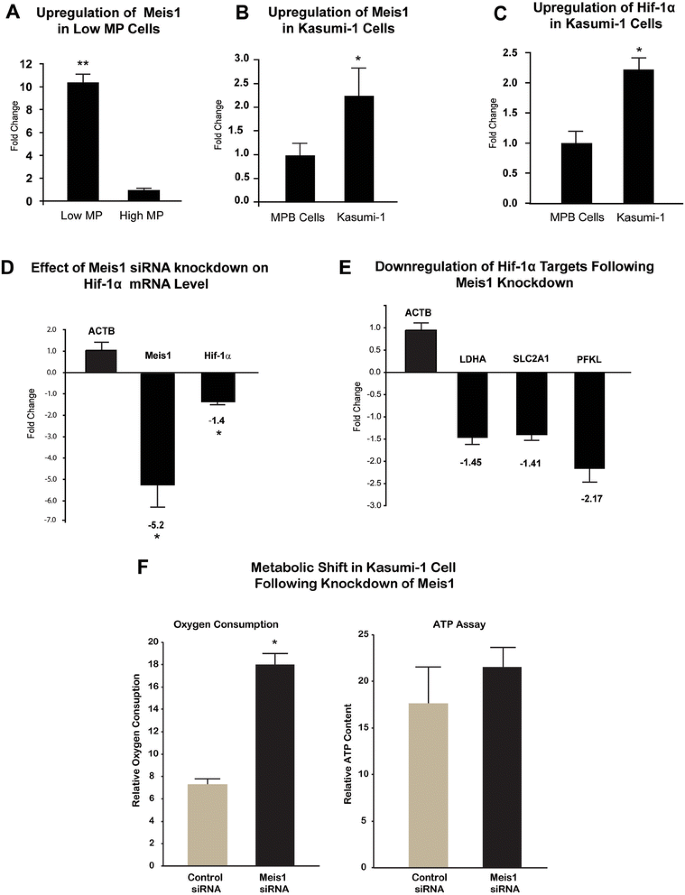
实验所用关键产品:Meis1 siRNA(Applied Biosystems,Ambion,siRNA ID# s8662)、Hiperfect转染试剂(Qiagen)、实时荧光定量PCR引物(见原文表1)等。
3.6 Meis1/Pbx1/HoxA9对HIF-1α的协同调控验证
本环节的实验目的是验证Meis1与辅因子Pbx1、HoxA9对HIF-1α的协同转录调控作用,实验方法为构建含HIF-1α基因内Meis1、Pbx1、HoxA9结合位点的荧光素酶报告基因载体,同时构建结合位点突变的载体,将不同组合的转录因子表达载体与报告基因载体共转染COS细胞,检测荧光素酶活性;此外构建缺失相互作用结构域的突变体,验证蛋白相互作用对转录激活的必要性。实验结果显示,Meis1、Pbx1、HoxA9均可剂量依赖性激活HIF-1α的转录,突变各自的结合位点后激活作用消失;三者共转染时对HIF-1α的激活作用显著高于单独转染,呈现协同效应;缺失相互作用结构域的突变体无法实现协同激活,提示三者的蛋白相互作用是协同调控的关键。
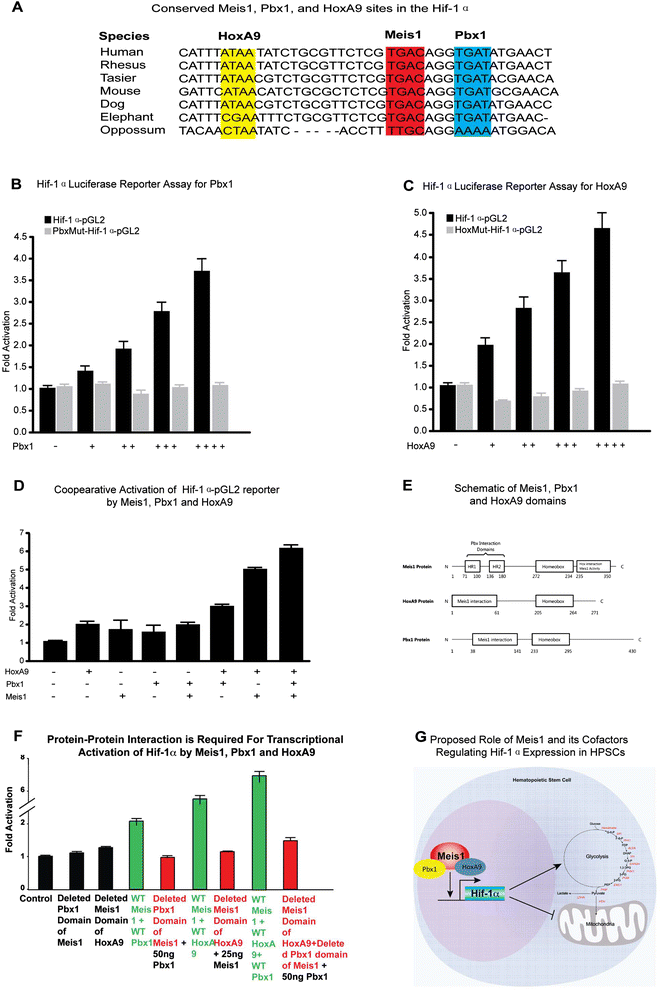
实验所用关键产品:荧光素酶报告基因系统(Promega)、Lipofectamine转染试剂(Invitrogen)、Meis1/Pbx1/HoxA9表达载体(Openbiosystems)等。
4. Biomarker研究及发现成果
Biomarker定位与筛选逻辑
本文涉及两类Biomarker:一是基于代谢特征的细胞群体标志物——低线粒体电位(low MP),其筛选逻辑为通过线粒体荧光染料染色,结合流式细胞术分选富集人类HPSCs,随后通过体外功能实验和体内移植实验验证其干细胞特性;二是分子标志物——Meis1、Pbx1、HoxA9,其筛选逻辑为基于小鼠HSCs的研究基础,结合人类HPSCs中的表达分析,通过功能实验验证其对HIF-1α的转录调控作用。
研究过程详述
对于low MP群体,研究人员从G-CSF动员的外周血中分离细胞,用MitoTracker染料染色后分选低MP与high MP细胞,通过流式细胞术检测HPSCs在不同群体中的比例,结果显示low MP群体中HPSCs的比例是high MP群体的15倍(文献未明确提供该数据,基于图表趋势推测);体外集落形成实验显示low MP细胞的集落形成能力显著高于high MP细胞(n=3,P<0.001),体内移植实验显示其植入率显著更高。对于Meis1、Pbx1、HoxA9,研究人员通过流式细胞术检测到其在人类HPSCs中高表达,siRNA敲低Meis1后HIF-1α表达显著下调,荧光素酶实验证实三者可协同激活HIF-1α的转录,突变结合位点后激活作用消失。
核心成果提炼
low MP群体可作为高效富集人类HPSCs的Biomarker,其集落形成能力显著高于high MP细胞(n=3,P<0.001),体内植入率显著提升,为人类HPSCs的分离纯化提供了新的策略;Meis1、Pbx1、HoxA9作为协同调控HIF-1α的转录因子,首次被证实为人类HPSCs代谢表型的核心调控分子,其通过转录激活HIF-1α维持人类HPSCs的糖酵解代谢特征,为人类HPSCs的体外扩增及代谢相关疾病的治疗提供了新的靶点。此外,研究还发现人类HPSCs的代谢表型是细胞固有特性,而非仅由低氧微环境诱导,这为后续研究HPSCs的代谢调控机制提供了重要基础。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。