RUNX1 promotes angiogenesis in colorectal cancer by regulating the crosstalk between tumor cells and tumor associated macrophages
RUNX1通过调节肿瘤细胞与肿瘤相关巨噬细胞之间的相互作用来促进结直肠癌的血管生成。
| 期刊: | Biomarker Research | 影响因子: | 9.500 |
| 时间: | 2024 | 起止号: | 2024 Feb 28;12(1):29. |
| doi: | 10.1186/s40364-024-00573-1 | 靶点: | RUNX1 |
| 研究方向: | 细胞生物学、肿瘤、免疫/内分泌 | 疾病类型: | 肠癌 |
| 细胞类型: | 巨噬细胞、肿瘤细胞 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:RUNX1 promotes angiogenesis in colorectal cancer by regulating the crosstalk between tumor cells and tumor associated macrophages;发表期刊:Biomarker Research;影响因子:未公开;研究领域:结直肠癌肿瘤微环境与血管生成。
结直肠癌(CRC)是全球范围内常见的恶性肿瘤之一,其发病率居恶性肿瘤第三位,死亡率居第二位,严重威胁人类健康。血管生成是CRC恶性进展的关键标志,它为肿瘤生长提供营养支持并促进转移,但目前临床抗血管生成治疗仅对少数患者有效,其潜在机制尚未完全阐明。Runt相关转录因子1(RUNX1)是一类参与造血和血管生成调控的重要转录因子,此前研究表明其在CRC中作为癌基因,通过激活Wnt/β-catenin、Hedgehog等通路促进肿瘤细胞增殖、转移及化疗耐药,但RUNX1在CRC血管生成中的作用及与肿瘤微环境(TME)中肿瘤相关巨噬细胞(TAMs)的串扰机制仍不清楚。针对这一研究空白,本研究旨在探究RUNX1介导的CRC细胞与M2型TAMs的相互作用及其与肿瘤血管生成的关系,揭示其潜在分子机制,为CRC的靶向治疗提供新的理论依据。
2. 文献综述解析
作者对现有研究的评述逻辑围绕三个核心维度展开:RUNX1在CRC中的功能、TAMs的极化状态与肿瘤进展的关系、血管生成的调控机制。现有研究结论显示,RUNX1在多种实体肿瘤中扮演“双重角色”,既可作为癌基因也可作为抑癌基因,而在CRC中其主要发挥促癌作用,通过激活多条信号通路促进肿瘤增殖、转移及化疗耐药;TAMs是TME中最丰富的免疫细胞群体,根据极化状态可分为促炎的M1型和促肿瘤的M2型,其中M2型TAMs通过分泌细胞因子(如IL-10、VEGF)促进血管生成、免疫逃逸及肿瘤进展,但RUNX1与TAMs的相互作用尚未被报道;血管生成是CRC恶性进展的关键环节,目前已知VEGF等因子是主要调控者,但RUNX1对血管生成的直接或间接调控作用仍缺乏研究。
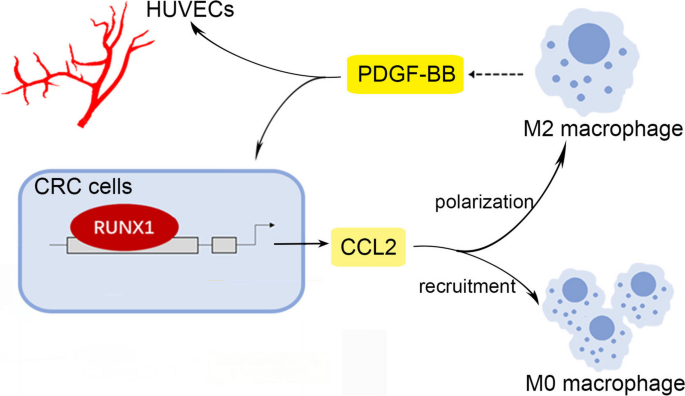
现有研究的局限性在于,缺乏RUNX1对CRC血管生成的具体机制探讨,以及RUNX1与TAMs相互作用在血管生成中的角色解析。本研究的创新价值在于,首次揭示了RUNX1通过促进趋化因子CCL2分泌和Hedgehog通路激活,招募并诱导TAMs向M2型极化,进而通过M2型TAMs分泌的血小板衍生生长因子BB(PDGF-BB)促进肿瘤血管生成,同时PDGF-BB可反式激活RUNX1表达,形成正反馈环路,这一发现填补了RUNX1在CRC血管生成中作用的空白,为CRC的联合靶向治疗提供了新的思路。
3. 研究思路总结与详细解析
本研究的整体框架围绕“RUNX1介导的CRC细胞与TAMs串扰对血管生成的影响及机制”展开,研究目标是明确RUNX1在CRC血管生成中的作用及与TAMs的相互作用机制,核心科学问题包括:RUNX1如何调控TAMs的招募与极化?RUNX1-TAMs串扰如何影响血管生成?其潜在分子通路是什么?技术路线遵循“生物信息学分析→临床样本验证→细胞实验机制探究→动物实验验证”的闭环逻辑。
3.1 生物信息学与临床样本验证
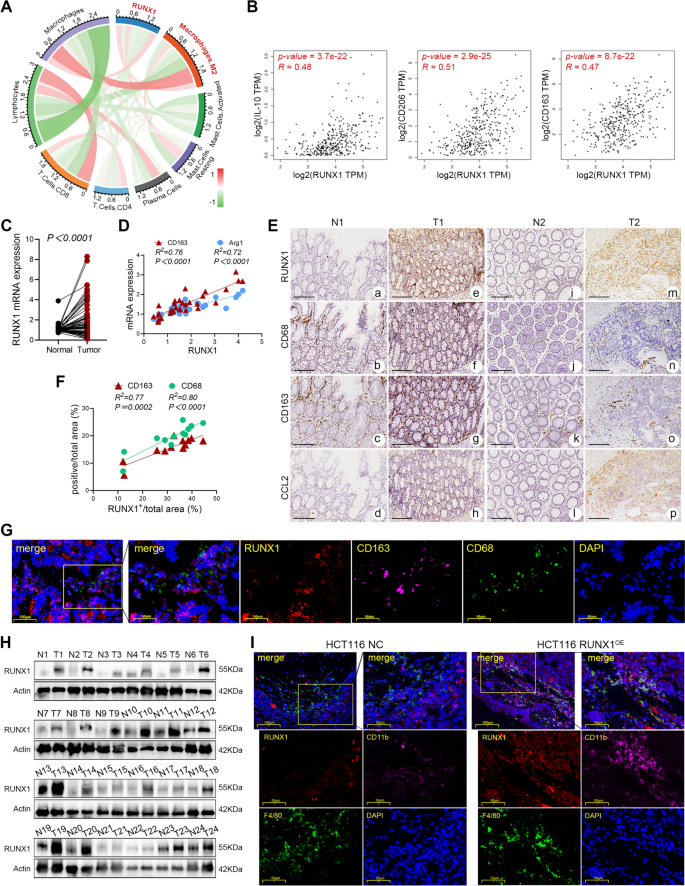
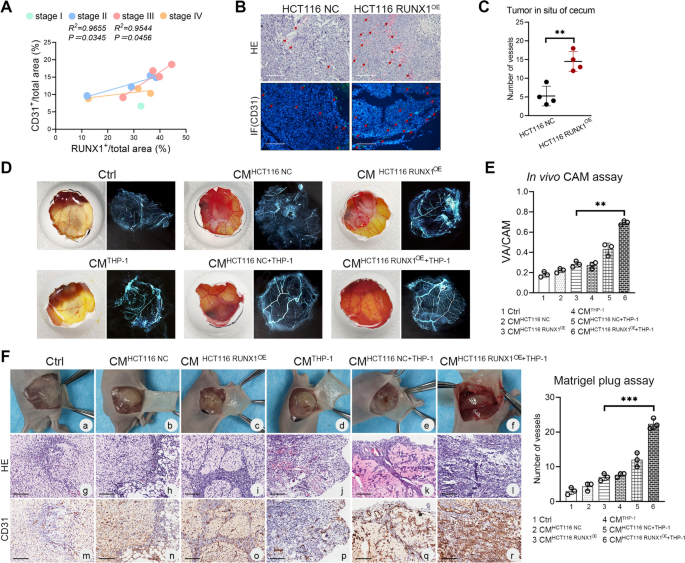
实验目的是通过生物信息学和临床样本分析,明确RUNX1与TAMs浸润、血管生成的相关性。方法上,利用TCGA、GEPIA、TIMER等数据库分析RUNX1与免疫细胞标记物(如CD163、CD206、IL-10)、血管生成相关基因(如SELE、CDH5、KDR)的表达关联;收集66对CRC临床样本进行qRT-PCR检测RUNX1 mRNA表达,24对样本进行Western blotting验证,12对样本进行免疫组化(IHC)分析RUNX1与TAMs标记物(CD68、CD163)、血管生成标记物(CD31)的相关性;通过多重免疫荧光(IF)染色验证RUNX1在肿瘤组织中的细胞定位。结果显示,RUNX1在CRC肿瘤组织中mRNA和蛋白水平均显著高表达(n=66,P<0.0001;n=24,20/24样本高表达);数据库分析及临床样本验证表明,RUNX1表达与M2型TAMs标记物(CD163、CD206、IL-10)呈正相关(P<0.05),与血管生成标记物(CD31)也呈正相关(P<0.05);多重IF染色显示RUNX1高表达位于肿瘤细胞而非巨噬细胞。实验所用关键产品:RUNX1抗体(Proteintech,25315-1-AP)、CD163抗体(ZSGB-BIO,ZM-0428)、CD31抗体(Proteintech,28083-1-AP)。
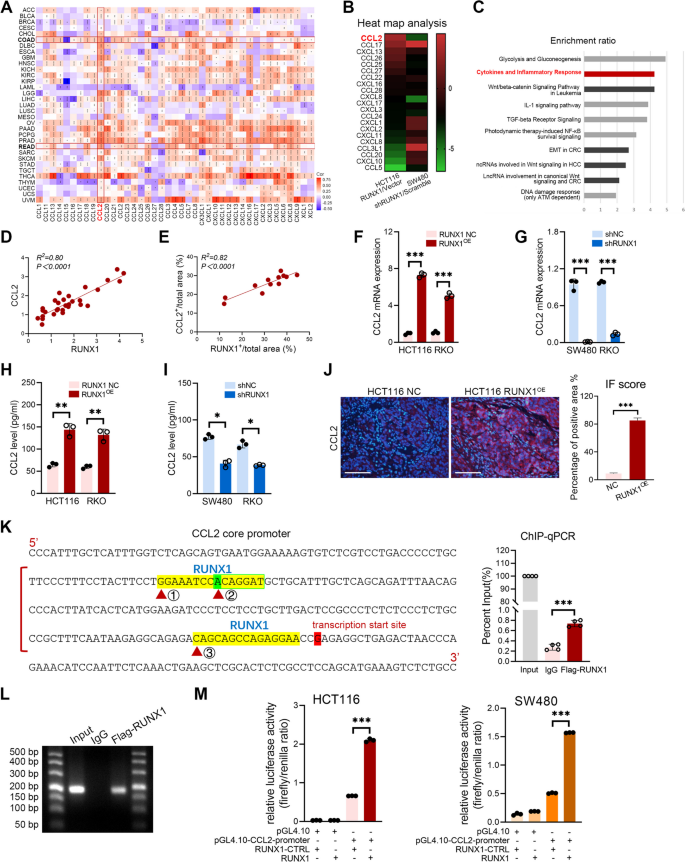
3.2 CRC细胞RUNX1对TAMs招募与极化的影响
实验目的是验证RUNX1是否通过分泌CCL2招募TAMs并诱导其向M2型极化。方法上,构建RUNX1过表达(HCT116、RKO)和敲低(SW480、RKO)CRC细胞系,收集条件培养基(CMs)处理THP-1细胞(经PMA诱导为M0型巨噬细胞);通过ELISA检测CMs中CCL2水平,ChIP-qPCR和双荧光素酶报告实验验证RUNX1对CCL2启动子的结合与调控;Flow cytometry检测THP-1细胞M2型标记物(CD68+CD206+、CD68+CD200R+)的表达,qRT-PCR检测M2相关基因(CD163、CD206、Arg1、IL-10)的mRNA水平,Western blotting检测Hedgehog通路分子(PTCH1、GLI1、Shh)的表达,并用Hedgehog通路抑制剂GDC-0449进行rescue实验。结果显示,RUNX1过表达显著增加CCL2的mRNA和蛋白水平(P<0.05),且RUNX1可直接结合CCL2启动子的ACAGGAT区域(ChIP-qPCR验证);RUNX1过表达CMs处理后,THP-1细胞中M2型标记物及相关基因表达显著升高(P<0.05),Hedgehog通路分子表达激活,而GDC-0449处理可显著降低M2型细胞比例(P<0.01);RUNX1敲低则呈现相反结果。实验所用关键产品:PMA(分化THP-1)、GDC-0449(Hedgehog抑制剂)、CCL2抗体(Proteintech,25542-1-AP)。
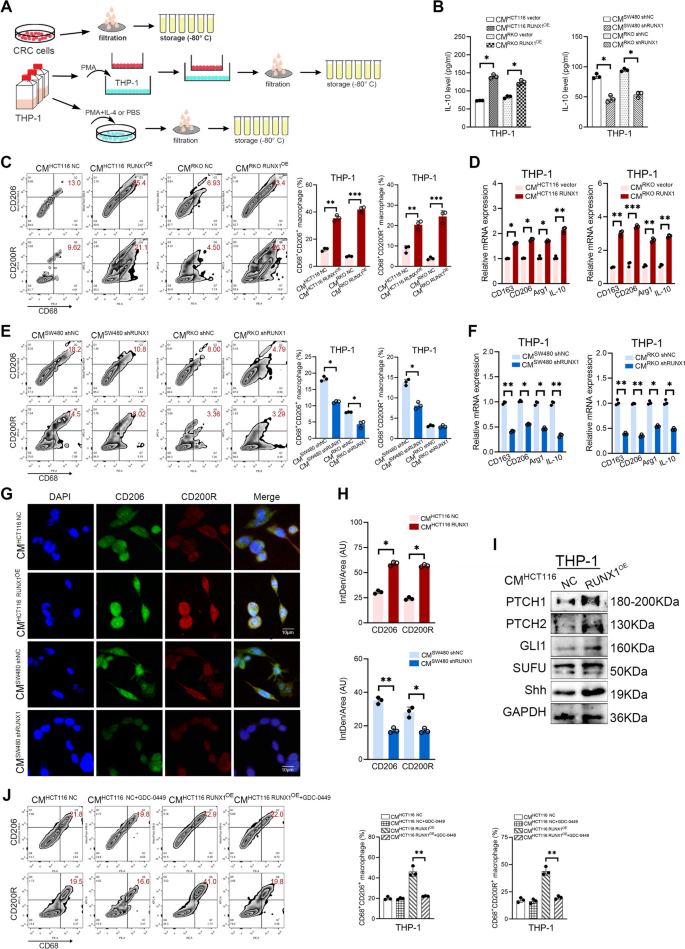
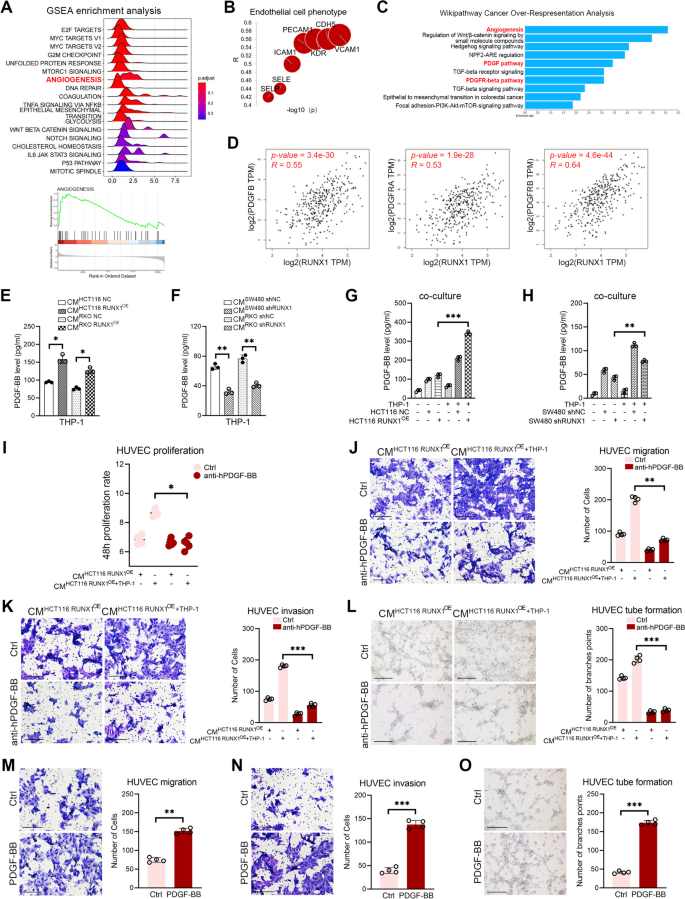
3.3 RUNX1介导的CRC细胞与TAMs串扰对血管生成的影响
实验目的是探究RUNX1-TAMs串扰对CRC血管生成的作用。方法上,将RUNX1过表达/敲低CRC细胞与THP-1细胞共培养,收集共培养CMs处理人脐静脉内皮细胞(HUVEC),进行细胞增殖(CCK-8)、迁移(Transwell)、侵袭(Transwell)及管形成(Matrigel)实验;通过鸡胚绒毛尿囊膜(CAM)实验、裸鼠Matrigel plug实验及原位瘤模型,检测体内血管生成情况;用PDGF-BB中和抗体验证其在血管生成中的作用。结果显示,RUNX1过表达共培养CMs显著促进HUVEC的增殖(P<0.05)、迁移(P<0.01)、侵袭(P<0.001)及管形成(P<0.001),而PDGF-BB中和抗体可逆转这些效应;体内实验中,RUNX1过表达组CAM血管面积比例(P<0.01)、Matrigel plug血管数目(P<0.001)及原位瘤血管密度(P<0.01)均显著高于对照组。实验所用关键产品:Matrigel(Corning,354248)、HUVEC细胞、PDGF-BB中和抗体。
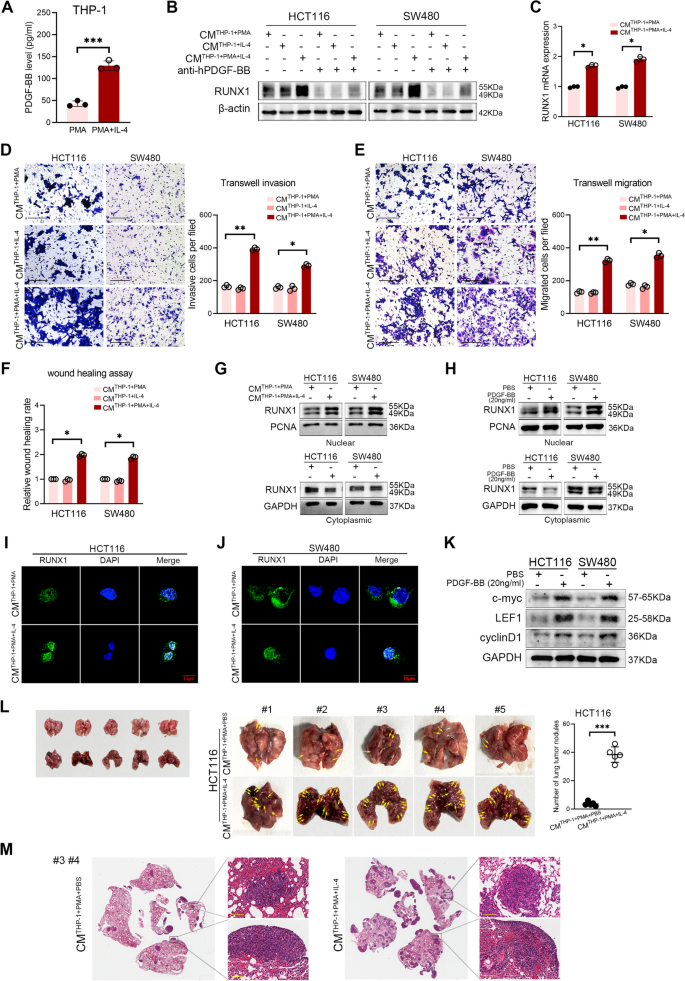
3.4 PDGF-BB对CRC细胞RUNX1表达及恶性行为的影响
实验目的是验证PDGF-BB对RUNX1的反馈调控及对CRC恶性行为的影响。方法上,用IL-4诱导THP-1细胞为M2型,收集CMs处理CRC细胞(HCT116、SW480),或用外源性PDGF-BB处理,通过WB、qRT-PCR检测RUNX1的mRNA和蛋白水平;进行迁移(Transwell)、侵袭(Transwell)及伤口愈合实验验证CRC细胞恶性行为;通过Western blotting检测RUNX1在细胞质和细胞核中的分布,以及Wnt/β-catenin通路分子(c-myc、LEF1、cyclinD1)的表达;构建裸鼠肺转移模型,验证PDGF-BB对CRC转移的影响。结果显示,M2型TAMs CMs或外源性PDGF-BB可显著增加RUNX1的mRNA和蛋白水平(P<0.05),并促进其核转位;PDGF-BB处理显著增强CRC细胞的迁移、侵袭及伤口愈合能力(P<0.05),同时激活Wnt/β-catenin通路;肺转移模型显示,M2型CMs处理的CRC细胞肺转移结节数目显著增加(n=5,P<0.001)。实验所用关键产品:IL-4(诱导M2极化)、PDGF-BB蛋白、Wnt通路分子抗体(c-myc、LEF1、cyclinD1)。
4. Biomarker研究及发现成果解析
Biomarker定位:本研究中RUNX1作为CRC血管生成与TAMs串扰的功能性生物标志物,其筛选与验证逻辑遵循“数据库分析→临床样本验证→细胞/动物实验机制验证”的完整链条。研究过程中,RUNX1的来源为CRC临床样本及细胞系,验证方法包括:通过qRT-PCR和Western blotting检测其在肿瘤组织中的表达水平;通过IHC和IF染色分析其与TAMs标记物、血管生成标记物的相关性;通过细胞实验验证其对TAMs极化和血管生成的调控作用;通过动物实验验证其在体内的功能。
特异性与敏感性方面,临床样本中RUNX1高表达与M2型TAMs浸润(CD163、CD206)、血管生成(CD31)呈显著正相关(P<0.05),提示其作为M2型TAMs和血管生成的关联标志物具有较好的特异性;数据库分析显示RUNX1在CRC中的表达显著高于正常组织(GEPIA分析),临床样本中RUNX1 mRNA高表达率达83.3%(55/66),提示其具有一定的敏感性。
核心成果方面,RUNX1被证实是CRC血管生成的关键调控因子,通过与M2型TAMs的串扰促进血管生成,并通过PDGF-BB形成正反馈环路,增强肿瘤恶性行为;统计学结果显示,临床样本中RUNX1 mRNA在肿瘤组织中显著高表达(n=66,P<0.0001),与CD163 mRNA表达呈正相关(n=30,P<0.05);动物实验中,RUNX1过表达组原位瘤血管数目显著增加(n=3,P<0.01),M2型CMs处理组肺转移结节数目显著增加(n=5,P<0.001)。本研究首次将RUNX1与TAMs串扰及血管生成关联,为CRC的靶向治疗提供了新的潜在biomarker。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。