Flavivirus prM interacts with MDA5 and MAVS to inhibit RLR antiviral signaling
黄病毒 prM 与 MDA5 和 MAVS 相互作用抑制 RLR 抗病毒信号传导
| 期刊: | Cell and Bioscience | 影响因子: | 6.100 |
| 时间: | 2023 | 起止号: | 2023 Jan 13;13(1):9. |
| doi: | 10.1186/s13578-023-00957-0 | 研究方向: | 微生物学 |
文献解析
1. 领域背景与文献引入
文献英文标题:Flavivirus prM interacts with MDA5 and MAVS to inhibit RLR antiviral signaling;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:黄病毒免疫逃逸与天然免疫信号通路调控
领域共识:黄病毒科虫媒病毒是全球新发和再发传染病的重要病原体,涵盖蜱传脑炎病毒、寨卡病毒、西尼罗病毒、登革病毒等,可引起脑炎、出血热、胎儿畸形等严重疾病,全球超40%人口面临登革病毒感染风险,年感染量超5000万。天然免疫中的I型干扰素(IFN-I)是宿主抗病毒的第一道防线,通过视黄酸诱导基因I样受体(RLR)通路识别胞质病毒RNA,其中维甲酸诱导基因I(RIG-I)、黑色素瘤分化相关蛋白5(MDA5)作为核心受体,招募线粒体抗病毒信号蛋白(MAVS)后激活TANK结合激酶1(TBK1)和IKKε,进而诱导干扰素调节因子3(IRF3)二聚化和核转位,启动IFN-I及干扰素刺激基因(ISG)表达。黄病毒进化出多种免疫逃逸策略以拮抗IFN-I通路,现有研究主要聚焦于非结构蛋白(如NS1、NS2A、NS5)的作用,而结构蛋白(如前体膜蛋白(prM))在免疫逃逸中的功能及分子机制尚未系统阐明,部分研究存在矛盾结论(如寨卡病毒prM可能抑制干扰素但机制未明,登革病毒prM被报道无此作用),这一研究空白限制了对黄病毒致病机制的全面理解,也为新型治疗靶点和疫苗开发带来瓶颈。本研究针对这一核心问题,系统解析黄病毒prM蛋白对RLR抗病毒信号通路的调控作用及分子机制,具有重要的学术价值和临床转化意义。
2. 文献综述解析
作者以黄病毒蛋白的功能分类(结构蛋白vs非结构蛋白)为核心评述逻辑,系统梳理了黄病毒免疫逃逸领域的现有研究进展,明确了结构蛋白在免疫逃逸中的研究缺口。现有研究证实,黄病毒非结构蛋白是免疫逃逸的主要效应分子,例如西尼罗病毒NS1通过结合RIG-I和MDA5抑制IFN-I产生,登革病毒NS2B3切割干扰素刺激基因刺激蛋白(STING),寨卡、登革、黄热病毒NS5通过结合STAT2抑制JAK-STAT通路;这些研究主要采用细胞转染、荧光素酶报告实验、免疫共沉淀等技术,在细胞水平验证了非结构蛋白的功能,但部分研究存在样本量有限、缺乏体内验证的局限性。针对结构蛋白,早期研究认为其主要参与病毒组装和成熟,prM作为M蛋白的前体,主要功能是辅助E蛋白折叠和病毒粒子成熟,仅少数研究提及寨卡病毒prM可能抑制干扰素但机制未明,登革病毒prM被报道无此作用,相关结论存在争议且机制解析不足。本文创新价值在于,首次系统对比了6种黄病毒prM蛋白的免疫逃逸功能,明确了不同黄病毒prM通过结合MDA5和/或MAVS抑制RLR通路的分子机制,填补了黄病毒结构蛋白免疫逃逸研究的空白,为黄病毒致病机制的统一解析提供了新视角。
3. 研究思路总结与详细解析
本研究以“筛选黄病毒中抑制IFN-I的蛋白→验证prM的功能→解析分子机制→扩展至多种黄病毒→验证对病毒复制的影响”为闭环技术路线,核心研究目标是阐明黄病毒prM蛋白的免疫逃逸功能及分子机制,解决的核心科学问题是prM如何调控RLR抗病毒信号通路,以及不同黄病毒prM的作用是否存在物种特异性差异。
3.1 蜱传脑炎病毒(TBEV)蛋白筛选与prM抑制干扰素作用验证
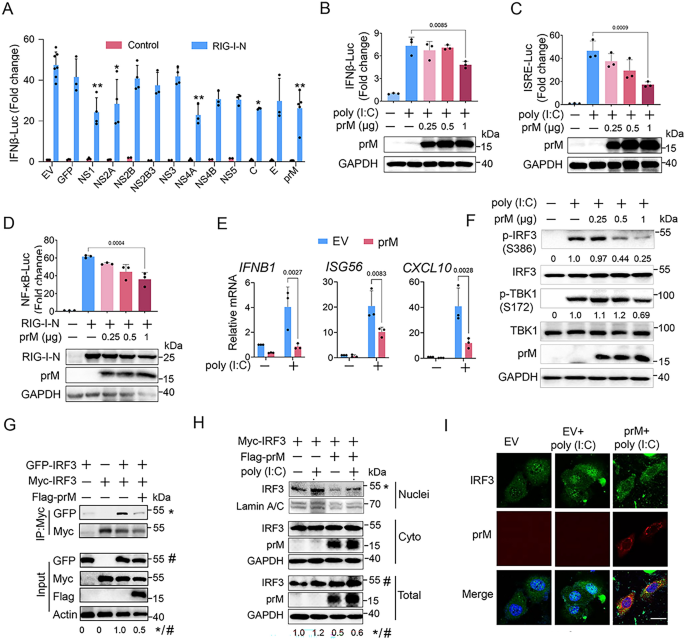
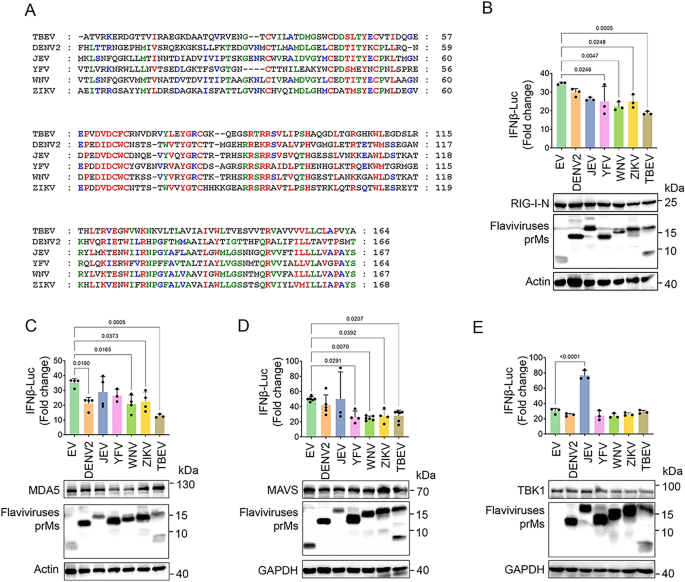
实验目的为筛选TBEV中能够抑制I型干扰素产生的病毒蛋白,并验证prM蛋白的具体作用。研究采用人胚肾HEK293T细胞、人神经母细胞瘤DAOY细胞等细胞模型,转染TBEV各结构蛋白(prM、C、E)和非结构蛋白(NS1、NS2A等)质粒,结合poly(I:C)(病毒RNA模拟物)、RIG-I-N(RIG-I激活域)等RLR通路激活剂,通过荧光素酶报告实验检测IFNβ、干扰素敏感应答元件(ISRE)、NF-κB启动子活性,实时荧光定量PCR(qPCR)检测IFNB1、ISG56、CXCL10的mRNA表达水平,免疫印迹(Western Blot,WB)检测IRF3和TBK1的磷酸化水平、IRF3的二聚化及核转位,免疫荧光共定位观察IRF3的核转位情况。结果显示,荧光素酶报告实验表明TBEV prM能显著抑制poly(I:C)或RIG-I-N诱导的IFNβ、ISRE、NF-κB启动子活性(n=3,P<0.01);qPCR结果显示prM过表达显著降低IFNB1、ISG56、CXCL10的mRNA水平(n=3,P<0.05);免疫印迹结果显示prM减少poly(I:C)诱导的IRF3和TBK1磷酸化,抑制IRF3二聚化和核转位;免疫荧光结果进一步证实prM阻断IRF3的核转位。文献未提及具体实验产品,领域常规使用荧光素酶报告试剂盒、SYBR Green qPCR试剂盒、磷酸化IRF3抗体等。
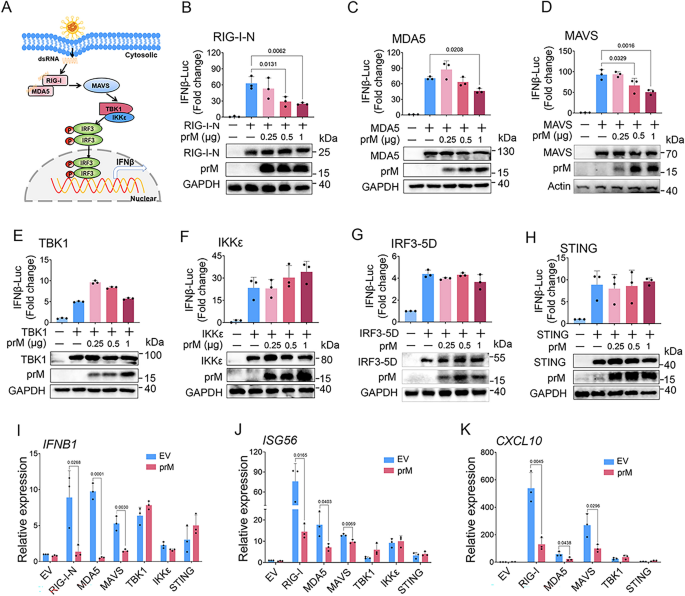
3.2 prM对RLR通路关键节点的调控定位
实验目的为明确prM在RLR信号通路中的作用靶点(上游或下游节点)。研究在HEK293T细胞中分别过表达RLR通路关键分子(RIG-I-N、MDA5、MAVS、TBK1、IKKε、组成型激活的IRF3-5D、STING),同时转染prM质粒,通过荧光素酶报告实验检测IFNβ启动子活性,qPCR检测IFNB1、ISG56、CXCL10的mRNA水平。结果显示,荧光素酶报告实验表明prM能剂量依赖性抑制RIG-I-N、MDA5、MAVS诱导的IFNβ启动子活性,但对TBK1、IKKε、IRF3-5D、STING诱导的活性无显著影响;qPCR结果进一步证实prM抑制RIG-I-N、MDA5、MAVS诱导的IFNB1等基因表达(n=3,P<0.05),表明prM的作用靶点位于MAVS或其上游的RLR受体。文献未提及具体实验产品,领域常规使用基因过表达质粒、荧光素酶检测系统等。
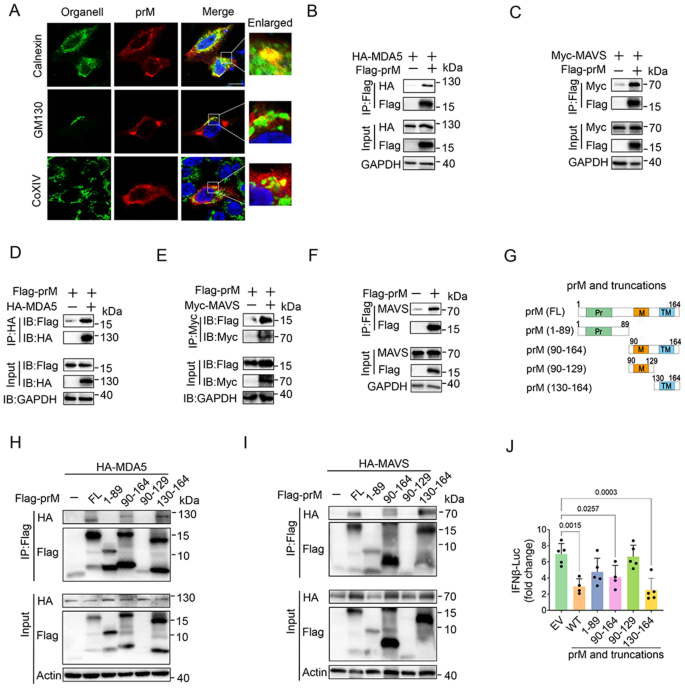
3.3 prM与MDA5、MAVS的相互作用及结构域鉴定
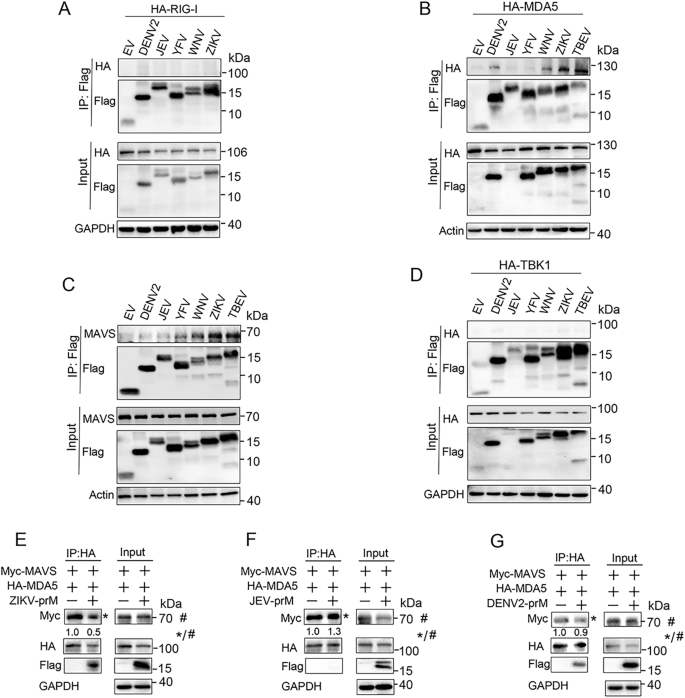
实验目的为验证prM与RLR通路分子的相互作用,并鉴定关键结合结构域。研究通过免疫荧光共定位观察prM与RIG-I、MDA5、MAVS等的亚细胞定位,采用免疫共沉淀(正向、反向)、荧光共振能量转移(FRET)技术验证蛋白相互作用;构建TBEV prM的截断体(N端1-89aa、成熟M区90-164aa、跨膜区130-164aa等),通过免疫共沉淀鉴定与MDA5、MAVS结合的关键结构域,同时通过荧光素酶报告实验验证截断体的功能。结果显示,免疫荧光显示prM主要定位于内质网和线粒体,与MDA5、MAVS共定位;免疫共沉淀和FRET实验证实prM与MDA5、MAVS直接结合,且能结合内源性MAVS,但与RIG-I、TBK1、IKKε、IRF3无显著相互作用;截断体实验显示,prM的成熟M区(90-164aa)和跨膜区(130-164aa)是结合MDA5和MAVS的关键结构域,且这两个区域也能抑制poly(I:C)诱导的IFNβ启动子活性(n=3,P<0.05)。文献未提及具体实验产品,领域常规使用免疫共沉淀试剂盒、FRET检测系统、蛋白截断体质粒等。
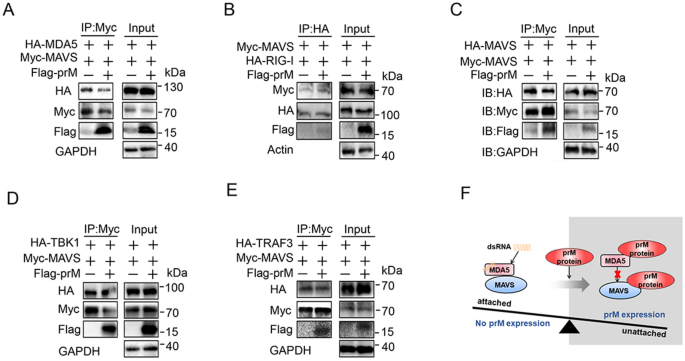
3.4 prM干扰MDA5-MAVS复合物形成的机制验证
实验目的为探究prM抑制RLR通路的具体分子机制,是否通过干扰MDA5与MAVS的相互作用实现。研究在HEK293T细胞中共转染MDA5、MAVS和prM质粒,通过免疫共沉淀检测MDA5与MAVS的结合水平,免疫荧光共定位观察MDA5与MAVS的共定位情况。结果显示,免疫共沉淀结果表明prM过表达显著降低MDA5与MAVS的结合水平;免疫荧光结果进一步证实prM破坏了MDA5与MAVS的共定位,表明prM通过结合MDA5和MAVS,干扰二者复合物的形成,进而阻断RLR信号传导。文献未提及具体实验产品,领域常规使用免疫共沉淀试剂盒、激光共聚焦显微镜等。
3.5 多种黄病毒prM的免疫逃逸作用及机制差异分析
实验目的为验证其他黄病毒(登革2型、日本脑炎、黄热、西尼罗、寨卡)prM的免疫逃逸功能,并分析机制差异。研究克隆上述5种黄病毒的prM基因,构建过表达质粒,在HEK293T细胞中分别与RIG-I-N、MDA5、MAVS、TBK1共转染,通过荧光素酶报告实验检测IFNβ启动子活性,qPCR检测IFNB1等基因表达;通过免疫共沉淀检测prM与MDA5、MAVS的相互作用,验证是否干扰二者复合物形成。结果显示,荧光素酶报告实验表明西尼罗、寨卡病毒prM能抑制RIG-I-N、MDA5、MAVS诱导的IFNβ启动子活性,黄热病毒prM抑制RIG-I-N、MAVS诱导的活性,登革2型病毒prM仅抑制MDA5诱导的活性,日本脑炎病毒prM无显著抑制作用;免疫共沉淀显示,西尼罗、寨卡病毒prM与MDA5和MAVS均结合,且干扰二者复合物形成,登革2型病毒prM仅结合MDA5,黄热病毒prM仅结合MAVS,日本脑炎病毒prM无结合。文献未提及具体实验产品,领域常规使用多种黄病毒基因克隆载体、免疫共沉淀试剂等。
3.6 prM促进病毒复制的功能验证
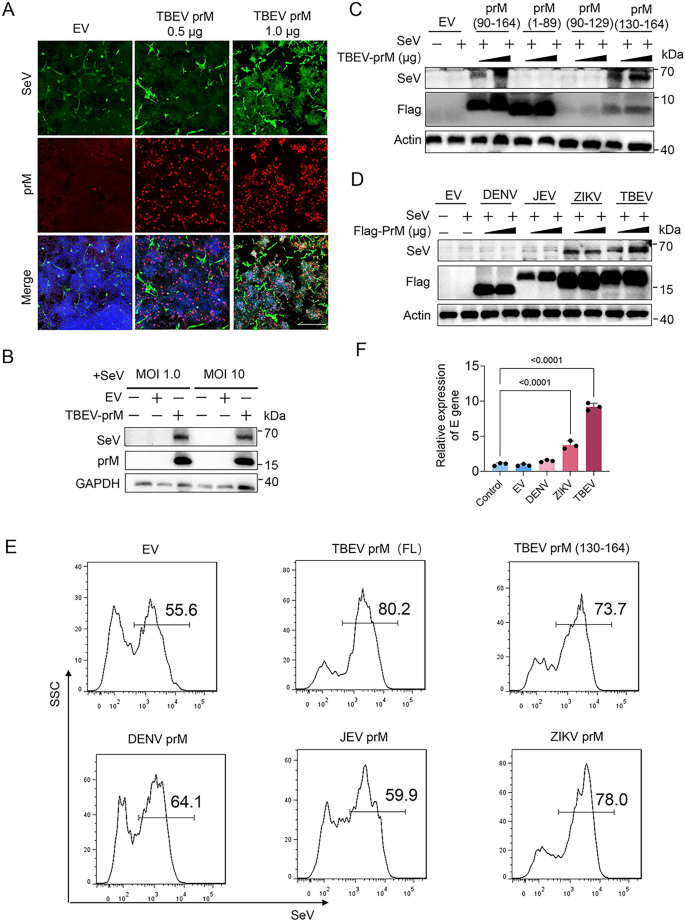
实验目的为验证prM的免疫逃逸功能是否能促进病毒复制。研究在HEK293T细胞中转染TBEV、寨卡、登革2型、日本脑炎病毒prM质粒,感染仙台病毒(SeV)或TBEV,通过免疫荧光、流式细胞术、免疫印迹检测病毒复制水平,探针qPCR检测TBEV病毒载量。结果显示,免疫荧光和流式细胞术表明TBEV prM能剂量依赖性促进SeV复制,1μg转染组的SeV阳性细胞比例显著高于0.5μg组(n=3,P<0.05);免疫印迹显示TBEV、寨卡病毒prM过表达显著增加SeV蛋白水平;探针qPCR显示TBEV、寨卡病毒prM显著促进TBEV复制(n=3,P<0.05),而登革2型、日本脑炎病毒prM无显著作用。文献未提及具体实验产品,领域常规使用病毒感染模型、流式细胞仪、qPCR探针等。
4. Biomarker研究及发现成果
本研究中,黄病毒prM蛋白作为功能型Biomarker,其免疫逃逸活性与黄病毒的致病性密切相关,研究通过“细胞水平筛选→分子机制验证→多物种对比→功能验证”的完整逻辑链,明确了prM的免疫逃逸功能及分子机制。Biomarker定位:prM是黄病毒的结构蛋白,属于功能型Biomarker,筛选逻辑为:首先从TBEV中筛选出抑制IFN-I的蛋白,然后验证其与RLR通路分子的相互作用,进而扩展至多种黄病毒,明确不同物种prM的功能差异。研究过程详述:prM来源于黄病毒基因组编码的结构蛋白,验证方法包括免疫共沉淀、免疫荧光共定位、FRET、截断体实验等;特异性方面,TBEV、寨卡、西尼罗病毒prM能同时结合MDA5和MAVS,登革2型病毒prM仅结合MDA5,黄热病毒prM仅结合MAVS,日本脑炎病毒prM无结合活性;敏感性方面,prM过表达能显著抑制IFN-I产生,TBEV和寨卡病毒prM能显著促进病毒复制(n=3,P<0.05)。核心成果提炼:prM通过结合MDA5和/或MAVS抑制RLR抗病毒信号通路,促进病毒复制;其中TBEV和寨卡病毒prM的免疫逃逸活性最强,与病毒致病性正相关;本研究首次系统揭示了黄病毒结构蛋白prM的免疫逃逸机制,创新性在于明确了不同黄病毒prM作用的物种特异性,为黄病毒的致病机制解析、治疗靶点筛选和疫苗开发提供了新的理论依据;相关统计学结果显示,prM对IFNβ启动子活性的抑制作用及对病毒复制的促进作用均具有统计学显著性(P<0.05或P<0.01,n=3)。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。