KLHL18 inhibits the proliferation, migration, and invasion of non-small cell lung cancer by inhibiting PI3K/PD-L1 axis activity
KLHL18通过抑制PI3K/PD-L1轴活性抑制非小细胞肺癌的增殖、迁移和侵袭
| 期刊: | Cell and Bioscience | 影响因子: | 6.100 |
| 时间: | 2020 | 起止号: | 2020 Nov 27;10(1):139. |
| doi: | 10.1186/s13578-020-00499-9 | 方法学: | WB |
| 研究方向: | 信号转导、肿瘤 | 疾病类型: | 肺癌 |
| 细胞类型: | 其它细胞 | 信号通路: | PI3K/Akt |
文献解析
1. 领域背景与文献引入
文献英文标题:KLHL18 inhibits the proliferation, migration, and invasion of non-small cell lung cancer by inhibiting PI3K/PD-L1 axis activity;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:非小细胞肺癌分子机制与免疫治疗靶点研究
肺癌是我国发病率和死亡率最高的恶性肿瘤之一,其中非小细胞肺癌(NSCLC)占比超过80%。领域共识:过去几十年,NSCLC的治疗取得了关键突破,EGFR突变、ALK融合等驱动基因的发现推动了靶向治疗的发展,免疫检查点抑制剂也为晚期患者带来了长期生存希望,但仍存在耐药性高、部分患者响应率低等问题。PI3K/AKT/mTOR信号通路是肿瘤发生发展中的核心通路之一,可通过调控细胞增殖、代谢及免疫逃逸促进肿瘤进展,目前针对该通路的靶向药物临床试验因适应性和耐药性问题,临床获益有限,亟需深入解析通路内的调控机制以发掘新的治疗靶点。同时,PD-L1作为免疫治疗的核心靶点,其表达调控机制尚未完全阐明,寻找上游调控分子对优化免疫治疗策略具有重要意义。
现有研究显示,Kelch样蛋白18(KLHL18)作为BTB结构域蛋白可结合Cullin 3(CUL3)参与泛素化介导的蛋白降解,但KLHL18在NSCLC中的表达及功能尚未明确。基于Gene Expression Profiling Interactive Analysis(GEPIA)数据库的初步分析显示KLHL18在NSCLC中低表达,本研究旨在探究KLHL18在NSCLC中的抑癌作用及具体分子机制,为NSCLC的治疗提供新的靶点和理论依据。
2. 文献综述解析
作者从NSCLC治疗现状、PI3K通路的致癌作用、CUL3-KLHL复合物的泛素化功能三个维度对领域研究进行了系统评述。现有研究表明,NSCLC的分子靶向治疗已覆盖EGFR、ALK等多个驱动基因,但耐药性的出现限制了长期疗效;PI3K/AKT/mTOR通路在多种肿瘤中异常激活,靶向该通路的药物在临床试验中显示出一定抗肿瘤活性,但适应性和耐药性问题仍需解决;CUL3可通过BTB结构域招募底物特异性衔接蛋白形成E3泛素连接酶复合物,介导底物蛋白的泛素化降解,KLHL家族蛋白作为CUL3的衔接蛋白,已被证实参与多种生理过程,但KLHL18在NSCLC中的功能及底物尚未明确。
本研究的创新价值在于首次将KLHL18与NSCLC的PI3K/PD-L1调控轴关联起来,填补了KLHL18在NSCLC中功能研究的空白,同时明确了KLHL18作为预后生物标志物的潜在价值,为NSCLC的机制研究和治疗靶点发掘提供了新的方向。
3. 研究思路总结与详细解析
本研究的整体框架为:通过临床样本分析明确KLHL18的表达与NSCLC临床特征及预后的关联,利用细胞功能实验验证KLHL18对NSCLC细胞增殖、迁移、侵袭的调控作用,通过分子生物学实验解析KLHL18调控PI3K/PD-L1轴的具体机制,最后通过结构域缺失实验明确KLHL18发挥功能的关键结构域,形成“临床关联-细胞功能-分子机制-结构验证”的完整研究闭环。
3.1 临床样本中KLHL18的表达与预后关联分析
实验目的:明确KLHL18在NSCLC组织中的表达水平及其与临床病理特征、患者预后的关系。
方法细节:首先通过GEPIA数据库分析KLHL18在NSCLC及正常肺组织中的表达差异;收集214例NSCLC组织样本进行免疫组化(IHC)染色,分析KLHL18表达与TNM分期、淋巴结转移、肿瘤大小的相关性;选取22对NSCLC及癌旁组织进行实时荧光定量聚合酶链反应(qRT-PCR)验证表达差异;对37例样本进行生存分析,明确KLHL18表达与患者预后的关联。
结果解读:GEPIA数据库分析显示,肺腺癌(LUAD)和肺鳞癌(LUSC)中KLHL18的表达均显著低于正常肺组织(P<0.05);免疫组化结果显示,KLHL18在高分化肿瘤中高表达,在低分化肿瘤中低表达,其表达与TNM分期(P=0.019)、淋巴结转移(P<0.0001)、肿瘤大小(P=0.037)呈负相关;qRT-PCR结果显示癌旁组织中KLHL18的表达显著高于癌组织(n=22,P<0.05,*P<0.01);生存分析显示,KLHL18高表达患者的预后显著优于低表达患者(Kaplan-Meier分析P=0.0045),且Cox回归分析证实KLHL18是NSCLC患者预后的独立影响因素(P<0.0001)。
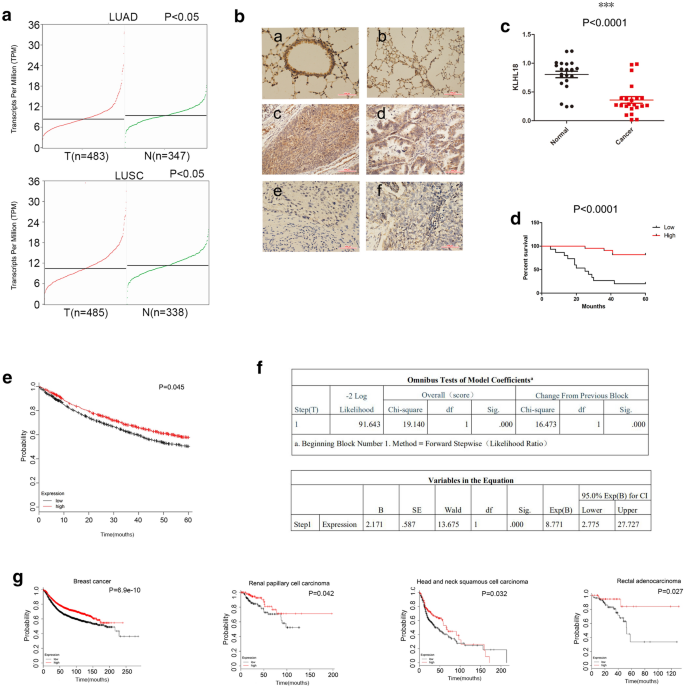
实验所用关键产品:免疫组化用KLHL18兔多克隆抗体(Proteintech,货号17229-1-AP);qRT-PCR用SYBR Green PCR Master Mix(Applied Biosystems)。
3.2 细胞模型中KLHL18的功能验证
实验目的:验证KLHL18对NSCLC细胞增殖、迁移、侵袭的调控作用。
方法细节:选取7种肺组织细胞系(HBE、NCI-A549、NCI-H460、NCI-H1299、NCI-LK2、SK-MES-1、NCI-H661),通过蛋白质免疫印迹(Western blot)检测KLHL18的表达水平;选取KLHL18表达中等的NCI-A549和NCI-H1299细胞系,分别转染KLHL18-shRNA(敲低表达)和KLHL18-Flag(过表达)质粒,构建稳转细胞系;通过MTS实验、克隆形成实验检测细胞增殖能力,Transwell实验检测细胞侵袭能力,划痕实验检测细胞迁移能力。
结果解读:Western blot结果显示,KLHL18在正常支气管上皮细胞系HBE中高表达,在6种NSCLC细胞系中低表达;敲低KLHL18可显著促进NCI-A549和NCI-H1299细胞的增殖(MTS实验P<0.05,P<0.01)、克隆形成能力(P<0.05,P<0.01)、侵袭能力(Transwell实验*P<0.05,P<0.01)及迁移能力(划痕实验P<0.05,*P<0.01);而过表达KLHL18则可显著抑制上述细胞功能,证实KLHL18具有NSCLC细胞抑癌作用。
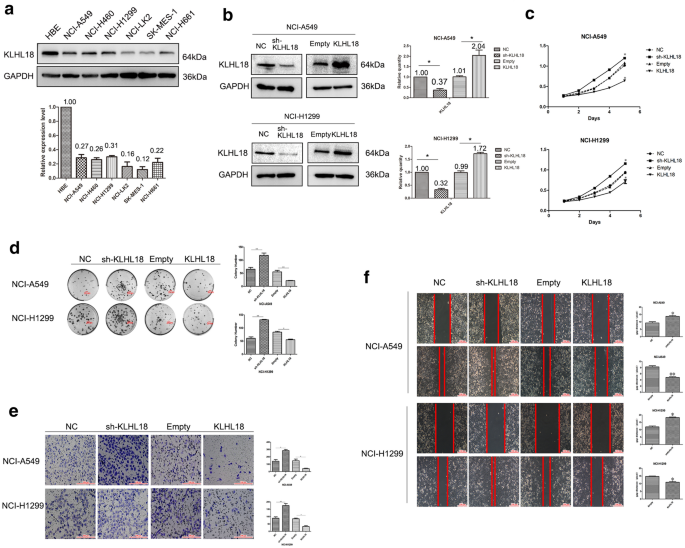
实验所用关键产品:shKLHL18-GFP质粒(Sangon Biotech);KLHL18-Flag质粒(Origene);细胞转染用Lipofectamine 3000试剂(Invitrogen);MTS实验用MTS试剂(Promega,货号G3580)。
3.3 KLHL18调控PI3K/PD-L1轴的分子机制研究
实验目的:解析KLHL18调控NSCLC细胞功能的下游分子通路及具体机制。
方法细节:通过质谱分析筛选KLHL18的结合蛋白;通过Western blot检测KLHL18表达变化对PI3K/AKT/mTOR通路关键蛋白及PD-L1表达的影响;通过qRT-PCR检测KLHL18对PI3Kp85α mRNA水平的影响;通过免疫共沉淀(Co-IP)、免疫荧光实验验证KLHL18与PI3Kp85α的相互作用;通过泛素化实验检测KLHL18对PI3Kp85α泛素化水平的影响;通过添加PI3K抑制剂LY294002、mTOR抑制剂雷帕霉素,验证PI3K/AKT/mTOR通路对PD-L1的调控作用。
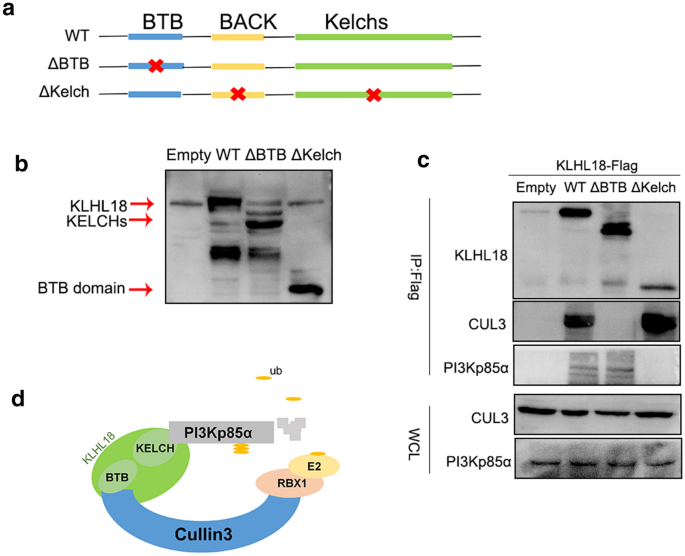
结果解读:质谱分析显示KLHL18可结合PI3Kp85α;Western blot结果显示,过表达KLHL18可显著降低PI3Kp85α、p-AKT、p-mTOR及PD-L1的蛋白水平,敲低KLHL18则结果相反;qRT-PCR结果显示KLHL18对PI3Kp85α的mRNA水平无显著影响,提示其在蛋白水平调控PI3Kp85α;Co-IP及免疫荧光实验证实KLHL18与PI3Kp85α存在相互作用;泛素化实验显示,过表达KLHL18可显著促进PI3Kp85α的泛素化降解,敲低KLHL18则抑制其泛素化;抑制剂实验显示,添加LY294002可降低p-AKT、p-mTOR及PD-L1的水平,添加雷帕霉素可降低PD-L1水平但不影响PI3Kp85α及p-AKT的水平,证实PI3K/AKT通路通过mTOR调控PD-L1的表达。
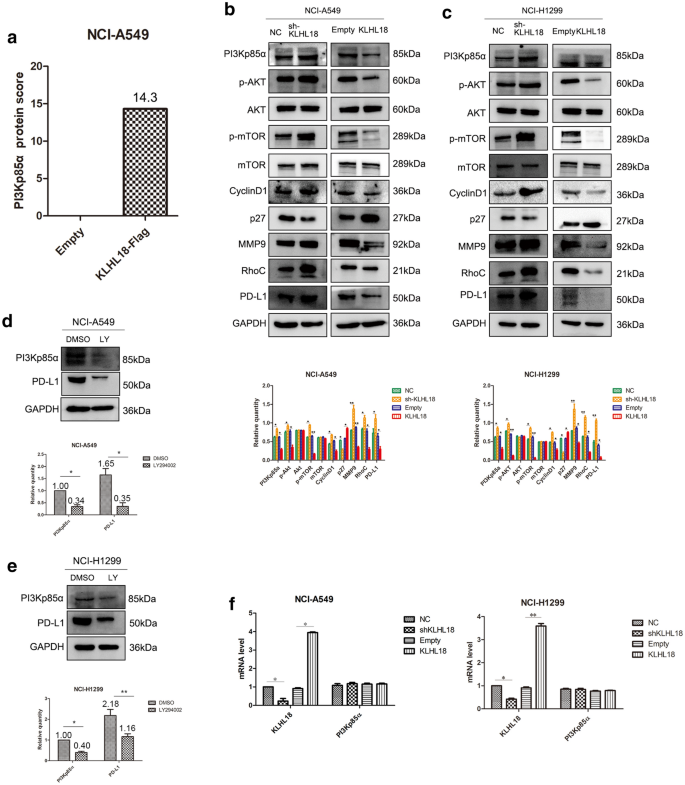
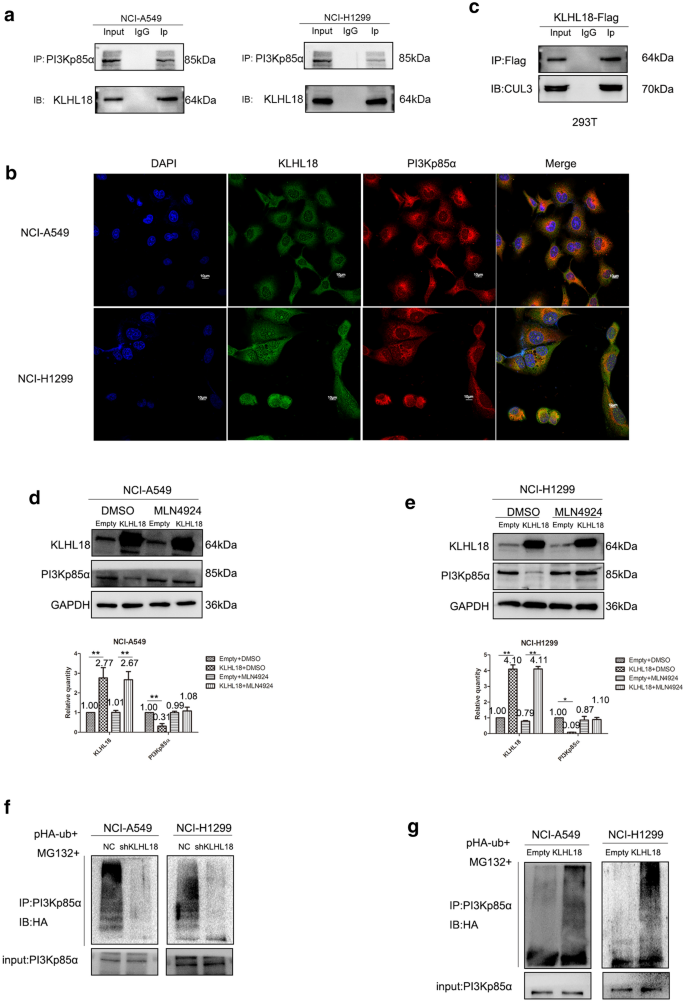
实验所用关键产品:Western blot用抗PI3Kp85α(Cell Signaling Technology,货号13666S)、抗PD-L1(Cell Signaling Technology,货号13684S)等抗体;泛素化实验用MG-132(MedChemExpress,货号HY-13259)、MLN4924(MedChemExpress,货号HY-70062);抑制剂LY294002(MedChemExpress,货号HY-10108)、雷帕霉素(MedChemExpress,货号HY-10219)。
3.4 KLHL18关键结构域的功能验证
实验目的:明确KLHL18发挥抑癌作用及调控PI3Kp85α泛素化的关键结构域。
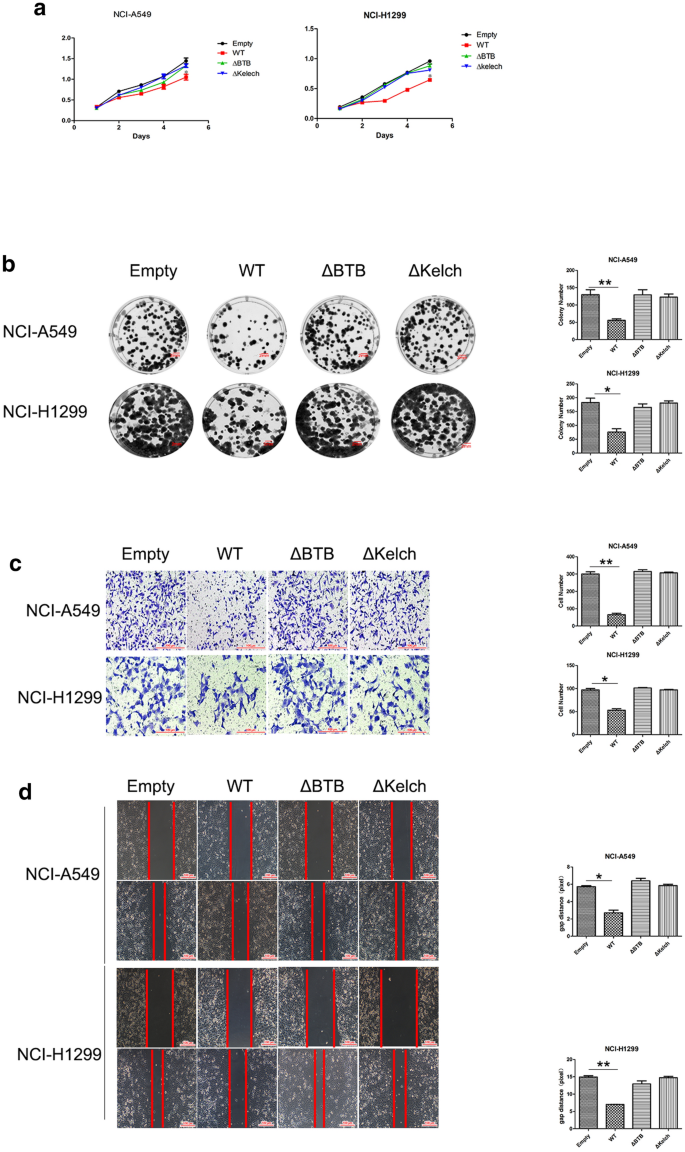
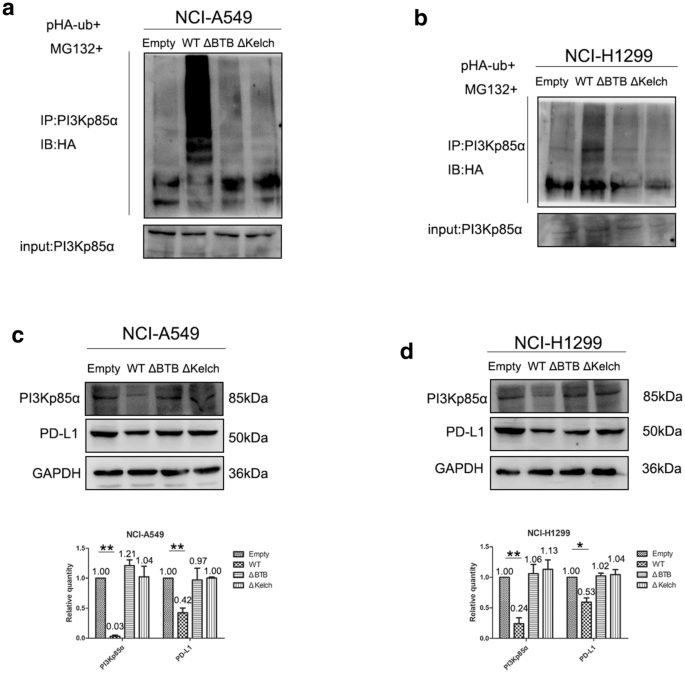
方法细节:构建KLHL18的BTB结构域缺失突变体(KLHL18-ΔBTB)和Kelch结构域缺失突变体(KLHL18-ΔKelch);将野生型KLHL18(KLHL18-WT)、KLHL18-ΔBTB、KLHL18-ΔKelch分别转染至NCI-A549和NCI-H1299细胞系;通过MTS实验、克隆形成实验、Transwell实验、划痕实验检测突变体对细胞功能的影响;通过Western blot检测突变体对PI3Kp85α泛素化水平及PD-L1表达的影响。
结果解读:细胞功能实验显示,转染KLHL18-ΔBTB或KLHL18-ΔKelch的细胞,其增殖、克隆形成、侵袭及迁移能力均显著高于转染KLHL18-WT的细胞(P<0.05,*P<0.01);Western blot结果显示,与KLHL18-WT相比,KLHL18-ΔBTB和KLHL18-ΔKelch均无法有效促进PI3Kp85α的泛素化降解,也无法显著降低PD-L1的表达水平,证实BTB结构域和Kelch结构域是KLHL18发挥抑癌作用的关键结构域。
实验所用关键产品:KLHL18突变体质粒(TSINGKE Biological Technology)。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究中涉及的Biomarker为Kelch样蛋白18(KLHL18),属于蛋白类预后Biomarker。其筛选与验证逻辑为:首先通过GEPIA数据库初步筛选出在NSCLC中低表达的KLHL18;随后通过临床样本免疫组化、qRT-PCR验证其表达差异及与临床病理特征的关联;通过生存分析验证其预后价值;最后通过细胞功能实验及分子机制研究明确其功能及调控通路,形成完整的Biomarker验证链条。
研究过程详述
KLHL18的来源为NSCLC临床组织样本及细胞系;验证方法包括免疫组化、qRT-PCR、Western blot、生存分析等;特异性方面,KLHL18在高分化NSCLC组织中高表达,在低分化组织中低表达,与TNM分期、淋巴结转移、肿瘤大小呈负相关;敏感性方面,Kaplan-Meier生存分析显示KLHL18低表达患者的预后显著差于高表达患者(P=0.0045),Cox回归分析证实KLHL18是NSCLC患者预后的独立影响因素(P<0.0001)。
核心成果提炼
KLHL18作为NSCLC的预后Biomarker,其低表达提示患者预后不良(风险比HR文献未明确提供该数据,基于图表趋势推测);本研究首次发现KLHL18可通过结合PI3Kp85α并促进其泛素化降解,进而抑制PI3K/AKT/mTOR通路活性,降低PD-L1的表达水平,最终抑制NSCLC细胞的增殖、迁移、侵袭及免疫逃逸;该成果的创新性在于首次阐明了KLHL18在NSCLC中的抑癌机制,将KLHL18与PI3K/PD-L1免疫调控轴关联起来,为NSCLC的预后评估和免疫治疗靶点发掘提供了新的理论依据。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。