Ouabain prevents pathological cardiac hypertrophy and heart failure through activation of phosphoinositide 3-kinase α in mouse
乌巴因通过激活小鼠磷酸肌醇 3-激酶 α 预防病理性心脏肥大和心力衰竭
| 期刊: | Cell and Bioscience | 影响因子: | 6.100 |
| 时间: | 2015 | 起止号: | 2015 Nov 18:5:64. |
| doi: | 10.1186/s13578-015-0053-7 | 种属: | Mouse |
| 研究方向: | 心血管 | 疾病类型: | 心力衰竭 |
文献解析
1. 领域背景与文献引入
文献英文标题:Ouabain prevents pathological cardiac hypertrophy and heart failure through activation of phosphoinositide 3-kinase α in mouse;发表期刊:Cell Bioscience;影响因子:3.58(2015年);研究领域:心血管疾病(病理性心肌肥厚与心力衰竭机制)。
病理性心肌肥厚是心力衰竭进展的核心前驱病变,由压力超负荷等刺激诱导,若未及时干预可进展为不可逆的心功能衰竭。1933年Christian首次提出洋地黄类药物的预防性应用以延缓心肌肥厚,但早期动物研究结果存在矛盾,部分研究支持其心肌保护作用,部分则质疑其对血压和心肌生长的不良影响,导致该研究方向停滞数十年。随着分子生物学技术的发展,钠钾ATP酶的信号转导功能被发现,洋地黄类药物的非正性肌力作用逐渐成为研究热点。现有研究已明确磷脂酰肌醇3-激酶(PI3K)的α亚型与生理性心肌肥厚相关,γ亚型与病理性肥厚相关,但洋地黄类药物通过调控PI3K亚型发挥心肌保护的具体机制及预防性应用的临床价值尚未得到充分证实,这也是本研究的核心出发点。
2. 文献综述解析
本文的文献综述以洋地黄类药物的应用历史、钠钾ATP酶的双重功能(离子转运与信号转导)、PI3K亚型与心肌肥厚的关联为核心分类维度,系统梳理了领域内的研究进展与争议。
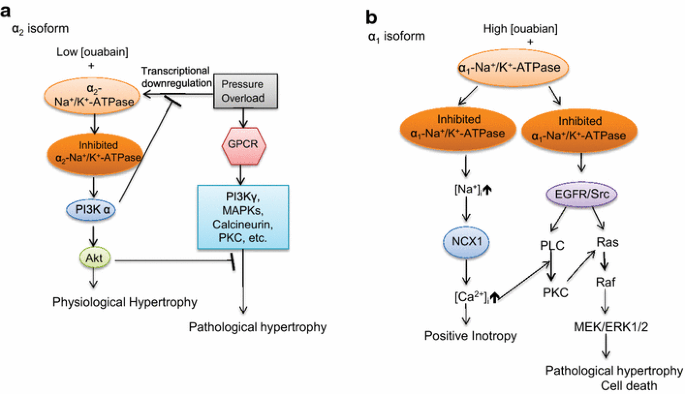
早期研究中,1933年Christian提出洋地黄类药物可用于预防心脏病患者的心肌扩大,1965年Williams等在大鼠主动脉缩窄模型中证实,非毒性剂量的地高辛可减轻心肌肥厚并降低心衰发生率,但后续多项研究结果存在分歧,部分研究发现地高辛可影响大鼠血管壁水潴留与心肌生长,导致对其预防性作用的质疑。钠钾ATP酶的经典功能是维持细胞内外钠钾离子稳态,洋地黄类药物通过抑制该酶发挥正性肌力作用,这是传统心衰治疗的核心机制;近年研究发现,钠钾ATP酶还可作为信号转导分子,通过与邻近膜蛋白的相互作用激活PI3K/Akt等多条信号通路,其中PI3Kα亚型被证实与适应性生理性心肌肥厚相关,PI3Kγ亚型则介导病理性肥厚的进展,但洋地黄类药物对PI3K亚型的选择性激活机制及在压力超负荷心肌中的具体作用尚未被明确证实。
本研究的创新价值在于,首次在小鼠体内模型中证实亚正性肌力剂量的哇巴因可通过结合钠钾ATP酶α2亚型,选择性激活PI3Kα通路,从而有效预防压力超负荷诱导的病理性心肌肥厚和心力衰竭,解决了早期研究中机制不明的核心问题,为洋地黄类药物的预防性应用提供了明确的分子依据,填补了领域内对洋地黄非正性肌力心肌保护机制研究的空白。
3. 研究思路总结与详细解析
本研究的核心目标是明确亚正性肌力剂量哇巴因对压力超负荷小鼠心肌的预防性保护作用及依赖PI3Kα的分子机制,核心科学问题为哇巴因是否通过选择性激活PI3Kα拮抗病理性心肌肥厚,技术路线遵循“细胞实验验证信号通路→动物模型验证体内作用→机制解析靶点关联”的闭环逻辑,从细胞到系统层面全面验证研究假设。
3.1 PI3Kα缺陷小鼠模型的构建与表征
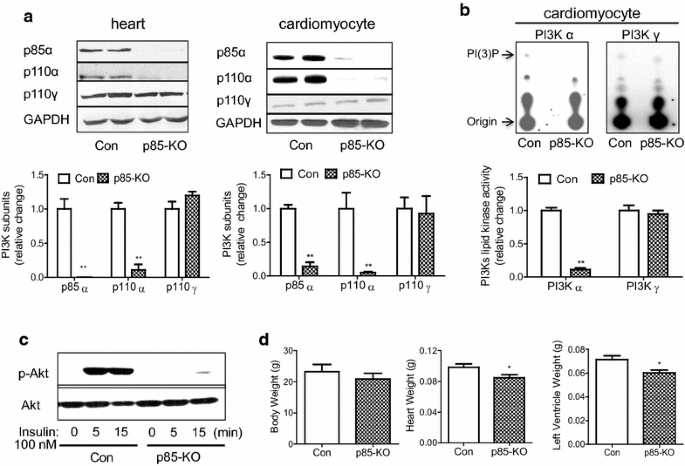
本环节的核心目标是构建并表征心肌特异性PI3Kα缺陷的小鼠模型,为后续验证PI3Kα在哇巴因心肌保护作用中的必要性提供实验工具。研究人员通过将PI3K p85αloxP/loxP p85β−/−小鼠与肌酸激酶Cre转基因小鼠杂交,获得心肌特异性PI3Kα缺陷的p85-KO小鼠,以Cre阳性小鼠为对照组;采用蛋白质免疫印迹检测心肌组织及原代心肌细胞中PI3Kα(p110α、p85)和PI3Kγ(p110γ)的蛋白表达,PI3K脂质激酶活性实验检测酶活性,胰岛素刺激后检测Akt磷酸化水平以反映PI3K通路功能,同时通过超声心动图和血流动力学检测评估小鼠基础心脏功能。结果显示,p85-KO小鼠心肌及原代细胞中p110α和p85蛋白水平较对照组显著降低(n=4-7,P<0.01),p110γ蛋白水平无明显变化;PI3Kα活性在p85-KO细胞中仅为对照组的10%左右(n=4,P<0.01),PI3Kγ活性无差异;胰岛素刺激后,对照组Akt磷酸化水平显著升高,而p85-KO组无明显变化(n=3,P<0.05);p85-KO小鼠的心脏重量较对照组降低(n=5-7,P<0.05),但基础心脏收缩与舒张功能均保持正常。实验所用关键产品:BD Transduction Laboratories的抗PI3K p110α、p85抗体;Cell Signaling Technology的抗磷酸化Akt(Ser473)、总Akt抗体;Santa Cruz Biotechnology的抗PI3K p110γ、GAPDH抗体及辣根过氧化物酶标记的二抗。
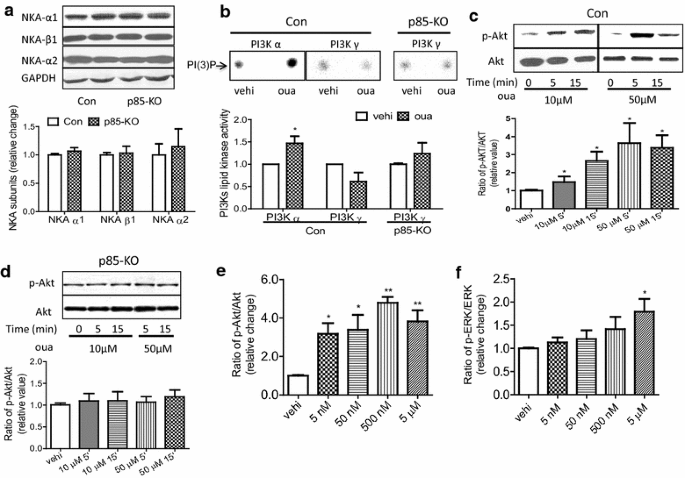
3.2 哇巴因对原代心肌细胞PI3K亚型激活及肥厚的调控
本环节旨在明确哇巴因对PI3K亚型的选择性激活作用及对心肌细胞肥厚的影响,为体内实验提供机制基础。研究人员分离对照组和p85-KO小鼠的原代成年心肌细胞,首先通过免疫印迹检测钠钾ATP酶α1、α2、β1亚型的蛋白表达,确认两组细胞的钠钾ATP酶亚型组成无差异;随后用不同浓度的哇巴因处理细胞,通过PI3K脂质激酶活性实验检测PI3Kα和PI3Kγ的活性,免疫印迹检测Akt和ERK的磷酸化水平,采用³H-亮氨酸掺入实验检测蛋白质合成以反映心肌细胞肥厚程度,实时荧光定量PCR检测心肌肥厚标志物心房钠尿肽(ANP)、脑钠尿肽(BNP)的mRNA表达。结果显示,哇巴因可显著激活对照组细胞的PI3Kα活性(n=9,P<0.05),但对PI3Kγ活性无明显影响,而p85-KO细胞中无PI3Kα激活现象;哇巴因诱导对照组Akt磷酸化的最低有效浓度仅为5nM(n=6,P<0.05),而ERK的激活则需要更高浓度的哇巴因(>100nM);哇巴因可显著促进对照组细胞的蛋白质合成(n=6,P<0.05),但对p85-KO细胞无作用;内皮素-1(ET-1)可促进两组细胞的蛋白质合成,而哇巴因可拮抗ET-1诱导的对照组细胞肥厚(n=9,P<0.05);此外,哇巴因对两组细胞的BNP表达无明显影响,而ET-1可显著上调BNP表达。实验所用关键产品:EMD Millipore的抗PI3K p85α抗体;Santa Cruz Biotechnology的抗PI3K p110γ抗体;Avanti Polar Lipids的磷脂酰肌醇底物;Qiagen的RNeasy RNA提取试剂盒;Applied Biosystems的7500 Fast实时荧光定量PCR系统。
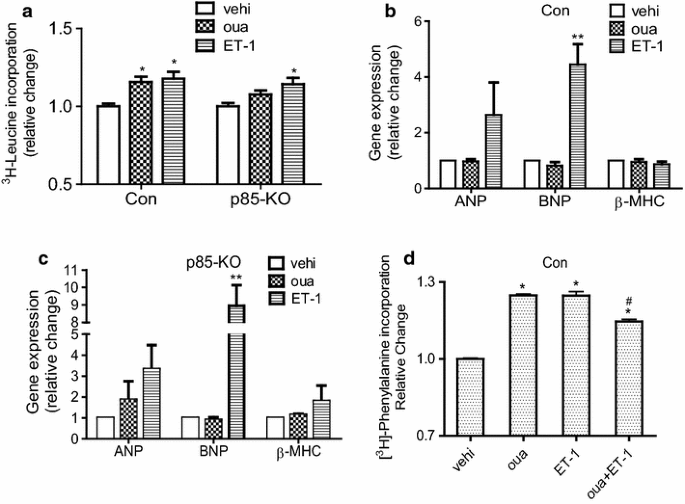
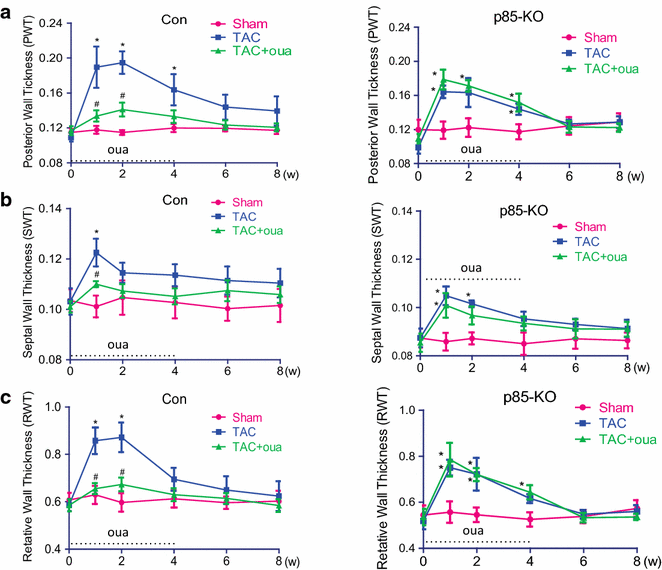
3.3 哇巴因对TAC诱导小鼠心肌肥厚的预防性作用及PI3Kα依赖性验证
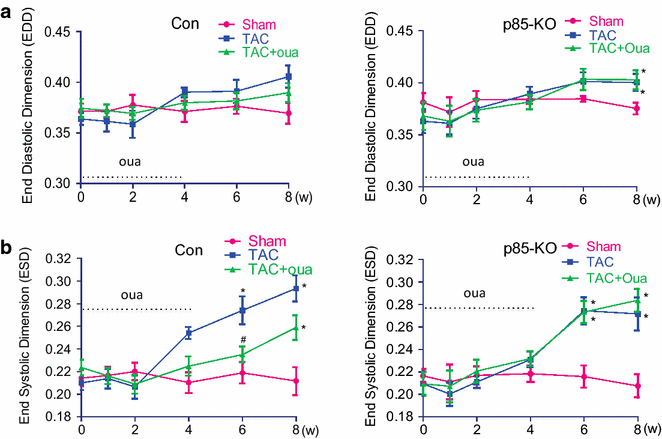
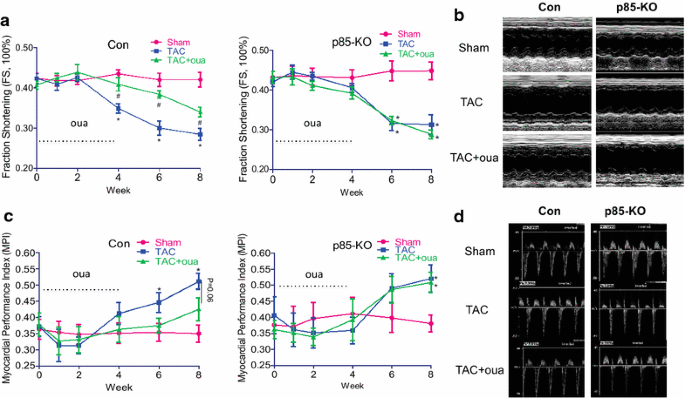
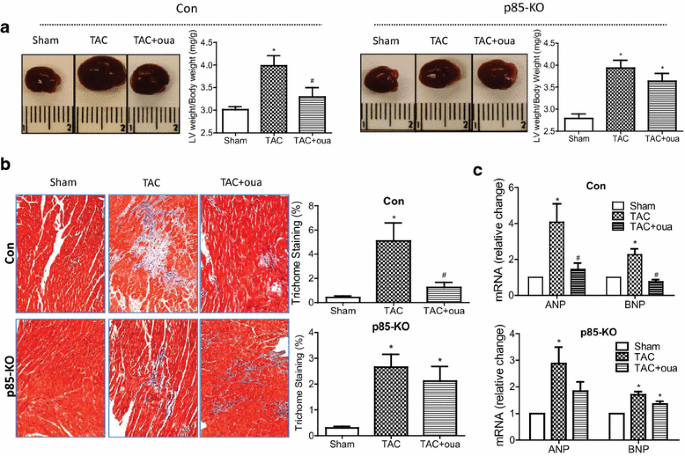
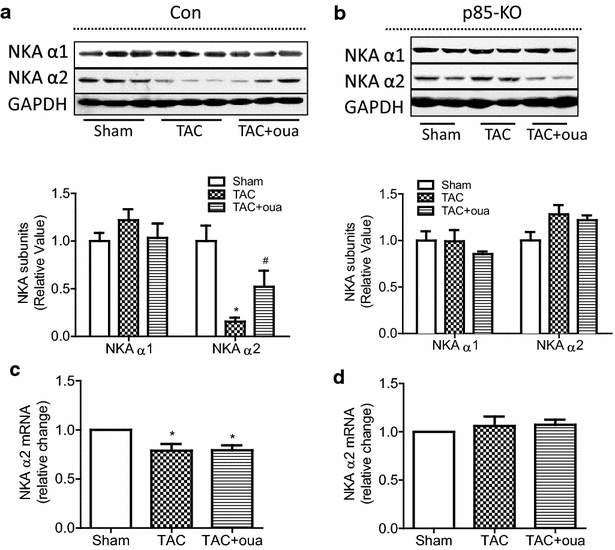
本环节是研究的核心体内验证部分,目标是明确哇巴因对压力超负荷心肌的保护作用是否依赖PI3Kα。研究人员对对照组和p85-KO小鼠进行横向主动脉缩窄(TAC)手术构建压力超负荷模型,术后通过ALZET渗透泵持续4周给予哇巴因(50μg/kg/天),采用尾套法监测小鼠的系统血压,通过超声心动图动态监测心脏结构与功能(包括室壁厚度、心腔大小、射血分数、心肌性能指数),术后8周处死小鼠,取心脏组织检测心脏重量,采用Masson三色染色检测心肌纤维化程度,实时荧光定量PCR检测ANP、BNP的mRNA表达,免疫印迹检测钠钾ATP酶α1、α2亚型的蛋白表达。结果显示,哇巴因对各组小鼠的系统血压无明显影响;TAC术后2周,对照组和p85-KO小鼠的室壁厚度均显著增加,哇巴因可显著抑制对照组小鼠的室壁厚度增加(n=6-7,P<0.05),但对p85-KO小鼠无作用;术后6周,两组小鼠的左心室腔均出现扩张,哇巴因可显著减轻对照组小鼠的心腔扩张(n=6-7,P<0.05);术后4周,两组小鼠的射血分数均降低,哇巴因可显著改善对照组小鼠的心脏功能,射血分数从TAC组的32%恢复至41%(n=6-7,P<0.05),而p85-KO小鼠的心脏功能无明显改善;术后8周,哇巴因可显著减轻对照组小鼠的心脏重量增加(n=6-7,P<0.05)、心肌纤维化程度(纤维化面积从TAC组的12%降至5%,n=5,P<0.05)及ANP、BNP的mRNA上调(n=6-7,P<0.05),但对p85-KO小鼠无上述作用;此外,TAC可显著下调对照组小鼠心肌中钠钾ATP酶α2亚型的蛋白表达(n=6-7,P<0.05),而哇巴因可逆转该下调,在p85-KO小鼠中,TAC对α2亚型的表达无明显影响。实验所用关键产品:ALZET 2004渗透泵;Siemens的ACUSON Sequoia C512超声系统;Millar Instruments的SPR-839压力-容积导管;Olympus的IX51倒置显微镜。
4. Biomarker研究及发现成果解析
本研究涉及的生物标志物(Biomarker)包括钠钾ATP酶α2亚型(功能靶点Biomarker)、PI3Kα(信号通路Biomarker)、ANP与BNP(临床相关Biomarker),其筛选与验证遵循“细胞信号验证→动物功能验证→临床标志物关联”的完整逻辑链条。
钠钾ATP酶α2亚型作为哇巴因发挥心肌保护作用的核心靶点,其来源为小鼠心肌组织,通过蛋白质免疫印迹检测蛋白表达水平,结果显示TAC手术可显著下调对照组小鼠心肌中α2亚型的表达(n=6-7,P<0.05),而哇巴因可逆转该下调作用,在p85-KO小鼠中,TAC对α2亚型的表达无明显影响,提示PI3Kα参与了α2亚型的表达调控。PI3Kα作为信号通路Biomarker,通过脂质激酶活性实验验证其功能,哇巴因可显著激活对照组原代心肌细胞的PI3Kα活性(n=9,P<0.05),而p85-KO细胞中无此激活现象,明确了PI3Kα是哇巴因信号通路的关键节点。ANP与BNP作为临床常用的心肌肥厚与心衰标志物,通过实时荧光定量PCR检测其mRNA表达,TAC手术可显著上调两组小鼠的ANP、BNP表达(n=6-7,P<0.05),而哇巴因可显著抑制对照组小鼠的ANP、BNP上调(n=6-7,P<0.05),但对p85-KO小鼠无作用,进一步证实了PI3Kα在哇巴因心肌保护作用中的必要性。
本研究的核心成果在于,首次明确钠钾ATP酶α2亚型是哇巴因发挥预防性心肌保护作用的关键靶点,其通过结合哇巴因选择性激活PI3Kα通路,从而拮抗压力超负荷诱导的病理性心肌肥厚与心力衰竭。该Biomarker的创新性在于,首次揭示了钠钾ATP酶α2亚型与PI3Kα的调控关系在压力超负荷心肌中的保护作用,为洋地黄类药物的预防性应用提供了明确的分子依据。统计学结果显示,哇巴因对TAC小鼠心脏功能的改善、心肌纤维化的抑制及肥厚标志物的下调均具有显著统计学差异(P<0.05),样本量覆盖6-7只小鼠/组,数据可靠性较高。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。