Puromycin-based vectors promote a ROS-dependent recruitment of PML to nuclear inclusions enriched with HSP70 and Proteasomes
基于嘌呤霉素的载体促进 ROS 依赖性的 PML 募集到富含 HSP70 和蛋白酶体的核内包涵体中。
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2009 | 起止号: | 2009 May 1;10:32 |
| doi: | 10.1186/1471-2121-10-32 | 靶点: | PML、SP7、HSP70 |
文献解析
1. 领域背景与文献引入
文献英文标题:Puromycin-based vectors promote a ROS-dependent recruitment of PML to nuclear inclusions enriched with HSP70 and Proteasomes;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学(蛋白质聚集与细胞应激响应)
早幼粒细胞白血病(PML)蛋白的研究始于1990年代初,当时发现其基因与急性早幼粒细胞白血病的t(15;17)染色体易位相关,后续研究逐步揭示PML蛋白定位于核内离散结构PML核小体,参与细胞周期调控、DNA损伤响应、蛋白质隔离等多种关键细胞过程。同时,蛋白质质量控制体系的研究表明,分子伴侣(如热休克蛋白70,HSP70)和蛋白酶体系统负责清除细胞内错误折叠蛋白,该系统功能异常会导致蛋白质聚集,进而引发神经退行性疾病、肿瘤等多种病理状态。活性氧(ROS)作为细胞代谢的副产物,其水平升高会诱导蛋白质错误折叠和聚集,长期培养的细胞系常存在ROS水平升高的氧化应激状态,但这一状态对细胞实验结果的干扰未被充分重视。当前细胞生物学研究的热点包括蛋白质聚集与疾病的关联、细胞培养条件对细胞表型的调控,但仍存在研究空白:筛选标记基因(如嘌呤霉素抗性基因)的表达对细胞内蛋白质稳态的潜在影响尚未被系统探究,这可能导致细胞实验结果出现偏差。本研究针对这一空白,揭示了嘌呤霉素载体诱导的ROS依赖的蛋白质聚集现象,为细胞实验设计提供了重要警示。
2. 文献综述解析
作者从PML核小体的功能、蛋白质质量控制体系的作用、ROS与蛋白质聚集的关联三个维度对领域内现有研究进行分类评述,系统梳理了PML核小体在细胞过程中的调控作用、蛋白质质量控制体系的组成与功能,以及ROS在细胞应激中的角色。
现有研究的关键结论包括,PML核小体是动态调控的核内结构,参与DNA修复、细胞凋亡等多种细胞过程,其功能异常与肿瘤发生密切相关;分子伴侣和蛋白酶体系统构成细胞内蛋白质质量控制的核心,分子伴侣结合错误折叠蛋白以促进其正确折叠,蛋白酶体负责降解无法修复的错误折叠蛋白,二者功能失调会导致蛋白质聚集并引发如阿尔茨海默病、帕金森病等神经退行性疾病;ROS水平升高会通过氧化修饰蛋白质结构诱导错误折叠,进而促进蛋白质聚集,长期培养的细胞系由于代谢压力、频繁传代等因素常存在ROS水平升高的状态。现有研究的技术方法优势在于,广泛使用细胞系模型进行高通量实验,免疫荧光技术能够精准定位蛋白质的亚细胞分布,流式细胞术可定量检测细胞内ROS水平;但局限性也较为明显,多数研究未考虑筛选标记基因表达对细胞表型的潜在干扰,且未充分评估长期培养细胞的氧化应激状态对实验结果的影响,导致部分实验结论可能存在偏差。通过对比现有研究的未解决问题,本研究的创新价值凸显:首次发现嘌呤霉素抗性基因的表达会诱导PML、HSP70、SUMO-1和20S蛋白酶体形成核内包涵体,且该过程依赖ROS水平;同时揭示长期培养细胞的氧化应激状态会增强这一效应,填补了细胞实验设计中筛选标记潜在干扰的研究空白,为细胞生物学实验的严谨性提供了新的参考依据。
3. 研究思路总结与详细解析
本研究的整体框架为“现象发现→特异性验证→组分鉴定→机制探究→细胞状态影响分析→稳定细胞系验证”的闭环逻辑,研究目标是明确嘌呤霉素载体诱导蛋白质聚集的机制及影响因素,核心科学问题是嘌呤霉素抗性基因是否及如何通过ROS依赖途径诱导细胞内蛋白质聚集。
3.1 嘌呤霉素载体诱导PML聚集的现象发现与验证
该环节的实验目的是验证不同筛选标记载体对PML蛋白亚细胞定位的影响。实验方法细节为,选取U2OS、MCF7、HeLa三种细胞系,分别转染含嘌呤霉素抗性基因的载体(pBABE Puro、pSIREN Puro、pLKO.1 Puro)和含新霉素抗性基因的对照载体(pcDNA3.1 Neo、pCMV Neo),采用Fugene-6转染试剂进行瞬时转染,转染后24小时和48小时通过免疫荧光技术检测PML蛋白的定位;同时通过共转染pEGFP Neo和pBABE Puro载体,以EGFP表达标记转染细胞,定量分析PML聚集的细胞比例。结果解读方面,免疫荧光图显示,未转染或转染新霉素载体的细胞中,PML蛋白以离散的核小体形式分布,每个细胞内有11±5个PML核小体;而转染嘌呤霉素载体的细胞中,PML蛋白形成多个核内聚集物,该现象在转染后24小时和48小时均可见,且在三种细胞系中均存在。共转染实验的定量结果显示,21±6%的EGFP阳性细胞出现PML聚集(n=5,P<0.05),证明PML聚集特异性发生在转染嘌呤霉素载体的细胞中。实验所用关键产品:Fugene-6转染试剂(Roche)、PML抗体(Santa Cruz Biotechnology,货号PGM3、H238)、DAPI核染色试剂(领域常规使用Sigma Aldrich产品)。
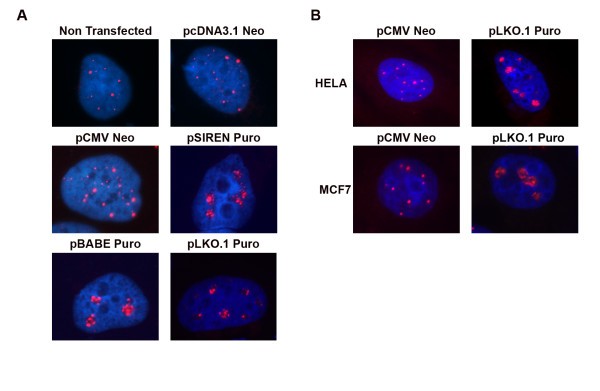
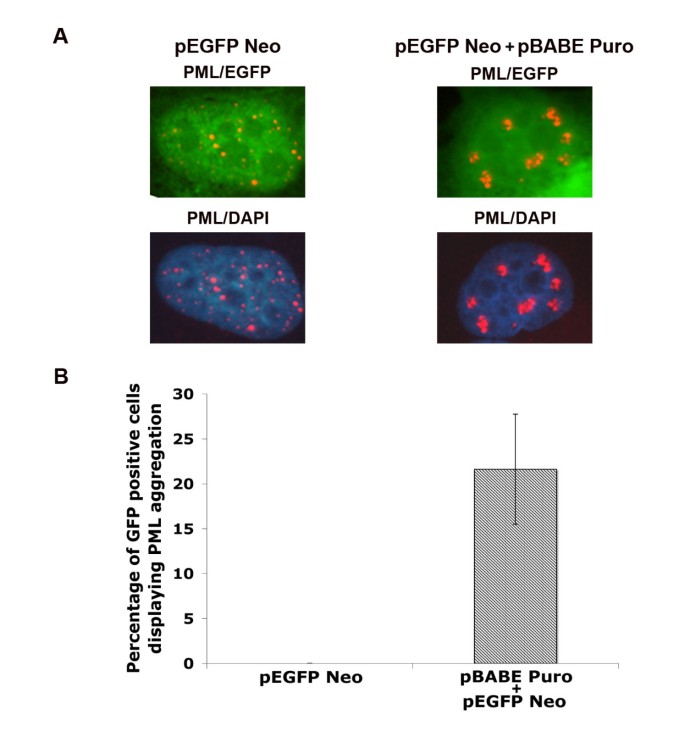
3.2 核内包涵体组分的鉴定
该环节的实验目的是确定PML聚集物的伴随蛋白质组分,明确其与蛋白质质量控制体系的关联。实验方法细节为,在U2OS细胞中转染pBABE Puro载体或pCMV Neo对照载体,转染后48小时采用免疫荧光双标记技术,分别检测PML与HSP70、SUMO-1、20S蛋白酶体的共定位,同时检测PML与核仁标记蛋白Fibrillarin的定位以排除核仁区域聚集的可能性。结果解读方面,免疫荧光图显示,在转染嘌呤霉素载体的细胞中,HSP70、SUMO-1、20S蛋白酶体均与PML在核内包涵体中共定位;其中HSP70在核内形成大的聚集物与PML共定位,同时还存在不与PML共定位的小斑点状聚集;SUMO-1主要定位于PML聚集物内部或周围区域;20S蛋白酶体则在核内和胞质中均形成聚集物,且核内聚集物与PML共定位。而PML聚集物与核仁标记蛋白Fibrillarin无共定位,证明该聚集发生在非核仁的核内区域。实验所用关键产品:HSP70抗体(Cell Signaling Technology,货号D69)、SUMO-1抗体(Santa Cruz Biotechnology,货号FL-101)、20S蛋白酶体抗体(Biomol International)、Fibrillarin抗体(Santa Cruz Biotechnology,货号A-16)。
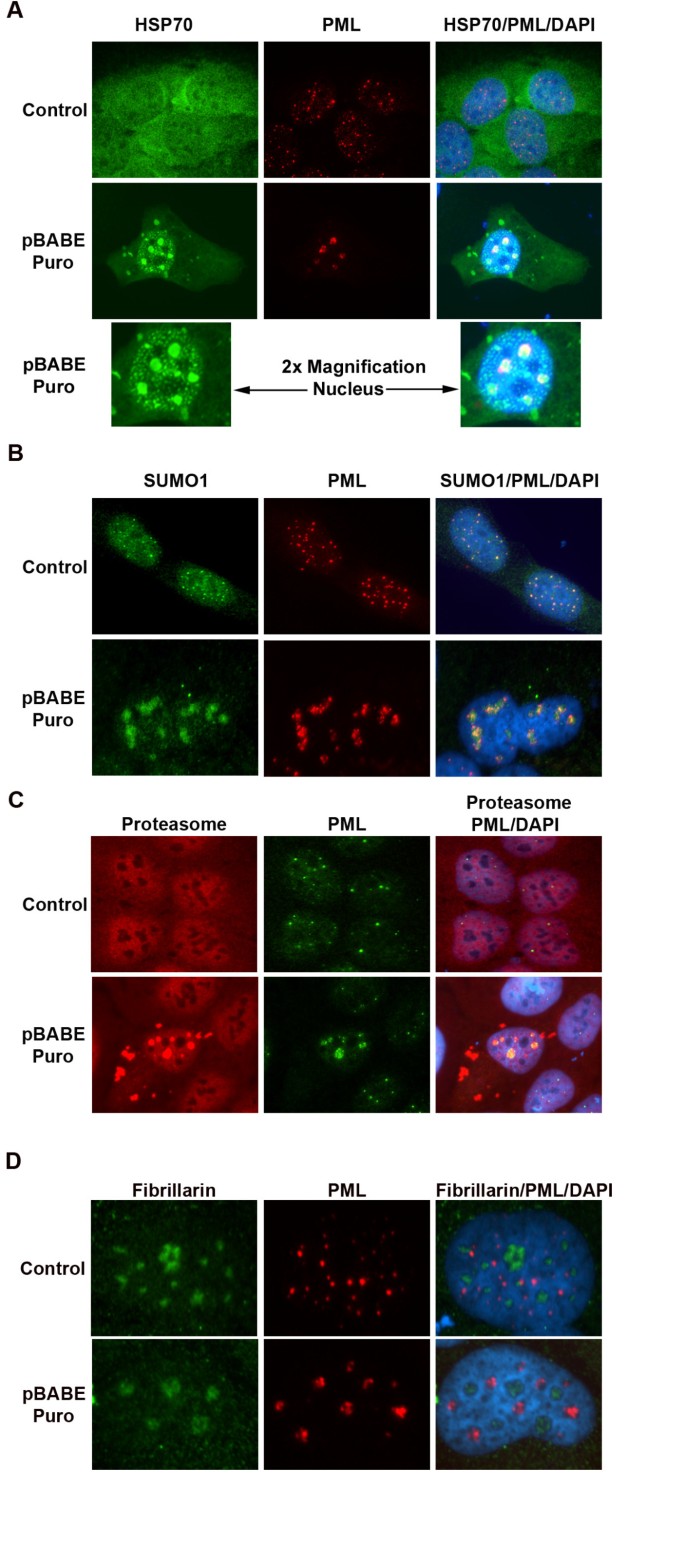
3.3 嘌呤霉素抗性基因的特异性验证
该环节的实验目的是明确嘌呤霉素抗性基因(puromycin n-acetyl transferase,pac)是否为诱导蛋白质聚集的关键因素。实验方法细节为,使用携带不同筛选标记的pBABE系列载体(Puro、Hygro、Neo、GFP、HcRed)转染U2OS细胞,同时通过Quikchange XL突变试剂盒构建缺失pac基因的pBABE Puro del载体并转染细胞,转染后48小时通过免疫荧光技术检测PML和HSP70的定位。结果解读方面,免疫荧光图显示,仅携带pac基因的pBABE Puro载体能诱导PML和HSP70聚集,而携带其他筛选标记的pBABE载体及缺失pac基因的pBABE Puro del载体均无此效应,证明pac基因的表达是诱导蛋白质聚集的必要条件。实验所用关键产品:Quikchange XL突变试剂盒(Stratagene)、pBABE系列载体(Addgene)。
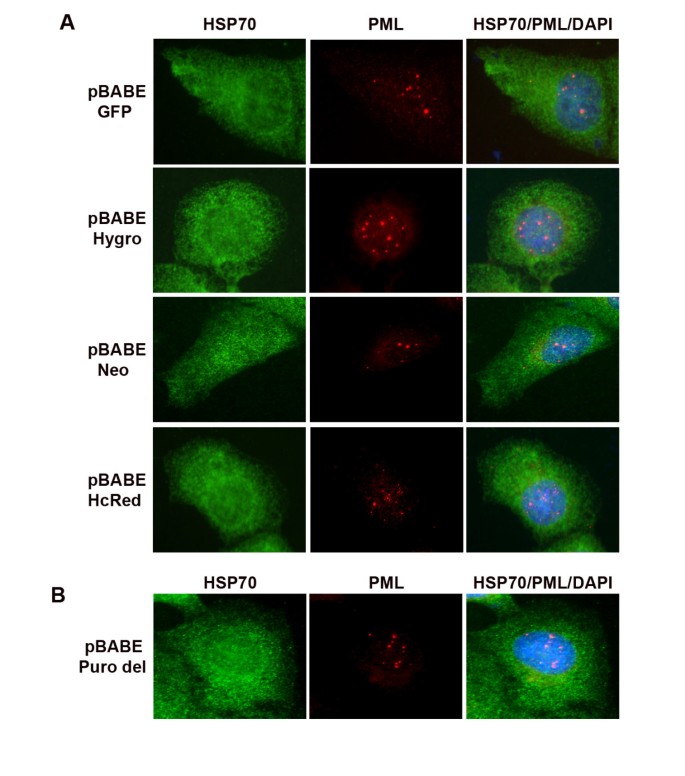
3.4 ROS在蛋白质聚集过程中的调控作用验证
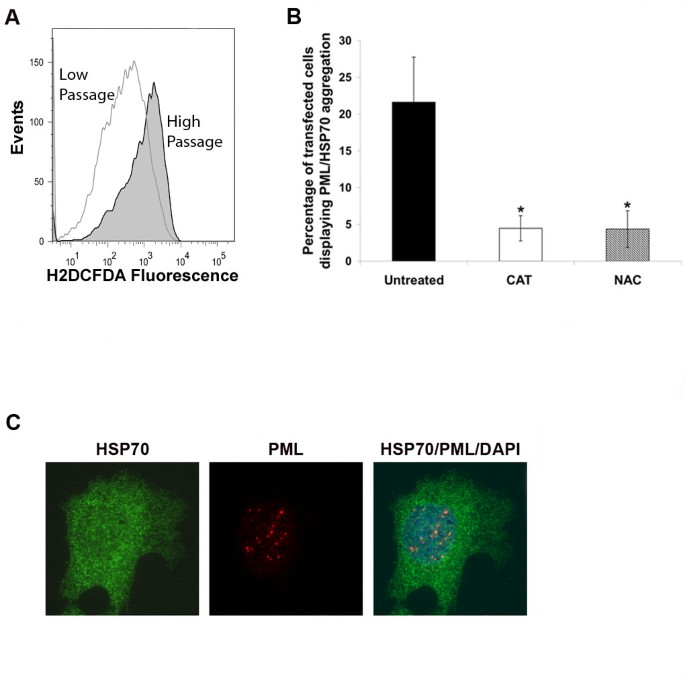
该环节的实验目的是探究ROS水平对嘌呤霉素载体诱导蛋白质聚集的调控作用。实验方法细节为,首先采用H2DCFDA荧光探针结合流式细胞术,检测高代次(长期培养)和低代次(<10代)U2OS细胞内的ROS水平;随后在转染pBABE Puro载体的高代次U2OS细胞中,分别添加ROS清除剂N-乙酰半胱氨酸(NAC)或过氧化氢酶,转染后15小时添加清除剂,48小时后通过免疫荧光技术检测PML和HSP70的聚集情况,并以EGFP表达标记转染细胞以定量分析聚集率。结果解读方面,流式细胞术结果显示,高代次U2OS细胞的ROS水平是低代次细胞的2.7±0.69倍(n=3,P<0.05);低代次细胞转染嘌呤霉素载体后无PML和HSP70聚集现象。添加ROS清除剂后,PML/HSP70聚集率降低80%(n=3,P<0.01),证明嘌呤霉素载体诱导的蛋白质聚集依赖于细胞内的ROS水平。实验所用关键产品:H2DCFDA荧光探针(Invitrogen)、BD FACSCanto流式细胞仪(BD)、N-乙酰半胱氨酸(Sigma Aldrich)、过氧化氢酶(Sigma Aldrich)。
3.5 稳定转染细胞系的蛋白质聚集状态检测
该环节的实验目的是验证经过嘌呤霉素筛选获得的稳定抗性细胞系是否仍存在蛋白质聚集现象。实验方法细节为,在U2OS细胞中转染pBABE Puro载体,转染后4天添加嘌呤霉素(0-15μg/mL)进行筛选,持续培养2周获得稳定抗性细胞系,随后将稳定细胞系接种于盖玻片,培养3天后通过免疫荧光技术检测PML和HSP70的定位。结果解读方面,免疫荧光图显示,稳定抗性细胞系中PML和HSP70恢复正常的离散分布,无聚集现象,证明经过筛选后,细胞已清除或适应了pac基因表达诱导的蛋白质聚集。文献未提及具体实验产品,领域常规使用嘌呤霉素(Sigma Aldrich)进行细胞稳定系筛选。
4. Biomarker研究及发现成果解析
本研究中涉及的Biomarker为PML、HSP70、SUMO-1和20S蛋白酶体组成的蛋白质复合物标记物,其筛选与验证逻辑为从现象观察到组分鉴定,再到机制验证的完整链条,精准反映了嘌呤霉素载体诱导的ROS依赖型错误折叠蛋白响应。
Biomarker定位方面,该标记物属于蛋白质复合物类生物标志物,筛选与验证逻辑为:首先通过免疫荧光技术观察到PML聚集现象,随后通过双标记实验验证HSP70、SUMO-1、20S蛋白酶体与PML的共定位,最后通过ROS清除实验验证该聚集的ROS依赖性,形成完整的验证链条。研究过程详述:该Biomarker的来源为转染嘌呤霉素载体的长期培养细胞系样本,验证方法为免疫荧光共定位技术和流式细胞术;特异性表现为仅在转染含pac基因载体的高代次细胞中出现聚集,低代次细胞或转染其他筛选标记载体的细胞中无此现象;敏感性数据显示,21±6%的转染细胞出现该Biomarker的聚集(n=5,P<0.05)。核心成果提炼:该Biomarker组合反映了细胞内错误折叠蛋白响应的激活状态,其功能关联在于,PML、HSP70、20S蛋白酶体均为细胞内关键的功能蛋白,它们的聚集会影响细胞内蛋白质质量控制、DNA修复等多种细胞过程,进而干扰实验结果的准确性;创新性在于首次将嘌呤霉素抗性基因表达与ROS依赖的蛋白质聚集关联起来,为细胞实验设计提供了新的警示;统计学结果方面,高代次细胞ROS水平是低代次细胞的2.7±0.69倍(n=3,P<0.05),ROS清除剂处理后聚集率降低80%(n=3,P<0.01),充分证明了该Biomarker的ROS依赖性。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。