Comparison of size distribution and (Pro249-Ser258) epitope exposure in in vitro and in vivo derived Tau fibrils
体外和体内来源的Tau蛋白原纤维的尺寸分布和(Pro249-Ser258)表位暴露情况的比较
| 期刊: | BMC Molecular and Cell Biology | 影响因子: | 2.700 |
| 时间: | 2020 | 起止号: | 2020 Nov 12;21(1):81 |
| doi: | 10.1186/s12860-020-00320-y | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Comparison of size distribution and (Pro249-Ser258) epitope exposure in in vitro and in vivo derived Tau fibrils;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:神经退行性疾病(阿尔茨海默病)中的Tau蛋白聚集机制
阿尔茨海默病(AD)是最常见的神经退行性疾病,其核心病理特征为β淀粉样蛋白斑块和Tau蛋白异常聚集形成的神经原纤维缠结(NFTs)。领域共识:Tau病理的朊样传播假说认为,异常聚集的Tau蛋白可作为“种子”诱导正常Tau发生错误折叠并在脑内扩散,这一机制是Tau病进展的关键驱动因素。该领域的关键发展节点包括2009年首次在转基因小鼠中证实Tau病理的传播性,2014年发现不同Tau病存在特异性的Tau“菌株”,2016年通过PET成像证实AD患者脑内Tau病理进展与认知下降相关。当前研究热点集中于Tau聚集体的播种机制、Tau菌株鉴定及靶向Tau的免疫治疗开发,但未解决的核心问题包括:Tau聚集体的大小对其播种能力的影响尚未完全阐明,超声处理作为Tau聚集研究中常用的实验技术,其对不同来源Tau聚集体的生化、生物物理及功能特性的影响缺乏系统分析,且缺乏针对微管结合域(MTBD)附近表位的特异性检测工具。
针对上述研究空白,本研究旨在通过系统对比体外重组、AD患者脑来源及P301S转基因小鼠来源的Tau纤维,分析超声处理对其大小分布、表位暴露及播种效率的影响,明确Tau聚集体大小与播种活性的关联,为Tau聚集机制研究及相关实验技术的优化提供重要依据,同时开发基于PT76抗体的聚集特异性检测方法,为Tau聚集体的定量分析提供新工具。
2. 文献综述解析
作者按Tau聚集体的来源(重组蛋白、动物模型、人类病理样本)及研究技术(生化分析、细胞播种实验、体内传播模型)的维度,对Tau聚集及传播领域的现有研究进行分类梳理,明确了当前研究的进展与不足。
现有研究的关键结论包括:Tau聚集体具有朊样播种能力,可在细胞及体内模型中诱导正常Tau发生错误折叠;不同来源的Tau聚集体结构存在显著差异,如肝素诱导的重组Tau聚集体为直丝结构,而AD患者脑来源的Tau聚集体为双螺旋丝(PHF)结构;不同Tau病的Tau聚集体具有不同的“菌株”特性,其传播模式及病理表现存在差异。现有技术方法的优势在于:表达荧光共振能量转移(FRET)传感器的细胞模型可灵敏检测Tau聚集体的播种活性,蔗糖梯度超速离心技术可有效分离不同大小的Tau聚集体,为分析聚集体特性提供了工具;但同时存在局限性:现有研究多关注Tau聚集体的播种能力,对聚集体大小与播种活性的关联分析不足,超声处理作为常用实验技术,其对不同来源Tau聚集体的影响缺乏系统对比,且缺乏针对微管结合域附近表位的特异性检测方法,限制了对Tau聚集体结构与功能关系的深入研究。
本研究的创新价值在于,首次系统对比了体外重组、AD患者脑来源及P301S转基因小鼠来源的Tau聚集体经超声处理后的大小分布、PT76表位暴露及播种效率的变化,明确了超声处理通过破碎大聚集体为小纤维并提高内在播种能力的双重作用机制;同时开发了基于PT76抗体的聚集特异性检测方法,可特异性识别K18及AD脑来源的Tau聚集体,为Tau聚集体的定量分析提供了新工具,弥补了现有研究在Tau聚集体结构-功能关系分析及实验技术优化方面的空白。
3. 研究思路总结与详细解析
本研究的整体研究目标为阐明Tau聚集体大小与播种效率的关联,以及超声处理对不同来源Tau聚集体的生化、生物物理及功能特性的影响;核心科学问题包括Tau聚集体的大小如何调控其播种活性,超声处理是否通过改变聚集体大小和表位暴露影响播种能力;技术路线遵循“样本制备-处理与对照-多维度分析-机制总结”的闭环逻辑,即构建不同来源的Tau聚集体样本,设置超声处理与未处理对照,通过生化分析、大小分离、细胞功能实验及电镜观察等技术,系统解析超声处理对Tau聚集体的影响及机制。
3.1 重组K18 Tau纤维制备与PT76抗体特异性验证
实验目的:制备均一的重组Tau聚集体,验证PT76抗体对Tau聚集体的特异性检测能力,为后续实验奠定基础。
方法细节:构建含P301L突变的4R Tau重复域K18蛋白(仅包含微管结合域及附近序列),在肝素钠存在下于37℃孵育5天形成纤维,经超速离心(184000×g,1小时)收集沉淀,分为超声处理组与未处理组;超声处理采用Branson探头超声仪,振幅15%,总超声时间2分钟,采用2秒脉冲/10秒间隔的模式,样本全程置于冰浴以避免温度影响;开发基于PT76抗体的Meso Scale Discovery(MSD)聚集特异性检测方法,对比K18纤维样本、单体样本及超速离心上清样本的信号差异。
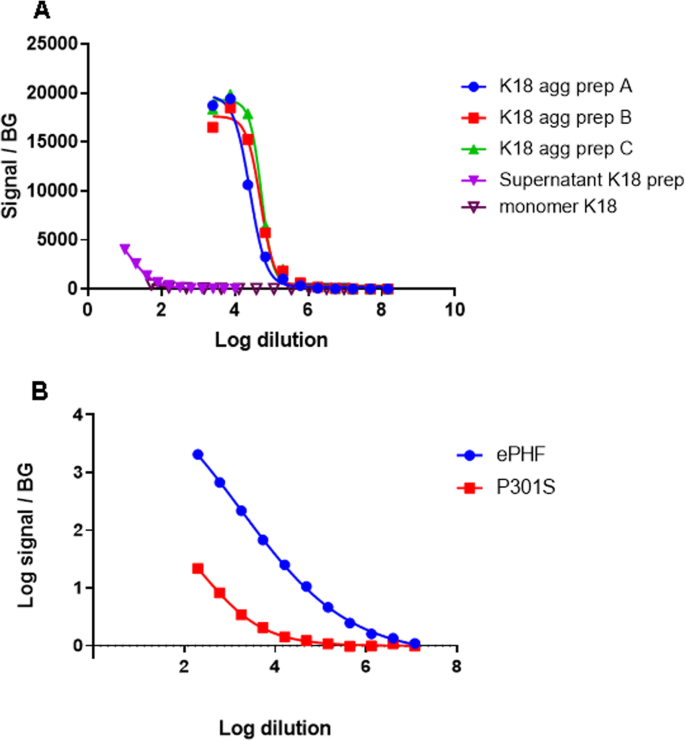
结果解读:PT76/PT76 MSD检测显示,3种独立制备的K18纤维样本均呈现剂量依赖的信号,而未聚集的单体K18样本及超速离心上清样本几乎无信号(图1),证实该方法对Tau聚集体具有高特异性;同时检测发现,AD患者脑来源的双螺旋丝样本的PT76信号显著高于P301S转基因小鼠来源的Tau聚集体样本,提示不同来源的Tau聚集体的PT76表位暴露水平存在差异。
产品关联:实验所用关键产品:Tebu Bio的myc标签K18-P301L Tau蛋白、MP Biomedicals的肝素钠盐、Branson探头超声仪、Meso Scale Discovery的MSD检测平台、FEI/ThermoFisher的Tecnai12 Biotwin透射电镜。
3.2 超声处理对重组K18 Tau纤维播种能力的影响
实验目的:明确超声处理对重组Tau聚集体播种效率的影响,分析其作用机制。
方法细节:将超声处理与未处理的K18纤维样本进行梯度稀释,分别在有无Lipofectamine2000转染试剂的条件下,与表达K18 FRET传感器的HEK293细胞共孵育;转染组孵育48小时,无转染组孵育7天,随后收集细胞并通过流式细胞术检测FRET阳性细胞比例,评估Tau聚集体的播种效率;实验设置至少3次独立重复,采用双向ANOVA分析统计学差异。
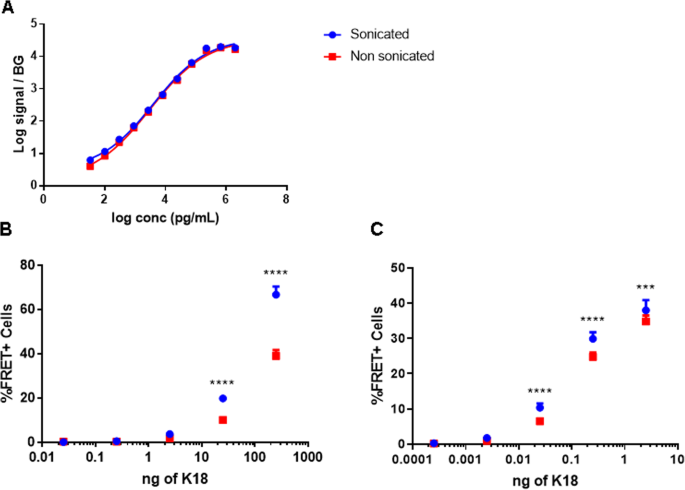
结果解读:PT76/PT76 MSD检测显示,超声处理与未处理的K18纤维样本的聚集信号无显著差异,但细胞FRET实验显示,超声处理组的FRET阳性细胞比例显著高于未处理组,且无转染试剂时差异更为显著:无转染条件下,最高剂量组的超声处理样本FRET阳性率约为80%,未处理样本约为20%(P<0.0001);转染条件下,最高剂量组的超声处理样本FRET阳性率约为70%,未处理样本约为40%(P<0.001)(图2);该结果提示超声处理未改变Tau聚集体的总量,但显著提高了播种效率,且该效果部分依赖于细胞对小尺寸聚集体的摄取改善,同时也存在内在播种能力的提升。
3.3 超声处理对AD患者脑来源双螺旋丝的影响分析
实验目的:验证超声处理对体内来源的人类病理Tau聚集体的作用是否与重组K18一致,明确其普适性。
方法细节:从Braak VI期AD患者的额叶组织中分离双螺旋丝聚集体,分为超声处理组与未处理组;采用AT8、PT51、PT76三种抗体的MSD聚集特异性检测方法,分析不同表位的暴露水平;同时在有无转染试剂的条件下,与HEK293 FRET细胞共孵育,检测其播种效率。
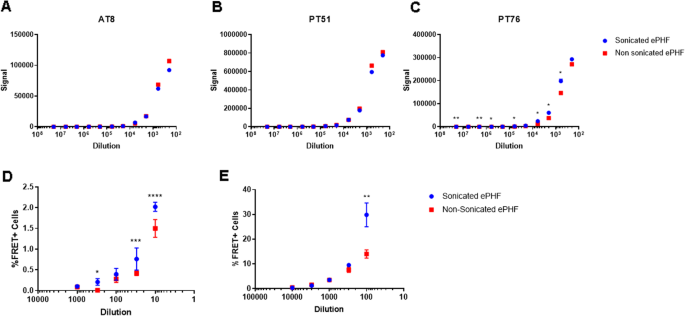
结果解读:AT8和PT51抗体的MSD检测显示,超声处理与未处理的双螺旋丝样本信号无显著差异,而PT76抗体的检测显示超声处理组信号略有升高(图3);细胞FRET实验显示,超声处理组的播种效率显著高于未处理组,且无转染试剂时差异更明显(P<0.05至P<0.0001)(图3);该结果提示超声处理对AD患者脑来源的Tau聚集体的播种能力提升作用与重组K18纤维类似,且可改变部分表位的暴露水平,为理解人类病理Tau聚集体的特性提供了依据。
3.4 Tau聚集体大小分布与播种活性的关联分析
实验目的:明确超声处理对Tau聚集体大小分布的影响,分析大小与播种活性的关联。
方法细节:采用Native PAGE技术分析超声处理与未处理的Tau聚集体的大小分布,通过Western blot检测不同抗体识别的Tau条带;采用蔗糖梯度超速离心(200000×g,16小时,4℃)分离不同大小的Tau聚集体,收集各梯度组分并通过MSD、Western blot及细胞FRET实验分析其特性;采用透射电镜观察超声处理与未处理的K18纤维的形态。
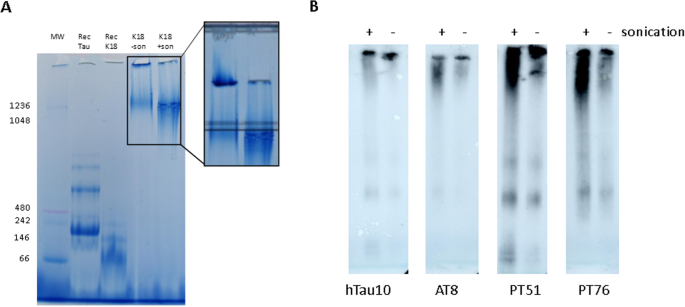
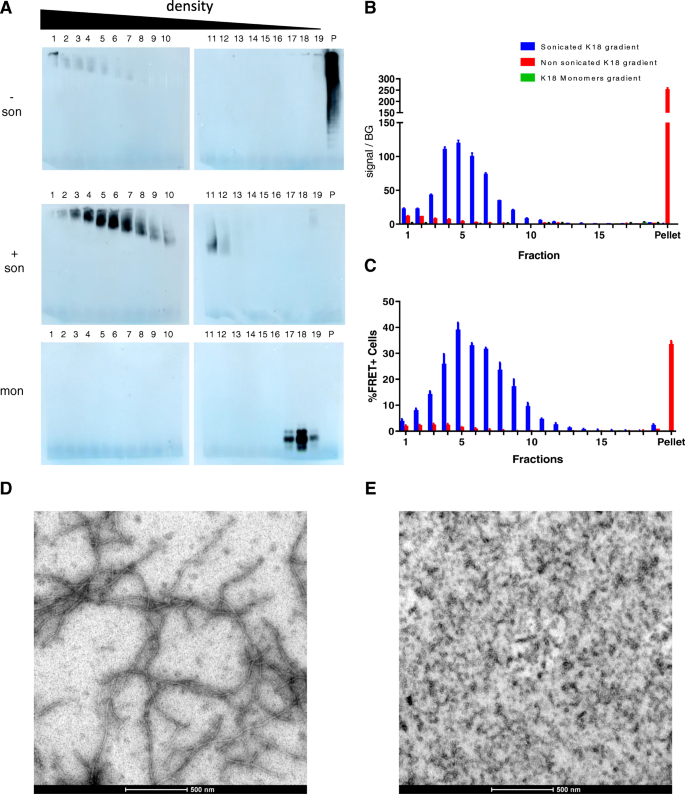
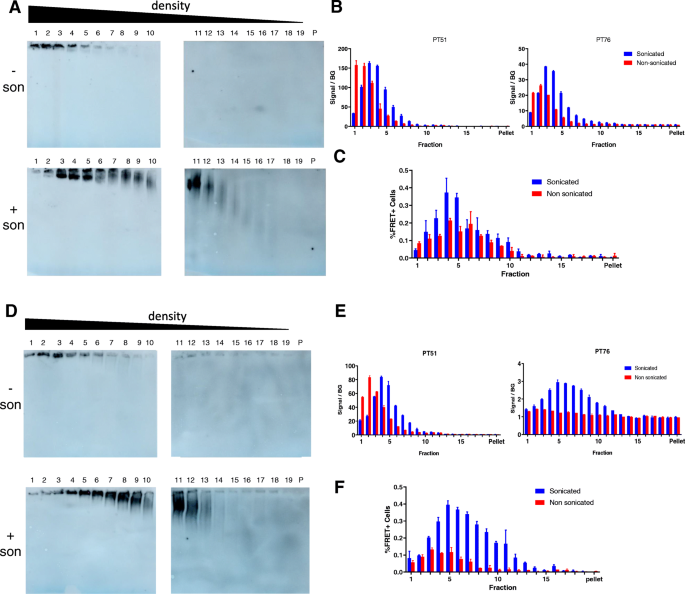
结果解读:Native PAGE结果显示,未处理的K18纤维因分子量大无法进入凝胶,而超声处理后的K18纤维可进入凝胶且信号增强;AD患者脑来源的双螺旋丝经超声处理后,不同Tau抗体检测的条带均向低分子量偏移(图4),证实超声处理可减小Tau聚集体的大小。蔗糖梯度超速离心结果显示,未处理的K18聚集体信号主要集中在沉淀组分,而超声处理后的K18聚集体信号分布在中高密度组分(图5);细胞FRET实验显示,超声处理后的中高密度组分的播种效率是未处理沉淀组分的8倍以上,且与MSD检测的聚集信号呈良好的相关性(图5);透射电镜观察显示,未处理的K18为长纤维结构,而超声处理后的K18为短纤维结构(图5)。对AD患者脑来源双螺旋丝及P301S转基因小鼠来源Tau聚集体的分析显示,超声处理均导致其大小分布向低分子量偏移,播种效率显著提升(图6);该结果明确了小尺寸的Tau聚集体具有更高的播种活性,超声处理通过破碎大聚集体为小纤维,显著提高了Tau聚集体的播种效率。
4. Biomarker研究及发现成果解析
本研究聚焦于Tau聚集体的大小及PT76表位暴露水平这两类功能性Biomarker,通过系统的生化分析及功能实验,明确了其与Tau聚集体播种活性的关联,为Tau病的机制研究及实验技术优化提供了关键依据。
Biomarker定位:本研究中涉及的功能性Biomarker包括Tau聚集体的大小及PT76表位(249-258位氨基酸)的暴露水平;其筛选与验证逻辑为:通过蔗糖梯度超速离心技术分离不同大小的Tau聚集体组分,结合MSD聚集特异性检测、Western blot及细胞FRET播种实验,验证聚集体大小与播种活性的关联;通过PT76抗体检测不同来源、不同处理的Tau聚集体的表位暴露水平,分析其与聚集体大小及播种活性的相关性。
研究过程详述:Tau聚集体样本来源于重组K18-P301L蛋白、AD患者额叶组织(Braak VI期)及P301S转基因小鼠脊髓组织;验证方法包括Native PAGE分析大小分布、蔗糖梯度超速离心分离不同大小组分、MSD聚集特异性检测表位暴露水平、HEK293细胞FRET实验检测播种活性;特异性与敏感性方面,PT76/PT76 MSD方法对Tau聚集体具有高特异性,未聚集的单体Tau样本无明显信号;细胞FRET实验可灵敏检测低剂量Tau聚集体的播种活性,超声处理后的小尺寸Tau聚集体播种效率显著高于大尺寸聚集体,如超声处理的K18聚集体中高密度组分的播种效率是未处理沉淀组分的8倍以上。
核心成果提炼:小尺寸的Tau聚集体具有显著更高的播种活性,是Tau病理传播的关键功能性Biomarker;超声处理可通过双重机制增强Tau聚集体的播种效率,一是将大聚集体破碎为小纤维,提高细胞摄取效率,二是提高Tau聚集体的内在播种能力;PT76表位的暴露水平与Tau聚集体的大小及播种活性相关,AD患者脑来源的双螺旋丝的PT76表位暴露水平高于P301S转基因小鼠来源的Tau聚集体,超声处理可增加该表位的暴露;本研究未提供ROC曲线、风险比(HR)等临床Biomarker相关数据,但明确了Tau聚集体大小作为功能性Biomarker的价值,为Tau聚集机制研究、实验技术优化及靶向Tau的治疗开发提供了重要参考。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。