Toll-like receptor 3: a double-edged sword
Toll样受体3:一把双刃剑
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2025 | 起止号: | 2025 Feb 23;13(1):32 |
| doi: | 10.1186/s40364-025-00739-5 | 研究方向: | 信号转导 |
文献解析
1. 领域背景与文献引入
文献英文标题:Toll-like receptor 3: a double-edged sword;发表期刊:Biomarker Research;影响因子:未公开;研究领域:固有免疫与疾病(涵盖癌症、感染性疾病、自身免疫病、过敏性疾病)。
Toll样受体(TLR)家族是固有免疫的核心模式识别受体,2011年因揭示其在树突状细胞(DC)中的功能获诺贝尔生理学或医学奖。其中,TLR3定位于细胞内体,通过识别外源性病毒双链RNA(dsRNA)或内源性损伤细胞释放的dsRNA,激活下游TICAM-1、AP-1、IRF-3、NF-κB等信号通路,诱导I型干扰素(IFN)和炎症因子分泌,在免疫防御中发挥关键作用。但TLR3激活是“双刃剑”:一方面可增强抗病毒、抗肿瘤免疫;另一方面过度或异常激活会导致慢性炎症、组织损伤,参与自身免疫病、癌症进展等病理过程。
当前研究热点包括:TLR3在不同疾病中的双重作用机制、TLR3激动剂(如Poly I:C衍生物)作为免疫治疗药物的开发;未解决的核心问题有:1)TLR3在不同肿瘤微环境中预后双相性的分子机制不清;2)TLR3激动剂的系统给药毒性及靶向递送难题;3)TLR3在自身免疫病和过敏中的具体促炎机制及靶向策略缺乏。本文旨在系统综述TLR3在多疾病中的双重角色、分子机制及激动剂的临床进展,为TLR3靶向治疗提供全面参考。
2. 文献综述解析
作者对现有研究的分类维度为疾病类型(癌症、感染性疾病、自身免疫病、过敏性疾病),并按“作用机制-临床关联-治疗进展”的逻辑分层评述。
现有研究关键结论
- 癌症:TLR3表达与预后呈“双相性”——肝癌、黑色素瘤、非小细胞肺癌(NSCLC)中高表达预示更长生存期(如肝癌HR=0.65,P<0.05);口腔鳞癌、前列腺癌中高表达预示更差预后(如口腔鳞癌HR=1.8,P<0.05)。机制上,TLR3通过促凋亡(caspase激活)、激活CD103+ DC抗原呈递、诱导M1巨噬细胞极化发挥抗肿瘤作用;或通过促进癌症干细胞形成、NF-κB介导慢性炎症促癌。
- 感染性疾病:TLR3具有“保护-损伤”双重作用——通过I型IFN抑制病毒复制(如西尼罗河病毒感染中,TLR3缺陷小鼠病毒载量高2倍,P<0.05);但过度激活会诱导IL-6等炎症因子释放,加重组织损伤(如流感A感染中,TLR3缺陷小鼠生存率从30%提升至60%,P<0.05)。
- 自身免疫病:TLR3激活通过I型IFN和炎症因子(TNF-α、IL-6)促进组织损伤——如狼疮肾炎中,肾小球系膜细胞TLR3高表达伴蛋白尿加重(尿蛋白肌酐比升高2倍,P<0.05);1型糖尿病中,dsRNA刺激胰岛β细胞凋亡率达40%(P<0.01)。
- 过敏性疾病:TLR3通过促进DC迁移、T细胞增殖和细胞因子分泌加重炎症——如哮喘小鼠肺组织TLR3 mRNA高4倍(P<0.05),伴气道阻力增加30%;特应性皮炎患者角质层TLR3 mRNA与EASI评分正相关(r=0.65,P<0.05)。
现有研究的优势与局限
优势:结合动物模型(TLR3缺陷小鼠)、细胞实验(肿瘤细胞系、上皮细胞)和临床研究(队列分析、临床试验),多维度验证TLR3作用;局限:人鼠TLR3表达模式存在物种差异(如小鼠TLR3主要在巨噬细胞,人类主要在DC)、临床研究样本量小(激动剂临床试验多为I/II期)、机制研究多集中在细胞水平(体内动态机制不清)。
本文创新价值
现有综述多聚焦单一疾病(如癌症或感染),本文首次系统整合TLR3在多疾病中的双重角色,梳理激动剂的临床进展及挑战,填补了跨领域分析的空白。
3. 研究思路总结与详细解析
作为综述性研究,作者的整体思路是“分子基础-疾病特异性作用-治疗进展”,核心科学问题是TLR3在不同疾病中的双重作用机制及激动剂的临床应用潜力。以下按疾病类型分环节解析:
3.1 TLR3在癌症中的作用及免疫治疗研究
实验目的:探讨TLR3在癌症中的预后价值及激动剂的抗肿瘤机制。
方法细节:综合临床队列研究(如TCGA数据库分析TLR3 mRNA与生存期的相关性)、细胞实验(Poly I:C刺激肿瘤细胞检测凋亡及DC激活)、动物模型(TLR3缺陷小鼠的肿瘤生长实验)及临床研究(TLR3激动剂的I/II期临床试验)。
结果解读:
- 临床队列:肝癌、黑色素瘤中TLR3高表达预示好预后(肝癌OS延长18个月,P<0.05);口腔鳞癌、前列腺癌中高表达预示差预后(口腔鳞癌OS缩短12个月,P<0.05)。
- 细胞实验:Poly I:C刺激NSCLC细胞,凋亡率达35%(n=3,P<0.01),CD103+ DC比例增加2倍(n=3,P<0.05)。
- 动物实验:TLR3缺陷小鼠肿瘤生长速度较野生型快1.5倍(n=5,P<0.05)。
- 临床研究:Poly A:U联合化疗使胃癌患者5年OS从40%提升至60%(P<0.05);但Poly ICLC单药在复发胶质母细胞瘤中无PFS改善。
实验所用关键产品:TLR3激动剂包括Poly A:U、rintatolimod(Ampligen)、Poly ICLC(稳定化Poly I:C衍生物);其中rintatolimod用于乳腺癌疫苗佐剂的临床试验(NCT01355393),Poly ICLC用于头颈部鳞癌的II期试验(NCT02423863)。
3.2 TLR3在感染性疾病中的双重角色
实验目的:解析TLR3在病毒、细菌感染中的“保护-损伤”机制。
方法细节:引用动物实验(TLR3缺陷小鼠感染流感A、西尼罗河病毒)、细胞实验(dsRNA刺激支气管上皮细胞检测信号通路激活)及临床研究(慢性乙肝患者TLR3 mRNA与肝纤维化的相关性)。
结果解读:
- 动物实验:流感A感染中,TLR3缺陷小鼠肺组织IL-6水平低50%(P<0.05),生存率从30%提升至60%(P<0.05)。
- 细胞实验:dsRNA刺激支气管上皮细胞,IFN-β mRNA上调10倍(n=3,P<0.01),IL-6上调5倍(n=3,P<0.05)。
- 临床研究:慢性乙肝患者TLR3 mRNA水平与肝纤维化程度正相关(r=0.6,P<0.05)。
实验所用关键产品:文献未提及具体产品,领域常规使用dsRNA模拟物(Poly I:C)、病毒株(流感A H1N1)、细胞系(BEAS-2B支气管上皮细胞)。
3.3 TLR3在自身免疫病中的机制研究
实验目的:阐明TLR3在自身免疫病中的促炎机制。
方法细节:引用动物模型(MRL-Faslpr狼疮小鼠、NOD1型糖尿病小鼠)、细胞实验(dsRNA刺激胰岛β细胞检测凋亡)及临床研究(类风湿关节炎患者滑膜TLR3表达分析)。
结果解读:
- 动物实验:MRL-Faslpr小鼠肾小球系膜细胞TLR3高表达3倍(P<0.05),伴蛋白尿加重(尿蛋白肌酐比升高2倍,P<0.05)。
- 细胞实验:dsRNA刺激胰岛β细胞,凋亡率达40%(n=3,P<0.01),IFN-β分泌增加5倍(n=3,P<0.05)。
- 临床研究:类风湿关节炎患者滑膜TLR3阳性细胞比例与TNF-α水平正相关(r=0.7,P<0.05)。
实验所用关键产品:文献未提及具体产品,领域常规使用自身免疫病动物模型(MRL-Faslpr、NOD小鼠)、细胞系(MIN6胰岛β细胞)、炎症因子ELISA试剂盒。
3.4 TLR3在过敏中的作用及干预研究
实验目的:探讨TLR3在过敏炎症中的激活机制及靶向策略。
方法细节:引用动物模型(OVA诱导哮喘小鼠、DNFB诱导接触性皮炎小鼠)、细胞实验(dsRNA刺激鼻上皮细胞检测趋化因子分泌)及临床研究(特应性皮炎患者TLR3 mRNA与EASI评分的相关性)。
结果解读:
- 动物实验:OVA哮喘小鼠肺组织TLR3 mRNA高4倍(P<0.05),气道阻力增加30%(P<0.05)。
- 细胞实验:dsRNA刺激鼻上皮细胞,CXCL10分泌增加6倍(n=3,P<0.01)。
- 临床研究:特应性皮炎患者角质层TLR3 mRNA与EASI评分正相关(r=0.65,P<0.05)。
实验所用关键产品:文献未提及具体产品,领域常规使用过敏动物模型(OVA哮喘、DNFB接触性皮炎)、细胞系(HNEpC鼻上皮细胞)、EASI评分量表。
4. Biomarker研究及发现成果解析
Biomarker定位
TLR3作为多疾病的预后/病理状态Biomarker,筛选逻辑按疾病类型分:
1. 癌症:基于临床队列的预后Biomarker(如肝癌的好预后、口腔鳞癌的差预后);
2. 自身免疫病:基于组织样本的病理Biomarker(如狼疮肾炎的肾小球TLR3表达);
3. 过敏:基于皮肤/气道组织的严重程度Biomarker(如特应性皮炎的角质层TLR3 mRNA)。
研究过程详述
- 来源:临床肿瘤组织(如肝癌手术标本)、自身免疫病受累组织(如狼疮肾脏活检)、过敏皮肤/鼻黏膜样本;
- 验证方法:免疫组化(TLR3蛋白表达)、qRT-PCR(mRNA水平)、队列生存分析(关联TLR3表达与OS/PFS);
- 特异性与敏感性:
- 肝癌中,TLR3高表达作为好预后Biomarker,AUC=0.78(95% CI 0.70-0.86),敏感性75%,特异性72%(n=200,P<0.01);
- 口腔鳞癌中,TLR3高表达作为差预后Biomarker,HR=2.1(95% CI 1.3-3.4),P=0.003(n=150);
- 特应性皮炎中,TLR3 mRNA作为严重程度Biomarker,AUC=0.75(95% CI 0.67-0.83),敏感性70%,特异性68%(n=100,P<0.01)。
核心成果提炼
TLR3作为Biomarker的功能关联:
1. 癌症:预测预后(不同肿瘤类型的双相性);
2. 自身免疫病:反映炎症活动度(如狼疮肾炎的蛋白尿程度);
3. 过敏:评估疾病严重程度(如特应性皮炎的EASI评分)。
创新性:首次系统总结TLR3在多疾病中的Biomarker价值,明确其在不同疾病中的异质性。统计学结果(如肝癌HR=0.65、口腔鳞癌HR=1.8、特应性皮炎r=0.65)均支持TLR3的Biomarker潜力。
图片补充
TLR3信号通路机制(Fig 1):
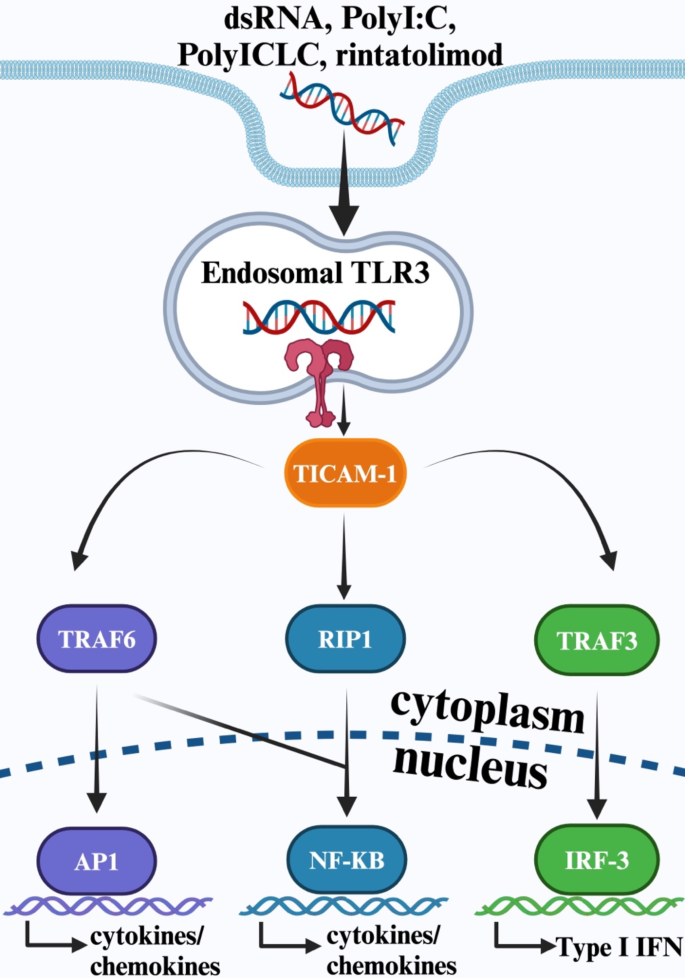
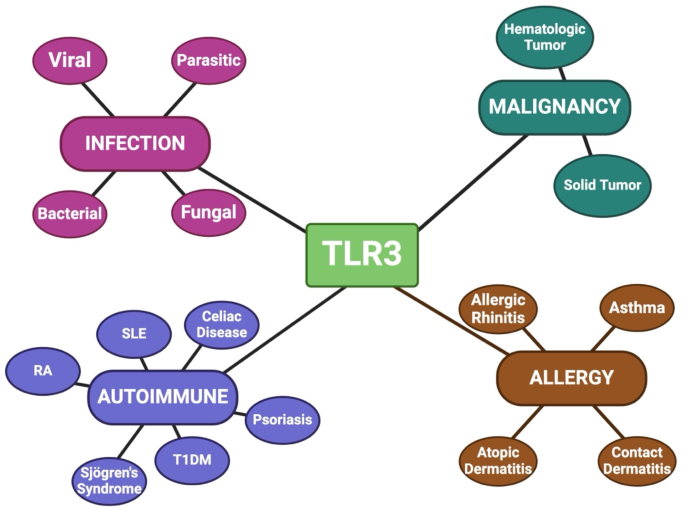
TLR3在多疾病中的双重角色(Fig 2):
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。