Comprehensive brain tissue metabolomics and biological network technology to decipher the mechanism of hydrogen-rich water on Radiation-induced cognitive impairment in rats
利用综合脑组织代谢组学和生物网络技术解析富氢水对辐射诱导大鼠认知障碍的机制
| 期刊: | BMC Molecular and Cell Biology | 影响因子: | 2.700 |
| 时间: | 2023 | 起止号: | 2023 Sep 26;24(1):30 |
| doi: | 10.1186/s12860-023-00491-4 | 种属: | Rat |
| 研究方向: | 神经科学、代谢 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Comprehensive brain tissue metabolomics and biological network technology to decipher the mechanism of hydrogen-rich water on Radiation-induced cognitive impairment in rats;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:辐射神经生物学、代谢组学与网络药理学交叉研究
电离辐射可通过产生大量自由基损伤生物大分子,其中约60%-70%的损伤由羟自由基介导,大脑因富含多不饱和脂肪酸、抗氧化酶水平相对较低,对氧化损伤高度敏感,辐射可通过抑制神经发生、促进脑细胞凋亡引发长期认知障碍,儿童等神经系统未发育完全的群体风险尤为显著。领域共识:目前唯一经FDA批准的辐射防护剂WR-2721存在头晕、呕吐等不良反应,亟需安全有效的替代方案。氢分子因能快速透过血脑屏障与细胞膜,选择性中和毒性活性氧,在新生儿脑损伤、脑缺血再灌注损伤等疾病中展现出良好的神经保护效果,但针对辐射诱导认知障碍的机制研究仅停留在表型层面,缺乏分子水平的系统解析。代谢组学可通过分析代谢物水平反映生理病理状态的代谢终点,网络药理学则能从整体层面解析药物-靶点-疾病的复杂调控网络,二者结合已在中药抗抑郁等研究中应用,但尚未用于富氢水辐射防护机制的研究。本研究正是针对这一空白,通过整合两种技术系统阐明富氢水的作用机制,为其临床转化提供分子依据。
2. 文献综述解析
作者从电离辐射损伤机制、氢分子神经保护作用、代谢组学与网络药理学技术应用三个维度梳理领域研究现状,明确现有研究的进展与局限性,为自身研究的创新点奠定基础。
首先,作者总结了电离辐射的损伤逻辑,指出电离辐射产生的自由基可损伤核酸、蛋白质、碳水化合物与脂质等生物大分子,大脑的结构特性使其对氧化损伤高度敏感,辐射可引发学习记忆等认知功能障碍,甚至导致长期神经退行性改变,儿童群体的风险更高。其次,关于氢分子的神经保护研究,现有结论表明氢能快速透过血脑屏障与细胞膜,选择性中和毒性活性氧,在多种神经系统疾病中展现防护效果,但针对辐射诱导认知障碍的机制研究仅停留在表型层面,缺乏分子层面的系统解析。再者,代谢组学作为新兴组学技术,可通过分析代谢物水平反映生理病理状态,在药物机制研究中能揭示代谢终点变化;网络药理学则能从整体层面解析药物-靶点-疾病的复杂调控网络,二者结合已在中药机制研究中取得进展,但尚未用于富氢水辐射防护机制的研究。现有辐射防护剂存在不良反应,而富氢水的安全性优势明显,但缺乏机制支撑限制了其临床转化,本研究通过整合代谢组学与生物网络技术,填补了这一研究空白,为富氢水的临床应用提供分子依据。
3. 研究思路总结与详细解析
本研究以“验证富氢水对辐射诱导大鼠认知障碍的防护作用→解析其分子机制→筛选潜在生物标志物”为核心逻辑,通过构建大鼠模型、认知功能评估、代谢组学检测、生物网络分析、通路富集与ROC验证的闭环实验设计,系统阐明富氢水的作用机制。
3.1 辐射诱导认知障碍大鼠模型构建与认知功能评估
实验目的:构建辐射诱导认知障碍大鼠模型,验证富氢水对大鼠认知功能的改善作用。
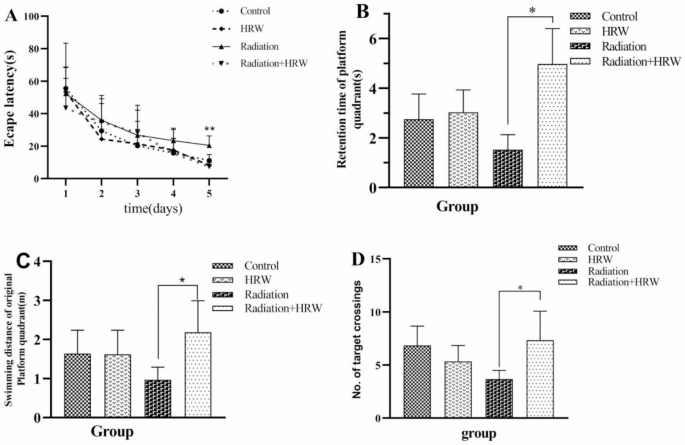
方法细节:将24只6周龄雄性SD大鼠随机分为4组(每组n=6):对照组(纯水灌胃+无辐射)、富氢水组(富氢水灌胃+无辐射)、辐射组(纯水灌胃+30Gy全脑辐射)、辐射-富氢水组(富氢水灌胃+30Gy全脑辐射)。灌胃剂量为20ml/kg/天,从辐射前10分钟持续至辐射后30天;辐射采用6MeV电子束,剂量率3Gy/min。辐射后第30天进行莫里斯水迷宫实验,包括5天定位航行实验(记录逃避潜伏期)和第6天空间探索实验(记录原平台象限停留时间、穿越平台次数等)。
结果解读:定位航行实验显示,辐射组大鼠的逃避潜伏期显著长于对照组、富氢水组和辐射-富氢水组(P<0.05);空间探索实验中,辐射-富氢水组大鼠的原平台象限停留时间、游泳距离及穿越平台次数均显著高于辐射组(P<0.05),表明富氢水可显著改善辐射诱导的大鼠认知障碍。
实验所用关键产品:便携式富氢水机(中国辐射防护研究院、山西中辐核仪器有限公司)、直线加速器(Elekta Synergyt,英国Crawley);文献未提及具体实验试剂,领域常规使用戊巴比妥钠、莫里斯水迷宫分析系统等。
3.2 脑组织代谢组学样本制备与检测
实验目的:制备大鼠脑组织代谢组学样本,通过超高效液相色谱-高分辨质谱检测代谢物谱。
方法细节:辐射后第36天处死大鼠,取脑组织,准确称取30mg样本,加入内标(2-氯-L-苯丙氨酸)、提取溶剂(甲醇/水=4/1,v/v),经-80℃冻存、研磨、超声、-20℃静置后离心,取上清冻干,复溶后过滤,采用超高效液相色谱-高分辨质谱在ESI正负离子模式下检测,色谱柱为ACQUITY UPLC HSS T3柱,流动相为含0.1%甲酸的水和乙腈,设置梯度洗脱程序,质谱采用全扫描结合MSE模式采集数据。
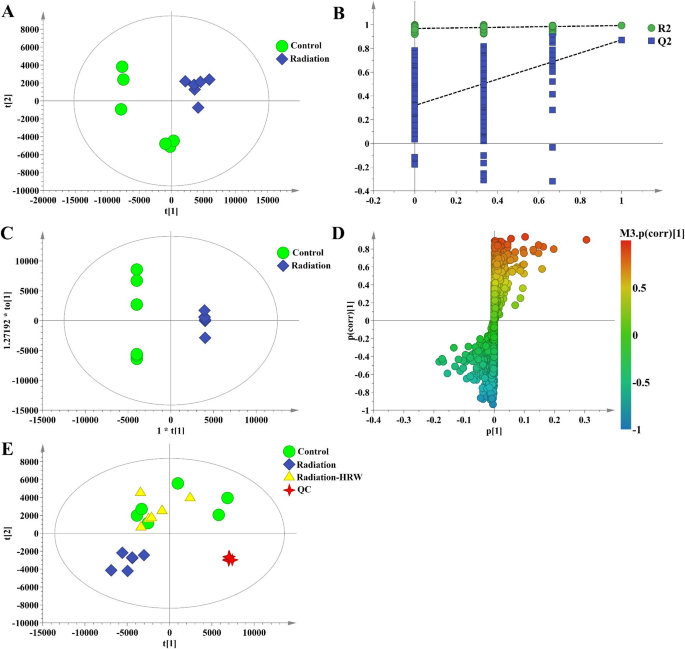
结果解读:QC样本在PLS-DA分析中聚集良好,表明检测系统的重复性与可靠性;对照组、辐射组、辐射-富氢水组的PLS-DA得分图可明显区分,表明富氢水可逆转辐射诱导的脑组织代谢紊乱。
实验所用关键产品:超高效液相色谱仪(Dionex Ultimate 3000,赛默飞世尔科技,美国)、高分辨质谱仪(Q-Exactive Plus,赛默飞世尔科技,美国);文献未提及具体提取试剂品牌,领域常规使用色谱级甲醇、乙腈等。
3.3 差异代谢物筛选与通路富集分析
实验目的:筛选辐射诱导的差异代谢物及富氢水逆转的代谢物,解析关键代谢通路。
方法细节:采用正交偏最小二乘判别分析(OPLS-DA)分析对照组与辐射组的代谢数据,以VIP>1(S-plot)且P<0.05(t检验)为标准筛选差异代谢物;将富氢水逆转的差异代谢物导入MetaboAnalyst 5.0进行通路富集分析,以通路效应值>0.1为关键通路标准。
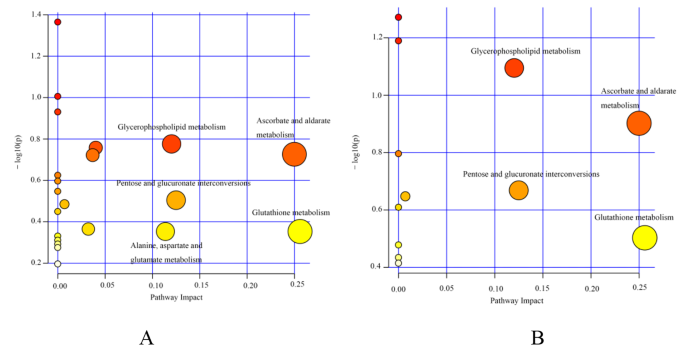
结果解读:辐射组与对照组相比共鉴定出80种差异代谢物,富氢水干预后可逆转其中54种代谢物的变化;通路富集分析显示,谷胱甘肽代谢、抗坏血酸和醛糖酸代谢、戊糖与葡萄糖醛酸相互转化、甘油磷脂代谢是富氢水调控的关键通路,这些通路均与氧化应激损伤修复相关。
文献未提及具体分析软件的授权信息,领域常规使用SIMCA-P、MetaboAnalyst等工具。
3.4 生物网络构建与功能分析
实验目的:构建基因-代谢物调控网络,解析富氢水作用的分子调控机制。
方法细节:通过GeneCards和DisGeNET数据库筛选与电离辐射相关的潜在基因,将差异代谢物导入Cytoscape的MetScape插件进行代谢酶分析,构建“基因-代谢物”调控网络;采用DAVID数据库对93个关键靶基因进行KEGG和GO富集分析(P<0.05)。
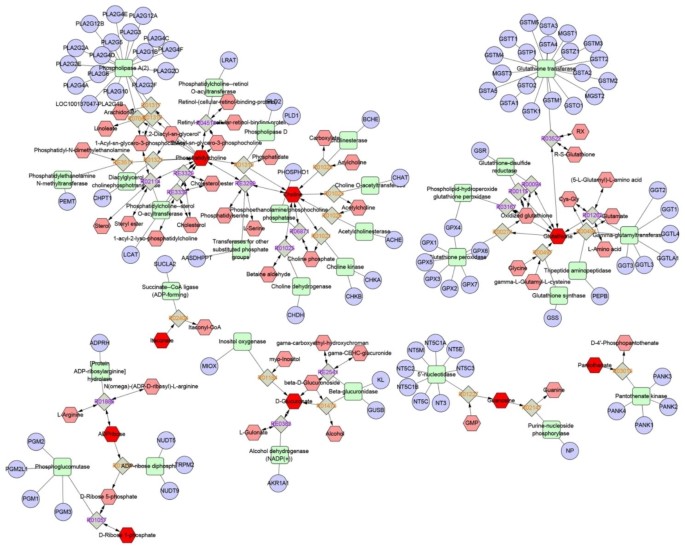
结果解读:构建的生物网络显示,磷脂酰胆碱、胆碱、葡萄糖醛酸盐等关键代谢物与93个靶基因存在调控关联;KEGG富集分析显示,谷胱甘肽代谢、花生四烯酸代谢、甘油磷脂代谢等通路显著富集,且通路间存在交互作用,协同参与富氢水的辐射防护作用。
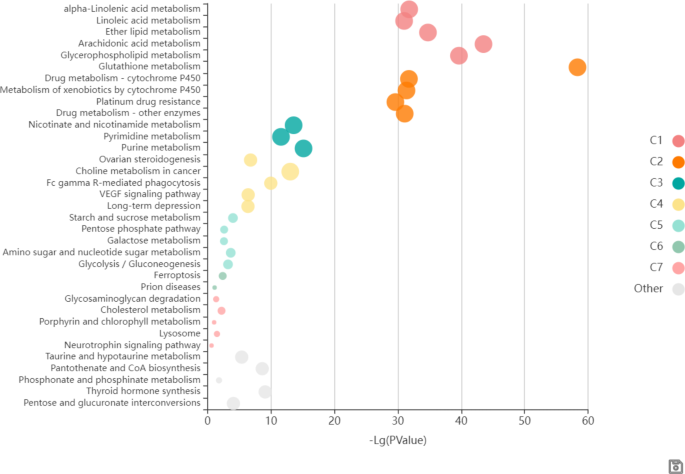
实验所用关键工具:Cytoscape 3.9.2、DAVID数据库;文献未提及具体数据库的使用细节,领域常规使用这些工具进行网络构建与富集分析。
3.5 生物标志物的ROC评估
实验目的:筛选富氢水治疗辐射诱导认知障碍的潜在生物标志物,评估其诊断效能。
方法细节:选取磷脂酰胆碱、胆碱、D-葡萄糖醛酸盐三种关键代谢物,采用Omicstudio工具进行ROC曲线分析,计算AUC值;通过逻辑回归分析构建代谢物组合,评估其联合诊断效能,以P<0.05、95%置信区间为统计学标准。
结果解读:单个代谢物的AUC值分别为磷脂酰胆碱0.8147、胆碱0.6843、D-葡萄糖醛酸盐0.6503;三者联合后的AUC值为0.8771,诊断效能高于单个代谢物,表明这三种代谢物可作为富氢水治疗辐射诱导认知障碍的潜在生物标志物。
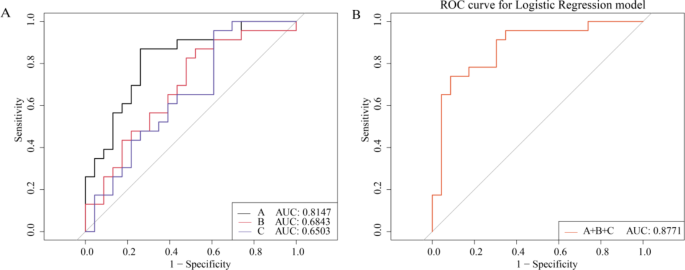
文献未提及具体分析工具的授权信息,领域常规使用Omicstudio、SPSS等工具进行ROC分析。
4. Biomarker研究及发现成果
本研究通过代谢组学筛选、生物网络关联与ROC验证的完整逻辑链,鉴定出磷脂酰胆碱、胆碱、D-葡萄糖醛酸盐三种富氢水治疗辐射诱导认知障碍的潜在生物标志物,明确了其代谢通路关联与诊断效能。
Biomarker定位:三种代谢物均属于富氢水逆转的关键差异代谢物,筛选逻辑为“辐射诱导代谢紊乱→富氢水逆转代谢变化→生物网络关联靶基因→ROC验证诊断效能”,从细胞代谢、分子调控到临床诊断效能形成完整验证链条。研究过程详述:这些生物标志物来源于大鼠脑组织样本,通过超高效液相色谱-高分辨质谱进行定量检测,ROC曲线分析显示,磷脂酰胆碱的AUC为0.8147(95% CI文献未明确提供),胆碱为0.6843,D-葡萄糖醛酸盐为0.6503;三者联合后的AUC为0.8771(95% CI文献未明确提供),具有更高的诊断效能,统计学分析显示P<0.05,结果具有显著性。核心成果提炼:这三种代谢物与谷胱甘肽代谢、甘油磷脂代谢等辐射防护关键通路直接相关,其中磷脂酰胆碱作为甘油磷脂代谢的核心组分,其水平变化可反映脑组织氧化损伤修复状态;本研究首次在辐射诱导认知障碍模型中发现这三种代谢物与富氢水防护作用的关联,为富氢水的临床转化提供了潜在的诊断与疗效评估标志物,其中联合标志物的风险比等数据文献未明确提供,需进一步临床样本验证。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。