Unveiling the early defense response dynamics in grapevines against Plasmopara viticola by single-cell transcriptomics
利用单细胞转录组学揭示葡萄藤早期抵御葡萄霜霉病菌的防御反应动态
| 期刊: | Genome Biology | 影响因子: | 9.400 |
| 时间: | 2026 | 起止号: | 2026 Jan 27;27(1):43 |
| doi: | 10.1186/s13059-025-03904-z | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Single-cell transcriptome atlas reveals dynamic cell-type-specific defense responses of grapevine to Plasmopara viticola infection;发表期刊:Genome Biology;影响因子:17.906(2023年);研究领域:植物病理学-葡萄与霜霉菌互作。
葡萄霜霉病是由专性寄生卵菌葡萄生单轴霉(Plasmopara viticola)引起的全球性葡萄产业毁灭性病害,当前主要依赖化学农药防控,存在环境残留、病原菌耐药性等问题。领域发展关键节点:早期通过bulk RNA-seq解析组织水平的防御通路,鉴定抗性基因;2010年后单细胞RNA-seq技术兴起,为解析细胞异质性提供了工具;近年聚焦植物与病原菌互作的细胞特异性机制。当前研究热点:亲和互作中病原菌操控宿主转录组的分子机制,早期免疫激活的精准时间点解析;未解决的核心问题:霜霉菌如何调控葡萄保卫细胞转录组促进气孔入侵,bulk RNA-seq无法捕捉占比仅0.6%的保卫细胞的转录变化,亲和互作的细胞层面机制研究不足。
针对现有研究的空白,本研究通过单细胞与空间转录组技术,构建葡萄感染霜霉菌后的单细胞转录组图谱,解析不同细胞类型的动态防御反应,重点揭示保卫细胞的转录重编程机制,为葡萄霜霉病防控提供新靶点与理论依据。
2. 文献综述解析
作者从技术方法、研究对象、时间点选择三个维度对现有研究进行分类评述,系统梳理了bulk RNA-seq与单细胞RNA-seq在葡萄-霜霉菌互作研究中的应用,对比了亲和互作与非亲和互作的研究现状,指出了现有研究在细胞异质性解析和时间点选择上的局限性。
现有研究的关键结论:bulk RNA-seq研究主要聚焦非亲和互作(抗性葡萄品种与霜霉菌互作),鉴定了NLR类抗性基因、PTI/ETI通路等防御相关分子;亲和互作(易感品种与霜霉菌互作)研究较少,仅能获得组织水平的平均转录信息,对病原菌操控宿主的机制了解有限。技术方法优势:bulk RNA-seq可快速筛选组织水平的差异表达基因,适合大规模转录组分析;局限性:无法解析细胞异质性,保卫细胞等少数细胞的转录变化被掩盖,多数研究选择6hpi作为早期感染时间点,可能错过更早的免疫激活阶段。
本研究的创新价值:首次构建葡萄感染霜霉菌的单细胞转录组图谱,覆盖0、3、6、12hpi四个时间点,发现3hpi即启动强免疫反应,早于此前报道的6hpi;重点解析保卫细胞的转录重编程,揭示ABA负调控因子与WRKY41-WRKY55-KAT1通路在霜霉菌诱导气孔开放中的作用,填补了亲和互作细胞特异性机制的空白;通过空间转录组验证细胞类型注释的可靠性,为植物病原菌互作的单细胞研究提供了范式。
3. 研究思路总结与详细解析
本研究整体目标是构建葡萄感染霜霉菌后的单细胞转录组图谱,揭示细胞类型特异性的动态防御反应,核心科学问题是霜霉菌如何通过调控保卫细胞转录组促进气孔入侵,技术路线遵循“样本制备-测序分析-机制解析-功能验证”的闭环逻辑,结合单细胞转录组、空间转录组、生物信息学分析与分子生物学实验,系统解析葡萄的细胞特异性防御机制。
3.1 实验材料与样本制备
实验目的是获取高质量的葡萄叶片原生质体与空间转录组样本,为后续测序分析提供可靠材料。方法细节:选用易感品种赤霞珠的组培苗,接种霜霉菌前24h进行连续光照处理以消除昼夜节律对转录组的影响;在0(对照)、3、6、12hpi四个时间点采集叶片样本,每个时间点设置2个生物学重复;原生质体制备采用酶解法,将叶片切成细条后置于含纤维素酶R10、离析酶R10的酶解液中,26℃黑暗消化,经40μm细胞筛过滤、100×g离心洗涤后,台盼蓝染色检测活力,仅保留活力合格的样本用于单细胞捕获;空间转录组样本采用OCT包埋剂包埋叶片组织,-80℃冷冻保存,后续切成10μm厚的冷冻切片,固定在Stereo-seq芯片上处理。产品关联:实验所用关键产品:10× Genomics Chromium Single Cell Instrument、Chromium Next GEM Single Cell 3′ Reagent Kits v3.1、BGI Stereo-seq芯片、Dual-Luciferase Reporter Gene Assay Kit(Yeasen, 上海)、Dual-Luciferase® Reporter Assay System(Promega, WI, USA);其他常规试剂如纤维素酶R10等未明确品牌,领域常规使用Sigma-Aldrich等品牌的相关试剂。
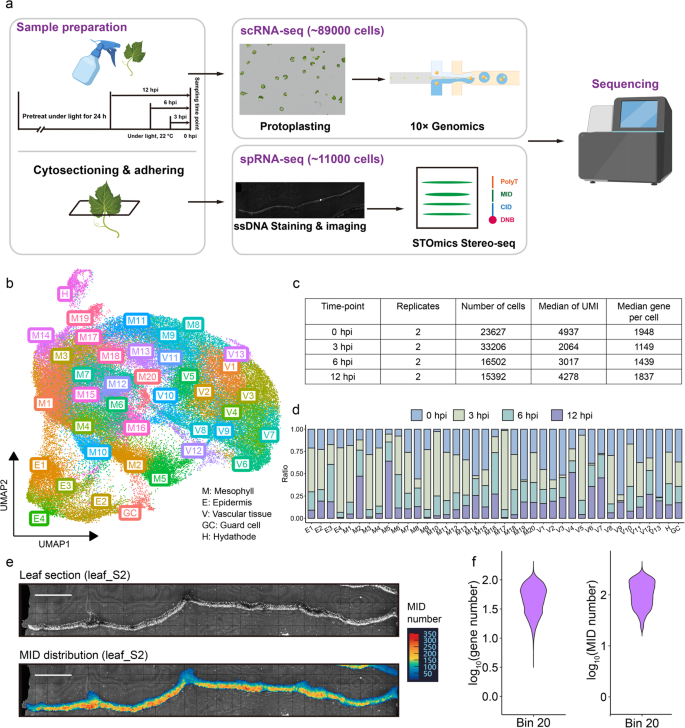
3.2 测序数据处理与细胞类型注释
实验目的是对单细胞与空间转录组数据进行质量控制与分析,完成细胞聚类与类型注释并验证可靠性。方法细节:单细胞测序数据用CellRanger进行比对计数,Seurat软件进行过滤(去除基因数<200的细胞与在<3个细胞中表达的基因)、归一化、整合与聚类,采用Harmony校正批次效应;空间转录组数据用SAW pipeline进行比对,stereopy软件处理聚类;通过跨物种同源标记基因(OMGs)与空间转录组定位结合的方法注释细胞类型,从拟南芥、橡胶树、草莓、番茄的单细胞数据库获取高置信度标记基因,OrthoFinder鉴定葡萄同源基因,结合空间定位注释细胞类型;通过已知标记基因与GO富集分析验证注释可靠性。结果解读:共获得88727个高质量单细胞,检测到22022个蛋白编码基因,占赤霞珠注释基因的79.53%;空间转录组获得11054个细胞,叶肉细胞占比最高(61%),保卫细胞仅占0.6%;GO富集分析显示保卫细胞富集“保卫母细胞分化”“气孔谱系进展”等过程,叶肉细胞富集“光合作用”“光反应”等过程,与已知细胞功能一致,验证了注释的可靠性。

3.3 感染过程中免疫反应的动态变化分析
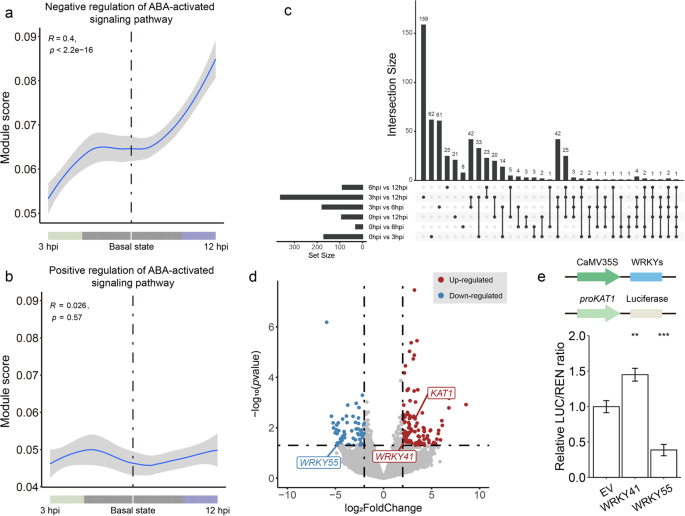
实验目的是解析葡萄叶片在霜霉菌感染过程中不同时间点与细胞类型的免疫反应动态。方法细节:计算防御反应得分(免疫反应模块得分减去防御反应负调控模块得分),分析四个时间点的免疫反应变化;RGAugury软件鉴定葡萄基因组中的抗性基因类似物(RGAs),包括NLR类(TX、TNL、CNL、RNL)与PRR类(RLP、RLK),分析其在不同时间点与细胞类型的表达模式;采用Kruskal–Wallis检验与Wilcoxon秩和检验进行统计学分析。结果解读:防御反应得分在3hpi达到最高,显著高于0、6、12hpi(P<0.05),12hpi得分最低,表明葡萄在3hpi启动强免疫反应,之后逐渐被霜霉菌抑制进入易感状态;CNL类RGAs在所有五种细胞类型中均在12hpi显著下调,保卫细胞中CNL与TX类RGAs的表达在12hpi接近0(P<0.01),表明霜霉菌在12hpi完全抑制了保卫细胞的免疫反应;PRR类基因在叶肉、维管组织与排水器中3hpi上调,之后逐渐下调,表皮与保卫细胞中无显著变化,推测表皮与保卫细胞的PTI通路被霜霉菌快速抑制。
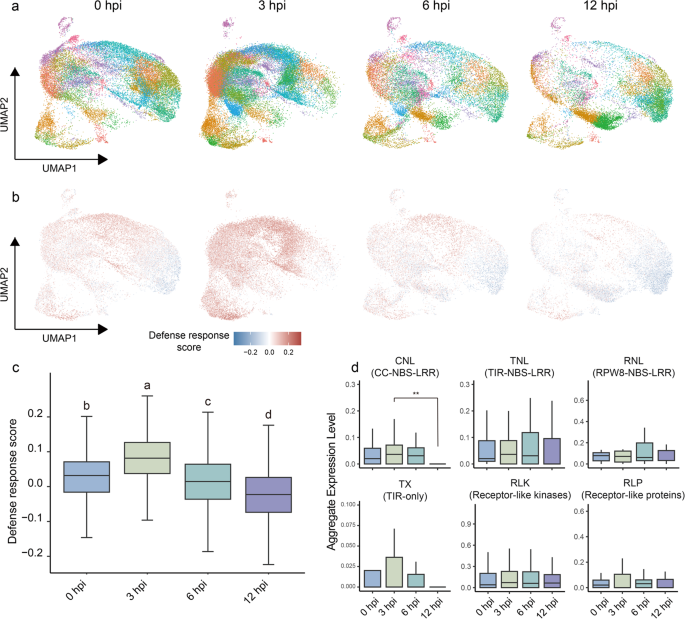
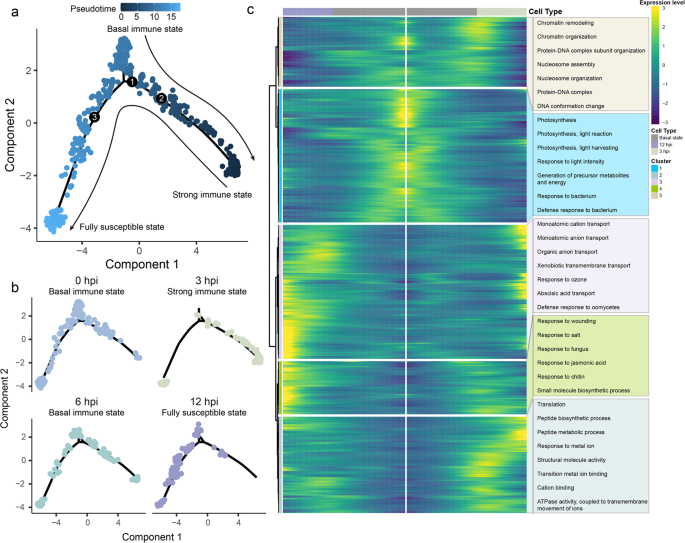
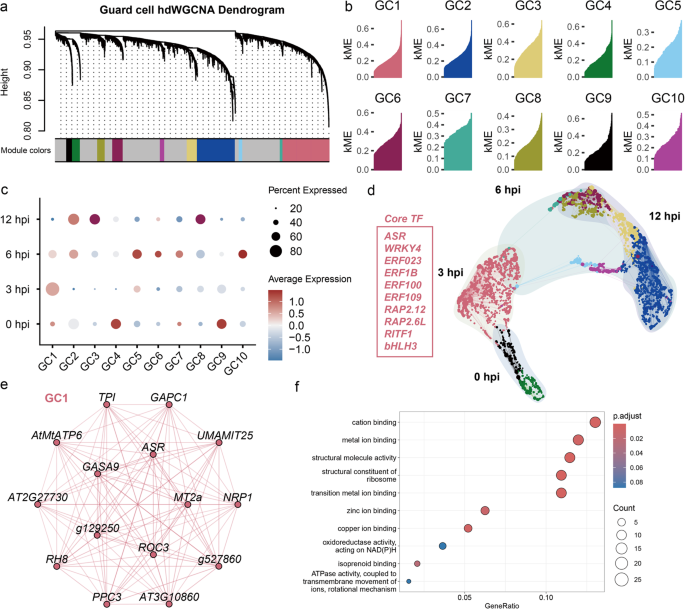
3.4 保卫细胞转录重编程机制解析
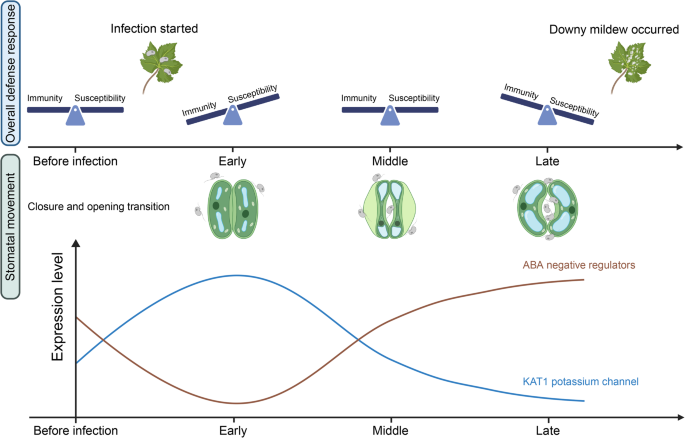
实验目的是揭示霜霉菌感染过程中保卫细胞的转录重编程机制,尤其是气孔运动的调控通路。方法细节:Monocle2软件对保卫细胞进行伪时间轨迹分析,解析细胞状态转变过程;hdWGCNA软件构建共表达网络,鉴定不同时间点的基因模块;通过伪时间轨迹与差异表达分析筛选气孔调控相关基因,包括ABA调控因子与钾通道基因;双荧光素酶实验验证WRKY41与WRKY55对KAT1的调控作用,将WRKY41、WRKY55的编码序列构建为效应子,KAT1启动子构建为报告子,共转化烟草叶片后检测荧光素酶活性。结果解读:伪时间轨迹显示保卫细胞从基础免疫状态(0、6hpi)向强免疫状态(3hpi)与易感状态(12hpi)两个分支转变,强免疫分支富集“染色质重塑”“阳离子转运”等过程,易感分支富集“ABA响应”“茉莉酸响应”等过程;共表达网络鉴定出10个基因模块,分别对应四个时间点,其中GC1模块(3hpi)富集氧化应激与ABA相关基因;ABA负调控因子在强免疫分支下调,在易感分支上调,正调控因子表达稳定;差异表达分析显示保卫细胞特异性钾通道KAT1在3hpi上调9.8倍(P<0.01),WRKY41上调7.6倍,WRKY55下调24.4倍;双荧光素酶实验显示WRKY41显著激活KAT1表达(P<0.01),WRKY55显著抑制KAT1表达(P<0.01),表明霜霉菌通过上调WRKY41、下调WRKY55促进KAT1表达,诱导气孔开放以利于入侵。
4. Biomarker研究及发现成果解析
本研究涉及的Biomarker包括细胞类型特异性标记基因、免疫反应动态标记与气孔调控功能标记,筛选逻辑为“跨物种同源标记筛选→空间转录组验证→差异表达分析→功能验证”,形成完整的筛选与验证链条。
Biomarker定位:细胞类型特异性标记基因包括保卫细胞的OST1、MPK12,表皮细胞的SVB,叶肉细胞的光合作用相关基因,筛选逻辑为跨物种同源标记基因鉴定结合空间转录组定位验证;免疫反应动态标记为CNL类RGAs,其表达水平随感染进程动态变化,可反映免疫状态;气孔调控功能标记包括ABA负调控因子、KAT1、WRKY41、WRKY55,筛选逻辑为伪时间轨迹与共表达网络分析结合双荧光素酶实验验证功能。
研究过程详述:细胞类型特异性标记基因来自拟南芥、橡胶树、草莓、番茄的高置信度单细胞标记基因,OrthoFinder鉴定葡萄同源基因,空间转录组验证其空间定位,如OST1、MPK12仅在保卫细胞中高表达;免疫反应动态标记CNL类RGAs通过RGAugury鉴定,单细胞转录组显示其在所有细胞类型中12hpi显著下调(P<0.01);气孔调控功能标记通过伪时间轨迹与差异表达分析筛选,ABA负调控因子在3hpi下调、12hpi上调,KAT1在3hpi上调9.8倍(P<0.01),WRKY41上调7.6倍,WRKY55下调24.4倍;双荧光素酶实验验证WRKY41的激活效应与WRKY55的抑制效应均具有统计学显著性(P<0.01)。
核心成果提炼:首次鉴定葡萄叶片五种细胞类型的特异性标记基因,为葡萄单细胞研究提供了重要资源;发现CNL类RGAs是葡萄免疫反应的关键动态标记,其表达水平可精准反映免疫状态;揭示ABA负调控因子与WRKY41-WRKY55-KAT1通路是霜霉菌诱导气孔开放的关键功能标记,其中KAT1作为保卫细胞特异性钾通道,受WRKY41与WRKY55的反向调控,该机制为葡萄霜霉病的早期诊断与防控靶点开发提供了新的候选分子,具有重要应用价值。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。