Cited2 regulates proliferation and survival in young and old mouse cardiac stem cells
Cited2 调控年轻和年老小鼠心脏干细胞的增殖和存活
| 期刊: | BMC Molecular and Cell Biology | 影响因子: | 2.700 |
| 时间: | 2019 | 起止号: | 2019 Jul 17;20(1):25 |
| doi: | 10.1186/s12860-019-0207-2 | 研究方向: | 信号转导、细胞生物学、发育与干细胞 |
| 细胞类型: | 干细胞 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Cited2 regulates proliferation and survival in young and old mouse cardiac stem cells;发表期刊:BMC Molecular and Cell Biology;影响因子:3.418;研究领域:心脏干细胞老化的分子调控机制。
心脏干细胞(CSCs)是心脏内具有自我更新和多向分化能力的成体干细胞,是心脏损伤后再生修复的关键细胞来源。自2003年CSCs首次被分离鉴定以来,其“定向分化为心肌细胞、平滑肌细胞”的功能被证实,推动了心脏再生领域的发展。但随着年龄增长,CSCs的增殖能力下降、凋亡增加,其再生潜力显著降低,成为限制CSCs临床应用的核心问题。当前研究热点聚焦于解析CSCs老化的分子机制,尤其是转录因子、microRNA等调控因子的作用,但CSCs老化的分子调控网络仍不完整——具体哪些转录因子参与调控CSCs的增殖与存活,尚不明确。
Cited2作为一种转录共激活因子,已被证实调控胚胎干细胞的自我更新(通过维持Nanog表达)、造血干细胞的静息与凋亡,以及肌腱干细胞的老化与分化,但在CSCs中的作用尚未被研究。此外,Cited2在心脏发育中不可或缺(Cited2-/-小鼠出现心脏间隔缺损、流出道畸形),提示其可能参与CSCs的功能调控。因此,本研究旨在探究Cited2对年轻与年老小鼠CSCs增殖、存活及分化的调控作用,为CSCs老化的分子机制提供新见解。
2. 文献综述解析
文献综述围绕“Cited2的功能演进”展开核心评述:作者首先回顾Cited2在胚胎发育中的核心作用——敲除Cited2导致小鼠胚胎致死,且出现心脏畸形(如动脉间隔缺损、流出道异常);接着阐述其在多种成体干细胞中的调控功能——包括维持胚胎干细胞的自我更新(通过调控Nanog表达)、调控造血干细胞的静息与凋亡、影响肌腱干细胞的老化与分化(Cited2下调与肌腱退化相关);随后重点强调Cited2在心脏发育中的必要性,但指出其在CSCs老化中的作用尚未被探索。
现有研究的关键结论可归纳为三点:① Cited2是干细胞功能的重要调控因子,参与分化、自我更新与凋亡的平衡;② Cited2在心脏发育中不可或缺,其缺陷导致严重心脏畸形;③ 干细胞老化的核心表型(增殖下降、凋亡增加)与调控因子的表达变化密切相关。技术方法上,基因敲除/过表达、流式细胞术、免疫荧光等是研究干细胞功能的常规手段,但局限性在于缺乏针对CSCs的特异性研究——现有研究未明确Cited2是否参与CSCs的老化调控。
本研究的创新价值在于首次将Cited2与CSCs老化关联:聚焦Cited2对CSCs增殖与存活的调控,且排除了对分化能力的影响,填补了Cited2在CSCs研究中的空白,为CSCs老化的分子机制提供了新的调控因子。
3. 研究思路总结与详细解析
本研究以“Cited2在CSCs中的表达变化→Cited2对CSCs分化的影响→Cited2对CSCs增殖与存活的调控”为核心逻辑,研究目标是明确Cited2对年轻(Y-)与年老(O-)小鼠CSCs增殖、存活及分化的作用;核心科学问题是Cited2如何调控CSCs的老化表型(增殖下降、凋亡增加);技术路线为“表达验证→功能干预(过表达/敲低)→表型检测(分化、增殖、凋亡、细胞周期)”的闭环。
3.1 Cited2在老化心脏与CSCs中的表达验证
实验目的:确认Cited2在老化小鼠心脏组织及CSCs中的表达变化。
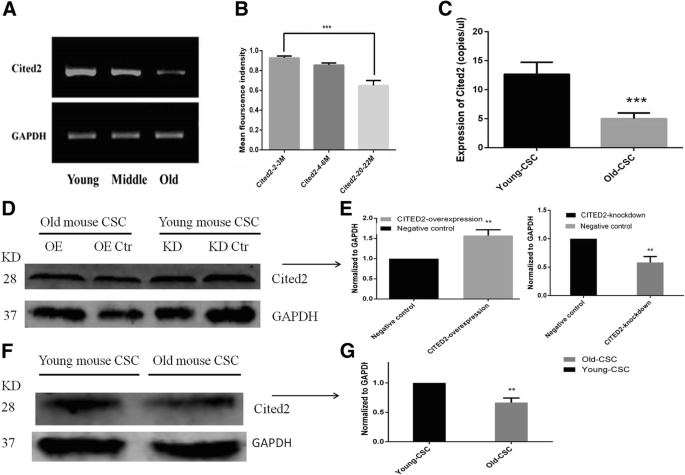
方法细节:收集2-3月龄(年轻)、4-6月龄(中年)、20-22月龄(年老)小鼠的心脏组织,通过RT-PCR检测Cited2 mRNA水平;分离年轻(2-3月龄)与年老(20-22月龄)小鼠的CSCs(Y-CSCs、O-CSCs),采用 droplet digital PCR(dd-PCR)定量检测Cited2 mRNA(因CSCs数量少,dd-PCR灵敏度更高);同时通过免疫印迹检测CITED2蛋白水平(使用Abcam的CITED2抗体、Cell Signaling Technology的GAPDH抗体)。
结果解读:RT-PCR显示,心脏组织中Cited2 mRNA水平随年龄增长显著下降(年轻 vs 年老,P<0.01);dd-PCR结果表明,O-CSCs的Cited2 mRNA水平显著低于Y-CSCs(n=3,P<0.01);免疫印迹显示,O-CSCs的CITED2蛋白水平同样显著降低(n=3,P<0.01)。
实验所用关键产品:TRIzol试剂(Invitrogen)、OneStep RT-PCR试剂盒、EvaGreen Supermix(Bio-Rad)、CITED2抗体(Abcam)、GAPDH抗体(Cell Signaling Technology)。
3.2 Cited2对CSCs分化能力的影响
实验目的:验证Cited2是否调控CSCs的多向分化能力(心肌细胞、平滑肌细胞、内皮细胞)。
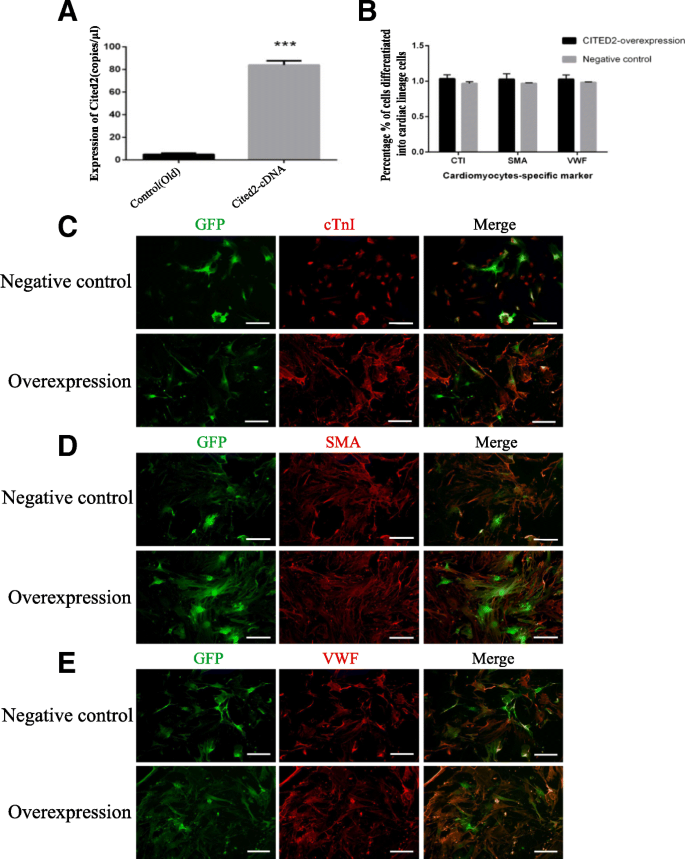
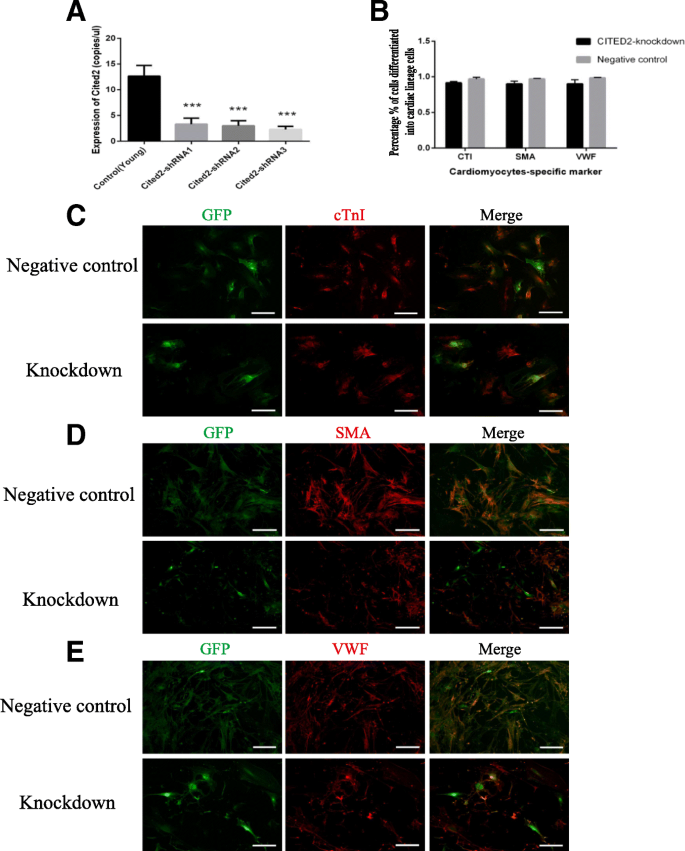
方法细节:构建Cited2过表达慢病毒(Cited2-cDNA)转染O-CSCs,构建Cited2敲低慢病毒(Cited2-shRNA)转染Y-CSCs(共设计3条shRNA,筛选出敲低效率最高的shRNA3),以空载体转染为阴性对照;转染后3天,将CSCs置于心肌细胞、平滑肌细胞、内皮细胞诱导培养基中培养14天,通过免疫荧光检测分化标志物——心肌肌钙蛋白I(cTnI)、α-平滑肌肌动蛋白(α-SMA)、血管性血友病因子(VWF)的表达(GFP标记慢病毒转染阳性细胞)。
结果解读:免疫荧光结果显示,无论O-CSCs过表达Cited2还是Y-CSCs敲低Cited2,其分化标志物(cTnI、α-SMA、VWF)的阳性细胞比例与对照组无显著差异(n=5,P>0.05),表明Cited2不影响CSCs的多向分化能力。
实验所用关键产品:慢病毒载体(Hanbio)、Alexa Fluor系列免疫荧光二抗(领域常规使用)。
3.3 Cited2对CSCs增殖与细胞周期的调控
实验目的:探究Cited2对CSCs增殖能力及细胞周期分布的影响。
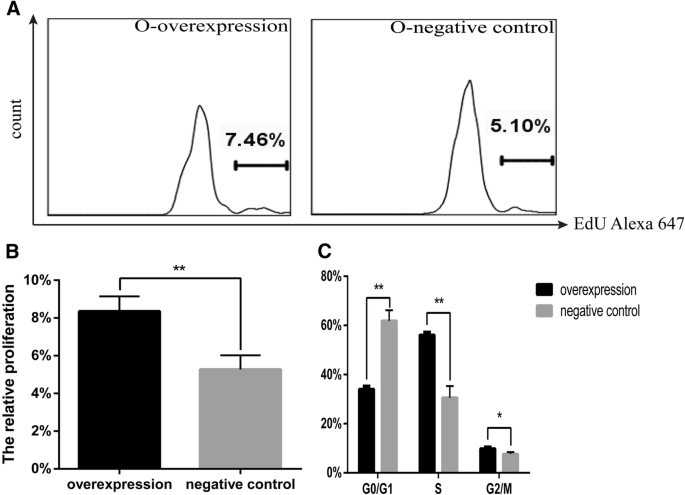
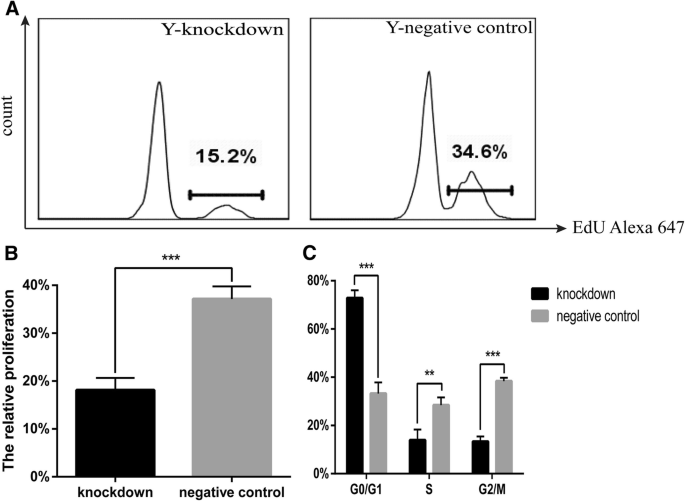
方法细节:对于O-CSCs,转染Cited2过表达慢病毒后,采用EdU assay(5-乙炔基-2"-脱氧尿苷掺入法)检测增殖(EdU标记增殖细胞,流式细胞术定量);同时通过7-AAD染色流式细胞术分析细胞周期分布(G0/G1、S、G2/M期比例)。对于Y-CSCs,转染Cited2-shRNA3后,重复上述实验。
结果解读:O-CSCs过表达Cited2后,EdU阳性细胞比例显著增加(对照 vs 过表达,P<0.01),细胞周期中G0/G1期比例降低(从约65%降至50%),S+G2/M期比例增加(从约35%升至50%,n=3,P<0.01);Y-CSCs敲低Cited2后,EdU阳性细胞比例显著降低(对照 vs 敲低,P<0.01),G0/G1期比例增加(从约55%升至70%),S+G2/M期比例减少(从约45%降至30%,n=3,P<0.01)。
实验所用关键产品:EdU试剂盒(RiboBio)、7-AAD Flow Cytometry Assay kit(Ebioscience)。
3.4 Cited2对CSCs凋亡的影响
实验目的:明确Cited2对CSCs凋亡的调控作用。
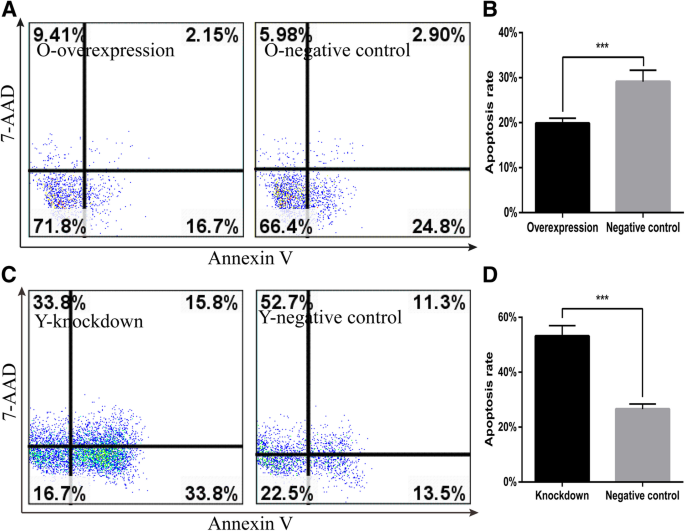
方法细节:采用Annexin V-PE/7-AAD双染色流式细胞术检测凋亡——Annexin V-PE标记早期凋亡细胞,7-AAD标记晚期凋亡/坏死细胞,两者双阳性为晚期凋亡细胞。分别检测O-CSCs过表达Cited2、Y-CSCs敲低Cited2后的凋亡率。
结果解读:O-CSCs过表达Cited2后,凋亡率显著降低(对照 vs 过表达,从约15%降至8%,n=3,P<0.01);Y-CSCs敲低Cited2后,凋亡率显著增加(对照 vs 敲低,从约10%升至20%,n=3,P<0.01)。
实验所用关键产品:Annexin V-phycoerythrin(PE)Apoptosis Detection kit(Invitrogen)。
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
本研究中Cited2可作为“CSCs老化的潜在分子Biomarker”,其筛选遵循“数据库挖掘→组织验证→细胞验证”的完整链条:首先通过基因芯片分析老化小鼠心脏组织的差异基因,筛选出随年龄下降的Cited2;随后通过RT-PCR验证心脏组织中的表达下降;最后通过dd-PCR(细胞mRNA)和免疫印迹(细胞蛋白)验证CSCs中的表达下降。
研究过程详述
Cited2的来源为小鼠心脏组织(2-3、4-6、20-22月龄)和CSCs(年轻与年老);验证方法包括RT-PCR(组织mRNA定量)、dd-PCR(细胞mRNA定量,解决细胞量少的问题)、免疫印迹(细胞蛋白定量);特异性方面,Cited2在年老心脏组织和CSCs中的表达显著低于年轻组(P<0.01),且与CSCs的老化表型(增殖下降、凋亡增加)直接相关;敏感性数据未明确提供,但多次重复实验(n=3)的统计显著性表明其表达差异具有可靠性。
核心成果提炼
Cited2作为CSCs老化的潜在Biomarker,其核心功能关联与创新性如下:
1. 功能关联:Cited2表达下降与CSCs的增殖能力降低、凋亡增加及细胞周期阻滞(G0/G1期)直接相关——O-CSCs中Cited2低表达导致增殖减少、凋亡增加,而过表达Cited2可部分恢复其增殖能力并抑制凋亡;Y-CSCs中敲低Cited2则模拟了老化表型(增殖下降、凋亡增加)。
2. 创新性:首次发现Cited2是CSCs增殖与存活的关键调控因子,且不影响其分化能力——这与Cited2在其他干细胞(如肌腱干细胞)中的作用不同,为CSCs老化的分子机制提供了新的 Biomarker 候选。
3. 统计学可靠性:所有关键实验均重复3次(n=3),P值均<0.01,结果稳定可靠。
本研究通过系统验证Cited2在CSCs中的表达与功能,为CSCs老化的分子机制提供了新见解,也为CSCs的临床应用(如通过调控Cited2恢复老化CSCs的功能)提供了理论基础。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。